搅拌棒吸附萃取-液相色谱-串联质谱法测定农业废水中二氯吡啶酸残留量
2020-09-17王雪平朱惠斌
王雪平, 耿 悦, 朱惠斌*
(1.黄河水利职业技术学院,河南开封 475004;2.开封市绿色涂层材料重点实验室,河南开封 475004)
二氯吡啶酸(Clopyralid),又名3,6-二氯吡啶-2-羧酸、3,6-二氯吡啶羧酸,商品名毕克草Ⅱ号(CAS号1702-17-6),是一种人工合成的拟植物激素型除草剂,属内吸性农药,施药后会很快被杂草叶片、根部吸收,并传递到全株各部位。其除草作用机理为促进杂草DNA、RNA和蛋白质的合成,致使根部生长过量、茎及叶生长畸形、养分消耗,维管束输导功能受阻,导致杂草死亡,可彻底杀死敏感深根杂草[1 - 3]。二氯吡啶酸已成为农业废水中新型污染物,若过量滥用,二氯吡啶酸可通过多种途径污染土壤、水体,从而引发对非靶标植物、动物繁殖、植物群落等一系列问题[4 - 7]。欧盟规定饮用水中单个农药的残留量≤0.1 mg/kg;我国国家标准(GB 2763-2016)《食品安全国家标准 食品中农药最大残留限量》中规定,小麦、玉米、油菜籽中二氯吡啶酸最大残留量分别为2、1、2 mg/kg,但尚未制订水中二氯吡啶酸残留限量和分析方法。因此,建立高效、准确的水中二氯吡啶酸残留量检测方法具有重要意义。
目前关于二氯吡啶酸测定方法主要有高效液相色谱法[8 - 10]、气相色谱法[11,12]、液相色谱-质谱法[13],分析对象大多为二氯吡啶酸原药及其水溶性粒剂、油菜、土壤、植物源性食品等,而关于农业废水中二氯吡啶酸残留量检测报道较少。搅拌棒吸附萃取(Stir Bar Sorptive Extraction,SBSE)是一种新型固相微萃取样品前处理技术[14,15],该技术具有萃取容量高、无需外加搅拌子、可避免竞争性吸附、操作简便等特点,在痕量物质分析中具有广阔的应用前景。本文在优化搅拌棒吸附萃取条件和液相色谱-质谱法参数的基础上,建立了SBSE-液相色谱-串联质谱法(LC-MS/MS)测定农业废水中二氯吡啶酸残留量,以期为农业废水中二氯吡啶酸残留监控提供检测方法。
1 实验部分
1.1 仪器与试剂
ACQUITY型超高效液相色谱仪(美国,Waters公司);Xevo TQ MS型三重四极杆质谱仪(美国,Waters公司);Milli-Q超纯水器(美国,Millipore公司);ME204E电子分析天平(瑞士,Mettler公司);Vortex-Genie 2型涡旋振荡器(美国,Scientific Industries公司);AVANTI J-15型高速冷冻离心机(美国,Beckman Coulter公司);SKY-211D型恒温培养振荡器(江苏盛蓝仪器制造有限公司);TTL-DC氮吹仪(北京同泰联科技发展有限公司);搅拌棒(德国,Gerstel公司),棒长10 mm,聚二甲基硅氧烷(PDMS)膜厚0.5 mm,萃取相涂层25 μL。
二氯吡啶酸标准品(纯度98%,美国A Chemtek Inc.公司)。二氯吡啶酸标准储备液:准确称取适量的二氯吡啶酸标准品,用乙腈配制成质量浓度为100 mg/L的标准储备液。使用时用初始流动相进行稀释,现用现配。甲醇、乙腈为色谱纯;NaCl、HCl均为分析纯。实验用水为超纯水。
1.2 仪器工作条件
色谱条件:UPLC BEH C18色谱柱(150 mm×2.1 mm,1.7 μm);流动相A为0.1%甲酸溶液,B为乙腈;流动相梯度洗脱程序:0~2.0 min,90%~30%A;2.0~4.0 min,30%~10%A;4.0~4.1 min,10%~90%A;4.1~10.0 min,90%A。流速0.2 mL/min;柱温40 ℃;进样量3 μL。
质谱条件:电子轰击电离源(EI);负离子扫描;毛细管电压3.5 kV;离子源温度150 ℃;干燥气温度450 ℃;干燥气流速600 L/h;碰撞气氩气,流速0.15 mL/min。二氯吡啶酸多反应监测(MRM)模式条件:定性离子对m/z189.9/35.1;定量离子对m/z189.9/146.1;锥孔电压18 V;碰撞能量10 eV。
1.3 样品前处理
准确移取10 mL样品,置于50 mL离心管中,加入PDMS搅拌棒,控制NaCl质量浓度为100 g/L;在温度20 ℃下,以100 r/min搅拌萃取30 min;加入甲醇10 mL,以100 r/min振荡解吸30 min,解吸液在45 ℃ 氮吹浓缩近干,加入初始流动相溶解并定容至1 mL,过0.22 μm有机相微孔滤膜,滤液待测。
2 结果与讨论
2.1 质谱条件的优化

图1 二氯吡啶酸二级质谱图Fig.1 Secondary mass spectrum of clopyralid

图2 二氯吡啶酸标准溶液总离子流色谱图Fig.2 Total ion current chromatogram of clopyralid standard solution
以蠕动泵直接进样,将1.0 μg/mL二氯吡啶酸标准溶液连续注入电子轰击电离源中,分别采用正离子模式或负离子模式对二氯吡啶酸进行质谱分析。结果表明:采用负离子模式时,可获得质荷比(m/z)为189.9的高丰度[M-H]-准分子离子峰,这可能与二氯吡啶酸分子结构中羧基易失去H有关;以准分子离子峰为母离子进行子离子扫描,并在MRM模式下优化碰撞能量和锥孔电压,获得的二级碎片离子主要为m/z35.1、74.1、92.0、146.1(图1),其中m/z35.1信号最稳定,m/z146.1信号最强,因此选择m/z35.1为定性离子,选择m/z146.1为定量离子。
2.2 色谱条件的选择
分别考察色谱柱的类型(Diamonsil C18、Zorbox SB C18、Waters BEH C18、Shim-pack VP-ODS C18),流动相的组成(甲醇/乙腈-水、甲醇/乙腈-0.1%甲酸溶液、甲醇/乙腈-5 mmol/L NH4Ac溶液)对二氯吡啶酸的色谱分离效果和离子化效率的影响。结果表明:采用Diamonsil C18、Zorbox SB C18、Shim-pack VP-ODS C18色谱柱时,二氯吡啶酸色谱峰较宽,出峰时间较长(6.82~8.74 min),而Waters BEH C18色谱柱对二氯吡啶酸的出峰时间适中(5.32 min)、分离度好、灵敏度高、峰形对称且尖锐。采用Waters BEH C18作为分析柱,以甲醇/乙腈-水或甲醇/乙腈-5 mmol/L NH4Ac溶液为流动相时,二氯吡啶酸峰形较差,出现基线漂移;以甲醇/乙腈和0.1%甲酸溶液为流动相时,色谱图响应值较高,尤其有机相选择乙腈时,色谱峰峰形更窄,且峰形尖锐对称、分离效果最好,色谱分离情况见图2。
2.3 搅拌棒萃取条件的优化
2.3.1 搅拌棒萃取影响因素分析以PDMS搅拌棒对农业废水中二氯吡啶酸萃取率为考察指标,采用单一变量法分别研究萃取时间、萃取温度、搅拌速率、pH值、离子强度对二氯吡啶酸的萃取效率的影响。结果表明:当萃取时间在10~30 min时,二氯吡啶酸萃取效率随着萃取时间的延长而增高;当萃取温度在30~50 ℃时,二氯吡啶酸萃取效率随着萃取温度的升高而降低;当搅拌速率在50~150 r/min时,二氯吡啶酸萃取效率随着搅拌速率的增大而增高;离子强度可影响二氯吡啶酸在农业废水和PDMS搅拌棒涂层中的分配系数,加入质量浓度为50~100 g/L NaCl,二氯吡啶酸萃取效率随着搅拌速率的增大而增高;当农业废水中pH值在5~8时,二氯吡啶酸萃取效率受pH值的影响较少。因此,影响PDMS搅拌棒对农业废水中二氯吡啶酸萃取效率的因素主要为:萃取时间、萃取温度、搅拌速率、离子强度。
2.3.2 正交试验分析选取萃取时间(A)、萃取温度(B)、搅拌速率(C)、离子强度(D)四个因素,选用3个水平,设计因素水平表(表1),采用L9(34)正交试验设计(表2)和方差分析(表3)进行PDMS搅拌棒萃取条件优化。

表1 正交试验因素及水平
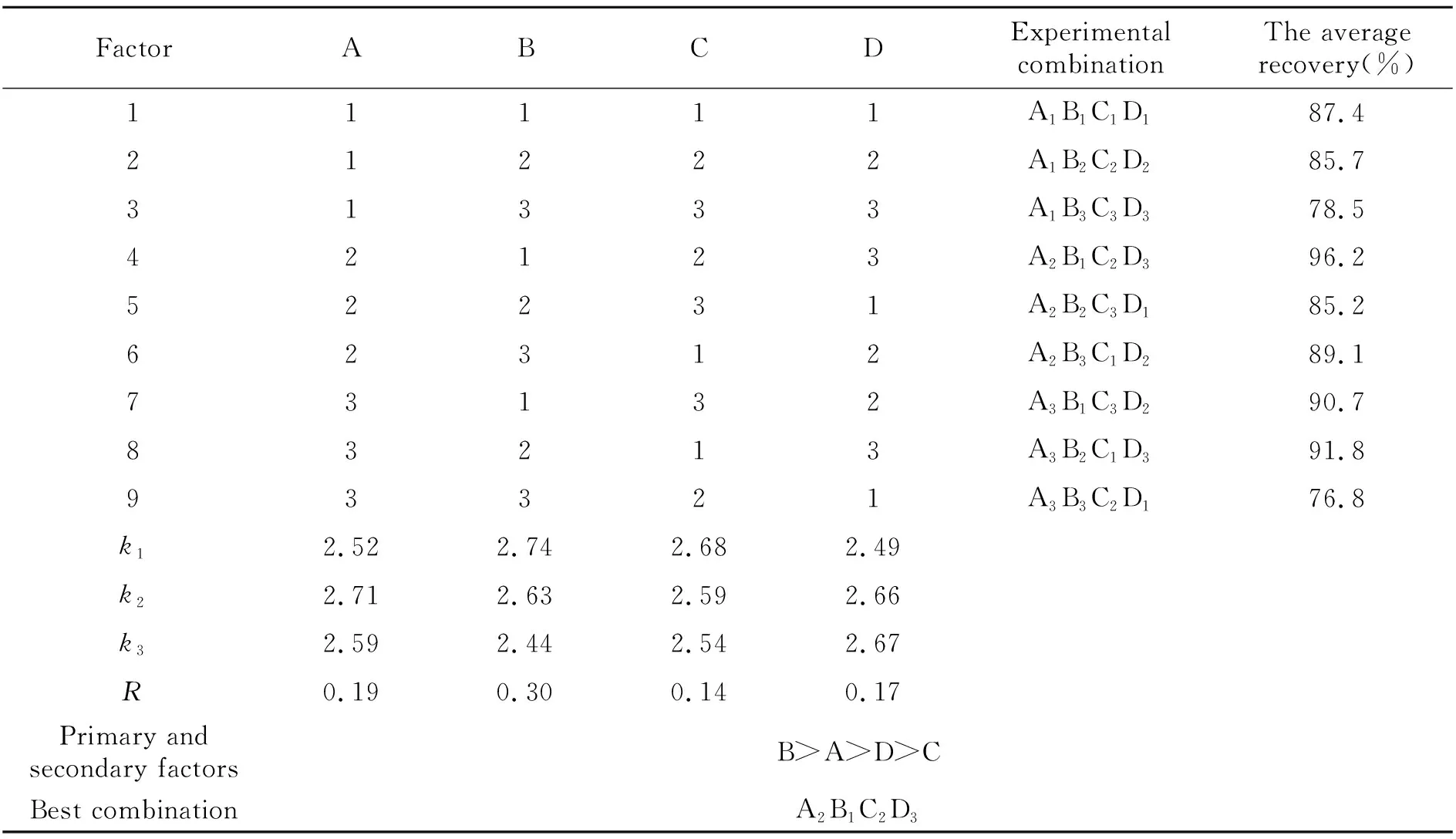
表2 L9(34)正交试验设计及实验结果

表3 方差分析表
从表3中可知,影响PDMS搅拌棒萃取条件的因素为;B>A>D>C;PDMS搅拌棒萃取最优条件为:A2B1C2D3,即PDMS搅拌棒萃取时间30 min,萃取温度20 ℃,搅拌速率100 r/min,离子强度100 g/L。从表4中可知,萃取时间、萃取温度、搅拌速率、离子强度对正交试验无显著性影响。
2.4 搅拌棒解吸条件的优化
分别考察了解吸液、解吸时间、解吸模式对PDMS搅拌棒对农业废水中二氯吡啶酸解吸效率的影响。结果表明:甲醇对搅拌棒PDMS涂层吸附的二氯吡啶酸具有良好的解吸效果,解吸率可达98.6%;解吸时间在5~15 min范围内,二氯吡啶酸的解吸率随着时间的延长而增大,当解吸时间增加到30 min时,二氯吡啶酸的解吸率不再发生变化,趋于平衡;与静态解吸模式相比,动态解吸模式经搅拌或振荡能显著提高甲醇溶剂传递,从而加速被搅拌棒吸附的二氯吡啶酸解吸。因此本实验解吸条件选择:采用动态解吸模式,以甲醇作为解析液,解吸时间30 min。
2.5 基质效应的影响
为避免农业废水中非目标物对搅拌棒萃取二氯吡啶酸时产生干扰,采用标准加入法分析二氯吡啶酸在纯乙腈和不含目标物的农业废水中的基质效应(ME=B/A×100%,B为农业废水基质中目标物质谱响应值,A为纯乙腈基质中目标物质谱响应值)[16]。结果表明:在纯乙腈和不含目标物的农业废水两种基质中分别加入终浓度为1.0 μg/L、25.0 μg/L、50.0 μg/L三种水平浓度的二氯吡啶酸标准溶液,按本文所建方法SBSE-液相色谱-质谱法测定二氯吡啶酸质谱响应值,经计算基质效应在92.1%~97.3%之间。这表明采用SBSE-液相色谱-质谱法测定农业废水中二氯吡啶酸时,不存在基质效应。
2.6 线性范围、检出限与定量限
依次配制质量浓度为1.0、5.0、10.0、25.0、50.0 ng/mL二氯吡啶酸标准系列溶液,按本文所建立的方法进行测定,以二氯吡啶酸的质量浓度(x)为横坐标,二氯吡啶酸的质谱响应值(y)为纵坐标,绘制标准曲线;对20份不含目标物的空白农业废水样品进行测定,以3倍信噪比(S/N=3)为检出限,以S/N=10为定量限。结果表明:二氯吡啶酸质量浓度在1.0 ng/mL~50.0 ng/mL范围内与其质谱响应值呈线性关系,线性回归方程为:y=8127.3x+654.2,相关系数(r)为0.9998;检出限为0.3 μg/L,定量限为1.0 μg/L。
2.7 加标回收率和精密度
随机选取具有代表性的3种农业废水,依次添加终浓度为1.0 ng/mL、25.0 ng/mL、50.0 ng/mL二氯吡啶酸标准,每个加标水平重复测定6次,按本文所建立的方法测定加标回收率和相对标准偏差(RSD)。结果见表4。从表4中可知:在1.0~50.0 ng/mL加标浓度范围内,二氯吡啶酸平均加标回收率在87.8%~97.8%范围,RSD在0.9%~4.7%之间。该方法准确度高、精密度好。

表4 回收率和精密度(n=6)

(续表4)

图3 农业废水样品中二氯吡啶酸总离子流色谱图Fig.3 Total ion current chromatogram ofclopyralid in agricultural wastewater
2.8 实际样品的测定
采用本文所建立的SBSE-LC-MS/MS法,对30份实际农业废水样品进行二氯吡啶酸残留量测定。结果表明:30份所检测的农业废水中,4份农业废水检出二氯吡啶酸,见图3。阳性检出率为13.3%,残留量在8.3~257.2 μg/L之间;4份阳性农业废水采集地附近为油菜、小麦种植区,二氯吡啶酸残留可能是由于防除阔叶杂草而喷施含有二氯吡啶酸的除草剂引起的。
3 结论
本研究在优化搅拌棒吸附萃取条件和液相色谱-质谱法参数的基础上,建立了SBSE-液相色谱-串联质谱法测定农业废水中二氯吡啶酸含量的分析方法。实验结果表明该方法具有操作简便、试剂消耗少、准确度高、检出限低等特点,可为农业废水中二氯吡啶酸含量监测提供检测方法。
