磁固相萃取结合气-质联用测定土壤中的有机氯农药
2020-09-17于爱民
曲 博, 王 慧, 丁 杰, 于爱民
(1.中国航空工业空气动力研究院质量安全处,黑龙江哈尔滨 150009;2.哈尔滨工业大学城市水资源与水环境国家重点实验室,黑龙江哈尔滨 150090;3.吉林大学化学学院,吉林长春 130012)
有机氯农药(Organochlorine Pesticides,OCPs)作为一种重要的杀虫剂,自20世纪40年代以来在世界范围内得到大规模生产和应用[1]。相关研究表明,有机氯农药能在生物脂肪层中积累,对人类健康构成威胁[2 - 4]。尽管大多数有机氯农药多年前已停止生产,但由于其在土壤中的持久性,土壤仍是有机氯农药的重要蓄积库和二次排放源,它可在地域和区域尺度上促进大气污染,因此,监测土壤中的有机氯农药残留对于评估排放和气-土分离至关重要。
近年来,利用气相色谱-串联质谱(GC-MS/MS)[5 - 7]或电子捕获检测器[8,9]等技术,分析环境样品中的有机氯农药已被大量报道。GC-MS/MS已被公认为一种灵敏度高、选择性强的测定方法。然而,由于土壤基质复杂,地表水中有机氯农药浓度低,很难通过GC-MS/MS直接检测,因此分析方法还应包括强有力的萃取分离富集步骤,以去除基质干扰,提高方法灵敏度。
磁性固相萃取(MSPE)作为一种很有前途的样品前处理技术已得到广泛的研究[10,11]。磁性吸附剂可以通过外加磁场快速实现相分离,这避免了传统固相萃取中装柱、上样、过滤等繁琐步骤。磁性脂质体是一种人工制备的磁性纳米颗粒,由类似细胞膜的磷脂双分子层包裹着水相介质组成。脂质体具有无毒性、无免疫源性和生物降解性等特点,常被作为药物载体用于临床医疗,以降低药物毒副作用并提高其疗效[12]。磷脂双分子层可以通过疏水作用吸附有机物,而且两性离子端赋予磁性脂质体的外表面亲水性,可以改善吸附剂在水溶液中的分散性能。Zhang等人[13]应用磁性磷脂双层膜分析环境水体和牛奶中的多环芳烃,获得了很好的吸附效果。本文提出了一种以磁性脂质体为吸附剂提取环境样品中9种有机氯农药的新方法。该方法简单快速,萃取分离和富集可一步完成。我们对磁性脂质体的几种性质进行了评价,并考察了影响吸附性能的主要实验因素。
1 实验部分
1.1 仪器、试剂与样品
7890A-7000B气相色谱-串联三重四极杆质谱联用仪(美国,安捷伦);SIGMA 500场发射扫描电镜(德国,卡尔蔡司);JEM-1400透射电子显微镜(日本,日立);FT-IR 360傅里叶变换红外光谱仪(美国,尼克莱);SB -5200DT超声清洗仪(宁波新芝生物科技股份有限公司)。
有机氯农药标准品:五氯苯、六氯苯、α-六六六、林丹、α-氯丹、十氯酮、p,p′-DDT、β-硫丹、灭蚁灵,均购于德国Dr.Ehrenstorfer公司;大豆卵磷脂和胆固醇购于德国Sigma-Aldrich公司;分析纯FeCl3·6H2O和FeCl2·4H2O购于上海阿拉丁试剂有限公司;分析纯乙腈、乙醇、甲醇、丙酮、正己烷、三氯甲烷、HAc和氨水等试剂购于北京化工厂。水为去离子水。
土壤样品取样于哈尔滨市、吉林市和敦化市境内5处不同区域的土地,包括化工厂附近、农田、公园、公路大桥等。土样经过风干,研磨,过10目筛子后,置于暗处保存。
1.2 气相色谱-串联质谱分析
气相色谱柱为HP-5MS毛细管柱(30 m×0.25 mm i.d.,0.25 μm;Agilent),固定相为(5%苯基)甲基聚硅氧烷。以氦气为载气,流速为1.2 mL/min。柱温箱梯度升温:初始温度80 ℃,以15 ℃/min速度升温至305 ℃,保持3 min。进样体积2 μL。进样口温度230 ℃,在不分流进样模式下工作。
质谱参数如下:输送线温度305 ℃,离子源温度230 ℃,四极杆温度150 ℃,电子冲击电离能70 eV,溶剂延迟时间5 min。在MS1质量为50~400 amu的范围内,对9种分析物进行全扫描监测,以获得它们的保留时间,并确定合适的前级离子。然后将识别出的前级离子进一步碎片化,进而在MRM的工作模式下进行数据采集。
1.3 磁性脂质体的准备
采用化学共沉淀法制备Fe3O4磁性纳米粒子[14]:氮气保护下,将100 mL含有0.01 mol FeCl2·4H2O和0.02 mol FeCl3·6H2O的水溶液加热至80 ℃,然后加入40 mL 2.0 mol/L的NaOH溶液,恒温水浴下搅拌60 min。用外加磁铁收集沉淀物,用去离子水和乙醇反复清洗。
采用改进的干脂膜水化法制备了磁性脂质体[12,15]:将Fe3O4纳米颗粒(1.0 g)用无水乙醇和三氯甲烷冲洗几次以去除水分,然后分散在含有卵磷脂(0.6 g)和胆固醇(0.12 g)的50 mL三氯甲烷中。所有组分经超声分散5 min后,在40 ℃旋转蒸发溶剂,并在旋蒸瓶上形成均匀薄膜。随后,将旋蒸瓶置于真空干燥箱中至少3 h,以去除残留有机溶剂。用超声波仪水合120 min,使所得的干脂膜分散在去离子水中。制得的磁性脂质体用外部磁铁分离,用乙醇清洗,然后分散到80 mL去离子水中。磁性脂质体悬浮液被储存在4 ℃的冰箱中。冻干后的磁性脂质体重量约为1.6 g,所以磁性脂质体悬浮液的浓度约为20 mg/mL。
1.4 实际样品分析
称取2 g土壤样品于锥形瓶中,再将10 mL乙腈加入锥形瓶,摇匀,超声萃取8 min后离心。将上清液取出并分散于200 mL的去离子水中,加入120 mg的磁性脂质体,吸附25 min后,在强磁场作用下快速从溶液中分离出捕获了有机氯农药的磁性脂质体。用1 mL乙腈超声洗脱吸附在磁性脂质体上的目标物。这个洗脱过程重复进行三次,每次超声辅助时间为40 s。用氮吹仪在50 ℃条件下,将合并后的洗脱液吹干。用0.5 mL正己烷回溶残渣并进行气相色谱-串联质谱分析。
2 结果与讨论
2.1 磁性脂质体的表征
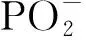

图1 Fe3O4(a)和磁性脂质体(b)的傅立叶变换红外(FT-IR)光谱(A)图和Fe3O4(a)和磁性脂质体(b)的磁化曲线(B)Fig.1 FT-IR spectra(A) and magnetization curves(B) of the obtained Fe3O4(a) and magnetoliposomes(b) nanoparticles
2.2 吸附容量的测定
以林丹、p,p′-DDT和灭蚁灵为模型目标物,用静态吸附法测定磁性脂质体对有机氯的吸附容量(图2A)。在5 mL离心管中制备了一系列初始浓度为5~500 mg/L的2 mL 有机氯农药溶液,每个溶液中均含有20 mg的磁性脂质体。将离心管置于恒温振荡器中,于25 ℃、150 r/min振荡。达到平衡后(6 h),用6 mL正己烷分三次萃取水溶液,合并有机相后浓缩至1 mL。采用气相色谱-串联质谱测定吸附后有机氯农药的平衡浓度。计算吸附剂对有机氯农药的吸附容量(qe):qe=(c0-ce)×V/m。其中,c0和ce(mg/L)分别是有机氯农药溶液的初始浓度和吸附后的平衡浓度,V(L)为水溶液体积,m(g)为磁性脂质体的质量。磁性脂质体对林丹、p,p′-DDT和灭蚁灵的吸附容量分别为20.73、21.43和17.42 mg/g。
2.3 吸附动力学
以林丹、p,p′-DDT和灭蚁灵为模型目标物,通过静态吸附法研究了吸附容量随吸附时间的变化。准确称量磁性纳米吸附剂20 mg,分散于2.0 mL 100 mg/L的有机氯农药标准溶液中,将离心管置于恒温振荡器上。在1~20 min内,磁性脂质体对有机氯农药的吸附容量迅速增大,20~30 min内,增大趋势渐缓,30 min后增大趋势不明显。因此,磁性脂质体对有机氯农药的吸附在30 min内达到平衡(图2B)。
图2 (A) 磁性脂质体对有机氯的静态吸附等温线;(B) 磁性脂质体对有机氯的吸附动力学曲线Fig.2 (A) Adsorption isotherms of OCPs;(B) Adsorption kinetic curves for OCPs OCPs:1.lindane(γ -HCH);2.p,p′-DDT;3.mirex.
2.4 实验条件的优化
2.4.1 磁性脂质体的用量在提取过程中,磁性脂质体分散在土壤萃取溶液中。通过改变吸附剂的用量(60~160 mg),考察其用量对回收率的影响。当磁性脂质体质量从60 mg增加到120 mg时,9种目标物的回收率均有明显提高,进一步增加吸附剂的用量对有机氯农药的回收率没有明显的提高。由于吸附剂用量越大,洗脱时间增加,洗脱溶剂用量增大。因此,选择120 mg作为吸附剂的用量。
2.4.2 萃取时间考察了萃取时间(5~35 min)对有机氯农药回收率的影响。随着萃取时间的延长,有机氯农药的回收率逐渐增加,达到25 min后,有机氯农药的回收率保持不变,即萃取平衡时间为25 min。选择萃取时间为25 min,9种目标物的回收率范围为80.1%~93.8%。
2.4.3 洗脱条件采用甲醇、乙腈、乙醇、丙酮、正己烷等一系列洗脱溶剂对洗脱步骤进行优化。由于丙酮、正己烷与水不互溶,单独使用丙酮或正己烷对有机氯农药的洗脱效果不明显。与其他有机溶剂相比,乙腈对有机氯农药的回收率最高,而且连续多次脱附后未见结转效应。随后,以乙腈为洗脱剂,考察洗脱溶剂体积(1~6 mL)对回收率的影响。当乙腈体积为3 mL时,9种有机氯农药回收率为78.4%~88.9%。继续增加乙腈体积,回收率上升幅度不明显。采用3 mL乙腈为洗脱溶剂。考察了超声时间(10~60 s)对有机氯农药回收率的影响。当超声时间从10 s增加至40 s时,有机氯农药的回收率逐渐增加。当超声时间为40 s时,有机氯农药的回收率达到最大值。实验表明,以3 mL乙腈为洗脱溶剂,分三次进行超声洗脱,每次洗脱超声时间为40 s,回收率为81.6%~90.1%。
2.5 磁性脂质体的重复使用性
将100 mg磁性脂质体吸附剂重复进行吸附-洗脱-吸附实验,重复8次,测定其吸附容量。重复利用6次以后,吸附容量虽然有所下降,但仍保持在初始吸附容量的85%左右。因此,该吸附剂具有较好的稳定性和重复利用性能。
2.6 方法验证
本方法的检出限(LOD)和定量限(LOQ)分别由信噪比的3倍信号和10倍信号所对应的浓度值得出。由表1可以看出,本方法的灵敏度高,线性范围宽。而且每种有机氯农药都呈现出了良好的线性,在测定浓度范围内,线性相关系数均大于0.99。
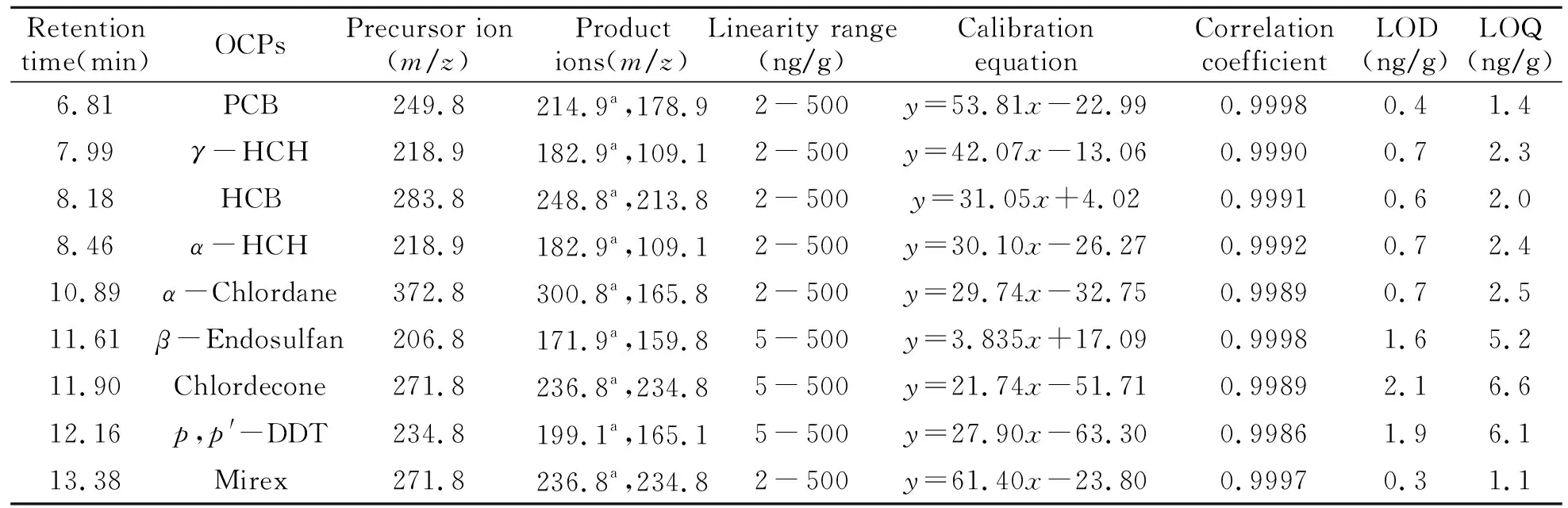
表1 方法的各分析参数
为了考察本方法的重现性,在一天之内平行测定5次3个加标浓度水平下的加标样品,得到的5次结果的相对标准偏差即为日内精密度;每天测定一次3个加标浓度水平下的加标样品,连续测定5 d,得到的5次结果的相对标准偏差即为日间精密度。九种有机氯农药的日内精密度为2.6%~4.9%,日间精密度为3.5%~7.7%。
2.7 实际样品分析
为了验证本方法的可行性及有效性,从不同的地方采集5种土壤样品进行分析。在方法的检测限范围内,在化工厂附近收集的土样中发现了五氯苯的存在,浓度为3.6 ng/g。在公路大桥附近收集的土样中发现了六氯苯的存在,浓度为8.0 ng/g。随后对5种土样分别进行加标测定,加标浓度分别为10,50,200 ng/g,五氯苯、六氯苯、α-六六六、林丹、α-氯丹、十氯酮、p,p′-DDT、β-硫丹、灭蚁灵的回收率分别为75.6%~83.7%,86.8%~93.6%,79.4%~92.9%,89.5%~99.4%,80.6%~91.7%,83.1%~91.8%,84.8%~96.0%,83.1%~90.2%和72.4%~88.0%。
3 结论
本研究制备了一种新型磁性纳米吸附剂,并成功将其应用于土壤样品中痕量有机氯农药的快速提取和富集。本方法简化了分析步骤,节约了分析成本。同时,磁性脂质体吸附剂所具有的良好的超顺磁性,使其能短时间内(<30 s)在外加磁场的作用下,从土壤基质溶液中分离出来,避免了传统方法中的过柱操作,大大的减少了分析时间。同时,该吸附剂对土壤中的大分子共萃取物具有天然的屏蔽作用,将其用于土壤样品的分离纯化,能够快速吸附有机氯农药并有效排除干扰。因此,磁性脂质体可用于实际样品中有机氯农药的分离富集,在环境样品前处理方面具有良好的应用前景。
