经皮肾镜术导致的肾盂压力变化对患者术后疼痛及住院时间的影响(附20例报告)
2020-09-11吴汉潮张雄伟
王 强,吴汉潮,张雄伟
(贺州市人民医院泌尿外科,广西 贺州 542899)
尽管经皮肾镜取石术被广泛使用并取得较好疗效,但其并发症发生率为15%以及死亡率高达0.3%[1-3]。因此,继续降低该术式有关并发症的发病率和死亡率至关重要。
经皮肾镜取石术(percutaneous nephrolithotomy,PCNL)是在整个手术过程中建立一个动态的流体通道环境并在其中进行操作。然而,正常肾脏解剖结构和生理结构的破坏导致由多个变量支配的肾盂压力(renal pelvic pressure,RPP)变化,这种组织间压力的变化可能会造成诸多不良后果,其中包括肾静脉回流异常[4]。一个重要的问题是原尿重吸收系统中的肾静脉回流液因压力变化导致异常进入全身静脉循环[5]。Abourbih等[6]认为叶间静脉逆流出现的最低压力阈值为30mmHg。高RPP是导致肾静脉逆流的重要因素,并且PCNL后发生的菌血症和发热可能至少部分是由于细菌在这一过程中被吸收所致[5,7],在最近的研究中,PCNL期间的高压灌注也与术后SIRS风险增加有关[8]。
尽管RPP与术后发热、全身炎症反应综合征(systemic inflammatory,SIRS)和尿脓毒症风险之间的关系已有研究,但有关内窥镜口径大小以及相关灌流压力对RPP影响及其与围手术期结果相关性的数据仍较少。本研究的目的是确定肾镜和输尿管软镜检查对RPP和围手术期结局的影响,包括术后疼痛和住院时间。
1 资料与方法
1.1 纳入及排除标准
纳入标准:所有患者均接受术前预防性应用静脉注射抗生素,并符合CUA(中国泌尿学协会)关于抗菌药物的治疗指南[9]。诊断为尿路感染或无症状性菌尿的患者术前均完善尿液细菌培养,并在PCNL之前根据培养结果接受常规敏感抗生素治疗,复查血尿常规正常后入组。
排除标准:①未满18岁的患者;②术前存在其他系统组织局部感染或全身感染者;③既往肾脏、输尿管、膀胱手术史者;④泌尿系畸形者;⑤身体存在异常及病变患者;⑥镇痛药物依赖人群及吸毒人群。
1.2 一般资料
经过贺州市人民医院伦理审查委员会批准后,2017年1月至2017年6月期间确定了20起PCNL病例。在所有患者术中我们通过输尿管软镜辅助前瞻性测量RPP,并排除可能存在的同侧输尿管结石。入组患者年龄范围(55.2±5.5)岁,BMI范围(32.4±3.8),男/女分布10/10,ASA麻醉评分(2.6±0.5),结石面积(596.9±4.6)mm2,鹿角结石比例70.0%。根据肾镜检查中平均RPP是否为30mmHg或更高的压力来进行比较和分层。
1.3 手术方法
PCNL中患者取半侧卧腿外展体位进行。使用输尿管软镜定向超声引导建立30Fr通路鞘。在建立通路后,将输尿管软镜的工作通道连接到校准的动脉管线压力监测器(Medical Data Electronics,Arleta,California)。输尿管软镜尖端位于肾盂输尿管连接处上方1 cm处,用于确定RPP基线值,当使用24 Fr肾镜进行灌注时不使用负压吸引抽吸,在使用14Fr输尿管软镜进行灌注时负压吸引。在护套放置后立即进行基线压力测量。灌注是通过一个标准的4L生理盐水袋在肾水平以上1.2米的标准高度上通过重力自行排出。吸引器是由Neptune2 System通过3.5mm超声波碎石机系统设定在530mmHg压力下抽吸(KarlStorz,Tuttlingen,Germany)。在任何情况下都不使用输尿管通路护套。在手术结束时,留置6Fr双J管,24Fr肾造瘘管和6Fr多用途接入导管。
术后第一天晨起所有患者均接受CT检查。患者根据疼痛需要开始口服镇痛药物(方案中未使用非甾体抗炎镇痛药物),并用静脉短效弱阿片类镇痛药物治疗突然疼痛。护理人员基于Likert量表按照规定在给药前后记录术后疼痛并给于评分[10]。关于术后第1d和第2d疼痛评分和镇痛需求的数据进行回顾性分析,并结合肾镜检查中的平均RPP分层数值进行比对。
主要研究终点是内窥镜口径和抽吸对RPP的影响。使用24Fr肾镜中,24Fr肾镜灌注与吸引和14Fr输尿管软镜灌注确定RPP从基线开始的变化。在肾镜检查中平均RPP为30mmHg或更高的患者与肾镜检查中平均RPP小于30mmHg的患者进行比较。我们确定了基线资料和围手术期特征,包括术后疼痛、麻醉要求、住院时间和SIRS发生率。
1.4 统计学方法

2 结 果
在20例接受输尿管软镜辅助PCNL的患者中共记录了220次测量结果。表1列出了患者人口统计。 所有患者都采取单通道通路操作。
在严格的经皮肾镜操作中平均RPP大于30mmHg(超过理论阈值并导致肾静脉回流7例(35.0%),而RPP低于30mmHg理论阈值的13例(65.0%)。值得注意的是,高于30mmHg理论阈值或更高的RPP仅在肾镜操作被观察到。这种高于RPP正常阈值的现象在输尿管软镜操作检查期间或在抽吸期间的肾镜操作中未被观察。肾镜操作期间的平均RPP明显高于输尿管软镜操作期间的RPP值(30.3±2.1)vs(12.9±2.7)mmHg,P=0.007,图1,封三)。与肾镜和输尿管软镜操作的患者相比,使用远端抽吸操作的肾镜检查可以导致RPP下降2.7mmHg(P<0.001)。应用肾镜,输尿管软镜和肾镜并负压吸引中操作中的RPP与基线RPP比较,结合负压吸引的肾镜操作可导致RPP发生显著变化(图2,封三)。
表1比较了在经皮肾镜操作期间通过平均RPP分层的患者之间的围手术期特征。两组之间的基线特征、偏侧性、手术时间或肾积水的程度没有显著差异。然而,经皮肾镜操作中RPP大于或等于30mmHg的患者组对比RPP小于30mmHg的患者组,前者对应的皮肤到肾盏的距离更长[(105.5±2.5)vs(79.7±2.2)mmHg,P=0.03]。各组肾镜下RPP对应的BMI值之间相比较无明显差异[(35.6±2.8)vs(30.5±2.2)kg/m2,P=0.21]。
表1也显示了2个队列的术后结果。两组患者术后静脉注射弱阿片类镇痛药的剂量要求没有差异[(10.7±1.8)vs(10.2±2.2),P=0.81]。在肾镜检查中,平均RPP为30mmHg或更高的患者与RPP小于30mmHg的患者相比较,术后平均总疼痛评分[(4.6±2.1)vs(3.0±2.5),P=0.004]和住院时间[(6.5±1.3)vs(4.7±2.1)d,P=0.04],平均RPP为30mmHg或更高的患者显著高于RPP小于30mmHg的患者。比较两组间SIRS发生率无差异(P=0.43)。
术后CT复查显示没有发现患者存在输尿管上段结石阻塞以及肾周血肿。
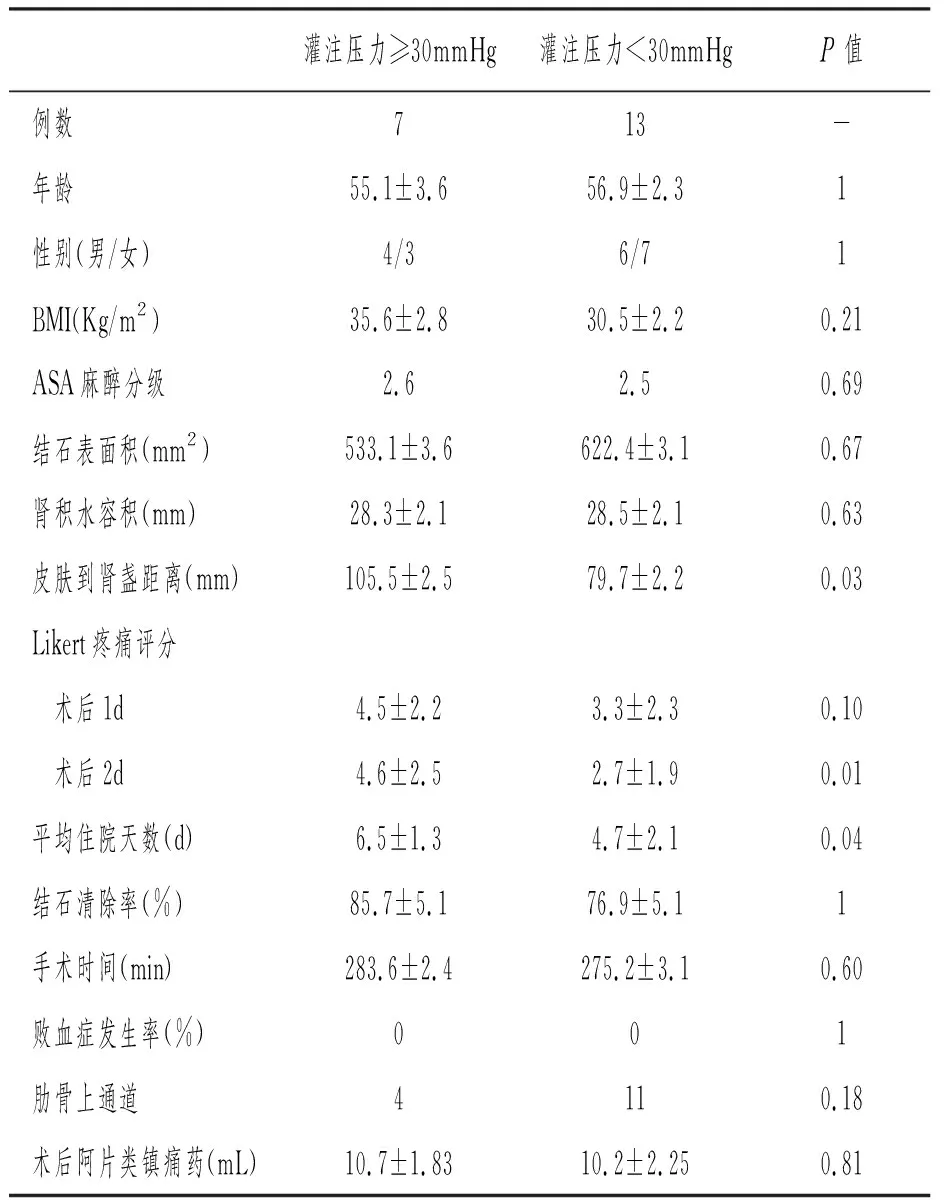
表1 灌注压在≥30mmHg与<30mmHg患者围术期特点及术后结果
3 讨 论
早在20世纪20年代,Hinman[4]首次报道了这种肾盂静脉回流现象存在于实体犬模型中。我们在接受PCNL的患者中使用临床模型,结果表明RPP在PCNL期间可以广泛变化,并且多个可预测的因素可以影响这种压力。在没有远端负压吸引的肾镜检查中,平均RPP比基线压力升高了212%。肾镜检查导致35%患者的平均RPP为30mmHg或更高,而输尿管软镜检查未导致RPP升高超过任何患者的肾静脉回流阈值。
RPP高于肾静脉回流阈值可导致一些不利影响,包括结石碎片的迁移,术后感染和液体超负荷[5,11-12]。Zhong等[11]发现在miniPCNL操作期间RPP>30mmHg与术后发热显著相关。综合过去文献的结论:任何因素导致PCNL引流不良都会引起RPP升高。在一项随机单盲试验中,Omar等[7]在PCNL期间依靠外部加压冲洗液对低压(80mmHg)和高压(200mmHg)进行了比较,他们发现高压灌溉增加了术后SIRS的风险。在另一项研究中,Berardinelli[12]在PCNL期间使用输尿管闭塞球囊导管和尿动力学系统直接测量肾内压,这些结果显示了基线和升高的压力(比30%高26% mmHg)与我们研究期间获得的相似(35%大于30mmHg)。与Omar等[7]的研究相比, Berardinelli F等的研究中没有发现RPP在30mmHg或更大时与术后发热的关联[12]。然而,他们认为RPP升高与不完全的肾镜鞘管定位和通过漏斗状狭窄的内镜检查相关,但他们没有检查与其他因素的关联。
我们也没有发现升高的RPP与术后发热或SIRS之间的任何相关性,但我们注意到与以前研究中未检查的其他因素的相关性。我们的研究表明,较长的皮肤到肾盏距离与平均RPP升高显著相关。该值可以在术前CT定位上测量,可用于术前计划中,并可能与其他因素结合以确定理想的进入位置。
在我们的研究中,这是第一项证明平均RPP升高的研究,肾镜检查与术后疼痛和住院时间较长相关。来自肾的疼痛被认为是由刺激位于肾周膜肾囊和肾盂的伤害感受器产生的。肾盂肾盏的内压增加引起的这些神经末梢的物理延伸是引发疼痛的主要原因,类似于急性输尿管梗阻[13]。这一理论将支持我们的研究结果,即由于神经末梢的伸展增加,RPP升高会导致更多的疼痛。
另一种理论是RPP到达峰值时可能导致肾脏中原尿收集系统黏膜穿孔,使尿液渗入腹膜[14]导致肠梗阻并引起强烈的化学性刺激。这也可以解释这两个队列之间住院时间显著延长和报告疼痛评分较高的原因。
相反,2个队列患者之间静脉注射弱阿片类镇痛药物的要求没有区别。我们用PCNL治疗患者的术后护理方案包括镇痛剂由护理人员根据需要施用疼痛药物,参数限制了医生设定的剂量和间隔时间。这可以解释发现组群之间静脉内弱阿片等效剂量没有差异,因为任何预期的差异将被医师放置在常规剂量参数中。也可以认为我们在术前两组患者预设的阿片类药物剂量是一样的,在相同的时间给药,按照相同的体重给药,但是两组患者的疼痛存在差异,因此,在统计学上显示出两组相似的阿片药物需要量。在这种情况下,患者报告的疼痛评分将反映术后疼痛更精确的测量值,而不是对弱阿片类镇痛药的要求。
肾盂充足压力的另一个潜在优势是增加的RPP对小静脉损伤具有填塞作用。李海昌等[15]发现肾盂充足压力与腹腔镜手术期间气腹所见的优势类似,在这些手术中使用更高的压力可以减少术区周围的静脉出血。如果在手术过程中RPP较低,在碎石术期间抽吸可能导致黏膜与碎石器接触,这将增加尿道内皮磨损、静脉损伤和出血或收集系统穿孔的风险。无论它是否被识别,细微的损伤都可能导致肾静脉回流的风险增加,并且在低于预期的压力下,腹膜后可能会泄漏尿液。
未来在PCNL期间研究理想的RPP的研究应该考虑维持可视化和减少静脉出血以及肾压低的压力升高的优势,这可以减少术后疼痛、住院时间和感染的可能性。
这项研究的局限性包括较小的样本量和我们报告单个外科医生病例的事实。虽然前瞻性收集了压力测量值,回顾性分析患者结果,但是这会影响不同范围有不同压力的结果,这对结果有潜在的重大影响。此外,本研究并未直接测量肾静脉回流,理论上讲在PCNL期间对肾盂原尿收集系统的任何伤害都会导致在较低压力下的肾静脉回流。尽管在肾脏黏膜上皮损伤之前我们收集了初始测量压力,但这并未在我们的文章中阐述。最后,虽然PCNL期间的输尿管软镜允许直接测量肾盂压力,但输尿管软镜可能会阻塞输尿管的一部分,这可能会人为地升高RPP。尽管以前的研究表明在PCNL中使用输尿管导管对RPP影响很小,这也可能导致了数据的误差。Saltzman等[16]报道了这一点,他们在PCNL期间测量了RPP,并得出结论:输尿管导管在PCNL期间不能充分减压肾脏。
综上所述,泌尿科医师应该意识到内窥镜口径和管道长度与肾盂压力的关系,以及在术前计划经皮穿刺时对术后疼痛和住院时间的潜在影响。了解影响肾盂压力的因素和控制肾盂压力的方法可能会提高PCNL患者的安全性,控制肾盂灌注压力可能会改善患者术后症状并缩短住院时间。
