酯化/球磨改性蜡质玉米淀粉及其皮克林乳液稳定与释放特性
2020-09-03安凤平王艺伟宋洪波
安凤平 万 成 何 洪 王艺伟 陈 雷 宋洪波
(福建农林大学食品科学学院1,福州 350002) (福建省特种淀粉品质科学与加工技术重点实验室2,福州 350002)
乳液分为水包油(O/W)型和油包水(W/O)型,由于组成乳液的两相互不相溶,故存在界面张力,且体系的界面能很大,属于热力学不稳定体系,因此乳液液滴间易发生聚结,通常需添加表面活性剂来稳定乳液[1]。皮克林(Pickering)乳液是在油滴表面形成一层固体颗粒层,从而稳定油和水两种互不相溶液体的乳液,这种乳液也被称为颗粒稳定乳液[2]。由于皮克林乳液不仅保留了传统乳液优良的性质,还具用量少、界面稳定性强等优势,在食品、药品、化妆品等领域具有巨大潜在应用价值[3]。淀粉因其来源广泛、可生物降解、安全可食、强界面稳定性等特点,近年来成为研究的热点[1,4]。但由于天然淀粉亲水性强,并不适合O/W型乳液[5]。淀粉经辛烯基琥珀酸酐(OSA)酯化改性后,可同时引入亲水性羧酸基团和疏水性烯基长链,因此赋予改性淀粉两亲性,可增强乳液的稳定性[6]。但多数淀粉仅依赖(OSA)酯化并不能形成稳定的皮克林乳液。
蜡质玉米淀粉是由蜡质玉米经湿磨提取得到,具有吸水性强、膨胀度高的优势[7]。因此,本研究以蜡质玉米淀粉为材料,比较研究OSA酯化改性、以及在些基础上的球磨改性淀粉对O/W乳液稳定性的影响,进而阐明酯化/球磨改性蜡质玉米淀粉稳定皮克林乳液及其释放机理,为拓展淀粉在O/W型皮克林乳液方面的应用提借鉴。
1 材料和方法
1.1 材料与主要仪器设备
蜡质玉米淀粉、大豆油、辛烯基琥珀酸酐;氢氧化钠、盐酸、无水乙醇、叠氮化钠、溴化钾:分析纯;D-葡萄糖试剂盒。
PHS-25数显pH,CJM-SY-B 型球磨机,T25高速剪切分散乳化机, MS 3000激光粒度仪,Quanta 200扫描电子显微镜,BH-2光学显微镜,Rigaku D/Max-1200 X衍射仪,VERTEX 70傅里叶红外光谱仪,UV-1780紫外可见分光光度计。
1.2 酯化玉米淀粉制备
参照Zhang等[8]的方法有所修改。称取120.0 g蜡质玉米淀粉(NS),配制成质量分数为35%淀粉乳,适时滴加5%NaOH溶液调节并维持pH至8.0,加入3%,基于淀粉干基)的OSA,于35 ℃匀速搅拌,反应4 h;用体积分数为3%HCl 溶液调节pH至6.5,5 000 r/min离心10 min,弃上清液,再用80%乙醇洗3次,水洗3次;将沉淀物置于烘箱,40 ℃干燥24 h,粉碎过100目筛,制得酯化淀粉(OSS)。按Królikowska等[9]的方法测定酯化淀粉的取代度为0.017。
1.3 酯化/球磨玉米淀粉制备
将OSS(100.0 g)与直径为10 mm的氧化锆球(1 000 g)混合,装入球磨机动腔内,以420 r/min分别处理0.5、2、3.5 h和5.0 h,过100目筛,分别命名为OS-BM0.5、OS-BM2、OS-BM3.5、OS-BM5。
1.4 皮克林乳液制备
将淀粉配制成质量分数为5%淀粉乳液,加入20%的食用大豆油,再加入0.01% NaN3,采用高速剪切分散乳化机以22 000 r/min均质1 min。将皮克林乳液转入玻璃瓶子密封,25 ℃下储存30 d。
1.5 淀粉扫描电镜观察
用导电胶将淀粉样品固定在样品台上,喷金处理后,用扫描电子显微镜以放大位数2 000×观察淀粉颗粒形貌。
1.6 淀粉X射线衍射分析
采用X-射线衍射仪进行测定,参数设置为:管压40 kV,电流40 mA,Cu靶,2θ角5°~35°,扫描速率6°/min,扫描步长0.02°。采用MDI Jade 6.0计算相对结晶度[10]。
1.7 淀粉结构表征
取1 mg淀粉样品,与100 mg KBr混合,于玛瑙研钵中研磨约5 min,压膜处理,灌注于压模中,抽真空压片,20 MPa压力下保持60 s,压至透明;傅立叶红外光谱分析仪的扫描范围为400~4 000 cm-1,分辨率0.8 cm-1,扫描累加64次。
1.8 皮克林乳液光学显微观察
取一滴乳液滴加在光学显微镜的载玻片上,盖上盖玻片,放大400×观察乳液。
1.9 皮克林乳液粒径分布
采用激光衍射法测定乳液的粒径分布,参数设置为:颗粒折射率1.460,颗粒吸收率0.001,以纯水作为分散剂,其折射率1.330,转速2 200 r/min。
1.10 荷载姜黄素皮克林乳液制备
姜黄素以1 mg/mL的比例添加到大豆油中,用高速剪切分散乳化机以22 000 r/min均质20 min。并以此替代大豆油,按1.4完成。
1.11 荷载姜黄素乳液体外模拟消化
1.11.1 体外模拟消化
模拟口腔消化:将10 mL KCl (1.2 mol/L)、10 mL KSCN(0.2 mol/L)、10 mL NaH2PO4(0.74 mol/L)、1.7 mL NaCl (1 mol/L)、20 mL NaHCO3(1 mol/L)、8 mL尿素 (0.42 mol/L) 混合均匀;再添加290 mg α-淀粉酶、15 mg尿酸、25 mg黏蛋白;将体系pH调节到6.8。4 mL模拟口腔液与4 mL乳液混合,37 ℃水浴5 min,再添加2 mL 1 mol/L HCl灭酶[11]。
模拟胃消化:2 g NaCl加到7 mL 1 mol/L HCl中,加水至1 000 mL容量瓶;用1 mol/L HCl和1 mol/L NaOH调节pH至1.2,配成模拟胃液。0.003 2 g蛋白酶溶解在1 mL 模拟胃液中,再与9 mL乳液混合,保持温度37 ℃,1 h后取样,用1 mol/L NaHCO3调节pH至6.5终止反应[12]。
模拟肠道消化: 10 mg/mL胰酶加到0.05 mol/L KH2PO4配成模拟肠液,用0.2 mol/L HCl或 0.2 mol/L NaOH调节10 mL乳液至pH=6.5。将乳液与10 mL 肠液混合37 ℃保温。取样,用冰浴10 min抑制酶反应[12]。
1.11.2 淀粉消化率
用淀粉水解度表示淀粉消化率。采用D-葡萄糖试剂盒测定样品中的葡萄糖含量。淀粉消化率按公式计算[13]:
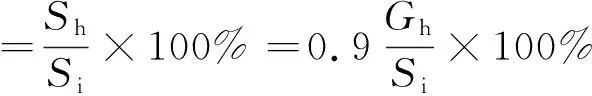
式中:Sh为水解淀粉的量/g;Si为淀粉的初始量/g;Gh为产生的葡萄糖量/g;0.9为从淀粉到葡萄糖的转换因子。
1.11.3 脂肪酸释放率
脂肪消化率为消化液中的脂肪酸含量与皮克林乳液中脂肪酸含量的百分比。脂肪酸含量的测定采用滴定法[14]。
1.11.4 姜黄素生物可给率
在脂肪水解过程中,乳液运载的活性物质会转移到由胆酸盐、脂肪酸和磷脂构成的胶束中,胶束中的活性物质容易被小肠吸收。因此,姜黄素的生物可给率可以用在体外消化过程中转化到胶束中的浓度来表示。根据Hélder等[14]的方法略有修改:将模拟肠消化2 h后的消化液样品转入离心管,以1 750 r/min、室温离心10 min。离心后,样品被分为3层,用注射器小心吸取中间层液体(胶束),采用紫外分光光度计以425 nm 测定姜黄素浓度。姜黄素生物可给率按公式计算[14]:
姜黄素生物可给率=
1.12 数据处理
采用DPS13.5统计分析软件,用Duncan 氏新复极差法进行不同处理间差异显著性分析;采用OriginPro 8.5软件绘制显著性差异标记柱状图。
2 结果与讨论
2.1 不同处理淀粉的特性比较
2.1.1 形貌特征
如图1所示,蜡质玉米原淀粉(NS)表面光滑,结构紧密,呈现球形、椭球体或不规则多面体,轮廓圆润。与NS相对,酯化淀粉(OSS)形态基本无变化。OSS经球磨处理0.5 h后(即OS-BM0.5),淀粉表面出现皱褶,且发生轻微破碎。随着球磨时间的延长,淀粉颗粒反复碰撞、摩擦、冲击、剪切,表面破碎现象加重,许多细小颗粒聚集成较大颗粒,团聚颗粒被进一步冲击破碎并聚集[15],如此反复形成大小不均的颗粒聚集体(见OS-BM2);另一方面,球磨处理还使得OSS出现了熔融现象。随着球磨时间持续延长,淀粉破碎、团聚与糊化现象不断加剧。

图1 不同淀粉的扫描电镜图(2 000×)
2.1.2 X衍射分析
由表1可知,NS在2θ约为15°等处有4个主要衍射峰,表现为典型的A型淀粉。与NS相比,OSS的衍射峰没有明显变化,这是因为酯化反应发生在无定型区,因此对淀粉结晶结构影响不大(P>0.05)。对OSA球磨0.5 h后,OS-BM0.5的衍射峰强度明显降低,结晶度显著下降(P<0.05);随着球磨时间的增加,衍射光谱显示出光滑且无特征峰,淀粉结晶度进一步显著降低(P<0.05)、但彼此之间无显著差异,说明足够的球磨处理时间,使得OSS结晶结构严重破坏,结晶区转变为无定型区,结晶完全消失[16]。
2.1.3 结构表征


图2 不同淀粉的红外光谱
2.2 不同处理淀粉的皮克林乳液特性比较
2.2.1 稳定性
稳定性实验表明,刚制备的NS乳液上面出现一层浮油,乳液主体呈浑浊状;储存30 d后,油、水和淀粉层分离清晰,表明原淀粉的乳化及稳定能力很差,这是由于天然蜡质玉米淀粉的强亲水性导致O/W乳液的不稳定[20]。OSS可以形成O/W乳液体系,是由于辛烯基琥珀酸酐的两亲性所决定的,但刚制备的皮克林乳液出现部分分层,储存30 d后部分淀粉颗粒沉积在底部,主要原因是淀粉的颗粒较大、沉降能力强[21]。酯化后经球磨处理的淀粉乳液稳定性大为改观,其中OS-BM0.5淀粉的新鲜乳液均匀,储存30 d后未析油,但出现了分层现象。OS-BM2、OS-BM3.5和OS-BM5制成的乳液储存30 d后依然均匀稳定。这表明酯化淀粉经球磨2 h以上,保证了皮克林乳液长期稳定性要求。其原因在于,除了酯化使淀粉具有对水和油的两亲性,足够的球磨处理不仅极大的减小淀粉颗粒尺寸,特别是球磨处理2 h以上,淀粉的结晶区转变为无定型区(参见表1),具有更强的膨胀和吸纳液体稳定两相界面的作用。
2.2.2 微观形貌与稳定性
由于蜡质玉米原淀粉不能形成O/W乳液,因此对比其改性淀粉的皮克林乳液微观形貌如图3所示。OSS乳液的液滴界面不清晰,油滴倾向于聚集,因此势必导致严重析油。OS-BM0.5的乳液液滴界面比较清晰,但颗粒大小差异大,出现明显的聚集与分离现象。OSS-BM2、OSS-BM3.5和OSS-BM5乳液的液滴界面清晰、大小比较均匀。

图3 不同淀粉的皮克林乳液液滴的显微图像(400×)
2.2.3 粒径分布
由于原淀粉的乳液稳定性极差,因此无法检测乳液液滴的粒径分布。如图4所示,OSS皮克林乳液液滴粒径分布图存在一个主峰和一个次峰,粒径范围为8~102 μm;OS-BM0.5乳液液滴粒径分布的主峰向左偏移、次峰减弱,粒径范围为1~30 μm;OS-BM0.5、OS-BM2和OS-BM3.5的乳液液滴粒径分布非常接近,均呈正态分布,粒径范围约为1~18 μm。

图4 不同淀粉的皮克林乳液液滴粒径分布
由表2可以看出,与OSS乳液相比,OS-BM0.5乳液液滴粒径各项指标均显著减小(P<0.05);OS-BM0.5、OS-BM2和OS-BM3.5乳液液滴粒的各项指标进一步显著减小(P<0.05),且各样品之间差异不显著(P>0.05)。
由此可见,OSS经球磨处理2~5 h,其乳液的液滴大小均匀,粒径微小。这是酯化处理增强淀粉的两亲性以及球磨处理提升淀粉乳化性和吸附性共同作用的结果。
2.3 不同淀粉荷载姜黄素乳液的消化及利用
2.3.1 淀粉消化率
由图5可知,在模拟口腔消化5 min和模拟胃消化60 min过程中,三种乳液中的淀粉消化率均接近零,这是因为模拟口腔消化液中淀粉酶浓度低、消化时间短,胃液中没有淀粉酶可消化淀粉[22]。在模拟肠道消化初期阶段,OSS、OSS-BM0.5和OSS-BM2的消化率快速增大,至120 min后三种淀粉的消化率增速都变慢;三种淀粉消化率由高至低的顺序为:OS-BM2>OS-BM0.5>OSS,至180 min时OS-BM2乳液的淀粉消化率高达89.1%,OS-BM 0.5消化率为74.34%,OSS乳液的淀粉消化率仅为35.7%,其主要原因OS-BM2结晶度很小,而淀粉结晶度越小越易消化[23]。

表2 不同淀粉的皮克林乳液液滴粒径对比

图5 不同淀粉的皮克林乳液在体外消化模型中淀粉的消化率
2.3.2 脂肪酸释放
由于皮克林乳液体系中的油脂液滴被淀粉颗粒包裹,而姜黄素溶解在油脂中,因此消化过程中脂肪酸释放特性好坏将影响姜黄素的释放和利用。由图6可知,在模拟肠道消化前20 min,三个样品中脂肪水解速度很快,之后逐渐变缓;至120 min时,OSS、OS-BM0.5和OS-BM2皮克林乳液中脂肪酸的释放量分别为53.22%、84.53%和92.34%,由此可见OS-BM2乳液中脂肪酸释放率明显高于其他2种,这是因为一方面OS-BM2最易被肠道消化(图5),使得液滴界面层上的淀粉颗粒被破坏,其中的脂肪酸得以释放;另一方面,皮克林乳液中油脂释放快慢与液滴的比表面积正相关[24],由于OS-BM2乳液液滴粒径最小,其表面积最大,因此也有利于脂肪酸的释放。

图6 三种皮克林乳液在模拟肠消化过程脂肪酸的释放率
2.3.3 姜黄素生物可给率
以皮克乳液体系运载活性物质,活性物质在模拟肠道消化过程中随着油脂释放而一同释放出来进入胶束中,其中胶束由胆盐、磷脂和游离脂肪酸所构成,最后活性物质以胶束的形式被小肠所吸收[25]。因此,采用体外模拟消化过程中转换到胶束中的活性物质百分比表示活性物质的生物可给率。
图7表明OSS、OSS-BM0.5和OSS-BM2三种皮克林乳液中姜黄素的生物可给率依次为(4.32±1.00)%、(6.48±3.32)%、(10.13±2.23)%,说明脂肪释放程度与姜黄素的生物可给率正相关。

注:不同字母表示差异显著(P<0.05)。图7 三种淀粉乳液中姜黄素生物可给率
3 结论
蜡质玉米淀粉经辛烯基琥珀酸酐酯化改性再球磨2~5 h,淀粉破碎并出现熔融现象,结晶区消失;另一方面,酯化过程中产生的酯基、羧基等新基团在球磨过程中保持稳定。与蜡质玉米淀粉、酯化淀粉相比,酯化/球磨2~5 h的淀粉制备的皮克林乳液液滴粒径小(1~18 μm)且分布均匀,油/水界面清晰,具有长期稳定性;得益于酯化改性所赋予的两亲性,以及球磨破坏结晶结构赋予改性淀粉优良的乳化性和界面吸附性。以酯化/球磨2 h的淀粉制备的荷载姜黄素乳液,淀粉的可消化性更好,释放特性佳,因此姜黄素的生物可利用度高。
