严重急性呼吸综合征冠状病毒2型 IgM/IgG、病毒核酸和白细胞介素6的联合检测在2019冠状病毒病诊断和治疗中的价值
2020-09-03薛晓婕陈美周张常亮汪宏良
薛晓婕,陈美周,张常亮,汪宏良
湖北省黄石市中心医院(湖北理工学院附属医院检验科), 肾脏疾病发生与干预湖北省重点实验室, 黄石 435001
2020年2月21日国家卫生健康委员会发布的《新型冠状病毒肺炎防控方案(试行第五版)》指出,根据流行病学和病原学检测研究发现,新出现的病毒性肺炎〔世界卫生组织正式将其命名为2019冠状病毒病(coronavirus disease 2019, COVID-19)〕由新型冠状病毒〔国际病毒分类委员会正式将其命名为严重急性呼吸综合征冠状病毒2型(severe acute respiratory syndrome coronavirus 2, SARS-CoV-2)〕引起[1-4],该病毒能发生人际传播[5-6]。国家卫生健康委员会发布的《新型冠状病毒肺炎诊疗方案(试行第七版)》[7]已明确,核酸检测是临床病原学确诊的唯一方法。
但由于病毒在人体中的多样性,不同时段的检出率不同,如何确诊核酸阴性而临床表现和影像学检查均符合诊断要求的患者?如何通过实验室相关检测指标提示疾病的转归?这些都是目前急需解决的问题。IgM是人体免疫系统最先产生的特异性抗体,提示近期有过感染,可用于早期诊断;IgG具有血中含量高、维持时间长、亲和力高等特点,当机体再次受感染时能迅速产生;白细胞介素6(interleukin 6,IL-6)是炎症感染指标。本研究拟通过对SARS-CoV-2核酸、患者血清中IgM/IgG和IL-6的联合检测来评估其在SARS-CoV-2感染的诊治和预后中的价值。
1 资料
1.1 病例纳入标准和排除标准
收集2020年1月29日—2月28日在鄂东医疗集团就诊的门诊和住院患者113例作为病例组,其中男性67例、女性46例,年龄3~87岁。病例组中93例为COVID-19确诊病例(核酸检测阳性),20例为疑似病例(核酸检测阴性但临床症状和CT检测结果均符合)。确诊病例中51例危重型,18例重型,15例轻型和9例普通型。选取来自儿科、妇科、肿瘤科、血液科和消化科等科室并排除COVID-19的患者110例作为对照组。其中男性54例、女性56例,年龄0.2~89岁。病人样本的采集时间以起病至抗体采集的时间来计算。本研究遵守国际协调理事会临床试验规范和《赫尔辛基宣言》,经医院伦理审查委员会审核通过(伦理号:WDRY2020-K30)并批准予以豁免患者知情同意。
2 方法
2.1 试剂与仪器
SARS-CoV-2 IgM和IgG抗体化学发光检测试剂盒(深圳亚辉龙生物科技股份有限公司),IL-6电化学发光检测试剂盒(瑞士Roche公司),新型冠状病毒核酸检测试剂盒(广东达安基因公司)。所用仪器:iFlash3000全自动化学发光免疫分析仪(深圳亚辉龙生物科技股份有限公司),CobasE602全自动电化学发光分析仪(瑞士Roche公司),ABI7500实时荧光定量聚合酶链反应仪(美国赛默飞公司)。
2.2 标本采集
在发病后3~48 d内采集患者空腹静脉血2~3 mL,置于无抗凝剂的红头真空采血管内,静置待血液凝固,3 000×g离心5 min,取血清备用。采集研究对象的咽拭子标本,进行SARS-CoV-2核酸检测。
2.3 血清SARS-CoV-2 IgM、IgG和IL-6的检测
血清SARS-CoV-2 IgM、IgG和IL-6检测采用化学发光和电化学发光技术,其操作步骤与结果判定均严格按试剂盒说明书要求进行。SARS-CoV-2 IgM或IgG的测试结果以相对发光强度(relative light unit,RLU)表示,检测结果10.0 AU/mL为有反应性(阳性);IL-6以检测结果7.0 Pg/mL为判读标准。
2.4 SARS-CoV-2核酸检测
采用实时荧光定量聚合酶链反应,检测 SARS-CoV-2 基因组中开放读码框(open reading frame,ORF) 1ab和核衣壳蛋白(nucleocapsid protein,N蛋白)基因片段。SARS-CoV-2核酸检测结果判读以靶标ORF1ab和靶标N蛋白同时检出为准,CT值结果<40判定为阳性,≥40判定为阴性。靶标ORF1ab和靶标N蛋白均未检出,则判定为阴性。
2.5 统计学方法
3 结果
3.1 SARS-CoV-2 IgM和IgG在COVID-19确诊病例和疑似病例中的阳性检出率较高
血清SARS-CoV-2 IgM和IgG在COVID-19疑似病例中的阳性率分别为85%和75%,在确诊病例中分别为98.9%和95.7%(其中危重型分别为100%和100%,重型分别为94.4%和100%,轻型分别为100%和93.3%,普通型分别为100%和66.7%),见表1。结果表明,SARS-CoV-2 IgM和IgG的联合检测在COVID-19患者特别是在核酸阴性的疑似临床病例中具有非常高的检出率,是核酸检测漏检的补充。

表1 SARS-CoV-2 IgM和IgG在COVID-19确诊病例和疑似病例中的阳性检出率
3.2 SARS-CoV-2 IgM和IgG在对照组的阳性检出率较低
对照组的110例患者选自儿科、妇科、肿瘤科、血液科和消化科等科室并排除了COVID-19,检测其SARS-CoV-2 IgM和IgG。结果显示,3例患者SARS-CoV-2 IgM为弱阳性,2例SARS-CoV-2 IgG阳性。出现假阳性的原因可能与肿瘤、血液科患者存在自身免疫系统疾病、受SSA-60 等抗体影响有关。
3.3 SARS-CoV-2 IgM、IgG和IL-6指标与COVID-19的病情进展有较强的相关性
113例研究对象在发病后3~48 d内监测其SARS-CoV-2 IgM、IgG和IL-6。IL-6阳性率在危重型患者中为100%、在重型患者中为97.9%、在轻型患者中为5%、在普通型患者中为0%。将结果进行比较,经χ2检验,发现COVID-19患者血清中IL-6和SARS-CoV-2 IgM/IgG水平的变化与疾病的严重程度存在一定的关联性, 差异有统计学意义(χ2=273.51,χ2=149.37;P<0.05)。结果发现,血清IL-6、SARS-CoV-2 IgM和IgG的联合检测对疾病的好转有提示作用(见表2和表3)。

表2 SARS-CoV-2 IgM/IgG和IL-6在COVID-19确诊病例和疑似病例中的检出情况
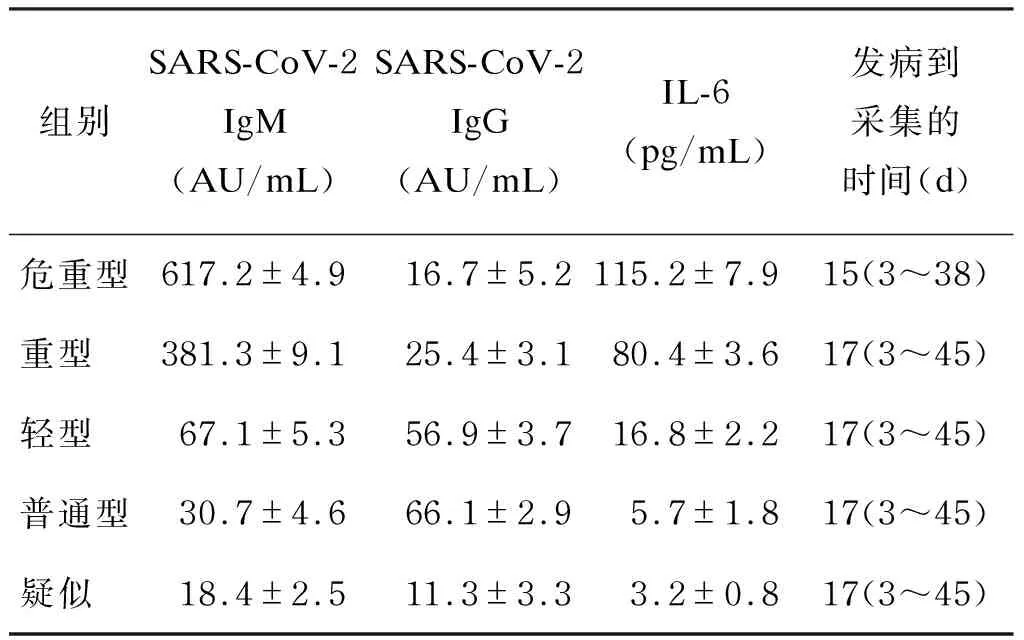
表3 血清SARS-CoV-2 IgM、IgG和IL-6表达水平在COVID-19不同临床分型中的比较
4 讨论
SARS-CoV-2是一种正链单股RNA冠状病毒,基因组与严重急性呼吸综合征冠状病毒(severe acute respiratory syndrome coronavirus, SARS-CoV)和中东呼吸综合征冠状病毒(Middle East respiratory syndrome coronavirus,MERS-CoV)不完全相同。在分类上与SARS-CoV相似, 同为β属冠状病毒B亚群(sarbecovirus亚属)[8-11]。由于SARS-CoV-2感染具有较强的隐匿性,潜伏期长,临床表现不一,根据《新型冠状病毒感染的肺炎诊疗方案(试行第七版)》规定,只有临床表现+影像学+病原学核酸检测阳性才能够确诊[7,12]。因此,如何确诊核酸检测阴性而影像学诊断阳性、临床表现符合标准的COVID-19疑似病例给我们提出了一个巨大的挑战。核酸标本检测的准确性受到样本采集与存放、病毒感染的部位、RNA的提取方法以及核酸检测试剂盒的质量问题等多方面因素的影响[13-14],而血清或血浆标本的采集和保存简单、易行,且抗体在血清标本中的稳定性很好。病毒感染存在潜伏期,一般情况下,特异性IgM在发病后5~7 d出现,特异性IgG在发病后10~15 d出现。
本研究运用SARS-CoV-2 IgM和IgG免疫检测试剂盒对血清样本进行SARS-CoV-2 IgM、IgG和IL-6的联合检测。研究发现,血清SARS-CoV-2 IgM、IgG和IL-6在疑似病例中的检出率分别为85%、75%和0%,在COVID-19确诊病例中的阳性率分别为98.9%、95.7%和75.2%(其中危重型分别为100%、100%和100%,重型分别为94.4%、100%和97.9%,轻型分别为100%、93.3%和5%,普通型分别为100%、66.7%和0%)。结果提示,SARS-CoV-2 IgM和IgG联合检测在COVID-19患者特别是在核酸阴性的疑似临床病例中具有非常高的检出率。核酸阴性但IgM和IgG阳性提示患者可能近期曾感染SARS-CoV-2并处于恢复期,体内病毒被清除,IgM尚未减低至检测下限;或提示核酸检测结果假阴性,患者处于感染活跃期。因此,血清SARS-CoV-2特异性抗体检测与病毒核酸检测可为良好互补,前者可协同核酸检测,用于辅助诊断和快速筛查,其结果与相关研究相一致[15]。但SARS-CoV-2 IgM和IgG也会出现假阳性,这可能与体内存在自身抗体、嗜异性抗体等有关:当患有某些基础疾病或免疫功能异常或长期服用某种药物时,机体可产生异常蛋白抗体或特殊物质(如类风湿因子、甲胎蛋白、补体等,均具有一定的非特异性吸附作用)。
在疾病的治疗过程中,综合分析患者的病症及其血常规、D二聚体、血气(分析氧饱和度)等指标发现,随着病情的好转,SARS-CoV-2 IgM水平降低,SARS-CoV-2 IgG水平升高,血清IL-6值降低。病情恶化时,SARS-CoV-2 IgM持续增高,IL-6值也持续增高。研究表明,IL-6和SARS-CoV-2 IgM/IgG表达水平的改变与COVID-19患者疾病的严重程度存在一定的关联性,差异有统计学意义(P<0.05)。综上所述,血清IL-6和SARS-CoV-2 IgM/IgG的联合检测既可以作为COVID-19核酸检测假阴性的有效补充,也可作为SARS-CoV-2感染诊断和治疗评价的动态指标。
