乌头碱皮肤微透析体外回收率的测定及其影响因素研究
2020-09-01郭丽蓉徐松李娜
郭丽蓉 徐松 李娜
[摘要]目的 考察乌头碱皮肤微透析体外回收率的影响因素。方法 分别采用增量法、减量法考察灌流液流速、乌头碱浓度及环境温度对微透析体外回收率的影响。结果 灌流液流速越高,微透析体外回收率越低;乌头碱浓度对微透析体外回收率的影响较小;环境温度越高,微透析体外回收率也越高。结论 乌头碱皮肤微透析体外回收率受灌流液流速及环境温度影响,与乌头碱浓度无关。
[关键词]乌头碱;液相色谱-质谱联用;微透析;回收率
[中图分类号] R651.15 [文献标识码] A [文章编号] 1674-4721(2020)7(a)-0012-05
Determination of recovery rate of Aconitine skin microdialysis in vitro and study on its influencing factors
GUO Li-rong XU Song LI Na
Yunnan Institute of Materia Medica, Yunnan Baiyao Group Innovation and R&D Center, Yunnan Province Company Key Laboratory for Traditional Chinese Medicine and Ethnic Drug of New Drug Creation, Kunming 650111, China
[Abstract] Objective To investigate experimental factors affecting recovery rate of Aconitine skin microdialysis in vitro. Methods The effect of persuate flow rate, Aconitine concentration and ambient temperature on the recovery rate of microdialysis in vitro was investigated by gain method and loss method. Results The recovery rate of microdialysis in vitro decreased with the increasing of perfusate flow rate. The Aconitine concentration has little effect on the recovery rate of microdialysis in vitro. The higher the ambient temperature, the higher the recovery rate of microdialysis in vitro. Conclusion The recovery rate of Aconitine skin microdialysis in vitro is affected by the perfusate flow rate and ambient temperature, and not affected aconitine concentration.
[Key words] Aconitine; Liquid chromatography-mass spectrometry; Microdialysis; Recovery rate
烏头碱是毛茛科乌头属植物中普遍含有的双酯型生物碱,其具有较强的镇痛活性[1],对中枢和外周疼痛都有抑制作用[2],同时也是强毒性成分[3],人口服0.2 mg即出现中毒症状[4-5]。有文献报道,乌头碱能够导致严重的心脏毒性[6-8]。乌头碱可以通过皮肤被吸收,研究表明,乌头碱经皮给药后可以提高用药安全性,并维持较长作用时间[9]。微透析技术是一种以透析原理为基础的膜取样技术,其可以对生物体进行在体、实时、在线取样,具有不影响动物体液量、减少实验动物数量、降低个体差异等特点[10],近年来已应用于生物化学、药理学、神经学、药动学等领域中[11-16]。为了建立将微透析技术应用于乌头碱的透皮药动学研究的方法,本研究对微透析体外回收率的影响因素进行考察。
1材料与方法
1.1仪器与试药
岛津LCMS8030液相色谱-质谱联用仪(liquid chromatography-mass spectrometry,LCMS)(岛津公司,Lab solution工作站);电子天平(AG135型,瑞士梅特勒公司);超声波清洗仪(KH-250B型,南京科尔仪器设备有限公司);乌头碱对照品(批号 110720-200410,中国药品生物制品检定研究院);甲酸(T8124-0500,色谱纯,ROE SCIENTIFIC INC.);乙腈(色谱纯,德国Merck公司);其他试剂为分析纯。
1.2 LCMS条件
1.2.1液相条件
Shim-pack VP-ODS色谱柱(150 mm×2.0 mm,4.6 μm,日本岛津公司,Serial No.1052247);流动相:乙腈-0.1%甲酸(60∶40);流速:0.2 ml/min;进样量:5 μl;柱温:40℃;运行时间:2.0 min。
1.2.2质谱条件
电喷雾离子源(ESI);干燥气(N2)流速:15.0 L/min;雾化气流速(N2):3.0 L/min;离子化方式:正离子模式;检测方式:MRM扫描;接口电压:4.5 kV;脱溶剂温度:250℃;热块温度:400℃;碰撞诱导解离电压35 eV。
1.3微透析试验条件
灌流液为30%乙醇林格液;流速为1 μl/min;灌流液温度为37℃。
1.4含药林格液的配制
分别取8.599 g氯化钠(NaCl)、0.144 g氯化钙(CaCl2)及0.298 g氯化钾(KCl)置于1000 ml量瓶中,加超纯水溶解定容至刻度,过0.45 μm微孔滤膜,即得林格液。林格液加入适量体积的乙醇,即得30%(V/V)乙醇林格液。
精密称取乌头碱对照品适量,加30%乙醇林格液使溶解,即得含药林格液。
1.5微透析回收率的计算方法
减量法:RL=(Cperfusate-Cdialysis)/Cperfusate×100%;增量法:RG=Cdialysis/CECF×100%。
其中,Cdialysis为微透析样品中的乌头碱浓度,Cperfusate为灌流液中乌头碱的浓度,CECF为乌头碱-30%林格液中的乌头碱浓度。
2结果
2.1 LCMS方法学考察
2.1.1线性关系考察
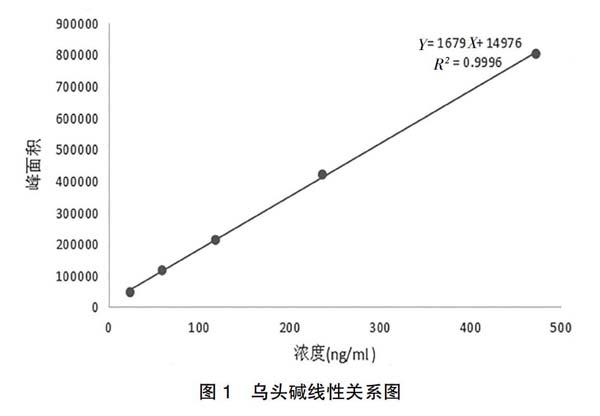
精密称取乌头碱对照品适量,置于100 ml量瓶中,加30%乙醇林格液溶解定容至刻度,得浓度为118 μg/ml的乌头碱对照品储备液。分别吸取乌头碱对照品储备液2、5、10、20及40 μl于10 ml量瓶中,加30%乙醇林格液定容至刻度,得系列乌头碱对照品溶液。取系列对照品溶液按检测条件进样,以色谱峰面积(A)为纵坐标,样品浓度(ng/ml)为横坐标进行线性回归,线性关系见图1。结果显示,乌头碱在23.6~472.0 ng/ml范围内线性关系良好。
2.1.2专属性考察
分别吸取空白灌流液(30%乙醇林格液)、乌头碱对照品储备溶液按上述色谱条件进样,记录色谱图,见图2。结果显示,方法专属性较好。
2.1.3日内精密度和日间精密度考察
取乌头碱对照品溶液,于同一天内各浓度分别进样5次,记录峰面积,计算RSD;連续3 d进样测定,记录峰面积,计算RSD。精密度考察结果见表1。结果显示,仪器日内精密度RSD为1.08%,日间精密度RSD为1.02%,方法精密度良好。
2.1.4稳定性考察
取乌头碱对照品溶液分别于0、2、8、12及24 h进样,按上述色谱条件测定峰面积,计算峰面积RSD,稳定性结果见表2。结果显示,峰面积RSD为1.29%,样品溶液在24 h内稳定。
2.2微透析体外回收率影响因素考察
2.2.1灌流液流速对微透析体外回收率的影响
2.2.1.1减量法 将皮肤微透析探针的透析膜完全浸没在空白-30%乙醇林格液中,持续搅拌,水温维持在37℃。分别以1、2、3 μl/min的流速灌注一定浓度的乌头碱-30%乙醇林格液,平衡1.5 h后,每个流速收集40 μl微透析样品。测定微透析样品中乌头碱浓度(Cdialysis)和灌注前乌头碱-30%乙醇林格液中的乌头碱浓度(Cperfusate),按减量法公式计算回收率RL。减量法灌流液流速对体外回收率的影响见图3。结果显示,随着灌流液流速的增加,微透析体外回收率逐渐下降。
2.2.1.2增量法 将皮肤微透析探针的透析膜完全浸没在含乌头碱浓度为0.1 μg/ml的乌头碱-30%乙醇林格液中,持续搅拌,水温维持在37℃。分别以1、2、3 μl/min的流速灌注空白-30%乙醇林格液,平衡1.5 h后,收集微透析样品,每个流速收集40 μl微透析样品。按测定微透析样品中乌头碱浓度(Cdialysis)和灌注前乌头碱-30%林格液中的乌头碱浓度(CECF),按增量法公式计算回收率RG。增量法灌流液流速对体外回收率的影响见图4。结果显示,随着灌流液流速的增加,微透析体外回收率逐渐下降。
2.2.1.3小结 增量法与减量法研究的灌流液流速对微透析体外回收率影响的结果一致,均显示随着灌流速度的增加,微透析体外回收率呈下降趋势。考虑到取样量及取样间隔时间,最终确定本实验研究用灌注速度为1 μl/min。
2.2.2乌头碱浓度对微透析体外回收率的影响
2.2.2.1减量法 将皮肤微透析探针的透析膜完全浸没在空白-30%乙醇林格液中,持续搅拌,水温维持在37℃。以1 μl/min的流速分别灌注乌头碱浓度为0.025、0.05、0.1 μg/ml的乌头碱-30%乙醇林格液,平衡1.5 h后,每个浓度收集40 μl微透析样品。测定微透析样品中乌头碱浓度(Cdialysis)和对应的灌注前乌头碱-30%乙醇林格液中的乌头碱浓度(Cperfusate),按减量法公式计算回收率RL。减量法灌流液中乌头碱浓度对体外回收率的影响见图5。结果显示,乌头碱浓度的变化对微透析体外回收率并无显著影响。
2.2.2.2增量法 将皮肤微透析探针的透析膜分别完全浸没在含乌头碱浓度为0.025、0.05、0.1 μg/ml的乌头碱-30%乙醇林格液中,持续搅拌,水温维持在37℃。以1 μl/min的流速分别灌注空白-30%乙醇林格液,平衡1.5 h后,每个浓度收集40 μl微透析样品。测定微透析样品中乌头碱浓度(Cdialysis)和灌注前乌头碱-30%林格液中的乌头碱浓度(CECF),按增量法公式计算回收率RG。增量法乌头碱浓度对体外回收率的影响见图6。结果显示,乌头碱浓度的变化对微透析体外回收率并无显著影响。
2.2.2.3小结 增量法与减量法研究的乌头碱浓度对微透析体外回收率影响的结果一致,均显示微透析体外回收率与乌头碱浓度无关。
2.2.3环境温度对体外回收率的影响
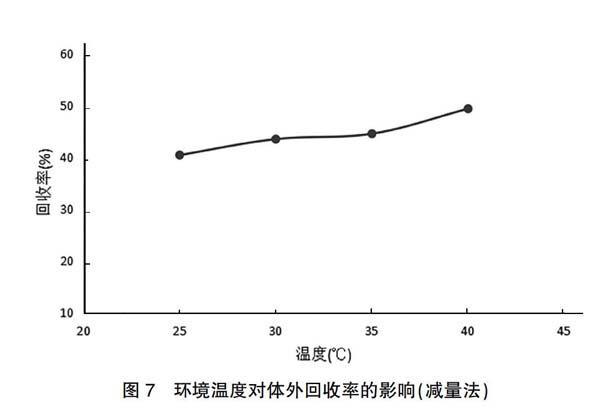
2.2.3.1减量法 将皮肤微透析探针的透析膜完全浸没在空白-30%乙醇林格液中,持续搅拌,水温分别维持在25、30、35、40℃。以1 μl/min的流速分别灌注一定浓度的乌头碱-30%乙醇林格液,平衡1.5 h后,每个温度收集40 μl微透析样品。测定微透析样品中乌头碱浓度(Cdialysis)和对应的灌注前乌头碱-30%乙醇林格液的乌头碱浓度(Cperfusate),按减量法公式计算回收率RL。减量法环境温度对体外回收率的影响见图7。结果显示,微透析体外回收率随环境温度的升高而增加。
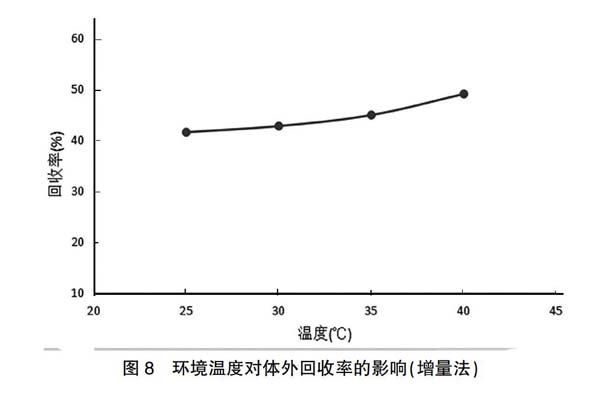
2.2.3.2增量法 将皮肤微透析探针的透析膜完全浸没在含乌头碱浓度为0.1 μg/ml的乌头碱-30%乙醇林格液中,持续搅拌,水温分别维持在25、30、35、40℃。以1 μl/min的流速灌注空白-30%乙醇林格液,平衡1.5 h后,每个温度收集40 μl微透析样品。按上述色谱条件测定透析样品中乌头碱浓度(Cdialysis)和灌注前乌头碱-30%林格液中乌头碱的浓度(CECF),按增量法公式计算回收率RG。增量法环境温度对体外回收率的影响见图8。结果显示,微透析体外回收率随着环境温度的升高而增加。
2.2.3.3小结 增量法与减量法研究的环境温度对微透析体外回收率影响的结果一致,均显示随着环境温度的增加,微透析体外回收率呈上升趋势,故在实验过程中要注意维持实验动物体温恒定。
综上所述,微透析可用于乌头碱贴剂的透皮研究,灌流液流速为1 μl/min,温度维持在37℃。
3讨论
目前常用的乌头碱测定方法有反相高效液相色谱(RP-HPLC)法、HPLC法等,但乌头碱贴剂中药物剂量较低,且由于皮肤的屏障作用,采用HPLC法不能准确测定微透析样品中的透过量,故本研究采用LCMS方法研究其透皮药动学,方法专属性较好,能准确测定其含量。
进行微透析取样时,由于灌流液处于流动状态,药物在微透析半透膜两侧的扩散不能达到绝对平衡,导致微透析样品中的药物浓度会低于体内实际的药物浓度[17]。为了获得生物体内真实的药物浓度,必须考察微透析探针对该药物的回收率,常用的方法有增量法和减量法。微透析探针的回收率作为微透析技术用于在体药浓度研究的关键,受灌流液速度、温度、待测药物性质、药物浓度的影响[18-20]。探针回收率的影响因素研究结果显示,随着温度的升高,探针回收率增加,提示在进行在体研究时要注意保持动物体温恒定。
[参考文献]
[1]安婧娴,刘芳.近年来乌头属植物二萜生物碱化学成分及其镇痛活性研究进展[J].中南药学,2016,14(5):521-525.
[2]李鸿燕,黄春英,叶朝钧,等.乌头乙醇提取物的抗炎镇痛作用[J].中国现代实用医学杂志,2006,5(6):27-29.
[3]江苏新医学院.中药大辞典[M].上海:上海可续技术出版社,1986:228.
[4]石军民.中药乌头的合理使用[J].中国当代医药,2010,12(27):92,97.
[5]许廷生,梁秀兰,卢壮.乌头类药物中毒的防治[J].河南中医杂志,2005,25(6):65.
[6]Yi M,Peng W,Chen X,et al.Effect of hypaconitine combined with liquiritin on the expression of calmodulin and connexin 43 in rat cardiac muscle in vivo[J].J Pharm Pharmacol,2012,64(11):1654-1658.
[7]周天梅,楊洁红,万海同,等.附子甘草主要成分配伍对乌头碱致大鼠传代心肌细胞损伤的保护作用[J].北京中医药大学学报,2014,37(1):22-26,75.
[8]Sun GB,Sun H,Meng XB,et al.Aconitine-induced Ca2+ overload causes arrhythmia and triggers apoptosis through p38 MAPK signaling path way in rats[J].Toxicol Appl Pharmacol,2014,279(1):8-22.
[9]孙虎,王平,龚彦胜,等.中药透皮吸收药理研究进展[J].中国现代中药,2008,10(9):7-9,32.
[10]季亚军.微透析取样技术在中药体内分析中的应用研究进展[J].实用药物与临床,2012,15(1):46-48.
[11]Darvesh AS,Carroll RT,Geldenhuys WJ,et al.In vivo brain microdialysis:advances in neuropsychopharmacology and drug discovery[J].Expert Opin Drug Dis,2011,6(2):109-127.
[12]Holmgaard R,Nielsen JB,Benfeldt E.Microdialysis sampling for investigations of bioavailability and bioequivalence of topically administered drugs:current state and future perspectives[J].Skin Pharmacol Phys,2010,23(5):225-243.
[13]Gallardo E,Madrona A,Palma-Valdés R,et al.Effect of intracerebral hydroxytyrosol and its nitroderivatives on striatal dopamine metabolism:A study by in vivo microdialysis[J].Life Sci,2015,134(8):30-35.
[14]Isaksson B,D■ouza MA,Jersenius U,et al.Continuous assessment of intrahepatic metabolism by microdialysis during and after portal triad clamping[J].J Surg Res,2011,169(2):214-219.
[15]Zhang Q,Wu D,Wu J,et al.Improved blood-brain barrier distribution:effect of borneol on the brain pharmacokinetics of kaempferol in rats by in vivo microdialysis sampling[J].J Ethnopharmacol,2015,162(5):270-277.
[16]Lu CM,Hou ML,Lin LC,et al.Development of a microdialysis system to monitor lamivudine in blood and liver for the pharmacokinetic application in herbal drug interaction and the gene expression in rats[J].J Pharm Biomed Anal,2014,96(8):231-240.
[17]张岩,何治芬,汤湛,等.氧化苦参碱体内外微透析回收率的研究[J].中华中医药杂志,2015,30(9):3108-3111.
[18]Tholance Y,Barcelos G,Quadrio I,et al.Analytical validation of microdialysis analyzer for monitoring glucose,lactate and pyruvate in cerebral microdialysates[J].Clin Chim Acta,2011,412(7-8):647-654.
[19]Stenken JA.Methods and issues in microdialysis calibration[J].Anal Chim Acta,1999,379(3):337-358.
[20]张岩,何治芬,汤湛,等.苦参碱体内外微透析回收率的研究[J].中国药学杂志,2014,49(22):2031-2035.
(收稿日期:2019-11-11)
