HPLC-MS-MS法测定克拉霉素血药浓度的含量
2016-11-21卞宝军丁礼琴金家骅
卞宝军+丁礼琴+金家骅


摘 要 建立一种用高效液相色谱-电喷雾离子化质谱(HPLC-MS-MS)联用技术测定克拉霉素血药浓度的方法。以甲醇-水(1%甲酸溶液)-乙腈(80∶10∶10)为流动相,罗红霉素甲醇溶液为内标,血浆样品经C18柱分离后,以质谱为检测器,采用选择性离子检测(SIM)测定人体血浆中克拉霉素的含量。
关键词 高效液相色谱-质谱联用 克拉霉素 血药浓度
中图分类号:R927.11; O657.63 文献标识码:A 文章编号:1006-1533(2016)21-0076-04
Determination of clarithromycin in human plasma by HPLC-MS-MS
BIAN Baojun*, DING Liqin, JIN Jiahua**(Shanghai Zhonghua Pharmaceutical Co. Ltd., Shanghai 200052, China)
ABSTRACT To establish a method for the determination of clarithromycin in human plasma by HPLC-MS-MS. The plasma samples were separated by C18 column and detected by the selective ion monitoring (SIM) with methanol-water (1% formic acid solution) -acetonitrile (80:10:10) as a mobile phase, methanol solution of roxithromycin as an internal standard and the mass spectrometer as a detector.
KEY WORDS HPLC-MS-MS; clarithromycin; plasma concentration
克拉霉素属大环内酯类抗生素,本公司产品为克拉霉素胶囊剂。为增加该品的溶出度,变更了辅料以及制备工艺,故拟进行新制剂的生物等效性评价。由于克拉霉素基本无紫外吸收,故本研究参照文献[1-5],并作适当修改后,采用高效液相-二级质谱法测定血浆中克拉霉素的浓度。我们对HPLC-MS-MS法测定克拉霉素血药浓度的方法学进行了研究,并测定了18名健康志愿者口服克拉霉素胶囊后的血药浓度,为临床用药提供依据。
1 材料与方法
1.1 仪器与试药
API 3000液相-质谱联用仪(美国ABI公司,包括:Agilent 1100 G1367A自动进样器;Agilent 1100 G1311A泵;Agilent 1100 G1316A柱温箱;API3000质谱仪及Analyst 1.4软件)。XW-80A微型旋涡混合仪(上海沪西分析仪器厂);TGL-16B台式高速离心机(上海安亭科学仪器厂);Millipore A超纯水系统。
克拉霉素标准品(每毫克相当于972单位)和内标罗红霉素标准品(每毫克相当于952单位),均由中国药品生物制品检定所提供;参比制剂为本公司生产的克拉霉素胶囊(每粒胶囊含克拉霉素250 mg),试验制剂1和2为经过变更药用辅料和生产工艺后本公司生产的克拉霉素胶囊(每粒胶囊分别含克拉霉素250 mg和125 mg);甲醇、乙腈均为色谱纯;甲酸为分析纯。
1.2 液相色谱与质谱条件
1)色谱条件 流动相:甲醇-水 (1%甲酸溶液)-乙腈(80∶10∶10);柱温:25 ℃;流速: 0.2 ml/min;进样量:2.5 μl;预柱:C18(ODS)(Phenomenex)。
2)质谱条件 扫描类型:MRM positive 选择性正离子检测;离子源:Turbo spray;电离模式:ESI;雾化气流速:8 L/min;Curtain gas:8 L/min;碰撞气流速:4 L/min;喷雾针电压:5 000 v;离子源温度:450 ℃。
1.3 克拉霉素和罗红霉素溶液的配制
精密称取克拉霉素对照品102.9 mg,用甲醇溶解并稀释成1 mg/ml 的溶液,再经系列稀释制备成0.2、 1、2、10、20和50 μg/ml 的克拉霉素对照溶液。所有溶液均在4 ℃条件下避光保存。
精密称取罗红霉素对照品10.5 mg,用甲醇溶解并稀释成含罗红霉素0.5 μg/ml的内标溶液。
1.4 血样预处理
精密吸取受试者血浆0.3 ml ,置于1.5 ml 离心管内,加入0.9 ml 蛋白沉淀剂,旋涡振荡2 min后,16 000 r/min离心10 min,取上清液2.5 μl进样分析。
1.5 方法学
1.5.1 标准曲线制备
取健康人空白血浆若干份,分别加入克拉霉素对照溶液,使其浓度分别为 10、50、100、500、1 000和2 500 ng/ml ,按“血样预处理”项下处理后进行HPLC-MS-MS分析。
以药物与内标峰面积比值(Y)对药物浓度(C,ng/ml),用线性回归方法拟合标准曲线(加权系数为1/C2),得回归方程为Y=0.006 695 C+ 0.006 649(r=0.998 5,n=6),线性范围为10~2 500 ng/ml,最低检测限为 5 ng/ml(S/N >10)。
1.5.2 质控点血样处理
按血样预处理方法操作,分别配制含10、500和2 500 ng/ml的克拉霉素标准血样,每一浓度配制3份,按血样预处理方法处理后进行HPLC-MS-MS分析,作为质量控制。质控样品测定结果的偏差应小于15%,低浓度偏差应小于20%。
1.5.3 绝对回收率
用流动相配制10 、100、2 500 ng/ml 的克拉霉素标准溶液,按血样预处理方法处理后进行HPLC-MS-MS分析,分别求得克拉霉素的峰面积(A1);按照1.5.2方法配制含血样的上述浓度的克拉霉素标准溶液作HPLCMS-MS分析,分别求得克拉霉素的峰面积(A2)。将A2/A1即为绝对回收率。
配制上述浓度的克拉霉素标准血样各5管,按血样预处理方法处理后的样品进行HPLC-MS-MS分析,计算测定数据的相对标准差,即为批内精密度。以后连续5 d,每天测定一个批次内的上述各浓度样品,计算批间精密度。
1.5.4 样品稳定性考察
将上述克拉霉素标准血样,放置在-20 ℃的冰箱中,分别于第0天和第40天取样分析,考察其长期存放的稳定性。将放置在-20 ℃冰箱中的克拉霉素标准血样,反复冻融3次后测定其浓度,考察其冻融稳定性。将上述经血样预处理后的克拉霉素标准血样即时或在室温放置24 h后取样进行HPLC-MS-MS分析,记录峰面积比值,考察样品在预处理后的稳定性。
2 结果
2.1 绝对回收率
绝对回收率的结果见表1。
2.2 批内、批间精密度
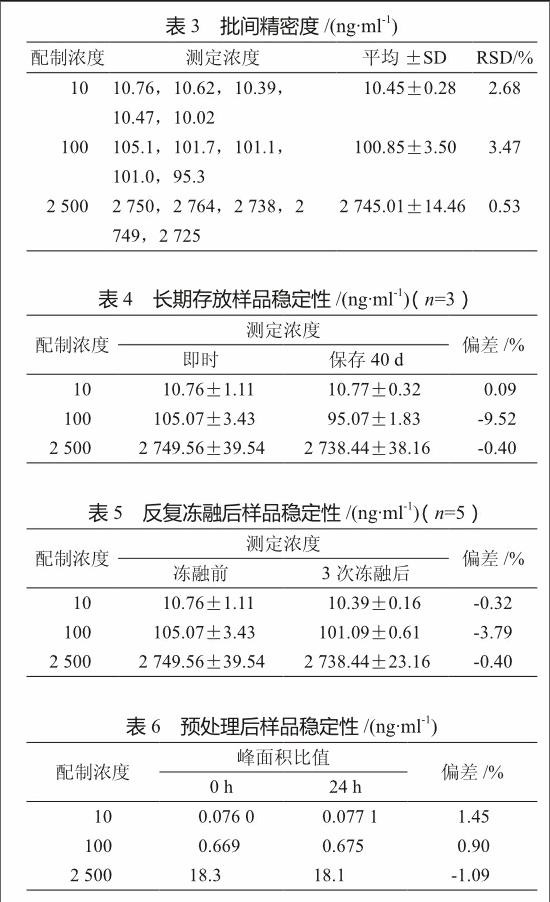
批内、批间精密度的结果见表2、3。
2.3 样品稳定性
本研究配制的样品在-20 ℃的冰箱中至少能保存40 d仍稳定(表4),反复冻融3次及在室温保存24 h后血药浓度无明显变化(表5、6)。
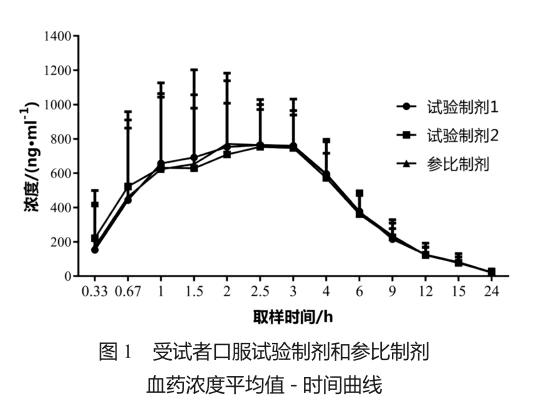
2.4 试验制剂和参比制剂血药浓度平均值—时间曲线
18名男性健康受试者随机分成3组,采用三制剂三周期二重3×3拉丁方交叉试验设计[6]的给药方案,分别单剂量口服试验制剂或参比制剂250 mg,在一定时间点抽取静脉血,采用HPLC-MS-MS测定克拉霉素的血药浓度,结果表明试验制剂1和2与参比制剂生物等效[7](图1)。
3 讨论
测定正常人体内克拉霉素的血药浓度通常多采用微生物法[8-9],该方法测定的并非克拉霉素单一组分,而是所有具有抗菌活性的多组分复合物;亦有采用HPLC-UV方法[10-11],紫外最大吸收波长约为210 nm,在此波长下血浆中内源性杂质干扰较多,其测定结果不够精确。目前国内有关克拉霉素HPLC法血样处理方法,都采用有机溶剂如苯、乙醚、乙酸乙酯等液-液萃取,亦有采用小柱活化[12-13],双蒸水洗脱,甲醇过柱,过程繁琐、复杂,而且样品受杂峰干扰大,最终影响到样品检定的精密度和准确度。本研究建立了测定人血浆中克拉霉素的HPLC-MS-MS检测方法,该方法预处理简单、快速,专属性强且灵敏、准确,最低检测限度为5 ng/ml,应用此方法测定样品均能得到很好的结果,尤其适合于几乎没有紫外吸收的药物克拉霉素的血药浓度测定,能够满足人体药代动力学研究需要。
参考文献
[1] 张春宝, 何世学, 何芳, 等. HPLC-MS/MS测定人体血浆中克拉霉素浓度的方法及方法学确证[J]. 河北医药, 2010, 32(16): 2170-2172.
[2] 石俊强, 程晓华, 李建美, 等. HPLC-MS法测定克拉霉素浓度[J]. 济宁医学院学报, 2009, 32(4): 287-288.
[3] 田开珍, 王峰, 李焕德, 等. HPLC-MS法测定人血浆中克拉霉素[J]. 中南药学, 2007, 5(2): 111-113.
[4] 吴筱丹, 楼健, 等. HPLC-MS法测定人血浆中克拉霉素含量的方法学研究[J]. 药物分析杂志, 2005, 25(12): 1433-1435.
[5] 张向荣, 陈笑燕, 李小燕, 等. LC-MS-MS法测定人血浆中克拉霉素含量及其在药物动力学中的应用[J]. 中国药学(英文版), 2004, 13(3): 166-170.
[6] 刘玉秀, 姚晨, 陈峰, 等. 多交叉设计生物利用度试验的等效性分析[J]. 中国临床药理学杂志, 2002, 18(3): 219-223.
[7] 云筠筠, 程泽能, 郭歆, 等. HPLC-MS/MS法测定克拉霉素血药浓度及国产克拉霉素片相对生物利用度研究[J]. 中南药学, 2010, 8(8): 585-588.
[8] 邓树海, 黄桂华, 张娜, 等. 克拉霉素颗粒剂和片剂的正常人体药物动力学和生物等效性[J]. 沈阳药科大学学报,2000, 17(2): 93-96.
[9] 乔海宁, 张莉蓉, 张启堂, 等. 克拉霉素分散片在健康人体内的相对生物利用度[J]. 河南医科大学学报, 2000, 35(4): 326-328.
[10] 李焕德, 张毕奎, 阎小华, 等. 克拉霉素片人体药动学及相对生物利用度研究[J]. 中国药学杂志, 1998, 33(7): 418-421.
[11] 赵静, 蒋哗, 李瑁沫, 等. RP-HPLC测定人血浆中克拉霉素的浓度[J]. 华西药学杂志, 2007, 22(2): 189-190.
[12] 王立新, 张文霞. 高效液相色谱法测定克拉霉素血药浓度[J]. 天津药学杂志, 2005, 17(5): 23-24.
[13] 张红, 李华, 李艳艳, 等. 克拉霉素血药浓度HPLC测定方法和生物等效性研究[J]. 中国临床药理药学与治疗学, 2004, 9(7): 792-794.