川芎嗪BCA-PLGA纳米粒的制备工艺研究
2020-08-31李冬静李欣宇封国溧王志翀张文君
李冬静,李欣宇,杨 阳,封国溧,王志翀,张文君
(哈尔滨商业大学 药学院,哈尔滨 150076)
川芎嗪(tetramethylpyrazine, TMP)是一种来源于川芎中的有效活性单体成分生物碱,对脑血管疾病有多种保护和治疗作用[1],在脑中风疾病中应用甚广[2].目前市售剂型主要有片剂、胶囊剂和注射剂,其中注射给药临床上使用最多[3-4].川芎嗪具有一定脂溶性,可透过血脑屏障,但其水溶性差,口服制剂在体内难以吸收,导致生物利用度低,为达到治疗浓度,须频繁给药易致蓄积川芎嗪浓度超过治疗窗甚至中毒,这一问题极大地限制了其开发应用.
聚乳酸-羟基乙酸共聚物(PLGA)作为一类具有良好生物降解性和生物相容性的纳米载体材料,该材料进入人体后降解为人体内存在的乳酸和羟基乙酸,对人体无害已广泛应用于载药纳米粒的制备[5-6].
聚氰基丙烯酸正丁酯(polybutylcyanoacrylate, BCA)由于其生物相容性好、可降解性、释药持续性并有良好的控制释放、靶向投递等功能而备受重视[7-9].目前BCA作为载体将药物送入脑内,取得明显效果,是目前药物传输系统研究中的热点.因此,本实验以BCA-PLGA为载体,采用改良的乳化溶剂挥发法[10-11]和界面缩聚法[12-13]制备BCA-PLGA双包载川芎嗪纳米粒[14-15],采用单因素试验考察处方及因素,正交优化确定制备工艺,以期制备包封率、载药量高的BCA-PLGA纳米粒,为研究川芎嗪纳米给药系统研究提供参考.
1 仪器和试药
1.1 仪器
紫外分光光度仪(UV-2021 PC型紫外可见分光光度计);激光粒径测定仪(马尔文NanoZS 90,英国);LE204E/02电子天平(梅特勒-托利多仪器上海有限公司);79-2型双向磁力搅拌器(江苏省金坛市荣华仪器制造有限公司);旋转蒸发仪(上海申胜生物技术有限公司).
1.2 药品
川芎嗪对照品(中国药品生物制品检定所);川芎嗪(上海源叶生物科技有限公司);聚氰基丙烯酸正丁酯(α-BCA,国药集团);PLGA(50/50,相对分子质量20 000,济南岱罡生物工程有限公司);聚乙烯醇(上海美梦佳化工科技有限公司);甲醇(分析纯,西陇科学股份有限公司);氢氧化钠(分析纯,天津市天力化学试剂有限公司);盐酸(天津市协和昊鹏色谱科技公司)
2 实验方法与结果
2.1 TMP-BCA-PLGA纳米粒的制备工艺
TMP纳米粒的制备采用改良的自乳化溶剂挥发法结合界面缩聚法.取处方量的TMP、PLGA和BCA,精密称量,溶于3 mL丙酮的有机相中,配制质量分数2 % PVA(pH为5)的水溶液40 mL,作为水相.有机相缓慢加入水相中,常温800 r·min-1磁力搅拌2 h,0.1 mol·L-1NaOH调pH为7,除净有机溶剂,0.45 μm微孔滤膜过滤,即得TMP-BCA-PLGA纳米粒.
2.2 TMP-BCA-PLGA纳米粒的包封率测定
2.2.1 紫外分光光度法
精密称取5 mg TMP对照品于10 mL容量瓶,用甲醇溶解并定容至刻度,质量浓度为0.5 mg/mL的储备液,从中吸取0.05、0.1、0.2、0.3、0.4 mL用甲醇稀释并定容至刻度,配制成2.5、5、10、15、20 μg/mL一系列质量浓度的对照液,在波长295 nm条件下测定吸光度,以质量浓度(C)为横坐标,吸光度(A)为纵坐标,绘制标准曲线,结果显示川芎嗪在2.5~20 μg范围内成呈良好的线性关系,得回归方程为A=0.041 6C-0.008 5(r2=1).
2.2.2 TMP-BCA-PLGA纳米粒的包封率测定
精密量取TMP-BCA-PLGA纳米粒混悬液1 mL放置超滤离心管中,16 000 r·min-1离心30 min,精密量取外管液200 μL,于10 mL容量瓶中,用酸水稀释至刻度,按2.2.1项下方法测定游离的TMP的含量;精密量取TMP-BCA-PLGA纳米粒混悬液200 μL放置10 mL容量瓶中,用甲醇破乳后稀释至刻度,按2.2.1项下方法测定TMP-BCA-PLGA纳米粒中TMP的总含量,计算纳米粒中TMP的包封率.
2.3 TMP-BCA-PLGA纳米粒的粒径、Zata电位测定
取TMP-BCA-PLGA纳米粒混悬液,用纯化水稀释后,25 ℃放置激光粒径测定仪中,测定其粒径分布及Zeta电位值.
2.4 TMP-BCA-PLGA纳米粒的处方筛选
2.4.1 水相pH的确定
配制pH 1~7的水溶液,其他组分的处方量不变,平行制备TMP-BCA-PLGA纳米粒.按2.2.2项下测定包封率,按2.3项下测定粒径.结果见表1.

表1 水相pH对纳米粒粒径和包封率的影响(n=3)
由表1可知,pH对纳米粒粒径和包封率影响较大,pH为6时粒径最小,在pH 1~5范围内包封率随pH的增加而增大,分析原因可能是TMP为生物碱,在pH低的溶液中由于酸性太大,药物可能还没被聚合物包裹就有一部分被酸溶解而成盐,导致包封率降低.pH 6包封率较低,pH 7包封率小幅增加,综合粒径及包封率结果确定pH为5.
2.4.2 PVA型号及质量分数的确定
医药的PVA 有PVA05-88,PVA17-88,PVA-124等规格,考虑到PVA-124的聚合度较大,因此主要对PVA05-88,PVA17-88的型号进行筛选.固定pH为5,分别配制不同质量分数PVA 的溶液为水相,保持处方中其他组分的量不变,平行制备TMP-BCA-PLGA纳米粒.按2.2.2项测定包封率,按2.3项测定粒径.结果见表2.

表2 PVA型号及质量分数对纳米粒粒径和包封率的影响
由表2可知,同一质量分数不同型号的PVA,17-88的粒径比05-88的大,但包封率比05-88的高很多,因此确定型号为17-88,不同质量分数的PVA(17-88)溶液,随PVA质量分数的增加,粒径变化不是很大,包封率呈上升趋势,但在PVA质量分数为3%时,在液下注入时针孔附近聚集成球,分析原因可能是PVA质量分数较大,黏度增加,导致有机相进入水相速度减慢,不易扩散,从而聚集成球,综合粒径和包封率结果确定PVA质量分数为1%.
2.4.3 PLGA质量分数的确定
PVA(17-88)质量分数为1%,体系中pH为5,筛选PLGA(50/50, 相对分子质量20 000)质量分数为1%、2%和3%,保持其他组分的处方量不变,平行制备三份TMP-BCA-PLGA纳米粒混悬液.按2.2.2项测定包封率,按2.3项测定粒径.结果见表3.
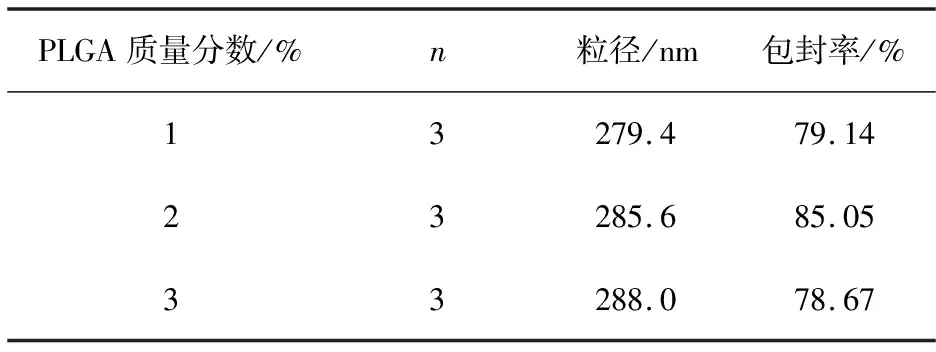
表3 PLGA质量分数对纳米粒粒径和包封率的影响(n=3)
由表3可知,PLGA质量分数对纳米粒粒径影响不大,随PLGA质量分数的增加,包封率增大.分析原因可能是随着聚合物浓度升高,有机相的黏度增加,阻碍了TMP分散到纳米液滴中,导致包封率降低粒径变大,综合表3结果确定PLGA质量分数为2%.
2.4.4 BCA质量分数的确定
PVA(17-88)质量分数为1%,体系中pH为5,PLGA(50/50, 相对分子质量20 000)质量分数为2%,保持其他组分的处方量不变,筛选不同质量分数的BCA丙酮溶液,平行制备三份TMP-BCA-PLGA纳米粒混悬液.按2.2.2项测定包封率,按2.3项测定粒径.结果见表4.

表4 BCA质量分数对纳米粒粒径和包封率的影响
由表4可知,随着BCA质量分数的增加,粒径也随之增大,原因可能为质量分数增加单位体积与水中OH-聚合加快,同时不易扩散,附近的纳米粒由于聚集而使粒径增加所致,但包封率相差不大,综合粒径和包封率结果确定BCA质量分数为0.75%.
2.4.5 PLGA、BCA有机相加入体积比
固定pH为5,PVA型号为17-88,PVA质量分数为1%,PLGA质量分数为质量分数2%,质量分数0.75%的BCA丙酮液,保持处方中其他组分的量不变,平行制备TMP-BCA-PLGA纳米粒.按2.2.2项测定包封率,按2.3项测定粒径.结果见表5.
由表5可知,PLGA、BCA有机相加入体积比对包封率影响不是很大,但随着BCA加入体积的增加,粒径变大,分析原因可能为BCA与水中OH-发生聚合,药物被包封后,多余的BCA也发生聚合,进一步包裹纳米粒从而使粒径增加,综合考虑确定PLGA、BCA有机相加入体积比为1∶1.

表5 PLGA、BCA有机相加入体积比对纳米粒粒径和包封率的影响
2.4.6 有机相和水相体积比
固定pH为5,PVA(17-88)、PLGA、BCA丙酮液质量分数分别为1%、2%、0.75%,VPLGA∶VBCA比例为1∶1,保持处方中其他组分的量不变,平行制备TMP-BCA-PLGA纳米粒.按2.2.2项测定包封率,按2.3项测定粒径.结果见表6.

表6 有机相和水相体积比对纳米粒粒径和包封率的影响
由表6可知,有机相和水相比例对纳米粒粒径影响不大,但随着有机相和水相比例的增加,包封率逐渐增大,分析原因可能是水相比例增加,在注射器液下注入时,相同体积的有机相与水相接触面积增大,载体与水相发生聚合几率增大,同时水相液面高度适宜,这样有机相可以很好的扩散到水相以减小有机相进入水相,由于空间不足造成粒径变大的影响.而降低两相比例能显著增加纳米粒包封率,减少突释.综合以上因素确定有机相和水相的比例为1∶40.
2.5 处方的确定
根据2.4处方筛选结果表明最优处方:有机相和水相体积比为1∶40,PVA(17-88)质量分数为1%,体系中pH为5,PLGA(50/50, 相对分子质量20 000)质量分数为2%,BCA质量分数为0.75%,PLGA、BCA有机相加入体积比为1∶1.
2.6 优化处方纳米粒的表征
2.6.1 TMP-BCA-PLGA纳米粒的包封率
按照2.2.2 项下测定按照优化处方制备的3 批纳米粒的包封率,结果见表7.

表7 不同批次川芎嗪纳米粒包封率
2.6.2 TMP-BCA-PLGA纳米粒的粒径、Zata电位
取TMP-BCA-PLGA纳米粒,用纯化水稀释,25 ℃下用激光粒径测定仪,测定其粒径分布及Zeta电位值,见图1.TMP-BCA-PLGA纳米粒平均粒径为234.9 nm.
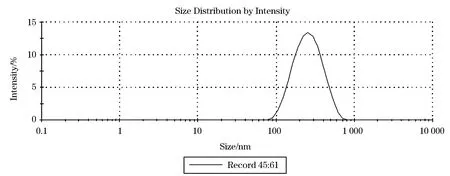
图1 川芎嗪纳米粒粒径图
3 讨 论
1)近年来,传统的药物剂型已不能满足人们的需求[6].本文采用改良的乳化溶剂挥发法和界面缩聚法制备TMP-BCA-PLGA纳米粒,PLGA作为药物载体材料优势为生物可降解相容性,而BCA也具有此性质、同时还具备释药持续性、低毒的特点,作载体能显著提高药物的生物利用度,并有良好的控制释放、靶向投递等功能.若单用BCA,由于BCA是在酸性条件下发生聚合,TMP为生物碱会造成其在酸性水相中溶解成盐而使药物的包封率降低,和PLGA合用主要考虑到其水相使用PVA溶液,黏度较大,可以减慢药物进入水相的速度,从而使TMP被PLGA包裹,之后再用BCA进行聚合,可以避免药物被酸性环境溶解,单用PLGA可能达不到药物靶向的作用,这样二者合用不仅可以减少药物在酸性水相中溶解同时可以发挥PBCA在靶向投递方面的作用.
2)川芎嗪为生物碱,pH对其影响因素较大,同时使用BCA及PLGA载体,BCA载体对pH也有一定的要求,主要与水中的OH-发生聚合进而包裹药物,若水相的pH过低,H+含量高,BCA的聚合太慢,会导致川芎嗪还没被包裹就被过高的酸性环境所溶解成盐,同时还不易形成纳米粒,pH过高,OH-浓度大,反应聚合太快,纳米粒容易聚集成球,PLGA在强酸强碱环境中容易降解,因此综合以上因素确定pH为5,既符合酸性条件BCA可以聚合,反应不至于太剧烈,又不会使PLGA在强酸性环境下而降解.
3)本文主要对处方进行筛选,但对PLGA的型号没有筛选,因有研究报道PLGA 50/50在体内降解较快,包封率较高[15].对反应时间、反应温度及转速以及PLGA与BCA加入时间进行考虑,后期会进一步研究.
