人源多能干细胞诱导GABA 能神经元移植缓解神经病理性疼痛
2020-08-25ManionJ,李雪莲
1.背景
慢性疼痛给全球越来越多的病人造成了巨大负担,其中神经病理性疼痛是由周围或中枢神经系统病变引起的一种严重的疼痛亚型,通常导致冷感和痛觉超敏(对非伤害性刺激的疼痛反应)。现有治疗方法可能有严重的不良反应,且长期服用镇痛药会导致耐受、成瘾和镇静,因此,研究全新、安全、持久的疼痛疗法至关重要。
研究表明神经病理性疼痛的核心病理改变是中枢抑制的减弱,包括脊髓GABA 合成的减少和抑制性突触后电位的降低,鞘内注射GABA 或GABA激动剂,如巴氯芬或麝香酚,可以缓解啮齿动物和人类病人的神经病理性疼痛。
目前,临床获批的方法均非对因治疗神经病理性疼痛。抑制性神经递质能在脊髓水平控制疼痛,增加脊髓水平GABA 可以缓解疼痛,基于以上理论,增强脊髓抑制很可能是治疗神经病理性疼痛的有效方法。已有研究人员使用胎儿祖细胞和永生化细胞系来缓解慢性疼痛,然而由于多能性、胎儿来源不适用于临床。
选择性神经损伤(SNI)可建立神经病理性疼痛的动物模型,本文作者将iGABA 能神经元移植到模型小鼠的脊髓背角,减轻了SNI 引起的疼痛;同时发现移植的iGABA 能神经元能够成功存活,且单次移植可长期缓解疼痛(长达两个月),这反映了移植措施可用于缓解已形成的神经病理性疼痛,有望建立一种安全有效的方案以填补临床空缺。
2. 方法
(1)研究设计:先验假设:GABA 能中间神经元移植可以减轻神经病理性疼痛。实验方法包括小鼠基础行为评估、建立SNI 模型、将iGABA 能神经元移植入脊髓。涉及动物实验均采用盲法。
(2)实验动物:所有动物实验符合澳大利亚国家健康和医学研究委员会动物使用规范。实验所用NOD prkdSCID 小鼠由华盛顿州动物资源中心提供,详见补充材料 (http://links.lww.com/Pain/A897)。
(3)细胞系:采用ATCC-BXS0116 人源多能干细胞诱导 (HiPSC) 细胞系 (ATCC, ACS1030)。
(4)细胞分化、行为学评估、手术、流式细胞术、免疫荧光、蛋白质组学、RNA 测序、钙成像、蛋白质印记、酶联免疫吸附。
3. 结果
为增强小鼠脊髓抑制,本文作者首先根据现有方案诱导人源多能干细胞获得GABA 能神经元。培养28 天后,成功观察到GAD65/67+(GABA 合成的标志物)、TUBB3+(神经元特异性标志物)说明神经元在体外成功分化(见图1A)。流式细胞术测得神经元纯度为95%。运用RNA 测序鉴定神经元的分子特征,并与来自同一供体诱导获得的感觉神经元(iSensory 神经元)进行比较,以确定GABA 能神经元的特异性。已分化的GABA 能神经元表达了与GABA 合成、包装和释放相关的转录本,以及GABA 能神经元发育的标志物。本领域中,已有学者使用了增殖的祖细胞进行研究,但这种细胞有致癌风险,而本研究中,通过转录组学和蛋白质组学分析检测增殖标志物和多能性标志物,发现Ki67 表达大幅下降;通过蛋白质组学未能观察到细胞周期蛋白1;通过RNA 测序发现核心多潜能基因大幅下降;同时荧光显微镜检查证实,Ki67+细胞数量明显减少(见图1B)。最后,还检测了GABA 合成标志物(GAD65 阳性)、甘氨酸能神经元标记物(GlyT2 阳性)、重要合成产物(见图1C)、以及释放GABA 所需的GABA 转运蛋白(囊泡型GABA/甘氨酸转运体[VGAT]),见图1D。
通过ELISA 检测证实了iGABA 能神经元可以分泌GABA 蛋白(见图2A)。钙成像测试了神经元对谷氨酸的反应性,观察到强烈的钙瞬变(见图2B)。

图1 人源多能干细胞诱导GABA 能神经元
为了评估iGABA 能神经元缓解神经病理性疼痛的效能,本研究将iGABA 能神经元移植到NODscid 小鼠(为避免异种移植排斥反应)的腰髓背角中。该过程包括以下步骤:建立SNI 模型1 周后,将iGABA 能神经元移植到小鼠体内;6 天内通过von Frey 和丙酮测试评估小鼠痛觉和冷觉阈值;从移植后2 周开始,观察到持续长达2 个月的有效镇痛(研究终点),表现为痛觉敏度降低和冷刺激反应曲线的改变(见图3A)。另外,由于GABA 能神经元也参与了运动神经回路,进行了旷场实验和步态分析,证明移植对运动行为没有产生重大影响。GABA 能神经元植入位置和自主神经系统在解剖学上比较接近,使得植入腰髓背角的GABA 能神经元可能会影响自主神经系统,但本实验中未观察到小鼠膀胱和大便存在任何问题。最后,将hiPSC 衍生的感觉神经元(iSensory 神经元)移植到小鼠腰髓背角,观察到不能产生镇痛作用,由此证明了该移植方案的特异性(见图3B)。总之,在外周神经损伤的神经病理性疼痛模型中,利用成熟iGABA 能神经元移植来增强中枢抑制作用,可起到长期镇痛作用。
为了评估神经元植入脊髓的潜力,本研究评估了细胞的存活、整合和突触融合的能力。移植3周后,在背角层I (CGRP1) 和II (IB41) 以及其他层中观察到了iGABA 能神经元放射状迁移。最初,iGABA 能神经元未迁移至腹侧和对侧脊髓,然而,在10 周后观察到大量iGABA 能神经元迁移,检测到了移植细胞与NCAM1、MAP2、TUBB3 的共表达,以及提示终末分化的NeuN,可以判断移植细胞保留了神经元特征。 iGABA 能神经元对GABA 具有免疫反应性,并保留了VGAT、GAD65/67、突触蛋白表达功能,表明移植的iGABA神经元保留了合成、包裹和释放GABA 的能力(见图4A-C)。此外,还发现小鼠突触前密度蛋白(以小鼠Bassoon 特异性抗体为标记物,与突触前蛋白RIM2 共定位)与iGABA 能神经元(以人特异性细胞质抗体HuCytoplasma 为标记物)直接相连,提示移植神经元和受体组织之间可能形成突触(见图4D)。 最后,观察到了抑制性突触后标记物Gephyrin(桥蛋白)与突触素结合,表明存在抑制性突触(见图4E,F)。实验中未观察到畸胎瘤或其他相关异常形态学现象,也没有证据表明iGABA 能神经元正在增殖(没有表达活跃的细胞周期蛋白Ki67),这表明本研究的治疗方案是安全的。

图2 iGABA 能神经元在体外具有功能
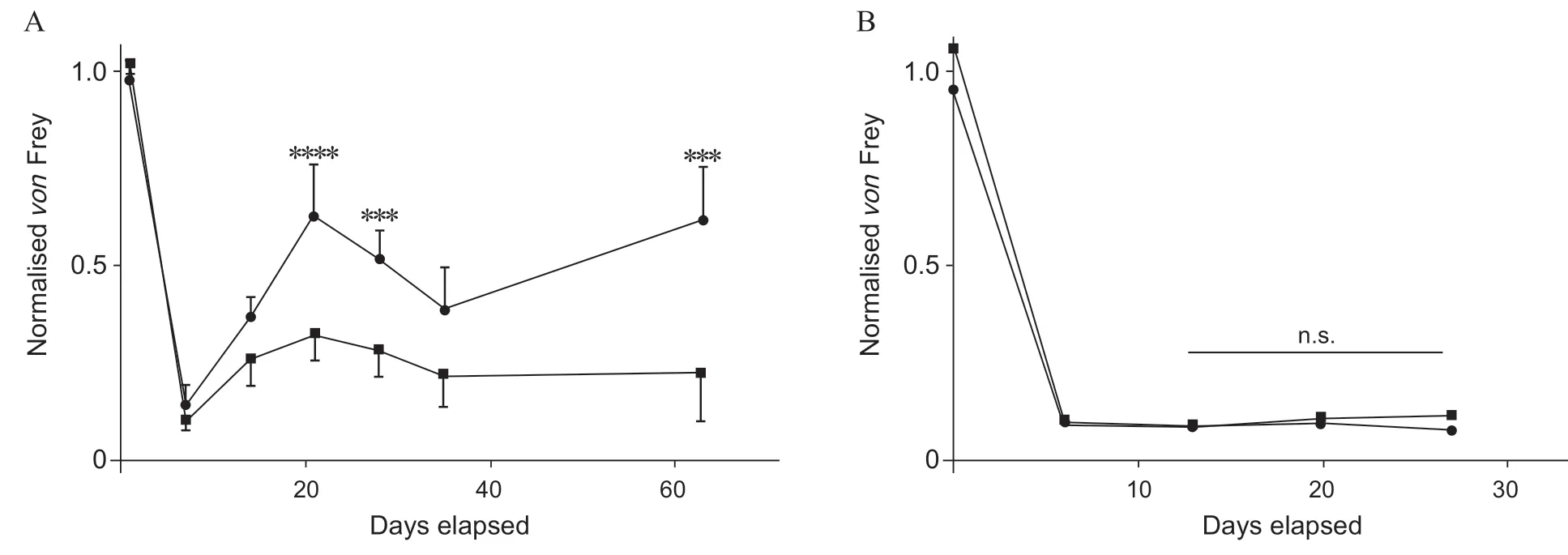
图3 iGABA 能神经元脊髓移植缓解疼痛
4. 讨论
本研究为IPSC 源GABA 能神经元可用于治疗已形成的神经病理性疼痛提供了第一个证据。基于已有研究,本研究未再使用小鼠前体细胞,改而使用可用于治疗的终末分化的HiPSC 源GABA 能神经元,将其移植到小鼠脊髓后能长期存活,此方法安全有效且对运动功能无明显影响。
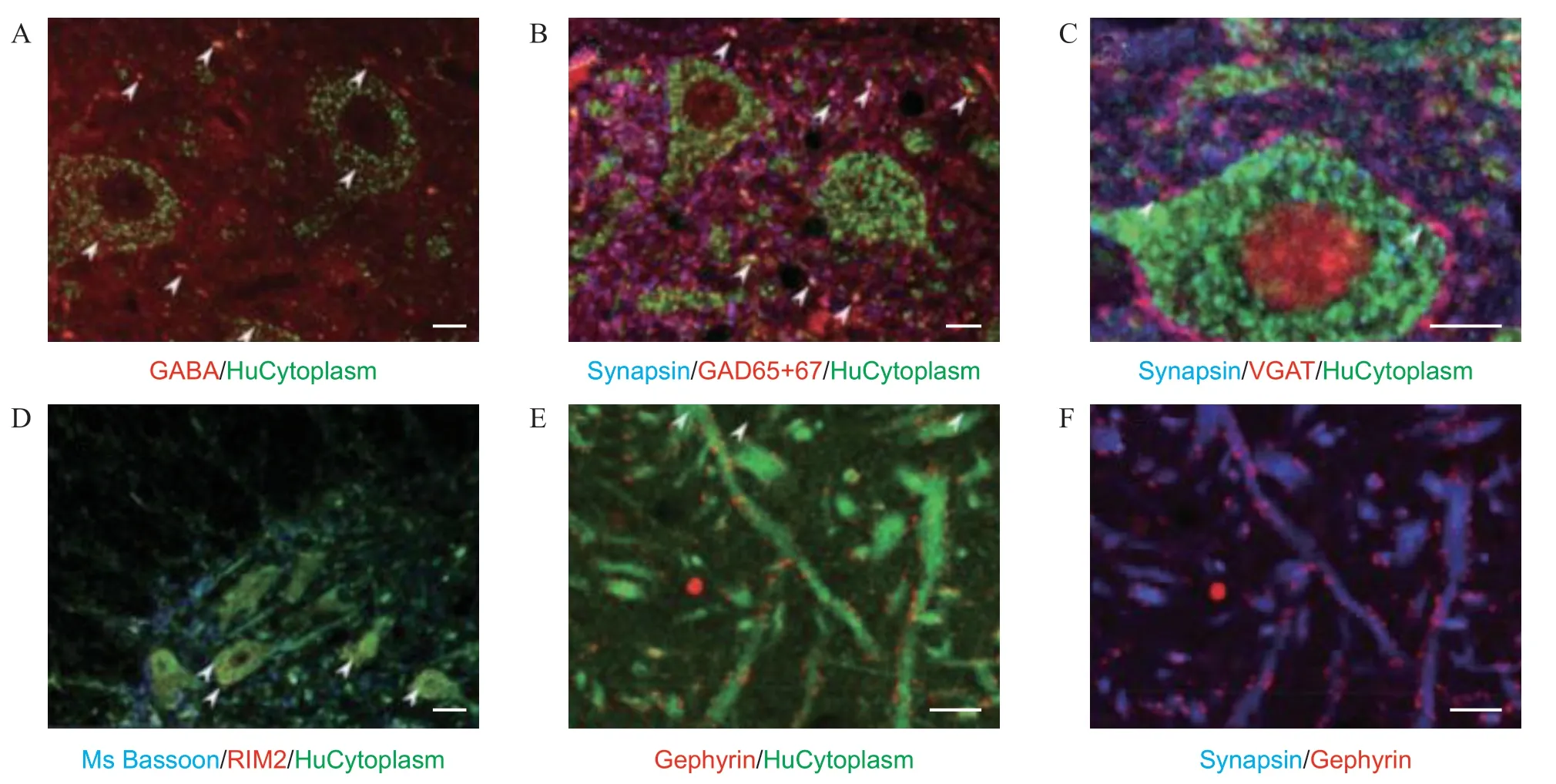
图4 iGABA 能神经元移植后成功存活
近年来有几项该类研究,给小鼠移植了从胚胎内侧神经节隆起 (MGE) 获得的原代GABA 能神经前体细胞用于治疗癫痫、神经病理性疼痛、化疗引起的周围神经病变和病理性瘙痒;也有学者给小鼠移植了人类胚胎干细胞源MGE 祖细胞,证明了可以长期缓解脊髓损伤小鼠的疼痛。本研究的数据与上述研究一致,这为神经细胞疗法治疗疼痛建立了基础。然而,MGE 祖细胞因其多能性、移植后的长期免疫抑制及致癌风险而不能用于治疗人类病人。
本研究发现通过移植途径增加GABA 能神经元不会影响小鼠基础痛阈,与相关研究结果一致。类似地,外源性激活钾氯协同转运蛋白2 (KCC2) 后,脊髓随后即恢复氯平衡,该过程对小鼠基础痛阈也没有明显的影响。但是,通过内源性途径如使用药物增加GABA 能神经元则会引起基础痛阈升高。这种明显差异可能表明正是诱发GABA 释放在缓解痛觉中起着核心作用。又或者,不同途径的GABA 能抑制可能通过不同通路调控痛觉。这一复杂过程需要进一步的深入研究以阐明。
本研究只证明了iGABA 能神经元移植在SNI模型上有明显疗效,若要全面评价,还需要在其他神经病理性疼痛模型上进行实验。神经病理性疼痛有很强的免疫学因素,已有人证明了移植细胞可在免疫活性小鼠体内存活,因此本研究中使用免疫缺陷小鼠进行了进一步实验。此外,虽然移植iGABA能神经元对已有神经病理性疼痛的小鼠疗效确切,但对临床上病情重、病程长病人的疗效尚需进一步研究;移植后神经元的整合能力,也需要通过电子显微镜和电生理学深入研究。
与其他方法相比,终末分化的iGABA 能神经元可以用于自体移植,具有更大的临床意义。临床中,镇痛药治疗时间窗口有限,有些有严重的不良反应,反复给药会加剧这些不良反应,本研究的方法通过单次移植即可有效、持久缓解神经病理性疼痛而不产生不良反应。但临床开发前,尚需在更大的动物模型和其他啮齿动物模型上进行更详细的安全性和有效性研究;而且由于解剖学差异,脊髓应用的安全性也需进一步研究;同时,高质量移植耗材的开发也至关重要。
神经病理性疼痛难以根治,严重影响病人日常生活和情绪。周围神经损伤导致脊髓水平痛觉抑制减弱,而通过移植安全的、终末分化的GABA 能神经元来加强中枢抑痛觉制,能够有效缓解疼痛,应被视为治疗慢性疼痛的一种新策略。
