淬火油泥的热解动力学分析及协同作用研究
2020-08-21袁朝兵李长江林顺洪
袁朝兵,李长江,林顺洪,杨 宇
(1. 重庆科技学院 机械与动力工程学院,重庆 401331;2. 重庆垃圾焚烧发电技术研究院,重庆 401331)
淬火油泥(QOS)是钢铁淬火工艺中产生的副产物,是一种由铁屑、淬火油、冷却水和其他杂质(如重金属等)组成的复杂混合物[1],外观呈黄褐色,易产生恶臭,黏度高,油水乳化程度高。QOS属于含油污泥[2-3]。2015年全球成品钢材表观消费量高达1 500 Mt[4]。而每生产1 t轧钢会产生0.86 kg的轧钢含油污泥[5]。轧钢含油污泥被列入《国家危废名录》HW08废矿物油条目。QOS中含有大量的矿物油和金属等可回收利用的资源[6]。轧钢含油污泥的无害化和资源化回收处理方式主要有两种:油分分离和热转化。章骅等[7]利用湿式减压蒸馏法对轧钢含油污泥的油分和残渣进行分离,通过优化温度、真空度和水蒸气流量等参数提高了油分的回收率,但其残渣需要进一步深度处理。赵浩川[8]提出了将轧钢含油污泥制成烧结矿返回高炉炼铁的方法,实验发现铁矿添加轧钢含油污泥后污染物的排放量降低和烧结成品的总铁含量降低。热解技术具有处理彻底、减量效果好的特点,是QOS无害化和资源化处理的有效方法[9]。热解与燃烧相比,具有更高的资源回收率,其残渣中的重金属具有耐浸出性,使污染物排放量降低。
本文采用热重差热分析和傅里叶变换红外光谱分析(TG-FTIR)联用的方法研究了QOS的热解特性,建立了热解动力学模型并求解动力学参数,分析了QOS中油分和残渣在热解过程中的相互作用,旨在为QOS的无害化、减量化处理及资源化利用奠定理论基础。
1 实验部分
1.1 实验样品
QOS样品取自重庆某弹簧钢厂。QOS的工业分析按照GB/T 212—2001标准进行;采用SDCHN435型元素分析仪(湖南三德公司)测定C、H、N元素含量;采用SDS350型红外定硫仪(湖南三德公司)测定S元素含量;由差减法得到O元素含量;采用SDACM 4000型量热仪(湖南三德公司)测定热值。QOS的工业分析和元素分析结果见表1。采用索氏提取法将QOS分离成矿物油(MO)和残渣(SR),SR占38.74%(w),MO占51.75%(w),水分占9.51%(w)。SR和MO的元素分析和热值测定结果见表2。

表1 QOS的工业分析和元素分析结果 w,%

表2 SR和MO的元素分析和热值测定结果 w,%
1.2 实验方法
取QOS样品(10±0.1)mg,置于Al2O3坩埚中,然后进行TG-FTIR分析,两者间采用聚四氟乙烯管连接。实验所用气体和保护气均为高纯N2(纯度99.999%),载气流量30 mL/min,升温速率分别为10,20,30 ℃/min,温度范围为35~1 100 ℃。MO和SR的分析同上。
1.3 分析方法
TG分析采用STA 409C型热重差热分析仪(德国NETZSCH公司);FTIR分析采用TENSOR27型傅里叶变换红外光谱仪(美国BRUKER公司)。
2 结果与讨论
2.1 QOS的热解过程
2.1.1 QOS热解反应过程
QOS在升温速率为20 ℃/min条件下的TG/DTG曲线见图1,QOS热解产物的FTIR谱图见图2。QOS的热解过程分为油分热解阶段和矿物质分解阶段,整个热解过程总失重率为75.85%,热解的主要反应区域集中在150~520 ℃。
油分反应阶段的温度范围为150~520 ℃。由图2a可见,在热解温度为295 ℃时,产物FTIR谱图中出现了H2O、甲酸、芳香烃、苯酚、CO和CO2的特征峰及高强度的烷烃特征峰。QOS的油分热解过程中部分挥发性组分在低温下未参与反应直接随载气排出,其FTIR谱图中特征峰波数为1 000~1 900 cm-1,根据文献[10]可知,这些有机化合物主要有甲醛、乙醛、甲醇和丙酮。羧酸的断裂、含氧杂环的开环裂解导致CO和CO2特征峰的生成[10]。失重主要源自QOS中低沸点轻质油分受热挥发。图2a出现的低强度烷烃、芳香烃、CO和CO2特征峰说明这个阶段内发生了重质油分热解,半焦热解发生缩聚和重排的碳化反应。
矿物质反应阶段的温度范围为800~980 ℃,DTG曲线上出现最后一个失重峰,峰值温度为915℃。由图2b 可见:烷烃的特征峰减弱,较弱的芳香烃特征峰说明此阶段出现了重质油分热解;CO和CO2的特征峰增强是由于QOS中Fe的氧化物与碳单质发生反应的结果[11]。

图1 QOS的TG/DTG曲线
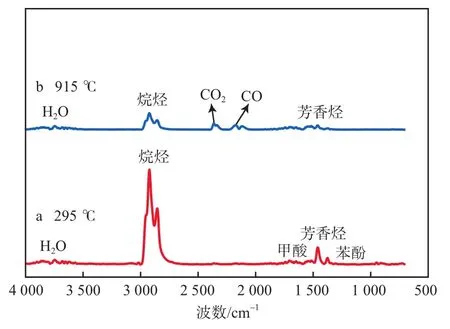
图2 QOS热解产物的FTIR谱图
2.1.2 升温速率对QOS热解过程的影响
不同升温速率下QOS的TG和DTG曲线分别见图3和图4,DTG峰值温度见表3。
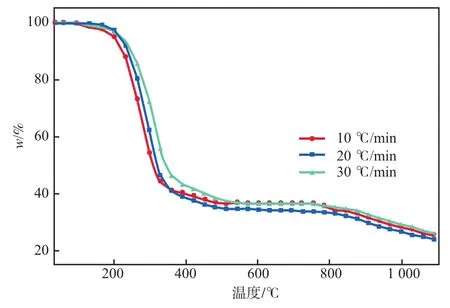
图3 不同升温速率下QOS的TG曲线
由图3、图4和表3可见,随着升温速率的提高,热解曲线的变化趋势基本一致,TG和DTG曲线均逐渐向高温范围移动,其他含油污泥的热解研究也出现了类似现象[12]。同时,随着升温速率的增大,DTG反应区间温度变宽。

图4 不同升温速率下QOS的DTG曲线

表3 不同升温速率下QOS的DTG峰值温度
2.2 SR和MO的热解过程
2.2.1 SR的热解过程
在升温速率为20 ℃/min条件下,SR热解过程的TG/DTG曲线见图5,峰值温度下产物的FTIR谱图见图6。由于SR是由QOS萃取而获得,索氏提取无法保证有机组分完全脱除,部分油分或其他有机物残留在SR中,导致SR的热解过程分为两个阶段,整个热解过程总失重率为45.96%,油分热解区和矿物质分解区的相对失重率分别为47.23%和46.87%。

图5 SR的TG/DTG曲线
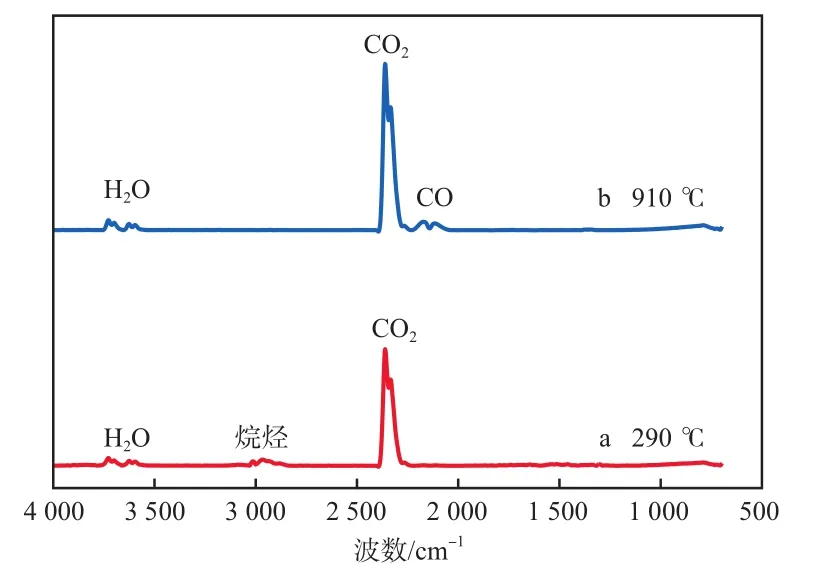
图6 SR热解产物的FTIR谱图
第一阶段160~540 ℃,最大失重峰的峰值温度为290 ℃,产物FTIR谱图(图6a)中出现低强度的烷烃、芳香烃和醛类特征峰及高强度的CO2特征峰,此阶段也发生了重质油分热解,半焦热解发生缩聚和重排的碳化反应。
第二阶段780~980 ℃,DTG曲线上出现最后一个失重峰,峰值温度为910 ℃,产物FTIR图谱(图6b)中出现CO特征峰和较强的CO2特征峰,由文献[7,13]可知,当温度为700~1 200 ℃时,会发生3C+Fe2O3→2Fe+3CO和Fe2O3+3CO→2Fe+3CO2还原反应。烷烃特征峰消失,说明油类物质已在第一阶段内完全分解。
2.2.2 MO的热解过程
在升温速率为20 ℃/min条件下,MO热解过程的TG/DTG曲线见图7,峰值温度下产物的FTIR谱图见图8。
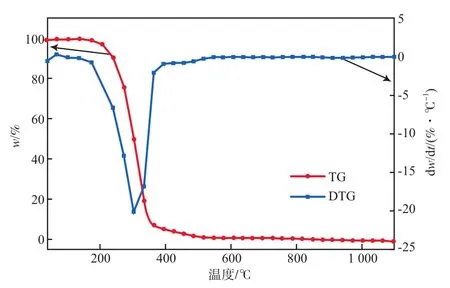
图7 MO的TG/DTG曲线
由图7可见,MO热解过程只有一个阶段,失重温度范围为160~520 ℃,失重率达99.90%,在160 ℃左右MO开始失重,200 ℃左右MO开始热解,最大失重峰的温度为310 ℃,370 ℃左右出现一个小的失重峰。由图8可见较弱的醛类特征峰和较强的烷烃特征峰。最大失重峰温度低于烃类有机物裂解温度(370 ℃),有机物的明显析出,证明轻质油分主要是柴油馏分[14]。在370 ℃之后产生了一个肩峰,失重量小,是MO中的重质油组分受热分解产生的。

图8 MO热解产物的FTIR谱图
在MO的热解过程中,主要是轻质油的挥发,失重率约为93%,重质油热解的失重率约为7%,表明了MO主要以轻质油分为主。
2.3 热解动力学
根据Arrhenius定律,QOS的热解可以通过如下微分方程来表达:
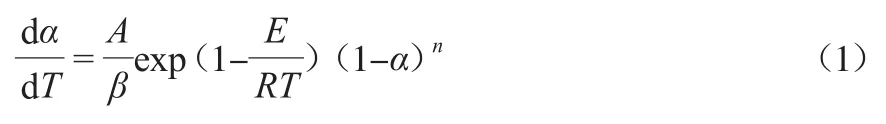
式中:α为t时刻的转化率,%,α=(m0-mt)/(m0-m∞),其中m0为初始质量,g,mt为t时刻的质量,g,m∞为反应结束的剩余质量,g;β为升温速率,℃/min;A为指前因子,s-1;E为反应活化能,kJ/mol;R为气体常数,8.314 J/(kg·K);T为热力学温度,K;n为反应级数。
采用Coats-Redfern法[15],假设反应级数为1,则可由式(1)得到如下近似表达式:

对于一般的反应温度区间和大部分的E值而言式(2)右端第一项为常数,因而作图能够得到一条直线,可通过直线的斜率和截距分别计算反应的活化能和指前因子。QOS、MO和SR热解过程中不同阶段反应的活化能、指前因子和R2见表4。
对热解主要失重阶段采用一级动力学模型进行动力学分析,由表4可知,R2均大于0.99,说明在实验温度范围内,采用一级动力学模型能够很好地描述QOS、MO和SR的热解过程。由于QOS中MO含量高于SR含量,可分解的矿物质较少。在SR的油分热解阶段,由于油分受热裂解,导致其化学键的断裂放出大量的能量,为SR中的金属氧化物发生还原反应提供了一部分能量,因此出现了QOS的热解过程中MO热解所需的活化能大于SR热解所需的活化能的现象。在残渣的热解过程中,矿物质反应阶段析出了CO和CO2气体,表明了在SR的油分反应阶段,SR中的所有油分已完全受热分解。油分反应所需的活化能(48.49 kJ/mol)大于矿物质反应所需的活化能(44.21 kJ/mol),这可能是由于在SR的油分反应产生的半焦含量少,导致了MO在矿物质反应阶段只有部分金属氧化物参与反应。

表4 QOS、MO和SR的热解动力学分析结果
2.4 MO和SR的相互作用
相对于其他矿物油(如原油或石化行业含油污泥等)的热解过程,QOS最大的不同就是其固体残渣中含有大量Fe的金属氧化物。为进一步研究MO和SR热解过程中的相互作用,通过样品热解残余质量的计算,求得样品实验失重率与理论失重率的误差值(RTG)[16],其计算式见式(3)。

式中:TG是样品MO和SR按0.572∶0.428的质量比混合而成的样品的热解失重率,TGEO和TGSR分别是同一温度点对应的MO和SR的失重率;x1和x2分别为MO和SR在QOS中的质量分数,根据表1中的数据x1=0.572(干基百分比,下同),x2=0.428;若RTG>0,则表示QOS中的残渣对油分的热解有抑制作用,反之,则有促进作用。
MO和SR共热解的RTG曲线见图9。由图9可知:在初温~480 ℃和850~1 000 ℃时,RTG<0,此时SR促进了MO的热解,初温~480 ℃时SR对MO的热解促进效果更明显,在300 ℃左右时,SR对MO的热解促进作用最大;在480~850 ℃和1 000~1 100 ℃时,RTG>0,此时SR对MO的热解有抑制作用,当温度高于1 000 ℃时,随着温度的升高抑制作用越强。
综合RTG分析可知:随着热解温度的升高,QOS中SR所含的Fe2O3对MO的热解促进作用越来越大;当温度达到300 ℃左右时,促进的效果最大;随着温度的继续升高,促进的效果逐渐减小;当温度升至480 ℃时,SR中的Fe2O3抑制了MO的热解。由此可见,在热解过程中,MO和SR有着相互作用。

图9 MO和SR共热解的RTG曲线
3 结论
a)QOS热解过程包含低温段的油分热解阶段和高温段的矿物质分解阶段。低温段热解温度为150~520 ℃,活化能为61.40 kJ/mol;高温段热解温度为800~980 ℃,活化能为16.23 kJ/mol。SR的热解过程和QOS的热解过程类似,分为油分热解反应和残渣中Fe2O3的还原反应。MO的热解过程只有一个反应阶段,即为轻质油分的挥发和重质油分的热解。
b)FTIR表征结果表明:在QOS热解过程中,析出的气体主要为小分子气体CO2、CO和有机化合物;在SR热解过程中,CO2的特征峰强度高于其他气体的特征峰强度;在MO热解过程中,烷烃的特征峰强度高于的其他气体的特征峰强度,且MO主要以轻质油分为主。
c)在QOS的热解过程中,MO和SR有相互作用。在初温~480 ℃时,QOS中SR所含的Fe2O3对MO的热解起促进作用,在300 ℃左右时,促进效果最明显。
