维持性血液透析患者肌少症发生情况及其影响因素分析
2020-08-18戴祺洁华建武
戴祺洁, 陶 静, 华建武, 孙 伟
(南京中医药大学附属医院, 江苏 南京, 210029)
肌少症是一种进行性、广泛性的骨骼肌疾病,可增高患者摔倒、骨折、残疾和死亡等风险[1]。尿毒症患者的肌少症发病率较高,可达51.9%, 且男性的发病率高于女性[2]。近年来,肌少症越来越受到临床医生的关注,但目前肌少症的起始、进展和后果等方面仍存在盲点,给防治工作带来许多困扰。本研究探讨了维持性血液透析(MHD)患者的肌少症发生率以及相关影响因素,旨在为临床防治肌少症提供更多参考,现报告如下。
1 资料与方法
1.1 一般资料
选择2019年1-12月在江苏省中医院行MHD治疗的55例患者作为研究对象,男35例,女20例,平均年龄(60.71±13.89)岁,平均透析龄(6.40±4.97)年,所有患者每周进行3次血液透析治疗, 4 h/次。纳入标准: 年龄≥18岁者;认知正常,言语表达清楚者;愿意参加本次研究者。排除标准: 近期合并肺部、胃肠道、泌尿系统等急性感染的患者; 近期行手术或有外伤的患者; 伴心肺功能不全、胃肠道溃疡、恶性肿瘤、精神异常的患者; 脑卒中后遗症、脊髓疾病、周围神经病变等神经内科疾病所致肌力下降者; 体内置有金属支架或心脏起搏器的患者; 老年痴呆患者或不能配合者。
1.2 方法
1.2.1 一般资料调查:在本院血液透析软件系统上收集患者的基本资料,包括性别、年龄、透析龄、原发病、合并症等,并以问卷形式询问患者的运动情况及运动意愿。
1.2.2 肌力测量: 手握力与身体其他部位的力量中度相关,可代替更复杂的手臂和腿部肌力测定,通常被作为肌力的测定指标。测量工具采用国产WCS-10000万庆电子握力计(上海万庆电子有限公司生产)。测试者于休息平静后呈站立状态,双臂自然下垂,用非造瘘手紧握握力器手柄,以最大力气握紧,待握力器显示屏数字不再变化时的数值为握力值,休息片刻后重复,每人测量3次,取最大值。
1.2.3 肌量测量: 使用Inbody720人体成分分析仪进行体成分测试。所有患者于透析结束后,排空二便,着轻便衣物,取下随身物品,测量身高,再脱去鞋袜,双脚立于足形电极上测体质量; 输入患者性别、年龄和身高,嘱患者双手握住手柄,拇指放于手柄上部,其他四指握于手柄下部,手臂伸直,离开躯体一定距离并保持静止。测定患者体蛋白质含量、体脂肪含量、骨骼肌量、四肢骨骼肌量,计算每例患者的相对骨骼肌质量指数(RSMI), 公式为RSMI=四肢骨骼肌量(kg)/身高的平方(m2)。
1.2.4 实验室检查: 所有患者于上机前抽取静脉血,检测甲状旁腺激素(PTH)、血红蛋白(Hb)、血清白蛋白(ALB)、血清前白蛋白(PA)、血钙(Ca)、血磷(P)、尿素氮(BUN)、尿酸(UA)、总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)等指标水平。
1.3 诊断标准
欧洲老年人肌少症工作组(EWGSOP)发表的最新共识[1]指出,肌力是衡量肌肉功能的最可靠指标,而低肌力是诊断肌少症的首要参数。EWGSOP建议的诊断阈值: ① 握力为男性<27 kg, 女性<16 kg; ② RSMI为男性<7 kg/m2, 女性<6 kg/m2。满足①时表明有肌力低下可能,满足②即可诊断肌少症。
1.4 统计学分析

2 结 果
2.1 肌少症发生情况
55例MHD患者中,诊断为肌少症者22例(40.00%), 男11例、女11例。
2.2 单因素分析
将55例患者根据有无肌少症分为2组,比较2组患者的性别、年龄、透析龄、原发病、合并症、运动情况、运动意愿、体质量指数(BMI)、体蛋白质含量、体脂肪含量、骨骼肌量、RSMI、握力及生化结果等指标。单因素分析显示,2组间年龄、体蛋白质、BMI、骨骼肌量、RSMI、握力指标比较,差异有统计学意义(P<0.05或P<0.01), 见表1。

表1 MHD患者肌少症的单因素分析
2.3 多因素Logistic回归分析
将单因素分析结果中有显著差异的变量进行Logistic回归分析(由于骨骼肌量、RSMI、握力为诊断肌少症的相关指标, 2组间差异具有必然性,故剔除),结果显示,年龄、体蛋白质含量和BMI是MHD患者发生肌少症的独立影响因素(P<0.05或P<0.01), 见表2。
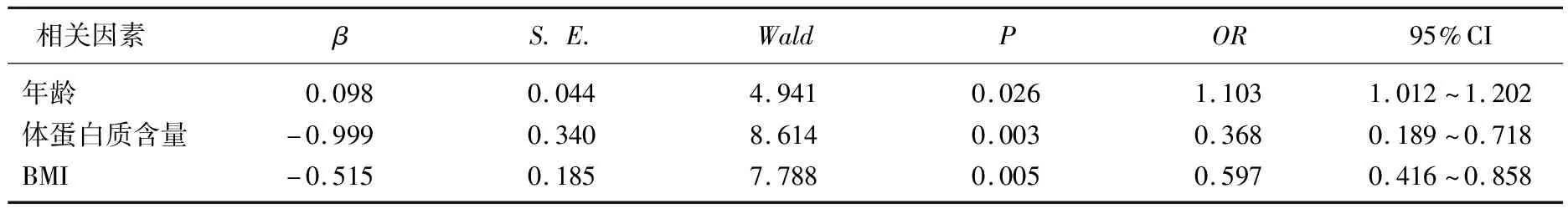
表2 MHD患者肌少症多因素Logistic回归分析
3 讨 论
肌少症是指人体肌肉功能逐步减退并走向衰竭的一种疾病,源于终生累积的不良肌肉变化,多见于老年人。其发病隐秘,危害性大,不仅严重影响患者的生活质量,引发焦虑、抑郁症状[3], 还与心脏疾病[4]、呼吸系统疾病[5]和认知功能障碍[6]等密切相关,增加了住院风险[1]。研究[7]显示,合并肌少症的老年患者住院费用比无肌少症的老年患者高5倍。MHD患者由于自身慢性疾病的不断消耗,肌少症发生率更高,早发现、早干预、早治疗,对于防治、延缓甚至逆转肌少症具有重要意义。
本研究中, MHD患者的肌少症发生率为40.00%, 与其他临床研究[8-9]结果相符。本研究还显示,年龄、蛋白质、BMI是MHD患者肌少症的独立影响因素。年龄与肌少症的发生呈正相关,体蛋白质含量及BMI与肌少症的发生呈负相关,表明随着患者年龄增长、体蛋白质含量下降、BMI降低,肌少症的发生率升高。蛋白质是人体肌肉的重要组成部分,如缺乏将直接提示肌肉质量不足及营养缺乏。BMI虽通常被作为肥胖的评价指标,但多项研究[3, 10]表明,高BMI与肌少症呈负相关。
体蛋白质含量和BMI还是反映患者营养状况的重要指标。研究[11]表明,营养状况差的血液透析患者肌少症的患病风险明显增高,重度营养不良还容易合并代谢性酸中毒,引起患者骨骼肌氨基酸氧化,使肌细胞凋亡加快。因此,欧洲最佳实践指南[12]提倡在患者刚开始血液透析时即行相关营养指标的监测。生物电阻抗法(BIA)无创、安全、可反复操作,能够较为精准地反映人体的组成成分,有利于更早地发现患者的营养不良情况[13], 又方便进行BMI、骨骼肌质量等指标的检测,值得临床推广。但由于BMI值的测定只参考身高和体质量,患者可能因水肿而掩盖早期营养不良情况,存在一定程度的局限性,故还需综合其他指标结果共同评估。
本研究还调查了患者的运动意愿与运动情况,组间差异无统计学意义,考虑与纳入患者例数太少有关,从总体概率来看,无肌少症组患者的运动情况及运动意愿更好,后期可开展更大样本量的研究进一步验证。本调查以患者自愿参与为原则,样本量较小,数据结果可能存在一定误差,高龄、中风、合并多种并发症、行动不便、生活不能自理及不愿配合的患者均未纳入调查,而其营养不良和肌少症的发生率可能更高。研究[14-15]发现,透析时间长、超敏C反应蛋白水平高、运动量不足和合并多种并发症等都是肌少症的相关影响因素,临床医生应加以关注。
综上所述, MHD患者的肌少症发生率较高,年龄、BMI及体蛋白质含量是患者发生肌少症的独立影响因素,对老年患者尽早评估肌少症发生情况,适当提高BMI和体蛋白质含量对于降低MHD患者肌少症发生率有重要意义。
