3-脱氧-D-甘露-2-辛酮糖酸寡糖的合成研究进展
2020-08-10庄丽琴邓妤曾铮楼琦欣杨友
庄丽琴,邓妤,曾铮,楼琦欣,杨友
(华东理工大学药学院 上海市新药设计重点实验室,上海 200237)
3-脱氧-D-甘露-2-辛酮糖酸(Kdo,1)是一种非哺乳动物源的八碳酮糖酸。作为高碳糖家族的一种重要类型分子,Kdo 主要存在于革兰阴性菌的脂多糖(LPS)核心结构中,也存在于大肠埃希菌和脑膜炎奈瑟菌等细菌的荚膜多糖以及产碱普罗登斯菌和肺炎克雷伯菌等细菌的O-抗原中[1-3]。并且,植物和藻类中也被发现含有Kdo 单元[4-5]。由于细菌的LPS 和荚膜多糖是重要的致病因子,可引发强大的免疫反应,所以Kdo 寡糖被认为是开发抗菌疫苗和诊断试剂的潜在靶标[6-7]。然而,由于Kdo 的1位含有吸电子的羧基,且3 位缺少邻基参与基团,在发生糖苷化反应时往往活性和立体选择性都不好,容易得到α-和β-异构体,并发生消除反应生成糖烯副产物。本文将按照给体类型综述Kdo 的糖苷化反应研究进展及代表性Kdo 寡糖的合成,为Kdo 寡糖的合成研究提供参考。
1 3-脱氧-D-甘露-2-辛酮糖酸的生物合成
从结构上看,Kdo 与唾液酸(sialic acid,2)、Kdn(3)、legionaminic acid(Leg,4)、pseudaminic acid(Pse,5)等均属于3-脱氧-2-酮糖酸家族分子(见图1),它们具有相同的结构特征和反应特性[8]。其中,α-Kdo 是细菌LPS 内核区域的重要单元,它将脂质A 区域与O-抗原多糖连接起来。β-Kdo 则更常见于细菌的荚膜多糖和O-抗原中。
Kdo 是细菌LPS 中重要的保守结构,对细菌的生存具有至关重要的意义。抑制Kdo 的生物合成可阻断LPS 的形成,从而破坏细菌细胞壁结构的完整性,影响细菌生理学功能的发挥。绝大多数细菌的LPS 都含有不同数量的Kdo 残基和脂质A,其中Kdo 的生物合成途径始于戊糖中间体Ru5P(6,见图2)[9]。首先,Ru5P 被D-阿拉伯糖-5-磷酸盐异构酶转化为A5P(7)。接着,A5P 在Kdo8P 合成酶的催化下与磷酸烯醇式丙酮酸酯发生缩合反应,生成Kdo 8-磷酸盐(Kdo8P,8)。然后,Kdo8P 被Kdo8P 磷酸酶催化水解成Kdo。Kdo 在胞嘧啶核苷酸(CMP)-Kdo 合成酶(CKS)催化下与胞嘧啶核苷三磷酸(CTP)反应,生成糖基核苷酸CMPKdo(9)这一重要的中间体。在Kdo 转移酶的促进下,糖基核苷酸CMP-Kdo 与脂质A 发生酶促反应生成Kdo-lipid A。
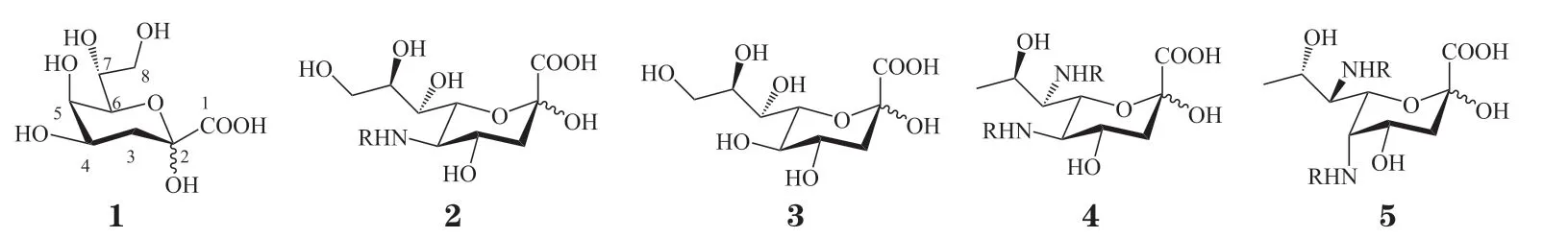
图1 3-脱氧-2-酮糖酸家族的代表性化合物Figure 1 Representative compounds of the 3-deoxy-2-ulosonic acid family
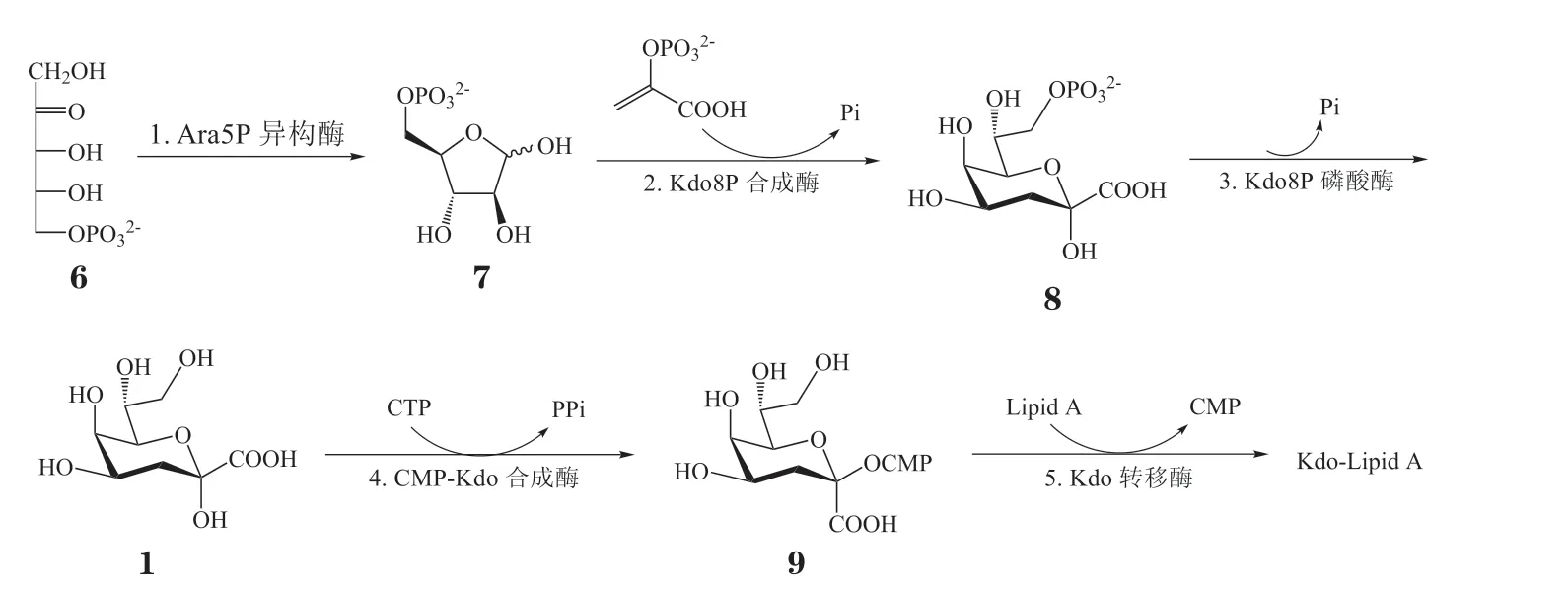
图2 Kdo 的生物合成途径Figure 2 Biosynthetic pathway of Kdo
在Kdo 的生物合成中,CKS 是将Kdo 转化成CMP-Kdo,从而引入到LPS 中的关键限速酶。基于此重要的酶促反应,CKS 成为抗菌药物开发中的潜在药物靶标。CKS 抑制剂可被用于阻断Kdo 的生物合成,从而使得细菌的脂质A 前体在体内大量聚积,无法形成完整的细胞壁结构,最终达到抗菌的目的。研究表明,2-脱氧-Kdo 类似物对CKS 具有较好的抑制作用[9-11]。基于此,笔者所在课题组合成了一系列3 位碳分枝的2-脱氧-Kdo 类似物,为进一步开发CKS 抑制剂打下了基础[12]。
2 3-脱氧-D-甘露-2-辛酮糖酸寡糖的合成
Kdo 寡糖中的糖苷键被认为是糖化学中最难构建的糖苷键之一。Kdo 自身的结构特点对其糖苷化反应造成了很大的影响,经常需要综合考虑离去基团、保护基团、促进剂、溶剂、温度和添加剂等众多影响因素。从结构上来说,Kdo 的3 位碳上没有邻基参与基团,从而无法通过邻基参与效应有效控制Kdo 糖苷化反应的立体选择性,经常生成α-和β-构型混合的异构体。并且,Kdo 的1 位碳上具有吸电子的羧基,降低了糖苷化反应的活性,容易发生消除反应,生成Kdo 糖烯副产物,因此糖苷化反应的收率一般较低,并给糖苷化产物的分离增加了困难。因此,Kdo 糖苷化反应中立体选择性的控制和糖烯副产物的抑制,是Kdo 寡糖合成中的关键问题。Kdo 糖苷化反应中常见的产物和副产物见图3。
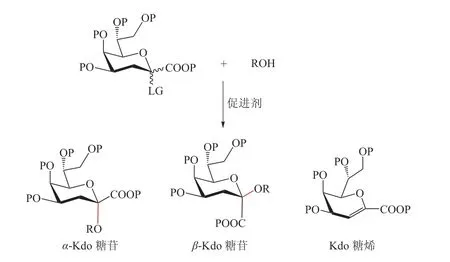
图3 Kdo 糖苷化反应中常见的产物和副产物Figure 3 Common products and by-products in Kdo glycosylation
迄今为止,在Kdo 糖苷的合成中,许多不同类型的Kdo 给体已经被开发出来,主要包括卤苷、糖烯、硫苷、N-苯基三氟乙酰亚胺酯、亚磷酸酯和邻炔基苯甲酸酯等。最近,Kosma 和Mong 课题组分别对Kdo 的糖苷化反应进行了综述[13-15]。以下将着重介绍Kdo 糖苷化反应的最新进展及其在复杂Kdo寡糖合成中的应用。
2.1 3-脱氧-D-甘露-2-辛酮糖酸卤苷给体
早在20 世纪80—90年代,Kdo 溴苷给体就被广泛地应用于α-Kdo 寡糖的合成。Kosma 等[16-17]利用溴苷给体合成了分枝状Kdo 四糖α-Kdo-(2→4)-[α-Kdo-(2→8)]-α-Kdo-(2→4)-α-Kdo(见 图4)。在HgBr2/Hg(CN)2催化下,Kdo 溴苷给体10 与Kdo 二糖11 反应生成α-Kdo 三糖12,收率为59%。化合物12 可被进一步转化为Kdo 三糖溴苷13。三糖给体13 与Kdo 受体14 在HgBr2/Hg(CN)2催化下反应2 d 可获得Kdo 四糖15,收率为32%。最后经过皂化反应可得到目标四糖16。由于该给体用于糖苷化时需要使用有毒重金属,易生成糖烯副产物,所以在Kdo 寡糖的合成中受到了一定的限制。
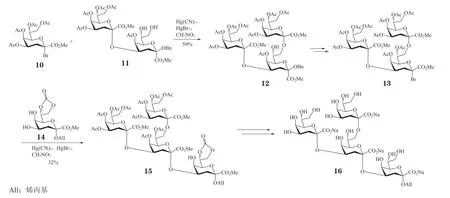
图4 利用Kdo 溴苷给体合成Kdo 四糖Figure 4 Synthesis of Kdo tetrasaccharide with Kdo bromide donor
与Kdo 溴苷的糖苷化反应相比,Kdo 氟苷的糖苷化反应的α-立体选择性更好,从而得到了更广泛的应用[18-22]。Yoshizaki 等[23]利用Kdo 氟苷首次合成了大肠埃希菌中的脂多糖片段(Re-LPS)(见图5)。在三氟化硼乙醚的促进下,4、5 位叔丁基二甲基硅基(TBS)保护的Kdo 氟苷给体17 与氨基葡萄糖二糖骨架18 发生糖苷化反应,以89%的收率立体选择性生成α-(2→6)-连接的三糖19。然后,化合物19 被转化为4′′-O-三乙基硅基(TES)保护的受体20。相似地,4、5 位丙叉保护的Kdo 氟苷21 与三糖受体20 在三氟化硼乙醚的促进下发生糖苷化反应,以75%的收率得到α-(2→4)-连接的四糖22。最后,经过脱保护操作获得了大肠埃希菌中的Re-LPS。合成的Re-LPS 与天然的Re-LPS 展示了相同级别的细胞因子[如肿瘤坏死因子(TNF)-α与白细胞介素(IL)-6]诱导活性。
Kong 等[24]利用双丙叉保护的Kdo 氟苷给体23与Kdo 受体24 在三氟化硼乙醚的促进下反应,得到α-(2→4)-连接的Kdo二糖25,但产率仅为25%(见图6)。在三氟甲磺酸银(AgOTf)和2,6-二叔丁基-4-甲基吡啶(DTBMP)存在下,全乙酰化的L-甘油-D-甘露庚二糖溴苷26 与含有5 位羟基的二糖受体25反应,可得到相应的α-(1→5)-连接的四糖,脱除所有保护基后获得目标四糖27。
为了进一步提高Kdo 糖苷化反应的α-立体选择性,可通过在Kdo 的3 位碳上引入碘基、硫基或苯硒基等辅基作为立体导向基团的策略来立体选择性合成α-Kdo 糖苷[25-27]。
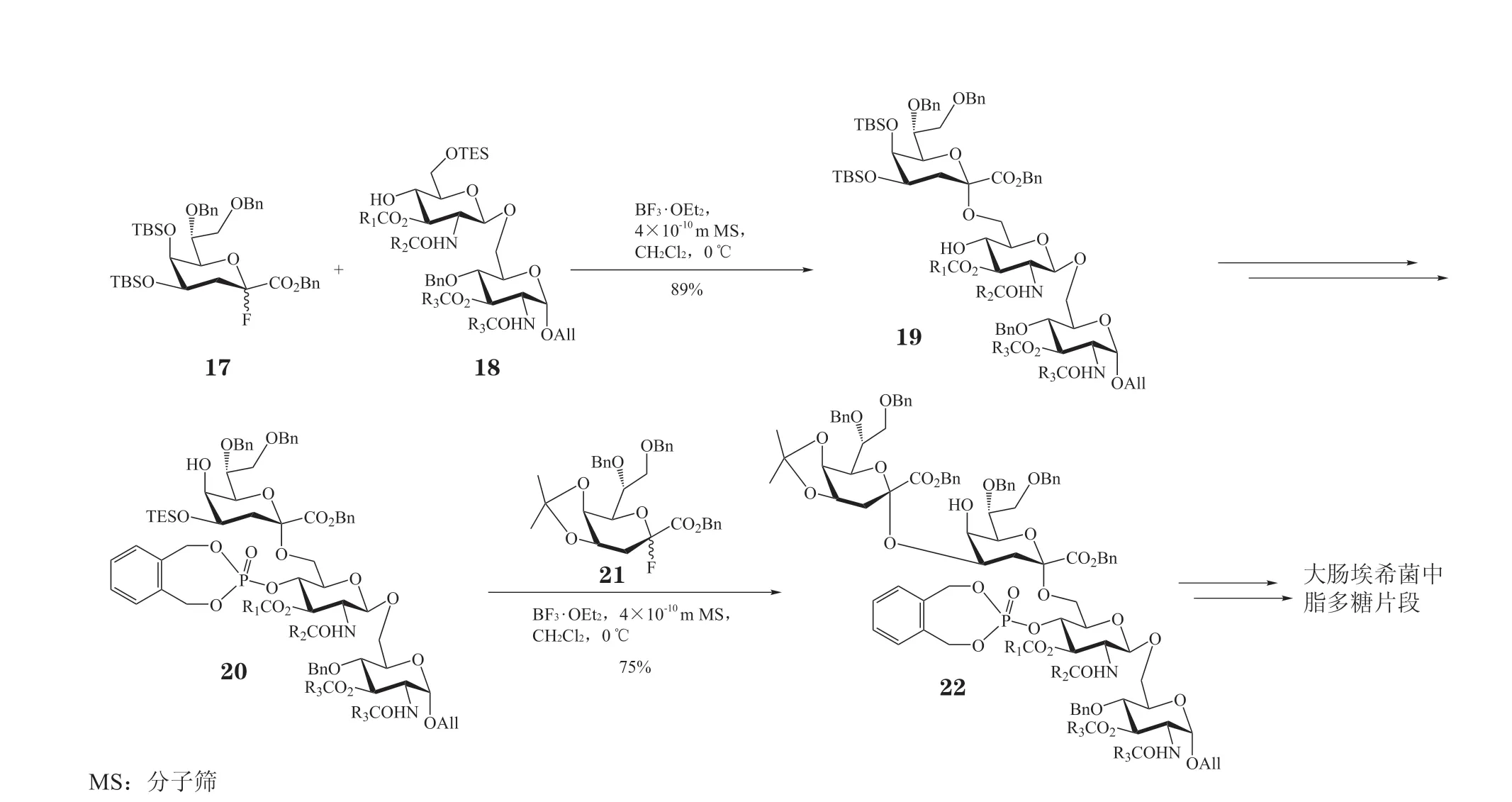
图5 利用Kdo 氟苷给体合成大肠埃希菌中的脂多糖片段Figure 5 Synthesis of the lipopolysaccharide fragment of E. coli with Kdo fluoride donor
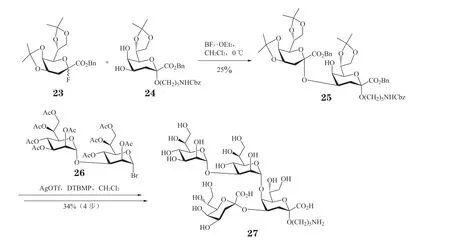
图6 利用Kdo 氟苷给体合成革兰阴性菌脂多糖中的核心四糖Figure 6 Synthesis of lipopolysaccharide core tetrasaccharide of Gram-negative bacteria with Kdo fluoride donor
如图7 所示,Pokorny 等[28]报道了将3-碘代-Kdo氟苷给体用于立体选择性合成衣原体相关的α-Kdo三糖。在三氟化硼乙醚的促进下,3-碘代-Kdo 氟苷给体28 与四醇29 反应可区域选择性得到4,8 位分枝的α-Kdo 三糖30,收率为58%。在该反应中,也会同时得到少量的α-(2→7)-连接的三糖异构体(7%)和糖烯副产物(11%)。之后,三糖30 经过乙酰化反应、脱碘基反应和皂化反应后,可得到衣原体相关的三糖31。相似地,3-碘代-Kdo 氟苷给体28与8-O-TES 的糖烯受体32 发生糖苷化反应,得到α-Kdo 二糖33。二糖33 经N-碘代丁二酰亚胺(NIS)和氟化氢吡啶处理后可被转化为3-碘代-Kdo 二糖氟苷给体34。接着,在三氟甲磺酸的催化下,34 与二醇35 反应,立体选择性形成α-Kdo 三糖36,收率73%。最后,经乙酰化反应、脱碘基反应和皂化反应得到衣原体相关的三糖37。
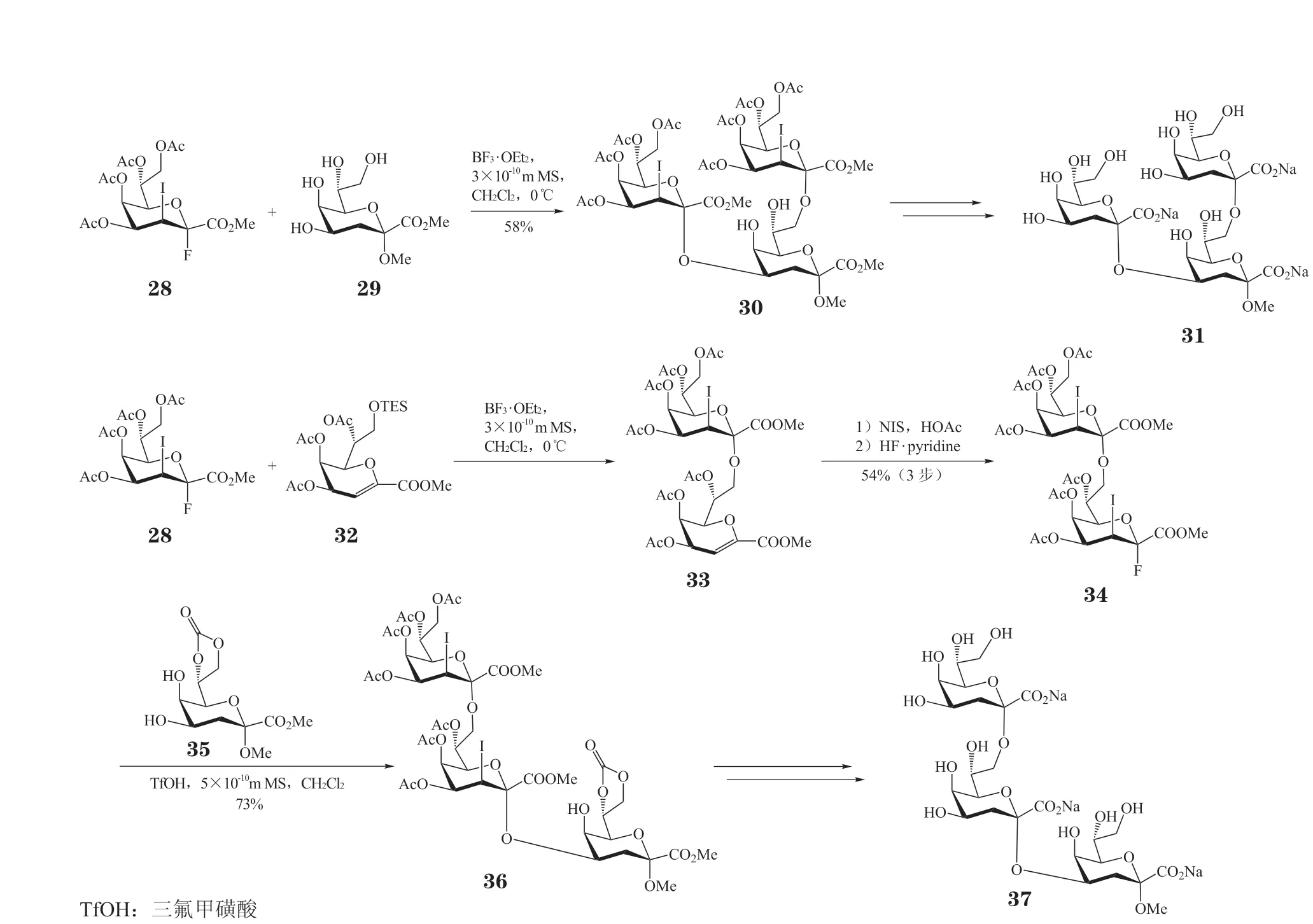
图7 利用3-碘代-Kdo 氟苷给体合成衣原体相关的α-Kdo 三糖Figure 7 Synthesis of chlamydia-related α-Kdo trisaccharide with 3-iodo-Kdo fluoride donor
此外,由于Kdo 的5 位羟基存在较大的空间位阻,所以4,5 位羟基裸露的Kdo 二醇受体发生糖苷化反应时,一般较难形成(2→5)-连接的产物。在三氟化硼乙醚促进下,全苄基保护的3-碘代-Kdo 氟苷给体38 与Kdo 受体39 的5 位羟基反应,可以71%的收率得到单一构型的α-(2→5)-连接的Kdo 二糖40(见图8)[29]。脱保护后可得到α-(2→5)-连接的Kdo 二糖41,这为合成含有此二糖的不动杆菌LPS提供了借鉴。
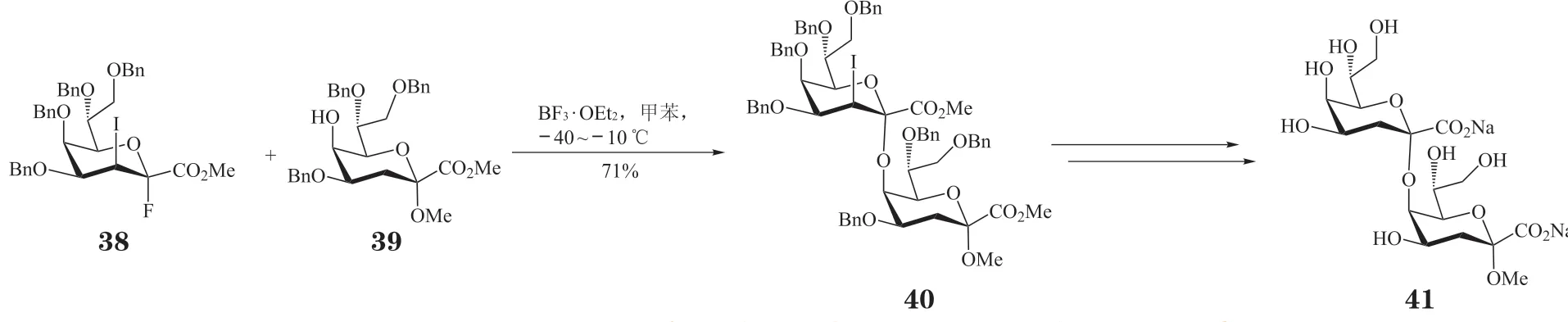
图8 利用3-碘代-Kdo 氟苷给体合成α-(2 →5)-连接的Kdo 二糖Figure 8 Synthesis of α-(2 →5)-linked Kdo disaccharide with 3-iodo-Kdo fluoride donor
2.2 3-脱氧-D-甘露-2-辛酮糖酸糖烯给体
Kdo 糖烯是糖苷化的副产物,将其用于Kdo 的糖苷化反应非常具有吸引力。在强酸的条件下,通过在Kdo 的3 位碳引入立体导向的辅基,如硒基和碘基等,可与活性高的伯醇反应得到α-Kdo 糖苷[30]。
基于在3 位碳引入立体导向的苯硒基的策略,Yang 等[31]利用全乙酰化的Kdo 糖烯给体42 合成了α-Kdo 糖苷45(见图9)。在苯基氯化硒(PhSeCl)、AgOTf 和三氟甲磺酸三甲基硅酯(TMSOTf)的促进下,Kdo 糖烯给体42 与五碳连接臂43 反应生成3 位苯硒基取代的中间体44。在三丁基氢化锡(Bu3SnH)和偶氮二异丁腈(AIBN)的自由基还原条件下,44 被还原成α-Kdo 糖苷45,两步收率63%。基于此Kdo 糖苷,脑膜炎奈瑟菌、流感嗜血杆菌、鼠疫杆菌和变形杆菌表面的LPS 核心结构被高效合成,用于免疫学研究[32-33]。
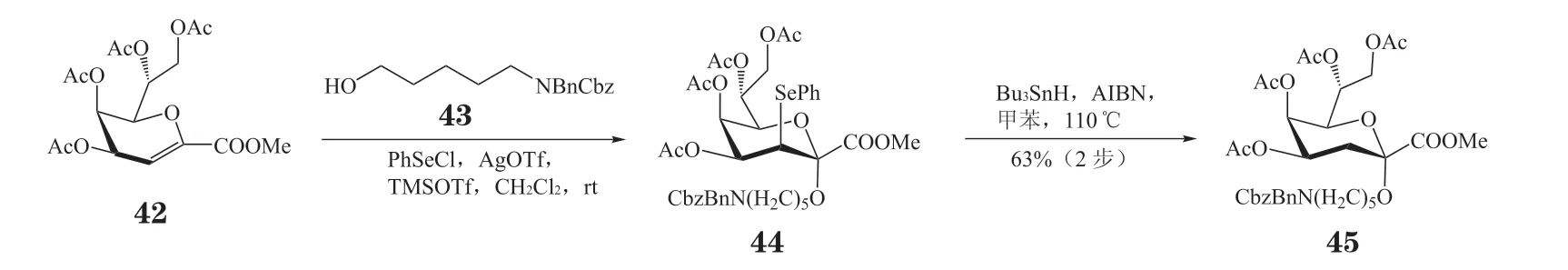
图9 利用Kdo 糖烯给体合成α-Kdo 糖苷Figure 9 Synthesis of α-Kdo glycoside with Kdo glycal donor
Tanaka 等[34]利用Kdo 糖烯与开环的Kdo 活性受体反应,合成了含有多个α-(2→8)-连接糖苷键的Kdo 寡糖分子51(见图10)。在NIS 和TfOH 的活化下,4、5、7、8 位苄基保护的Kdo 糖烯46 与开环的Kdo 受体47 反应,得到糖苷化产物48,收率89%,α/β比率大于95∶5。然后,在乙二酰氯((COCl)2)和AgOTf 的作用下发生环化和β-消除反应,得到二糖糖烯49。重复此两步反应过程,可进一步得到三糖糖烯50。最后,与葡萄糖受体发生糖苷化反应,并脱除所有保护基后,获得α-(2→8)-连接的Kdo 寡糖51。
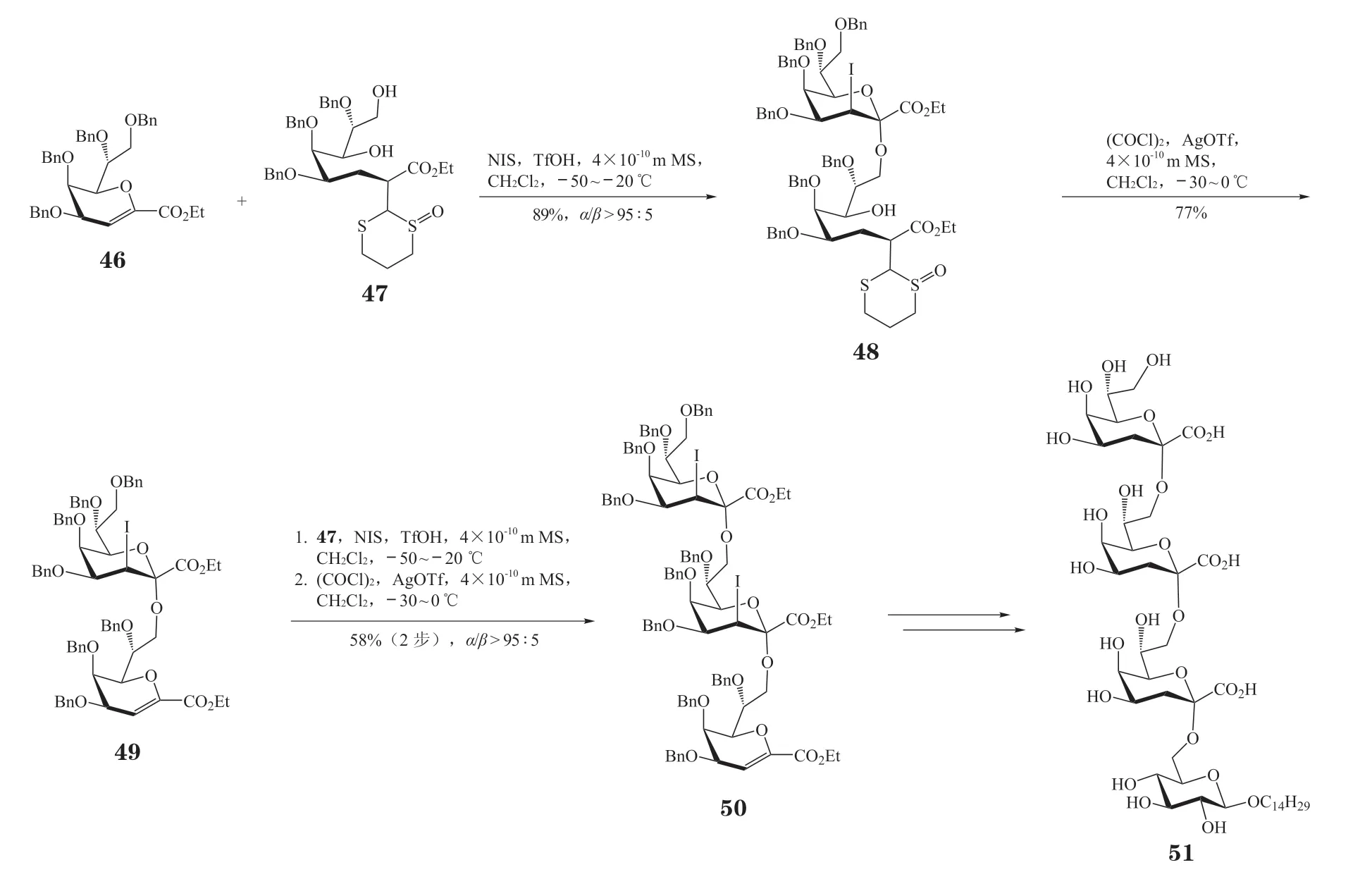
图10 利用Kdo 糖烯给体合成α-(2 →8)-连接的Kdo 寡糖Figure 10 Synthesis of α-(2 →8)-linked Kdo oligosaccharide with Kdo glycal donor
Pradhan 等[35]利 用4,5-O-丙 叉 保 护 的Kdo糖烯给体立体选择性合成了β-Kdo 糖苷(见图11)。4,5-O-丙叉保护基可能是通过对Kdo 糖烯给体的构象进行限制及其本身的空间位阻效应来实现Kdo 糖烯给体的β立体选择性糖苷化反应。首先,4,5-O-丙叉保护的Kdo 糖烯52 与甲醇在NIS和TMSOTf 的促进下,生成3 位碘代的β-Kdo 甲苷53。在相同条件下,双丙叉保护的Kdo 糖烯54 与53 反应,立体选择性生成β-(2→7)-连接的Kdo 二糖55,收率60%,非对映异构体比例(dr 值)约为10∶1。将55 转化为Kdo 受体56 后,与Kdo 糖烯54 再发生一次糖苷化反应,可得到β-(2→7)-连接的Kdo 三糖57,收率65%,dr 值约为10∶1。对三糖57 进行自由基脱碘反应,可得到苜蓿根瘤菌表面荚膜多糖重复单元相关的三糖骨架58。
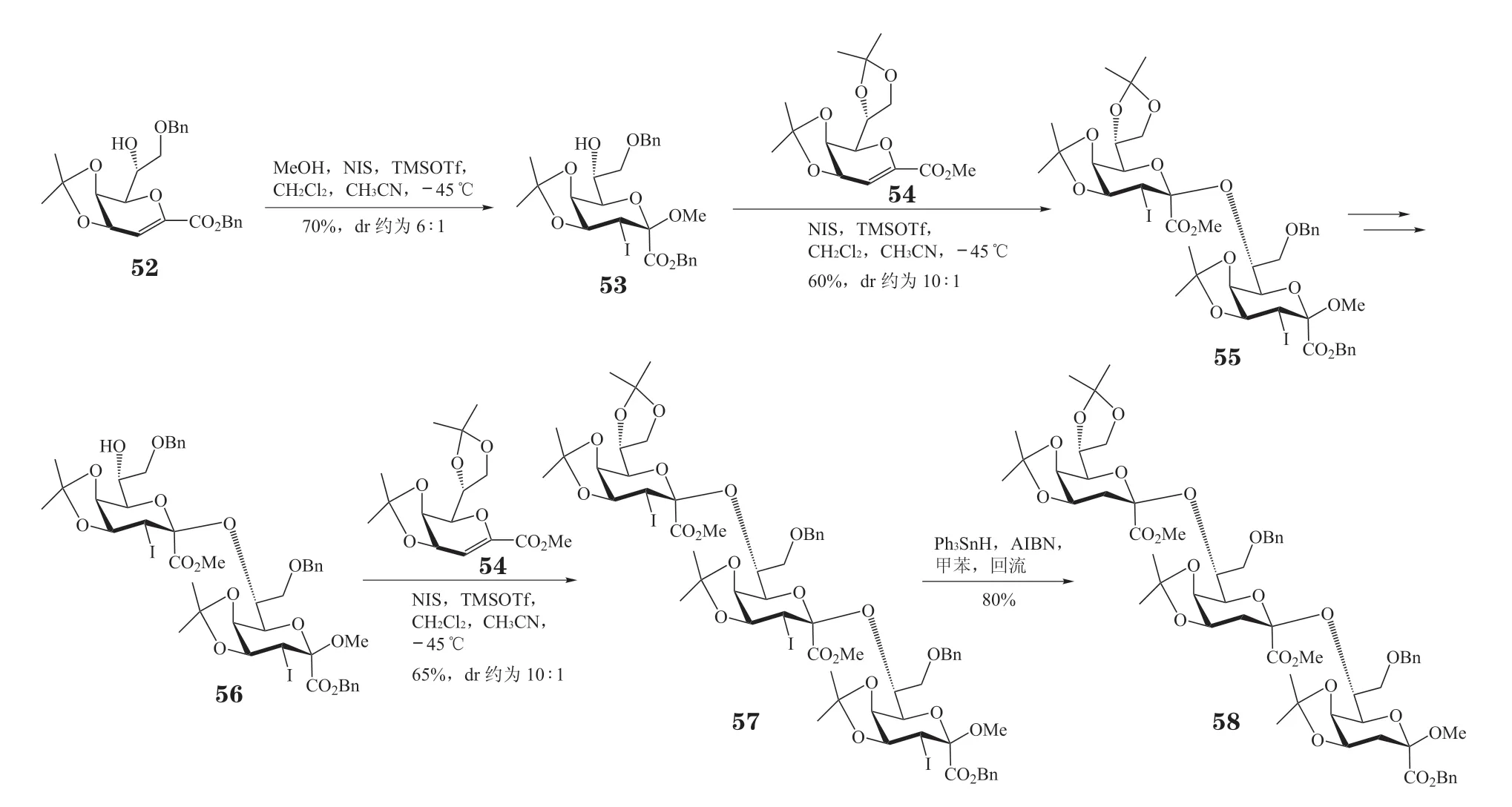
图11 利用Kdo 糖烯给体合成β-Kdo 糖苷Figure 11 Synthesis of β-Kdo glycoside with Kdo glycal donor
2.3 3-脱氧-D-甘露-2-辛酮糖酸硫苷给体
Kdo 硫苷给体与活性较低的糖苷化受体反应时容易发生消除反应,一般会生成α-和β-Kdo 糖苷的混合物。但一些研究表明,Kdo 硫苷与高活性的连接臂之间的糖苷化反应可用于构建β-构型Kdo 糖苷键[36-39]。
Solomon 等[40]报道了Kdo 二糖硫苷给体59 与氨基葡萄糖三糖受体60 在NIS 和TfOH 的促进下反应可得到五糖61,但产率中等(45%),基本没有立体选择性(α/β=1∶1)(见图12)。这一结果表明,当糖苷化底物变大时,糖苷化的选择性也会相应地变差。
Huang 等[41]利用5,7-O-二叔丁基硅基(DTBS)保护的Kdo 硫苷给体与不同类型受体进行糖苷化反应,均能立体选择性生成α-构型Kdo 糖苷,高效合成了衣原体LPS 相关的三糖骨架68(见图13)。在过氧化乙酸叔丁酯(TBPA)的促进下,5,7-O-DTBS 保护的Kdo 硫苷给体62 与烯丙醇反应,可以81% 的收率立体专一性生成α-Kdo 糖苷63。脱除3 位苯甲酰基得到Kdo 受体64 后,与5,7-O-DTBS 保护的Kdo 硫苷给体65 在TBPA的促进下反应,以72%的收率生成α-(2→4)-连接的二糖66。二糖66 在2,3-二氯-5,6-二氰对苯醌(DDQ)的作用下,氧化脱除其中的萘(Nap)保护基,获得二糖受体67。二糖受体67 与硫苷给体65 在NIS 和TfOH 的催化下发生糖苷化反应,可立体专一性生成α-Kdo 三糖68,收率为67%。尽管该给体制备略显繁琐,但此法也可被应用于多种不同连接方式的Kdo 二糖的合成中。基于此法,Zhou 等[42]还进一步合成了Kdo-α-(2→4)-[Kdo-α-(2→8)-]-Kdo 三 糖、Kdo-α-(2→8)-Kdo-α-(2→4)-Kdo 三 糖、Kdo-α-(2→4)-Kdo-α-(2→4)-Kdo 三 糖和Kdo-α-(2→4)-[Kdo-α-(2→8)]-Kdo-α-(2→4)-Kdo四糖。
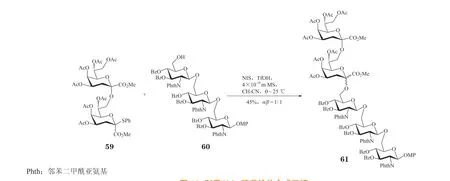
图12 利用Kdo 硫苷给体合成五糖Figure 12 Synthesis of a pentasaccharide with Kdo thioglycoside donor
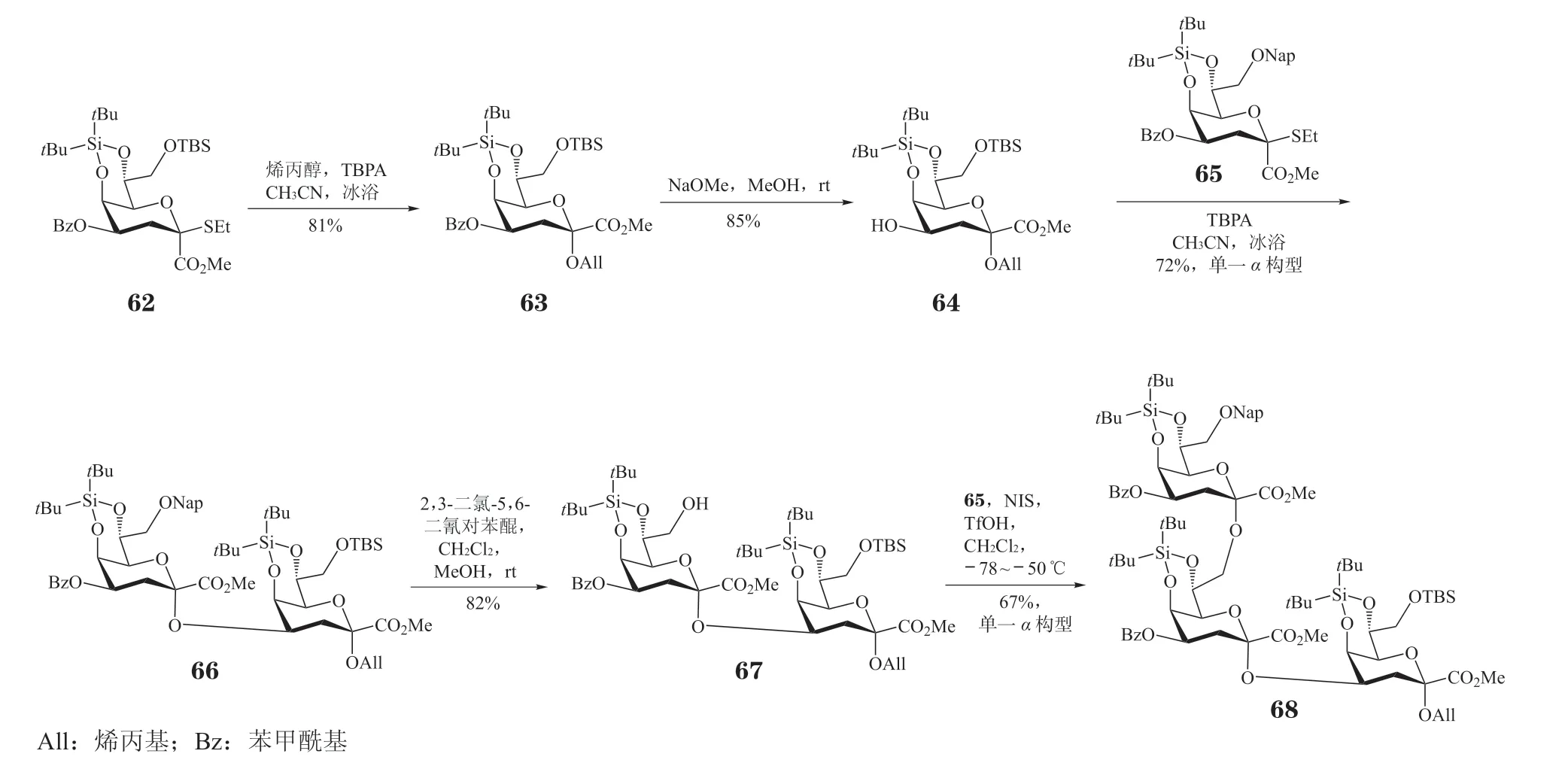
图13 利用Kdo 硫苷合成α-Kdo 三糖Figure 13 Synthesis of α-Kdo trisaccharide with Kdo thioglycoside donor
Huang 等[43]发现Kdo 分子5 位的取代基能够调节糖苷化反应的立体选择性。5-O-苯甲酰基或乙酰基保护的Kdo 硫苷给体的糖苷化产物以α选择性为主,而5-O-2-喹啉甲酰基(Quin)或5-O-4-硝基-2-吡啶甲酰基取代的Kdo 硫苷给体与伯醇反应,可立体专一性得到β-构型糖苷化产物。基于该方法,Huang 等完成了麦氏交替单胞菌ATCC 27126LPS 中三糖片段78 的合成(见图14)。在NIS 和TfOH的促进下,5-O-苯甲酰基保护的Kdo 硫苷给体69与三碳连接臂70 反应,可立体选择性得到α-Kdo糖苷71,收率为90%,α/β= 8∶1。将71 转化为受体72 后,与L-甘油-D-甘露庚糖硫苷73 在NIS 和TfOH 的活化下反应,以高产率高α-选择性得到二糖74。将74 上的硅基保护基脱除后得到化合物75,再在NIS 和TfOH 的促进下与5-O-Quin 保护的Kdo 硫苷给体76 反应,可立体专一性得到β-Kdo三糖骨架77,收率为88%。最后,脱除所有保护基后,获得目标三糖78。
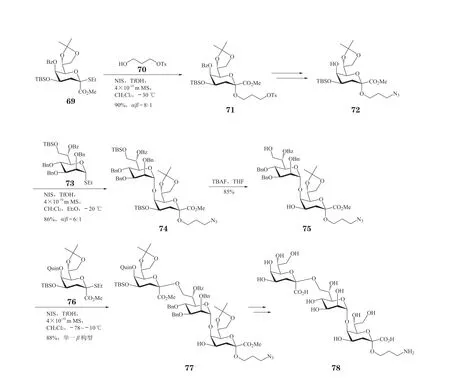
图14 利用Kdo 硫苷合成麦氏交替单胞菌ATCC 27126 脂多糖中三糖片段Figure 14 Synthesis of lipopolysaccharide trisaccharide fragment of Alteromonas macleodii ATCC 27126 with Kdo thioglycoside donor
2.4 3-脱氧-D-甘露-2-辛酮糖酸N-苯基三氟乙酰亚胺酯给体
相比于上述Kdo 卤苷和硫苷给体,KdoN-苯基三氟乙酰亚胺酯给体[44]发生糖苷化反应时一般仅需要催化量的促进剂,因而也受到了研究者的关注。Shimoyama 等[45-46]利用4,5-O-丙叉或4,5-di-O-TBS保护的KdoN-苯基三氟乙酰亚胺酯给体成功实现了α-Kdo 糖苷的合成,该4,5-O-丙叉或4,5-di-O-TBS保护基具有空间位阻效应,可以阻止糖苷化受体从Kdo 给体的β面进攻,从而有利于受体从给体的α面进攻,进而提高糖苷化反应的α-立体选择性。基于4,5-O-丙叉保护的Kdo 三氟乙酰亚胺酯给体,Shimoyama 等完成了幽门螺杆菌LPS 中Kdo-lipid A的合成(见图15)。在TBSOTf 的催化下,以环戊基甲基醚为溶剂,4,5-O-丙叉保护的Kdo 三氟乙酰亚胺酯给体79 与氨基葡萄糖二糖受体80 在微流反应体系中反应,以优秀的α-立体选择性得到Kdo 三糖81,收率为72%,α/β> 95∶5。课题组将化合物81 经过一系列官能团转化和脱保护操作后,得到目标三糖82 和83,用于免疫活性调节的研究。
2.5 3-脱氧-D-甘露-2-辛酮糖酸亚磷酸酯给体
Kdo 亚磷酸酯给体在Kdo 糖苷的合成中应用较少。Yi 等[21]利用4,5-O-丙叉保护的Kdo 亚磷酸酯给体84 与Kdo 受体85 在TMSOTf 的催化下反应,可得到α-(2→4)-连接的Kdo 二糖86,但产率较低(35%),选择性为α/β= 3.8∶1(见图16)。该糖基化反应中,亚磷酸酯给体仍然容易发生消除副反应,得到大量的糖烯。
2.6 3-脱氧-D-甘露-2-辛酮糖酸邻炔基苯甲酸酯给体
糖基邻炔基苯甲酸酯给体由于反应条件温和、促进剂用量少和底物适用范围广等优点而受到广泛的应用[47-48]。笔者所在课题组发展了金催化下Kdo邻炔基苯甲酸酯给体的β-立体选择性糖苷化反应,并将其应用在金格杆菌表面的Kdo 二糖抗原的合成中(见图17)[49-50]。首先,笔者所在课题组开发了一种制备一价金催化剂PPh3AuCl 的绿色合成方法[51]。然后,在该一价金催化剂衍生的三苯基膦金(Ⅰ)三氟甲磺酸盐(Ph3PAuOTf)的催化下,全乙酰基保护的Kdo 邻炔基苯甲酸酯给体87 与五碳连接臂43 反应,立体专一性生成β-Kdo 糖苷88,收率为80%。将化合物88 转化为5 位羟基的Kdo 受体89 后,氨基半乳糖N-苯基三氟乙酰亚胺酯给体90 与受体89在以TfOH 为催化剂、甲苯为溶剂的条件下反应,立体选择性得到β-(1→5)连接的氨基半乳糖-Kdo 二糖91,收率为89%,β/α= 3.3∶1。最后,经过脱保护操作,得到金格杆菌KK01 表面的β-Kdo 二糖抗原92。
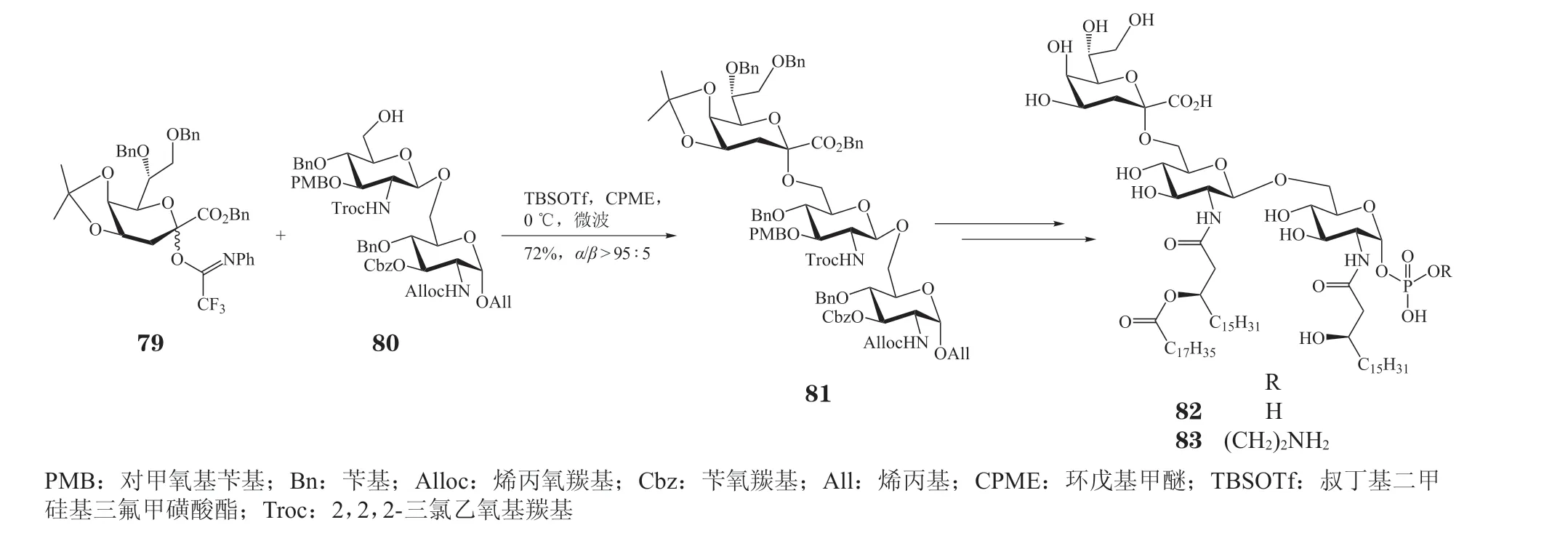
图15 利用Kdo N-苯基三氟乙酰亚胺酯给体合成Kdo-lipid AFigure 15 Synthesis of Kdo-lipid A with Kdo N-phenyl trifluoroacetimidate donor

图16 利用Kdo 亚磷酸酯给体合成Kdo 二糖Figure 16 Synthesis of Kdo disaccharide with Kdo phosphite donor
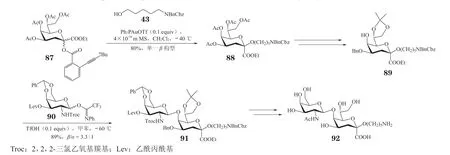
图17 利用Kdo 邻炔基苯甲酸酯给体合成金格杆菌KK01 表面的β-Kdo 二糖Figure 17 Synthesis of β-Kdo-containing disaccharide of Kingella kingae KK01 with Kdo ortho-hexynylbenzoate donor
在上述工作的基础上,笔者所在课题组希望能逆转该Kdo 糖苷化反应的立体选择性,从而实现用同一简单给体来构建α和β两种不同立体构型的Kdo 糖苷的目的。最近,我们建立了一种简单直接的方法,可通过外源性亲核试剂N,N-二甲基甲酰胺(DMF)来调节Kdo 的α-立体选择性,实现全乙酰化Kdo 邻炔基苯甲酸酯给体与多种受体的α-糖苷化反应,并将给体应用于α-连接的Kdo 二糖的潜伏-活化合成中(见图18)[52]。该方法无需安装复杂的保护基,通过全乙酰化的Kdo 邻炔基苯甲酸酯给体87 与异头位邻碘苯甲酸酯修饰的Kdo 受体93在以双(三氟甲磺酰)亚胺(2-二环己基膦-2',6'-二甲氧基-1,1'-联苯)金(I)(SphosAuNTf2)为促进剂、DMF 为添加剂的条件下发生糖苷化反应,可以79%的收率和α-立体选择性得到Kdo 二糖94(α/β>15∶1)。将化合物94 通过Sonogashira 偶联反应转化为Kdo 二糖邻炔基苯甲酸酯给体95 后,在相似的反应条件下与五碳连接臂43反应,能以93%的收率和α-立体选择性获得还原端含有五碳连接臂的Kdo 二糖96(α/β= 3∶1)。值得一提的是,通过低温核磁实验,笔者所在课题组首次成功检测到Kdo亚胺酯阳离子,合理地解释了DMF介导的α-Kdo糖苷的形成机制[52]。
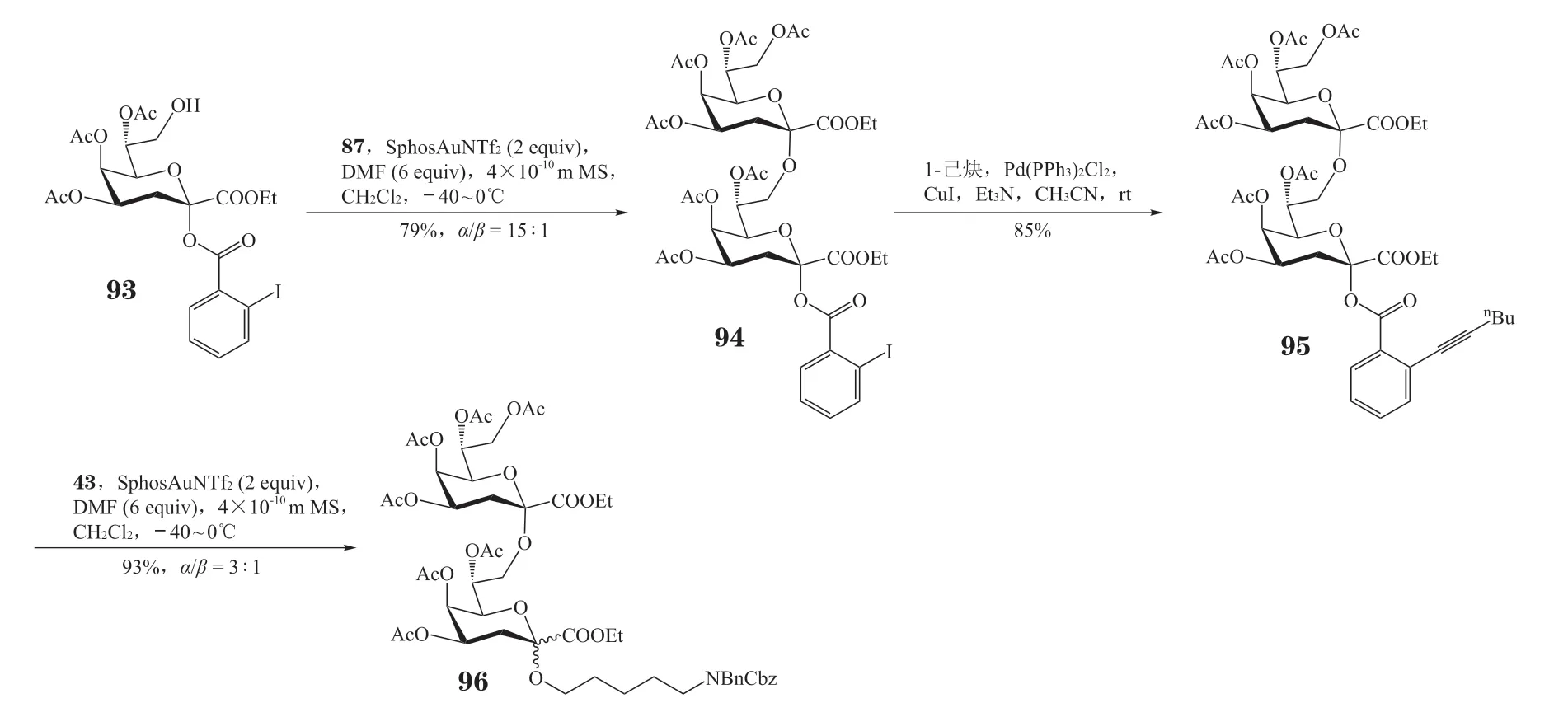
图18 利用Kdo 邻炔基苯甲酸酯给体合成α-Kdo 二糖Figure 18 Synthesis of α-Kdo disaccharide with Kdo ortho-hexynylbenzoate donor
2.7 其他方法
除上述方法以外,还有其他一些合成Kdo 糖苷的方法,但由于有较大的局限性而很少应用于复杂Kdo寡糖的合成中。Qian 等[53]用C-对甲氧基苯基的糖烯97 与甲醇在NIS 的作用下反应,β-立体选择性生成加成产物98,收率为87%(见图19)。由于4,5-O-丙叉阻止了NIS从β-面进攻,从而提高了糖苷化反应的β-选择性,仅形成4%的α-异构体。然后,98 经自由基脱碘反应得到99,随后对甲氧基苯基被氧化生成羧基,以较好的收率得到β-构型的Kdo 糖苷100。
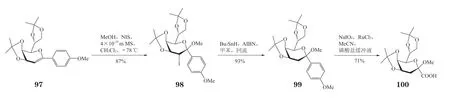
图19 基于1 位碳芳基糖烯合成β-Kdo 糖苷Figure 19 Synthesis of β-Kdo glycoside with 1-C-aryl glycal donor
3 结语
然而,Kdo 寡糖的合成仍然存在较大的困难,如在糖烯的形成、复杂给体的制备、低活性受体的糖苷化、立体构型的控制等方面还无法给出令人满意的解决方案。为解决上述问题,新型简单高效的Kdo 糖苷化方法和策略亟需被开发出来,用于Kdo 寡糖的高效合成和免疫活性评价。
Kdo 是细菌细胞壁的重要组成成分,开展Kdo寡糖的合成及生物活性评价对于基于Kdo 的药物研发具有重要的意义。目前已开发了多种类型的Kdo糖苷化给体,如Kdo 溴苷、氟苷、糖烯、硫苷、N-苯基三氟乙酰亚胺酯、亚磷酸酯和邻炔基苯甲酸酯等,用来立体选择性合成α-和β-构型的Kdo 寡糖。
