单克隆B淋巴细胞增多伴肾功能不全
2020-08-06王霞左科程震
王 霞 左 科 程 震
病史摘要
现病史57岁男性患者,因“血压升高伴肾功能减退2年”于2018-09-14入院。患者2016年9月体检测血压148/90 mmHg,尿常规尿蛋白++、隐血+++,进一步检查尿蛋白定量2.6 g/24h,血清肌酐(SCr)181.2 μmol/L,尿酸602.4 μmol/L,血常规:血红蛋白(Hb) 106 g/L,淋巴细胞百分比 38.2%,淋巴细胞绝对值 2.1×109/L,外院先后予缬沙坦胶囊、厄贝沙坦、金水宝、海昆肾喜胶囊、尿毒清颗粒保肾治疗,血压控制平稳,蛋白尿无缓解,SCr稳定。2018年7月复查血生化示SCr 206.9 μmol/L,尿酸455 μmol/L,血钾5.7 mmol/L,尿蛋白定量2.6 g/24h,尿隐血+++,Hb 110 g/L,淋巴细胞百分比 41.8%,淋巴细胞绝对值 3.3×109/L。9月10日至国家肾脏疾病临床医学研究中心门诊,测血压123/75 mmHg、心率73次/min,查尿蛋白定量2.4 g/24h、尿红细胞计数85.4/μl,白蛋白40.5 g/L、SCr 182.1 μmol/L、尿酸475 μmol/L、三酰甘油0.68 mmol/L、总胆固醇3.24 mmol/L、乳酸脱氢酶138 U/L、钾5.76 mmol/L,Hb 118 g/L,淋巴细胞百分比 57.1%,淋巴细胞绝对值 4.18×109/L、甲状旁腺激素20.38 pg/ml,B超双肾125 mm/115 mm、皮髓界限清楚。病程中患者精神、饮食、睡眠可,大便正常,无夜尿增多,无皮疹、关节痛,体重近1年下降5 kg。
既往史平素身体一般,否认肝炎、结核、疟疾等传染病史,否认手术史,否认外伤史,否认输血史,自诉无食物过敏史。对“罗红霉素”过敏、表现为皮肤瘙痒,预防接种史不详。
个人史及家族史吸烟20年,约5支/d。酒龄15年,每次150 ml,已戒酒2年。父亲74岁因“颅脑肿瘤”去世,母亲已故、生前有“高血压、糖尿病”病史。
体格检查身高167 cm,体重60 kg,体质量指数(BMI) 21.5 kg/m2,血压113/72 mmHg,神清,精神可,浅表未触及肿大淋巴结;心肺未及明显异常;腹软,无压痛及反跳痛,脾肋下2横指、质软地,肝肋下未触及,双下肢无水肿。
实验室检查
尿液 尿蛋白2.23 g/24h,尿红细胞231.5/μl、非均一型,C3 2 mg/L、α2巨球蛋白(α2-MG)2 mg/L,NAG 8.7 U/(g·Cr),RBP 0.6 mg/L,Lys<0.5 mg/L,NGAL 16.6 ng/mL,尿渗量341 mOsm/(kg·H2O)。
血液 WBC 7.1×109/L,L 63.1%,N 33.52%,Hb 108 g/L,PLT 118×109/L、CRP<0.5 mg/L。白蛋白36.9 g/L,球蛋白27.4 g/L,前白蛋白285 mg/L,尿素15.6 mmol/L,SCr 188.3 μmol/L,尿酸551 μmol/L,三酰甘油0.76 mmol/L,总胆固醇2.79 mmol/L,HDL-C 0.71 mmol/L,LDL-C 1.9 mmol/L,葡萄糖4.86 mmol/L,钾5.18 mmol/L、钠143.7 mmol/L、氯109.7 mmol/L、钙2.22 mmol/L、磷1.51 mmol/L、总二氧化碳24 mmol/L,eGFR(CKD-EPI)33 ml/(min·1.73m2)。脑利钠肽前体56.7 pmol/L、降钙素原0.08 μg/L、IL-6 4.03 ng/L。叶酸>6.8 nmmol/L、维生素B12 212 pmol/L,铁蛋白59.7 μg/L。
免疫学检查 IgA 2.32 g/L、IgE<20 IU/ml、IgG 15.6 g/L、IgM 1.79 g/L、RF<20 IU/ml、补体C3 0.935 g/L、补体C4 0.242 g/L、ASO 30.3 IU/ml、外周血T细胞:CD3+1 104个/μl、CD4+923个/μl、CD8+191个/μl、CD20+1 420个/μl。ANA 1∶ 128、抗ds-DNA、MPO阴性。血游离轻链:κ链194 mg/L、λ链64.40 mg/L、κ/λ比值3.01。免疫固定电泳未见单克隆免疫球蛋白条带。肿瘤标志物:细胞角蛋白19片段5.50 ng/ml、鳞状细胞癌相关抗原2.89 ng/ml、β2微球蛋白7.10 mg/L。自身免疫性coomb’s试验阴性。先令氏分类分叶核41、成熟淋54、异淋1。
辅助检查胸部CT:左肺上叶小结节;两肺轻度肺气肿;纵隔内及双侧腋窝多发小淋巴结;双侧胸膜稍增厚;脾脏明显增大。全腹部CT:肝右叶散在囊肿;右肾小囊肿;脾大,腹盆腔及腹膜后多发大小不等淋巴结;腹部侧位片:腰椎轻度退行性变。心脏彩超:房间隔所见待排卵圆孔未闭,EF 58%。颈部血管彩超:左侧颈总动脉球部前壁硬斑形成。CT冠状动脉钙化积分0分。 眼底检查:视乳头边界清、黄斑区视网膜正常,眼底动脉无硬化。
其他骨髓细胞学检查:大致正常骨髓像。骨髓流式:正常浆细胞占0.25%、异常浆细胞占0.02%。肿瘤细胞免疫分型(骨髓):淋巴细胞约占有核细胞的36.5%,其中B淋巴细胞约占淋巴细胞的78%,表达HLA-DR、CD5、CD19、CD20、CD22、sKappa(dim)。检测到免疫球蛋白(Ig)的IgVH和IGK基因发生重排。
肾活检病理
免疫荧光 IgG++、IgA trace、IgM trace、C3++、C1q+,呈颗粒状弥漫沉积于系膜区及血管袢。κ 轻链+、λ 轻链+,呈颗粒状弥漫沉积于系膜区及血管袢。IgG亚型染色:IgG3++,呈颗粒状弥漫沉积于系膜区及血管袢。IgG1、IgG2、IgG4阴性(图1)。
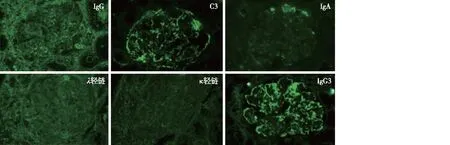
图1 免疫荧光见IgG++、IgA trace、C3++、κ轻链+、λ轻链+、IgG3++,呈颗粒状弥漫沉积于肾小球系膜区及毛细血管袢
光镜 36个肾小球中8个球性废弃,1个纤维细胞性新月体。余正切肾小球体积增大,增生分叶状(图2A),系膜区重度增宽,系膜细胞增殖伴基质增多,较多内皮细胞成对,单个核细胞及中性粒细胞浸润5~15个/球。PASM-Masson:肾小球系膜区、内皮下、上皮侧偶见嗜复红物沉积,较多外周袢分层(图2B)。肾小管间质中度慢性病变,间质灶性单个核细胞浸润并灶性聚集(图2C)。动脉未见明确病变。
肾间质炎性细胞浸润间质平均细胞数目(mm2)B细胞640 个/mm2,CD3 528 个/mm2、CD4 244 个/mm2、CD8 284 个/mm2,CD68 648 个/mm2,CD138 12 个/mm2。
电镜 电镜下观察2个肾小球,系膜区明显增宽,系膜细胞及基质增多,系膜区节段高密度电子致密物沉积。肾小球毛细血管袢开放尚可,袢腔内偶见内皮细胞成对,节段系膜插入、新的基膜形成,偶见内皮下区域增宽、疏松、基膜内皮下节段电子致密物沉积,上皮侧散在高密度电子致密物沉积(图2E),高倍镜下未见特殊结构(图2F)。肾小球基膜厚380~590 nm。肾小球足细胞足突融合约60%~70%。肾间质灶性单个核细胞浸润。
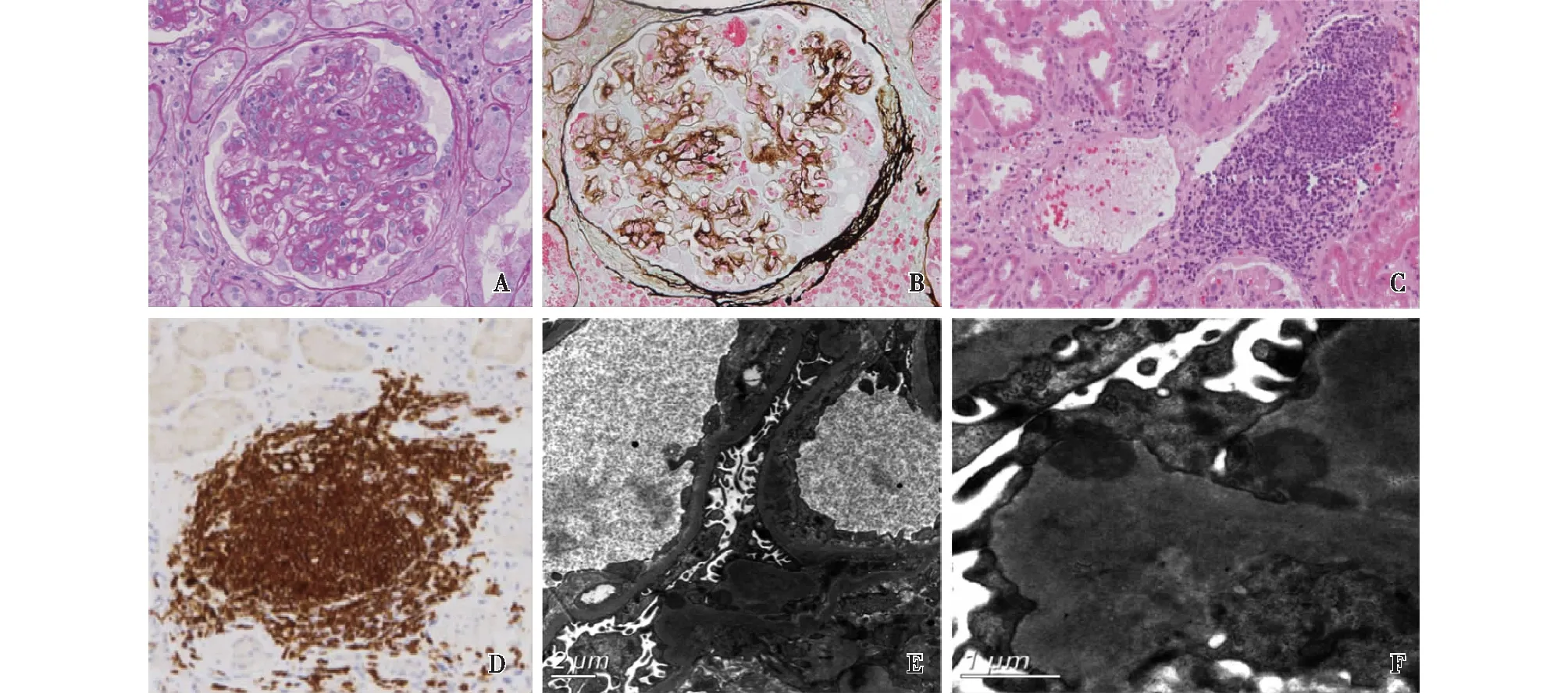
图2 A:肾小球增生分叶状,系膜区中~重度增生,较多内皮细胞成对,单个核细胞及中性粒细胞浸润(PAS,×400);B:肾小球系膜区、内皮下、上皮侧偶见嗜复红物沉积,较多外周袢分层(PASM-Masson,×400);C:肾间质灶性单个核细胞浸润并灶性聚集(HE,×400);D:CD20+细胞灶性聚集(IH,×400);E~F:肾小球毛细血管袢基膜内皮下节段电子致密物沉积,上皮侧散在高密度电子致密物沉积(EM)
诊疗分析病史特点:(1)中年男性;(2)起病隐匿,临床表现尿检异常伴血压、SCr升高;(3)轻度贫血,淋巴细胞比例升高,血小板轻度降低;(4)脾脏肿大,浅表未触及浅表淋巴结;(5)起病1年内体重降低5 kg;(6)血清游离轻链比值异常: κ链194 mg/L、λ链64.40 mg/L、κ/λ 3.01、免疫固定电泳未见异常;(7)外周血可见异常淋巴细胞、淋巴细胞CD20+显著升高、CT示多处深部淋巴结肿大:纵隔内及双侧腋窝多发小淋巴结;腹盆腔及腹膜后多发大小不等淋巴结;(8)骨髓免疫组化及免疫分型提示成熟B淋巴细胞增殖。(9)肾活检提示肾小球膜增生性病变伴单克隆IgG3沉积,肾间质较多CD20浸润。诊断需排除B细胞慢性淋巴增殖性疾病,临床应如何诊断及鉴别诊断?B细胞慢性淋巴增殖性疾病是否是肾小球膜增生性病变的病因呢?
本例患者血淋巴细胞计数升高、脾肿大、腹盆腔及腹膜后淋巴结肿大,骨髓免疫分型淋巴细胞约占有核细胞的36.5%,其中B淋巴细胞约占淋巴细胞的78%,表达HLA-DR、CD5、CD19、CD20、CD22、sKappa(dim)成熟B淋巴细胞增殖,且存在IgVH和IGK基因发生重排。诊断考虑B细胞慢性淋巴增殖性疾病-不能分类(B cell chronic lymphoproliferative disease,B-CLPD-U)。文献报道B淋巴细胞增殖性疾病可引起蛋白尿、急性肾损伤,病理上常见肾小管弥漫淋巴细胞或浆细胞浸润[2],肾脏其他病理改变类型包括AL淀粉样变性、冷球蛋白血症相关肾损害、伴单克隆免疫球蛋白沉积的增生性肾小球肾炎、单克隆免疫球蛋白沉积病(MIDD)、轻链肾小管病、血栓性微血管病等。该患肾活检光镜下表现为肾小球膜增生性病变,免疫荧光单一IgG3沉积,电镜下无特殊结构。肾间质CD20+细胞浸润,肾脏病变高度考虑继发于淋巴细胞增殖性疾病。
最后诊断(1)伴单克隆IgG3沉积的膜增生性肾小球肾炎 CKD 3期 ;(2) B-CLPD-U。
治疗及随访明确诊断后于9月26日给予利妥昔单抗375 mg/m2(600 mg),半年后给以小剂量利妥昔单抗100 mg治疗(2月28日、6月28日、9月22日),辅以降压、纠正贫血保肾等对症支持治疗,9月27日复查CD20+由1 421.00个/μl降至5个/μl,SCr降至132.6 μmol/L,血淋巴细胞比例降至26.27%,随访13个月,SCr 105.2 μmol/L,CD20+37个/μl,血淋巴细胞比例26.6%,复查腹部CT未见脾肿大(表1)。

表1 临床指标治疗前后的变化
讨 论
B-CLPD是一组累及外周血和骨髓的成熟B细胞克隆增殖性疾病。其共同的临床特征,好发中老年人,临床进展缓慢、多数呈惰性病程,可向侵袭性淋巴瘤转化,治疗后可缓解、但难以治愈。B-CLPD诊断与鉴别诊断一直是临床工作中的难点,依据《B细胞慢性淋巴增殖性疾病诊断与鉴别诊断中国专家共识(2018年版)》[1]可以从临床特征、通过流式细胞术确认B细胞单克隆性、淋巴结或脾脏等组织病理学以及骨髓细胞形态学及骨髓病理检查中肿瘤细胞浸润模式、免疫组织化学染色(IHC)、免疫分型四个方面进行诊断和鉴别诊断。其中临床有明显淋巴结肿大、白细胞显著升高且成熟淋巴细胞为主常见慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)、套细胞淋巴瘤(MCL)、滤泡淋巴瘤(FL)、边缘区淋巴瘤(MZL),而淋巴浆细胞淋巴瘤(LPL)/华氏巨球蛋白血症(WM)患者往往脾脏和淋巴结肿大都不明显。毛细胞白血病(HCL)和LPL/WM患者常白细胞正常或降低,少数升高,多见贫血和血小板减少。B-CLPD分类的诊断必须依赖流式细胞检测:表达成熟B细胞相关抗原(CD19、CD20、CD22)和表面免疫球蛋白(sIg)单一轻链(κ或λ);存在免疫球蛋白重链(IgH)和(或)轻链(IgL)基因重排。但该检查价格昂贵,国际上也是近10余年来才常规应用于临床检验,因此不做该检查容易导致漏诊误诊。少数患者外周血淋巴细胞计数低于5×109/L,且无淋巴结明显肿大,WHO把其列为“单克隆淋巴细胞增多症(MBL),并认为该疾病尽管暂不属于B-CLPD范畴,但部分患者可进展至CLL或者MZL[2]。
B-CLPD常常并发肾脏损害,但行肾活检明确诊断的病例不多,相关文献较少,多为个案报道,包括肿瘤细胞浸润、单克隆免疫球蛋白沉积或由于特异性细胞因子或不均衡淋巴细胞亚群的过度增殖导致的免疫功能紊乱。不同亚型并发肾脏损害的发生率尚不清楚,来自血液恶性肿瘤的尸检的数据[3-5]表明34%的患者发现异常淋巴细胞在肾脏浸润,其中低分化和高分化非霍奇金淋巴瘤浸润的比例为10%和50%,而在慢性淋巴细胞白血病(CLL)中肾实质淋巴细胞浸润比率63%,有的文献报道高达93%。合并肾脏损伤多见于多发性骨髓瘤、华氏巨球蛋白血症和非霍奇金淋巴瘤。大多数患者存在急性肾损伤、可表现为肾病范围蛋白尿、少数患者表现为急进性肾炎综合征。肾脏病理改变包括肾淀粉样变性、膜性肾病、膜增生性肾小球肾炎、冷球蛋白血症相关肾损害及管型肾病、轻链肾小管病等[6]。B-CLPD导致肾脏损伤的可能机制为大量单克隆B淋巴细胞在肾实质的恶性浸润导致肿瘤细胞直接损伤和B淋巴细胞分泌的致病性单克隆免疫球蛋白对肾脏的毒性作用。
Javaugue等[7]通过回顾性分析了52例经肾活检诊断的恶性B淋巴细胞浸润引起的肾脏损害,其中21例为华氏巨球蛋白血症、11例慢性淋巴细胞白血病、8例弥漫大B细胞淋巴瘤,其他未分类淋巴瘤11例,1例多发性骨髓瘤,所有的患者均接受化疗,长期预后差,5年总的生存率为60%,而影响总的生存率的因素主要为肾脏对化疗反应的高低,而肾小球硬化程度、肾脏体积、血液学反应是肾脏反应的决定因素,同样肾小球硬化程度、肾脏体积,故在诊断及预后评估中应该系统的评估肾脏病理改变。
Mayo医学中心一项关于CLL和B-CLPD肾脏并发症研究表明[8],常见的肾脏损伤表现为肾功能不全和或肾病综合征,常见的病理改变为膜增生性肾小球肾炎、慢性淋巴细胞白血病间质浸润、血栓性微血管病和微小病变。其中5例膜增生性肾小球肾炎接受利妥昔单抗、环磷酰胺-泼尼松龙和泼尼松为基础的方案治疗肾功能恢复。本例就诊时未达到CLL诊断标准,但因存在肾功能不全、肾脏病理提示膜增生性肾小球肾炎,免疫荧光IgG3沉积,电镜下未见特殊的结构,肾间质CD20+细胞浸润,故不除外淋巴细胞浸润引起的肾脏损害,查阅文献报道利妥昔单抗治疗B-CLPD有效[9],故给予利妥昔单抗治疗,随访13个月,SCr恢复,证实肾脏损伤的病因为B-CLPD。
小结:本例患者临床表现为血压升高伴尿检异常伴肾功能减退,外周血淋巴细胞增多,脾大,肾活检提示肾小球膜增生性病变伴单一IgG3沉积、肾间质多灶性CD20+细胞浸润,结合骨髓流式、免疫分型诊断最终考虑伴单克隆IgG3沉积的膜增生性肾小球肾炎、B-CLPD-U,给予利妥昔单抗治疗,肾功能恢复、尿蛋白下降。因此对于伴单克隆免疫球蛋白沉积的增生性肾小球肾炎,B细胞慢性淋巴增殖性疾病需要排除,做到及时诊断和治疗,避免漏诊和误诊。
