以肠套叠为首发表现的儿童非霍奇金淋巴瘤8例
2020-08-04潘俊涛崔西春张春英范应中王家祥
潘俊涛,张 大,崔西春,张 蛟,张春英,谢 潭,范应中,王家祥
郑州大学第一附属医院小儿外科 郑州 450052
肠套叠指肠管的一段收缩或内陷到邻近肠腔,常见于3岁内的儿童[1],是婴儿常见的急腹症之一。典型的临床表现包括间断性哭闹或腹痛、呕吐、腹部肿块和血便[2],延迟诊断和治疗可导致肠坏死甚至死亡。约90%为原发性肠套叠,除回肠末端淋巴组织增生外,无明显病因。其余为继发性肠套叠,套入的头部为一器质性病变,主要包括梅克尔憩室、肠重复囊肿、肠息肉和肠恶性淋巴瘤[3]。非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)是儿童时期常见的肿瘤,临床表现缺乏特异性,多数患儿起病隐匿,表现为非特异性的胃肠道症状,以腹部包块、腹痛、腹部不适、体重减轻、纳差、恶心、呕吐等症状较为常见。在少数情况下,NHL可表现为肠套叠,肿瘤可以在复位后发现,也可以在手术复位失败切除局部病变时发现,NHL诊断极为困难,术前误诊率极高。本研究回顾分析了8例以肠套叠为首发表现的NHL患儿的临床特征,报道如下。
1 对象与方法
1.1研究对象郑州大学第一附属医院2013年1月至2018年12月收治的以入院诊断为“肠套叠”、出院诊断包含“淋巴瘤”的8例患儿为研究对象。排除术中证实为肠道肿块而并非肠套叠的患儿。所有患儿均初次诊断为NHL。
1.2资料收集收集患儿性别、年龄、病程、临床表现、既往病史、肿瘤外观及部位、手术方式、术后并发症、术后化疗情况、化疗后评估结果及目前生活状况等资料。
1.3手术及病理所有患儿均先由门诊或急诊超声检查诊断,并试行空气灌肠复位,8例均空气灌肠复位失败,并提示“同心圆征”,即行急诊剖腹探查术。 8例患儿中,1例位于回盲部,行回盲部切除肠吻合术;7例位于回肠末端,行局部回肠切除肠吻合术。 术后标本进行HE染色和免疫组化染色。
1.4NHL分期方法术后标本参照胃肠道淋巴瘤Lugano分期系统[4]进行分析。
1.5化疗所有患儿均在病理明确诊断后按儿童NHL诊疗方案[5]进行化疗。
1.6随访采用门诊及电话随访,电话随访每3个月1次,术后第1、3、6个月和第1、2、5年至门诊复查。随访内容包括化疗情况、化疗后评估结果及目前生活状况。
2 结果
2.1一般资料8例患儿中男7例,女1例;年龄2.5~9.0岁。反复肠套叠史者1例,首次急性发作者7例。患儿的一般资料见表1。
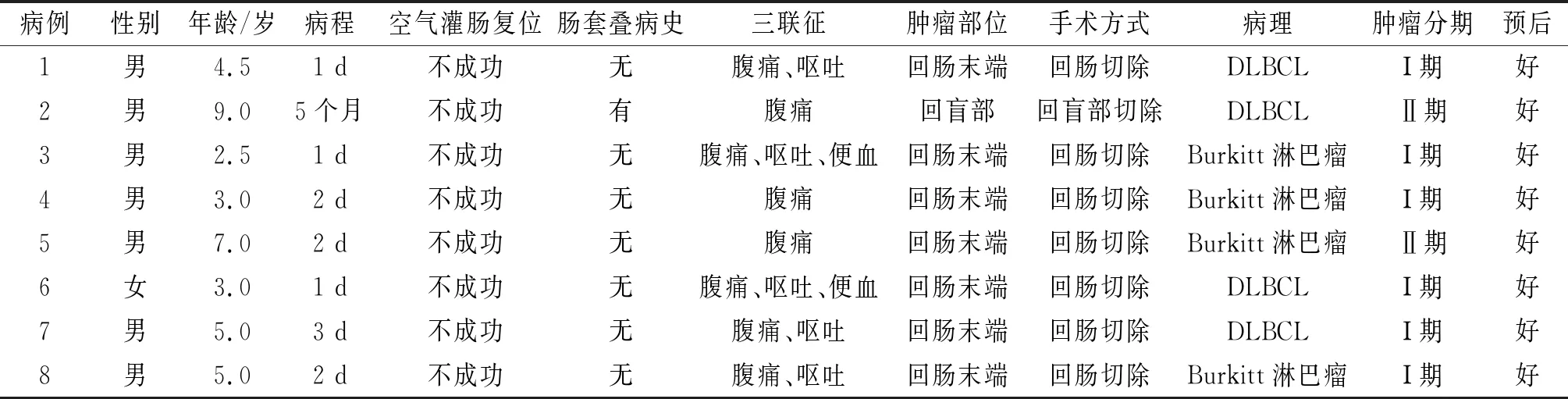
表1 8例患儿的一般资料
2.2手术情况8例均有不同程度的肠壁增厚,肿瘤均位于回盲部附近,其中6例肿瘤位于回肠末端,呈类圆形,质硬,边界清,两侧肠壁常伴有凹陷,直径小于5 cm,见图1A;1例肿瘤位于回盲部,回肠末端及回盲部与大网膜粘连,直径达6 cm,圆形,水肿明显,鱼肉状,质脆、易出血,可见多个肠系膜淋巴结肿大,见图1B;另1例无异常包块存在,仅表现为末端回肠套叠肠壁增厚,异常僵硬,周围散在点状白色可
疑坏死灶。8例均成功行局部病灶切除术,术后恢复良好,未发现肠梗阻、吻合口瘘和吻合口狭窄等。
2.3术后病理组织学结果见图2。DLBCL 4例,免疫组化结果:BCL-6(+),CD3(+),CD43(+),CD79α(+),CD20(+),CD99(+),Ki-67(+),P53(+),PAX-5(+);Burkitt淋巴瘤4例,免疫组化结果:Bcl-6(+),CD10(+),CD163(+),CD20(+),CD43(+),CD79α(+),CD99(+),Ki-67(+),P53(+),PAX-5(+),Vimentin(+)。
2.4随访结果所有患儿随访9~71个月,未发现有肿瘤复发者,3 a无病生存率为100%。

A:回肠末端1例;B:回盲部1例
3 讨论
NHL是一种常见的儿童肿瘤,30%~40%的病例腹腔内受累[5]。因肠套叠发作继而发现肠道淋巴瘤较为罕见[6],临床表现包括腹痛、呕吐和下消化道出血等[6-7],有时可以触到腹部肿块。在复发性肠套叠的病例中,NHL可能会有一个无症状的过程,最终发现时显示其已处于晚期,开始引起主要并发症,如肠梗阻、胃肠道出血甚至肠坏死[8]。另外,患儿可能出现非典型症状,包括腹痛、便秘、低烧和长期疲劳等[5-6],需要结合腹部CT、结肠镜、消化道造影、甚至腹腔镜检查等排除腹腔内淋巴瘤。本组2例患儿表现为典型的肠套叠三联征,3例表现为腹痛、呕吐,3例仅表现为腹痛;超声均提示“同心圆征”,诊断性空气灌肠复位均未成功,这些均给诊断带来困难,单纯依靠症状、体征和常规检查常常误诊。因此,对于3岁以上儿童的肠套叠,尤其是复发性肠套叠,应高度怀疑继发性肠套叠可能,以免造成诊断上的延误。
胃肠道是原发性结外NHL最常见的受累部位。小肠淋巴瘤占所有NHL的4%~20%,占原发性胃肠道淋巴瘤的20%~54%[9],85%的原发性胃肠道淋巴瘤和60%~80%的肠淋巴瘤是B细胞型[10]。本组以肠套叠为首发的NHL均处于回肠末端或回盲部,病理诊断均为B细胞淋巴瘤,其中Burkitt淋巴瘤4例, DLBCL 4例。有研究[11]显示症状持续时间长和体重下降是存在胃肠道淋巴瘤的两个重要线索。本研究中仅1例病程较长,8例均无体重下降,可能是因为8例患儿均为急诊入院,且均处于疾病早期的缘故。
腹部肠道NHL是否手术治疗仍有争议。儿童B细胞NHL的治疗,最初强调早期去肿瘤术后化疗,随着对NHL认识不断深入及化疗方案的合理化,目前认为化疗是最有效的手段[12],可通过避免手术或减少手术并发症来提高晚期疾病的生存率[13]。对于NHL继发肠套叠的患儿,手术的主要目的是解除急腹症,同时取得病理诊断,以便于确诊后及时化疗。如果在腹部探查中发现单部位的肠道肿瘤,建议切除这种病变,因为该病变一般处于Ⅰ期或Ⅱ期,技术上是可行的,避免了对肿瘤的广泛操作,同时还提供了明确的组织学诊断,并消除了术后进行强化化疗的必要性。如果在腹部探查过程中发现广泛的病变,判断该病变可能处于Ⅲ期以上,考虑到这些手术的高并发症发生率和死亡率,最好避免完全切除,甚至避免去除原发性肿瘤的任何尝试,因为它不会对患儿的总体生存率产生益处[14]。本组患儿2例肿瘤分期Ⅰ期,其余6例为Ⅱ期,术后经病理明确诊断后行规范化疗,随访未发现有肿瘤复发者,3 a无病生存率为100%。本研究中患儿的无病生存率较高,考虑与该疾病的早期发现、早期诊断、早期完整切除病灶、早期规范治疗有关。
本研究中1例Ⅰ期患儿术中手术复位后可见套叠肠壁增厚明显,同时肠壁异常僵硬,触之如革,且周围散在白色点状可疑坏死灶,考虑迟发性肠坏死穿孔可能性较大,术中行局部肠管切除术,术后病理确诊为Burkitt淋巴瘤,行规范化疗,效果满意。由此可见,肠道淋巴瘤早期可能不出现肿块或肿大淋巴结,而仅表现为异常僵硬或异常增厚。这给小儿外科医生带来了新的挑战。我们认为,对于肠套叠儿童,如果手术复位后套叠肠管的肠壁异常坚硬,应对该肠管进行热敷,热敷后仍异常坚硬者,应切除局部可疑病变进行组织学检查,以免漏诊误诊。
综上所述,对于肠套叠患儿,特别是年龄较大或有反复发作肠套叠的,应注意由NHL引起继发性肠套叠的可能。如术中发现肠壁包块或肠壁异常僵硬,应切除局部病变进行病理学检查,避免漏诊误诊,并在确诊为NHL后及时化疗,预后多良好。
