101例药物性肝损伤患者的临床特征分析*
2020-07-29陆云飞陈晓蓉
时 佳 陆云飞 陈晓蓉
上海市公共卫生临床中心中西医结合科 (上海,201508)
药物性肝损伤(DILI)是指由各类处方或非处方的化学药物、生物制剂、传统中药、天然药、保健品、膳食补充剂及其代谢产物乃至辅料等所诱发的肝损伤[1],可表现为无症状性肝功能异常、急慢性肝炎,重者可致急性肝衰竭甚至死亡[2,3]。已知全球有1 100多种上市药物具有潜在肝毒性,涉及临床用药各个方面,临床用药的安全性问题日益凸显。本文回顾性调查分析了我院收治的DILI患者的临床资料,寻找其发病特点和临床规律,为防治DILI提供参考依据。
1 资料与方法
1.1 研究对象 收集2017年1月至2018年5月于上海市公共卫生临床中心住院治疗的DILI患者101例,诊断治疗标准参照中华医学会肝病学分会药物性肝病学组2015年制定的《药物性肝损伤诊治指南》[1]。
1.2 研究方法 采用回顾性调查方法,查阅住院病历,根据诊断标准记录药物种类、剂量、给药途径、症状出现时间、既往有无肝病临床症状、体征、实验室检查(血、尿常规,肝、肾功能,嗜酸性粒细胞计数)等。采用化学发光法检测肝功能(雅培公司);采用SYSMES-Xn1000血球仪 (日本希森美康公司) 及其配套试剂检测血常规。

2 结果
2.1 DILI患者一般情况 101例DILI患者中男52例,占51.49%;女49例,占48.51%。年龄14~86岁,平均(53.30±14.67)岁。患者年龄分布见表1。
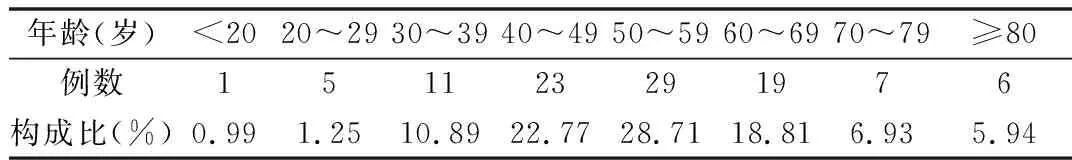
表1 101例DILI患者年龄分布
2.2 DILI患者入院时肝功能情况 101例DILI患者入院时肝功能检测结果多表现为中重度肝功能损伤,丙氨酸氨基转移酶(ALT)超过5倍正常值上限(ULN)共80例,占79.21%,天门冬氨酸氨基转移酶(AST)超过5ULN共54例,占53.47%,总胆红素(TBil)超过5ULN共49例,占48.51%,见表2。嗜酸粒细胞计数大于6%的共15例,占14.85%。
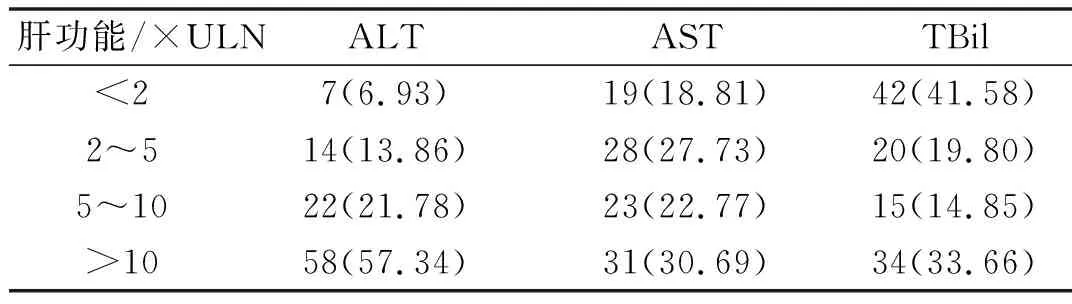
表2 101例DILI患者入院时肝功能情况 例(%)
2.3 DILI患者常见肝损伤药物分析 101例DILI患者中最常见肝损伤药物前五位依次为中药(29.70%)、抗感染药(20.79%)、中成药(19.80%)、解热镇痛消炎药(8.91%)、泌尿系统药物(7.92%)。见表3。
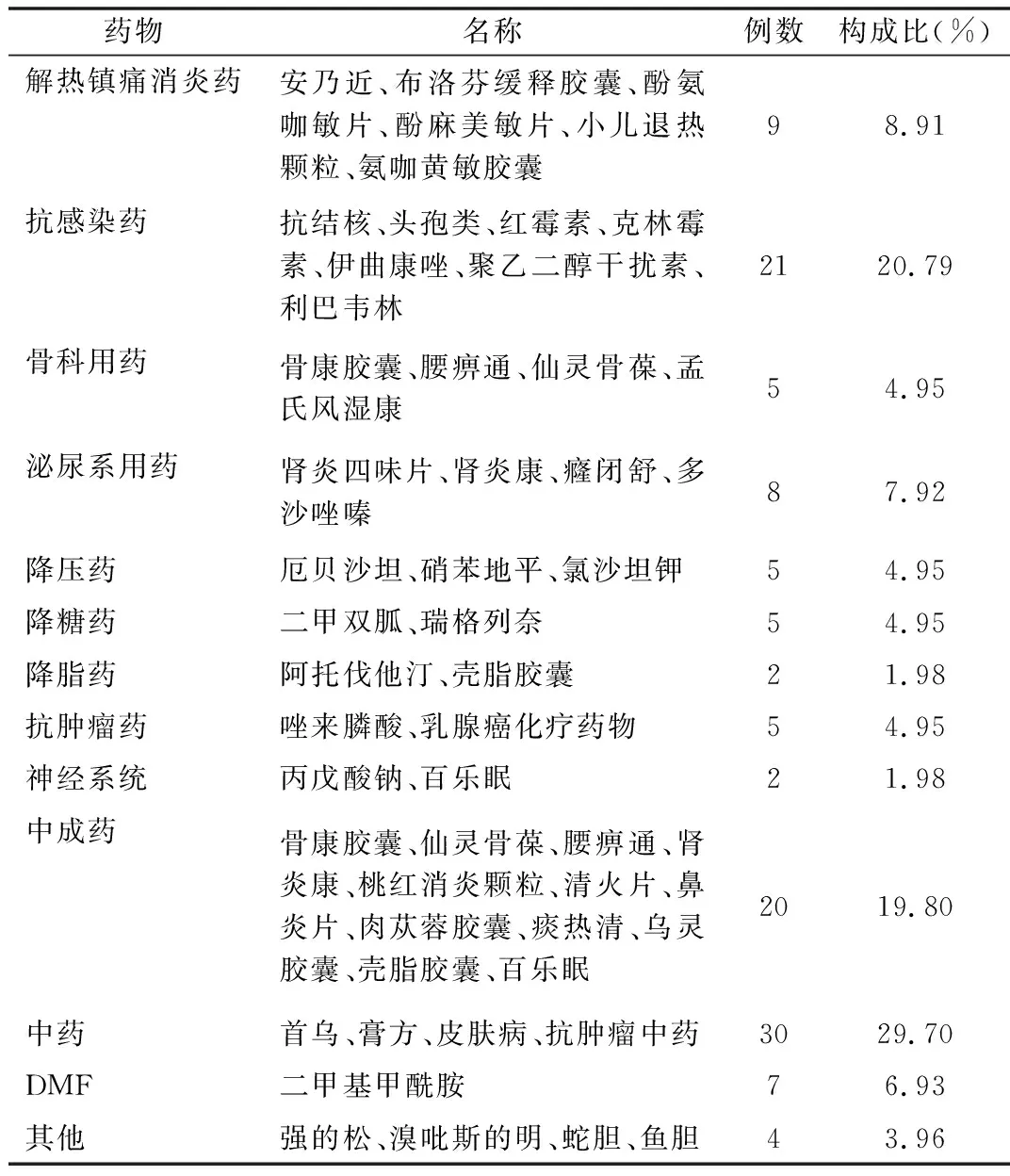
表3 101例DILI患者肝损伤药物分析
2.4 临床分型及预后 根据国际医学组织理事会(CIOMS)制订的DILI临床分型判断标准:①肝细胞损伤型:ALT≥3×ULN,且R≥5;②胆汁淤积型:ALP≥2×ULN,且R≤2;③混合型:ALT≥3×ULN,ALP≥2×ULN,且2 DILI的危险因素主要包括宿主因素、药物因素和环境因素。其中宿主因素分为遗传因素和非遗传因素,遗传因素主要是指与DILI相关药物代谢酶、药物转运蛋白和人类白细胞抗原系统(HLA)的基因多态性,不同种族的患者对DILI的易感性可能存在差异。非遗传因素包括:年龄、性别、妊娠、基础疾病[4]。有研究显示高龄、女性、妊娠及合并基础疾病者更易发生DILI[5,6]。药物的化学性质、剂量、疗程,以及药物相互作用常可影响DILI的潜伏期、临床表型、病程和结局,如屈格列酮常引起肝细胞型DILI而非胆汁淤积型DILI[7],阿莫西林克拉维酸常导致胆汁淤积性型DILI而较少导致急性肝衰竭[8]。西方人群中急性肝衰竭多由对乙酰氨基酚引起,且女性较男性更易出现[9,10]。环境因素如过量饮酒可能增加度洛西汀、对乙酰氨基酚、甲氨蝶呤及异烟肼等引起的DILI风险[11]。 DILI发病机制复杂,通常可概括为药物的直接肝毒性和特异质性肝毒性。药物的直接肝毒性是指摄入体内的药物和(或)其代谢产物对肝脏产生的直接损伤作用,通常通过自由基或代谢介质使细胞膜脂质过氧化,导致肝细胞损伤;此外,也可改变细胞膜或细胞内分子结构,激活凋亡途径等。直接肝毒性与剂量成正比,潜伏期短,常可预测。而特异质性肝毒性通常在用药后5~90d内发生,往往难以预测[12]。特异质肝毒性是中药及其活性代谢产物诱导的肝细胞线粒体受损和氧化应激导致DILI的主要机制,可通过多种分子机制引起肝细胞损伤和死亡[13]。药物及其代谢产物可活化多种死亡信号通路,促进细胞凋亡、坏死和自噬性死亡的发生[14],最终引起适应性免疫攻击导致DILI。 急性DILI临床多表现为用药后平均潜伏期内出现肝功能损伤,部分患者可有乏力、纳差、肝区不适等消化道症状,伴或不伴黄疸,与其他肝病临床表现无明显差异。当前,DILI的诊断尚无确切统一标准,仍属排他性诊断[15]。首先要确认存在肝损伤,其次排除其他肝病,再通过因果关系评估肝损伤与可疑药物的相关程度,推荐采用RUCAM量表对药物与肝损伤的因果关系进行综合评估。对难以确诊DILI的病例,必要时可行肝组织活检。DILI按发病机制可分为固有型和特异质型,按病程可分为急性和慢性,按受损靶细胞类型可分为肝细胞损伤型、胆汁淤积型和混合型肝损伤。本研究中患者以肝细胞损伤型为主,占81.20%;胆汁淤积型肝损伤3例,占3.00%;混合型肝损伤16例,占15.84%。由于样本量相对较小及取样误差可能,结果仅能从一定程度上反映DILI的临床特点。 本研究中患者多有明确用药史,可致肝损伤药物中最常见为中药,占29.70%,包括首乌、膏方、皮肤病及抗肿瘤中药,其中首乌临床及药理研究均证明其有明确肝损伤风险,中药引起的肝损伤多具有用药时间长、剂量大、药物种类多的特点[16]。其次为抗感染药,占20.79%,尤其需重视抗结核治疗药物,近年抗结核治疗引起DILI报道逐渐增多,抗结核治疗方案需多种药物联合且疗程较长,故而肝损伤风险增加[17]。中成药引起的肝损伤占19.80%,包括处方药和非处方药,种类繁多,如骨康胶囊、仙灵骨葆、腰痹通、肾炎康、桃红消炎颗粒、清火片、鼻炎片、肉苁蓉胶囊、痰热清、乌灵胶囊、壳脂胶囊、百乐眠等。解热镇痛消炎药(8.91%)及泌尿系统药物(7.92%)所致肝损伤亦为临床常见。Jeong 等[18]通过一项前瞻性研究发现,治疗组(n=87)单独使用中药未出现肝损伤,对照组(n=256)合并使用西药有6例患者出现肝损伤,认为中药单独使用相对安全,合并用药增加肝损伤风险。曾宏辉等[19]研究认为,解热镇痛消炎药是DILI主要原因,中药占比不高。相关DILI报道中由于未能详尽准确获得临床用药资料以及某些中成药中不规范添加其他药物成分致使相关中药致肝损伤数据偏高、报道失实。本研究中多数患者为合并用药,且部分患者未遵医嘱自行购药服用甚至迷信偏方,故实际致肝损伤药物尚有待进一步明确。 本研究中101例患者经治疗有效98例(97.03%),无效3例(2.97%)。DILI的治疗首先去除致病因素,停用相关肝损伤药物,其次可应用N-乙酰半胱氨酸、糖皮质激素、异甘草酸镁、熊去氧胆酸等保肝药物及综合治疗[20]。对出现肝性脑病和严重凝血功能障碍的肝功能衰竭患者及失代偿性肝硬化患者可考虑肝移植治疗[21]。急性DILI大多预后良好,通过治疗大多可恢复,少数患者进展至急性/亚急性肝功能衰竭,病死率较高。 我国于2014年建立了中国HepaTox网站,记录了400余种常见药物的肝损伤信息[22],为临床医生处方提供参考依据。本研究通过对相关病例观察研究,总结分析,期望能够引起重视并为临床用药提供帮助。在临床工作中,医务工作者应遵循相关指南合理用药,定期监测生化功能,保障用药安全。3 讨论
