还少丹治疗脾肾亏虚型轻、中度阿尔茨海默病临床观察※
2020-07-28杨雪萍邱雪梅陈卫银李炜弘
杨 芳 杨雪萍 徐 月 邱雪梅 陈卫银 李炜弘
(成都中医药大学附属医院神经内科,四川 成都 610072)
阿尔茨海默病(alzheimer's disease,AD)是一种病因未明的、慢性、进行性中枢神经系统退行性疾病,主要以不同程度的认知障碍和人格、行为障碍为临床表现。据报道,目前世界上有高达5 000多万AD患者,并且每隔3 s就会有1位患者被确诊为AD,到2050年,患病人数预计会增加3倍以上[1]。AD起病隐匿,进行性发展,给患者造成极大的身心损害,给患者家属及社会也带来巨大的经济负担。目前,针对AD的病因有多种假说,如Tau蛋白过度磷酸化假说、β-淀粉样蛋白(Aβ)沉积及毒性学说、胆碱能功能缺损学说、兴奋性氨基酸毒性学说等,但均无法明确解释AD的病因及其发病机制。因此,目前的治疗多以改善相关症状和针对已知的病机为主,并不能预防、终止和逆转AD。2017-09—2019-03,我们采用还少丹治疗脾肾亏虚型轻、中度AD 42例,并与盐酸多奈哌齐治疗42例对照观察,结果如下。
1 资料与方法
1.1 一般资料 全部84例均为成都中医药大学附属医院神经内科门诊(40例)和住院(44例)轻、中度AD患者,按照随机数字表法分为2组。治疗组42例,男23例,女19例;年龄61~82岁,平均(71.83±7.98)岁;病程2~7年,平均(4.54±2.18)年;病情程度:轻度20例,中度22例;文化程度:文盲1例,小学16例,中学20例,大学5例。对照组42例,男25例,女17例;年龄62~80岁,平均(70.75±7.23)岁;病程2~8年,平均(4.87±2.35)年;病情程度:轻度19例,中度23例;文化程度:文盲2例,小学14例,中学21例,大学5例。2组一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 病例选择
1.2.1 诊断标准 西医诊断参照美国国家衰老研究所(national institute of aging,NIA)和阿尔茨海默病学会(alzheimer's association,AA)制订的NIA-AA痴呆标准确诊[2]。痴呆程度判定标准采用Morris修订的临床痴呆分级量表(CDR)[3]。中医诊断参照《中药临床试验中的痴呆分期及辨证标准》[4],辨证为脾肾亏虚型。
1.2.2 纳入标准 ①符合以上中、西医诊断标准;②简易精神状态量表(MMSE)评分大学(包括大专)≤23分,中学≤22分,小学≤20分,文盲≤17分[5];③日常生活活动能力量表(ADL)评分≥23分(75岁以下),≥25分(75岁以上)[6];④CDR评分1分为轻度痴呆,2分为中度痴呆[3];⑤中医辨证分型为脾肾亏虚型,且痴呆证候分型量表(SDSD)评分脾肾亏虚型是唯一≥7分者[7];⑥Hachinski缺血评分量表评分<4分,或无卒中病史或卒中后3个月以上评分为5、6分者[8];⑦汉密尔顿抑郁量表(HAMD)评分≤7分[5];⑧年龄50~85岁;⑨受试者或监护人自愿参加临床试验,并签署知情同意书。
1.2.3 排除标准 ①近1个月使用过胆碱酯酶抑制剂或拟胆碱类药物者;②近1个月使用过利福平、苯妥英钠、卡马西平等药酶诱导剂者;③大量酗酒、有药物滥用史者;④需服用伊曲康唑、红霉素、酮康唑和奎尼丁等抑制多奈哌齐代谢药物者;⑤有严重的活动性内科疾病者;⑥患有严重的帕金森病、癫痫、精神分裂症等其他影响认知功能的神经精神类疾病者;⑦已知对多奈哌齐和还少丹过敏者;⑧其他持续存在的言语障碍或严重的视听障碍等影响认知功能评估疾病者;⑨同时使用健脾益肾的药物治疗(如已使用,在研究前至少停用4周),或其他影响疗效评价药物者;⑩妊娠期或哺乳期女性。
1.2.4 剔除与脱落标准 临床试验过程中出现变态反应、腹泻等不良反应而不能继续用药者;试验过程中继发感染,或发生其他并发症和特殊生理变化,不宜继续接受试验者;依从性差,不能配合完成研究者;其他原因要求退出者。
1.3 治疗方法
1.3.1 对照组 予盐酸多奈哌齐分散片(山东罗欣药业集团股份有限公司,国药准字H20080381)5 mg,日1次口服。
1.3.2 治疗组 予还少丹(太极集团重庆桐君阁药厂有限公司,国药准字Z50020189)9 g,日2次口服。
1.3.3 疗程 2组均治疗24周。
1.4 观察指标 观察2组治疗前后MMSE评分[5]、蒙特利尔认知评估量表(MoCA)评分[9]、阿尔茨海默病评定量表-认知分量表(ADAS-cog)评分[3]、ADL评分[6]、CDR评分[3]及SDSD评分[7]。MMSE评分:包括6个方面,评分范围为0~30分,27~30分为正常,21~26分为轻度痴呆,10~20分为中度痴呆,≤9分为重度痴呆(根据受教育年限调整)。MoCA评分:该量表满分为30分,≥26分为正常,18~26分轻度认知功能障碍,10~17分为中度,<10分为重度(如果受试者受教育年限≤12年,则将结果加1分)。ADAS-cog评分:该量表共12题,包括了定向力、语言、结构、观念的运用、词语即刻回忆与词语再认,满分70分。ADL评分:包括躯体生活自理量表6项和工具性日常生活能力量表8项,共14项内容,总分范围为14~56分,总分<16分为完全正常,>16分有不同程度的功能下降,分数越低说明患者的生活能力越强。CDR评分:评定的内容主要包括记忆、定向力、判断与解决问题的能力、工作和社会交往能力、家庭和业余爱好、个人自理能力,每项分别判定为正常、可疑、轻度、中度、重度,分别以0、0.5、1、2、3分表示。SDSD评分:该量表共有5个证型,分别为髓海不足型、脾肾亏虚型、瘀阻脑络型、痰浊蒙窍型、气血亏虚型。最高分为30分,总分≥7分,则证候成立,7~14分为轻度,15~22分为中度,23~30分为重度。

2 结 果
2.1 2组治疗前后MMSE评分、MoCA评分、ADAS-cog评分、ADL评分、CDR评分及SDSD评分比较 见表1。
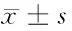
表1 2组治疗前后MMSE评分、MoCA评分、ADAS-cog评分、ADL评分、CDR评分及SDSD评分比较 分,
由表1可见,治疗后2组MMSE评分、MoCA评分均较本组治疗前升高(P<0.05),ADAS-cog评分、ADL评分、CDR评分及SDSD评分均较本组治疗前降低(P<0.05)。2组治疗后MMSE评分、MoCA评分、ADAS-cog评分、ADL评分、CDR评分组间比较差异均无统计学意义(P>0.05)。治疗后治疗组SDSD评分低于对照组治疗后(P<0.05)。
2.2 安全性评价 治疗组未发现与试验药物有关的不良反应;对照组出现2例不良反应,其中新发腹泻1例,头晕、恶心1例,反应程度较轻,未做特殊处理而自行消失。
3 讨 论
AD属于神经系统变性疾病,具有不可逆性和致死性。目前,AD的病因及发病机制尚不明确,主要以多种学说为主,针对不同的假说,AD治疗药物的研究方向包括:靶向神经递质、靶向Tau蛋白及Aβ、靶向炎性反应等。目前经美国食品和药物管理局(food and drug administration,FDA)批准上市的治疗AD的药物有乙酰胆碱酯酶抑制剂(多奈哌齐、他克林、利斯的明以及加兰他敏)、兴奋性氨基酸受体拮抗剂(盐酸美金刚)等以改善患者认知功能。多奈哌齐是第二代选择性乙酰胆碱酯酶抑制剂,通过有效选择性抑制中枢神经系统中乙酰胆碱的降解,增加中枢神经系统特别是大脑皮质和基底节神经突触间隙乙酰胆碱的浓度,以及减轻淀粉样蛋白的神经毒性作用,保护海马神经元等途径,改善患者的认知功能、总体印象及日常生活能力,为轻、中度AD患者的首选药。但此类药物只能暂时、有限地延缓患者病情发展,并不能治愈AD[10],近年研究发现其安全性尚不确定[11]。有报道显示,长期服用多奈哌齐导致的不良反应主要累及中枢和外周神经系统,肌肉骨骼系统及神经系统,主要临床表现有神经抑制药恶性综合征、锥体外系症状、比萨综合征及躁狂等,而腹泻为最常见的不良反应[12]。盐酸美金刚是另一类用于治疗AD的首选药物,同时也是FDA批准的第一个用于治疗中、重度痴呆的药物。多项大样本、随机、双盲、安慰剂对照试验均证实了盐酸美金刚能够改善中、重度AD患者的认知功能、日常生活能力及全面能力,因此《2018中国痴呆与认知障碍诊治指南》明确提出对于明确诊断的中、重度痴呆首选此药[13]。但与多奈哌齐一样,长期服用易出现眩晕、恶心、腹泻及激越等不良反应。因此,有必要探索更为安全、有效的治疗策略。
根据AD的临床表现,可将其归属于中医学“痴呆”“呆症”等范畴。多数医家认为,AD病位在脑,与心、肝、脾、肾功能失调密切相关,其关键在于肾、脾。肾为先天之本,藏精,主骨生髓,上输于脑。脾为后天之本,脾气的健运依赖肾气的资助、激发,而肾所藏之精亦赖于脾气所运化的水谷精气充养、培育。人至老年,肾精渐亏,髓减脑空,神机失用,脾气亏虚,失于运化,一则可致肾精失养,髓海失充,二则聚湿为痰,痰阻气滞,气滞血瘀,痰瘀蒙蔽脑窍。故AD属本虚标实证,本虚在于肾精不足,髓减脑消,神机失用;标实在于痰瘀闭阻脑络,蒙蔽脑窍。临证治疗多以补肾健脾为基本治则。
还少丹最早记载于《杨氏家藏法》中,具有补肾健脾、益气生精的功效。主治肾、脾、心三脏虚损,精血不足,神志俱耗,髓海空虚,智力减退,体倦腰痠,羸弱无力,不思饮食,发热盗汗,遗精白浊,牙齿浮痛等未老先衰之证。方中熟地黄、山茱萸、枸杞子、五味子滋阴补肾,固精益肾;肉苁蓉、巴戟天、小茴香温阳补肾助命火;杜仲、牛膝补肝肾,强筋骨;楮实子补益肝肾,清肝明目;茯苓、山药、大枣益气健脾;远志、石菖蒲宣窍安神[14-15],用于痰蒙心窍之神志昏乱、失语健忘、耳聋耳鸣诸证。诸药合用,共奏补肝益肾、填精生髓、健脾益气之效,既用于髓海空虚,智力减退,也用于体倦腰痠,羸弱无力,急躁易怒。现代药理研究表明,延缓衰老的中药如熟地黄、茯苓、黄芪等对神经生长因子受体有明显的增强作用,可能通过激活NGF受体而达到抗痴益智作用[16];还少丹具有明显增强衰老模型小鼠脑、肝脏组织抗氧化酶谷胱甘肽过氧化物酶(GSH-Px)和超氧化物歧化酶(SOD)活性,通过清除衰老模型小鼠体内的自由基延缓衰老的进程[17];还少丹可改善记忆障碍模型小鼠的空间参考记忆能力和工作记忆能力,明显增强脑内胆碱乙酰化转移酶(CAT)活性,促进乙酰胆碱合成,这一作用在缺血后的海马部位尤为明显,也与其改善学习记忆的行为变化相吻合[18];还少丹在细胞和动物水平均具有抗氧化、抗衰老的作用[19]。根据还少丹的主治功效及现代药理研究,目前应用还少丹治疗血管性痴呆已有多项临床研究,且疗效显著[20-23]。
本研究分别采用MMSE评分、MoCA评分、ADAS-cog评分、CDR评分及ADL评分对AD患者进行总体认知功能评估和日常生活功能评估。MMSE是目前国内外应用最广泛的认知筛查量表,其敏感度和特异度达到80%以上,但对识别正常老人与轻度认知功能障碍的作用有限[3]。MoCA主要是筛查轻度认知功能障碍患者,其识别正常老人与轻度AD患者的敏感度达100%[24-25]。ADAS-cog是美国推荐的临床试验认知评价的金标准,国内外评价抗痴呆药物改善认知功能的指标[26]。CDR用于痴呆严重程度的分级评定和随访[27]。ADL主要用于评定日常生活功能损害程度变化,可补充ADAS-cog在执行功能、日常生活能力和社会交往等社会功能条目的缺陷,其对痴呆筛查的敏感度和特异度分别达90.2%和78.8%[3,26]。采用SDSD评定临床疗效。
本研究结果表明,治疗后2组MMSE评分、MoCA评分均较本组治疗前升高(P<0.05),ADAS-cog评分、ADL评分、CDR评分及SDSD评分均较本组治疗前降低(P<0.05)。治疗后治疗组SDSD评分低于对照组(P<0.05)。说明还少丹能够改善轻、中度AD患者的认知功能,提高患者的日常生活能力,在改善痴呆中医证候上优于多奈哌齐。但本研究也存在不足之处,如未能揭示还少丹治疗AD的作用机制与环节,这也是课题组后续的研究方向,以期得到更有说服力的结果。
