Fe3O4改性水热炭活化过硫酸钠降解罗丹明B
2020-07-25张凯韦秀丽王冰蒋滔刘科
张凯,韦秀丽,王冰,蒋滔,刘科
(1 农业废弃物资源化利用技术与设备研发重庆市重点实验室,重庆401329;2 重庆大学环境与生态学院,重庆400045;3 重庆凯锐农业发展有限责任公司,重庆400020;4 重庆市农业科学院农业工程研究所,重庆401329)
罗丹明B(RhodamineB,RhB)是一种阳离子碱性染料,为典型的三苯甲烷衍生物,具有色泽鲜艳、着色率高、染色牢固等特点,常被作为染料广泛用于工业生产领域。但该类染料所产生的废水毒性强、难降解、易致癌,给人体健康和生态环境带来了极大风险,急需得到妥善处理。
高级氧化技术(advanced oxidation process,AOPs)是一种通过产生高反应活性自由基来实现有机物降解的方法,其中活化过硫酸盐(S2O2-8)产生的硫酸根自由基(⋅SO2-4)因其氧化电势较高,应用前景较为广泛[1]。然而在实际应用中,高级氧化技术存在催化活性低、氧化有机物不彻底以及难回收等特点而限制了其在污染治理领域的应用。目前,过硫酸盐(S2O2-8)常用的活化方法包括光[2]、热[3]、过渡金属活化[4]等,其中过渡金属活化效率高、成本低、能耗少,应用更为广泛。Fe3O4是一种良好的异相Fenton 催化剂[5],能够催化过硫酸盐产生⋅SO2-4、羟基自由基(·OH)等具有强氧化性的物质实现有机污染物的降解[6-8],同时,Fe3O4具有环境友好、易于磁分离等特点,但其在水体中由于磁性偶极矩作用常会发生团聚作用使得磁性、表面积和吸附容量降低,限制了其在环境修复领域的应用[9]。为了进一步提高Fe3O4的活化效率,通常在前表面包覆腐殖酸[10-11]、EDTA[12]、石墨烯[13]、生物炭[14]等。
水热炭(HTC)是指利用生物质进行炭化所制得的一种均质、疏水、能量密集、包含微米或纳米尺寸炭球的多孔结构固体[15]。与传统高温裂解制备生物炭相比,具有反应条件温和、操作简单、不受原料含水率限制、运行成本低等优点,受到了研究者的广泛关注[16]。目前,部分研究者对改性生物炭活化过硫酸盐展开了较为深入的研究,而改性水热炭对过硫酸盐活化降解难降解有机污染的研究较为鲜见。
微波加热是一种常见的加热技术,但微波加热具有选择性,并不是所有物质都能充分吸热达到反应温度[17-18]。Fe3O4是一种良好的微波催化剂,能够加快水热碳化过程,同时对反应产物的理化性质产生显著影响[19]。近年来,我国沼气工程得到持续发展,产生大量富碳沼渣,随着研究的深入,人们对沼渣的研究已从传统的植物营养领域转移至环境治理领域[20]。本文以微波为热源,Fe3O4作为微波催化剂制备改性水热炭,对微波催化剂在水热炭制备及过硫酸钠活化展开深入研究,并以罗丹明B(RhB)为降解对象,评价改性水热炭活化过硫酸钠的能力。
1 材料与方法
1.1 化学试剂与仪器
主要化学试剂:六水三氯化铁(FeCl3·6H2O)、乙酸钠(C2H3NaO2)、过硫酸钠(Na2S2O8)、无水乙醇(C2H5OH)、 乙 二 醇[(CH2OH)2]、 氯 化 钠(NaCl)、盐酸(HCl)、氢氧化钠(NaOH)、磷酸(H3PO4)、 碳 酸 氢 钠(NaHCO3)、 罗 丹 明B(C28H31ClN2O3)等,均为分析纯,所有溶液均采用去离子水配置。
主要仪器:元素分析仪(vario EL III CHNO,德国)分析CHN 含量,采用差量法计算O 含量(100%-C、H、N 和灰分%);采用N2吸附-脱附仪(BET,ASAP 2460)测定样品的比表面积;多通量微波消解/萃取系统(MDS-6G,上海新仪)用于水热炭的制备;紫外/可见光分光光度计(新世纪T6,北京) 用于测定RhB 吸光度(554nm);pH 计(PHS-3C,上海)用于测定溶液酸碱度;红外光谱分析仪(FTIR,Nicolet6700)用于测定表面官能团种类;X 射线粉末衍射仪(XRD,D8 ADVANCE)用于测定生物炭表面的物相结构;扫描电子显微镜(SEM,JSM-7500F)用于观察材料表面形貌;采用Babic 序批平衡法[21]测定水热炭等电点;样品磁饱和磁化强度采用综合物性测量系统(PPMS-9,美国Quantum Design)测定。
1.2 复合催化材料的制备
水热炭制备:沼渣原料取自重庆市巴南区某沼气工程运行良好的奶牛养殖场。简单预处理后,取15g沼渣置于聚四氟乙烯内衬的高压反应釜内,加入80mL 去离子水,搅拌30min 使其浸润。分别在180℃、200℃和220℃条件下(微波加热功率为400W)水热炭化2h后将其取出冷却至室温,分离黑色沉淀,去离子水洗涤至中性,冷冻干燥,研磨备用。不同温度下制备的样品分别记为HTC1、HTC2和HTC3。
Fe3O4/水热炭制备:称取一定量的水热炭于30mL 乙二醇中,超声处理10min 使其充分分散,随后将一定量的FeCl3·6H2O 溶解至乙二醇中,再加入一定量的无水乙酸钠,磁力搅拌20min使其充分混合,超声分散20min 后转移至反应釜中,密封,于200℃下反应2h,制备Fe3O4质量分别为水热炭质量的10%、15%、20%、25%的复合催化剂。反应结束后取出反应釜在空气中冷却,磁分离后,多次水洗和醇洗,冷冻干燥,研磨备用。
1.3 罗丹明B染料的降解
为考察Fe3O4/水热炭活化Na2S2O8的性能,以RhB作为对象进行评价,具体步骤如下:取150mL浓度为40mg/L 的RhB 溶液置于锥形瓶中,加入一定浓度的Na2S2O8,采用稀NaOH 溶液和H2SO4调节体系pH。加入一定量的复合催化材料,在27℃、160r/min的恒温摇床中振荡,每隔20min取样分析,测定RhB 的吸光度(554nm 波长处),每项实验重复2次。
为明确RhB 降解过程中的主要活性自由基,采用甲醇、叔丁醇和苯醌作为自由基捕获剂加以验证。
2 结果与讨论
2.1 Fe3O4/水热炭的结构表征
2.1.1 Fe3O4/水热炭复合材料理化性质分析
利用元素分析测定改性前后水热炭的元素含量。如表1 所示,其中H/C、O/C 和(O+N)/C(以上均为原子比)分别表示改性前后水热炭的芳香性、亲水性和极性大小[22]。改性水热炭H/C 和(O+N)/C均大于未改性水热炭,这可能是Fe3O4的氧化性促进了改性水热炭芳构化进程和表面含氧官能团的形成[23]。随着Fe3O4掺杂量的增加,H/C、O/C 和(O+N)/C 原子比均呈现出下降的趋势,这可能是因为Fe3O4的掺杂促进了H、O元素质量分数的快速下降所致[24]。其中H/C的降低是因为Fe3O4的掺杂促进了水热体系中脱甲基反应的发生,说明改性水热炭具有较好的稳定性[25-26]。起始时较高的O/C 表明水热炭表面具有丰富的含氧官能团产生,随着Fe3O4掺杂量的增加逐渐下降,这表明高的Fe3O4掺杂促进了脱水还原反应、脱羧反应等的发生[27-28],产生CO2等气体以挥发物形式逸出。(O+N)/C 的逐渐降低,表明改性水热炭极性逐渐减弱,水热炭中一些极性官能团如羧基、羟基等含量减少,水热炭疏水性增强,从而有利于疏水有机物的吸附[29-30]。观察水热反应过程中N的变化趋势发现,随着反应温度和Fe3O4掺杂量的改变,N元素含量发生一定变化,这可能是因为水热反应开始时一部分N 会进入液相,随着反应条件的改变,生物质所含的蛋白质发生美拉德反应生成杂环氮氧化物,缩合反应生成N芳香杂环[31],从而使得N元素表现为先减小后增加的趋势。
2.1.2 Fe3O4/水热炭复合材料XRD图谱
图1 分别为Fe3O4和20%Fe3O4/HTC2 的XRD 图谱,样品的衍射峰2θ=30.1°、35.5°、43.1°、57.0°、62.9°分 别 对 应 晶 面(220)、(311)、(400)、(511)和(440)且未出现其他杂峰,与Fe3O4标准图谱(JCPDS NO.19-0629)一致,衍射峰形尖锐说明结晶较为完整。通过对Fe3O4负载前后XRD图谱峰宽的研究发现,负载后峰形略微宽化,表明复合催化材料中Fe3O4纳米微球的颗粒略微变小,这与通过Scherrer 公式计算的结果相吻合并在SEM 图中得以证实。通过XRD分析证明Fe3O4确实已被负载在水热炭表面。

表1 水热炭的元素组成及比表面积

图1 样品的XRD图谱
2.1.3 Fe3O4/水热炭复合材料表面官能团分析(FTIR)

2.1.4 Fe3O4/水热炭复合材料SEM分析
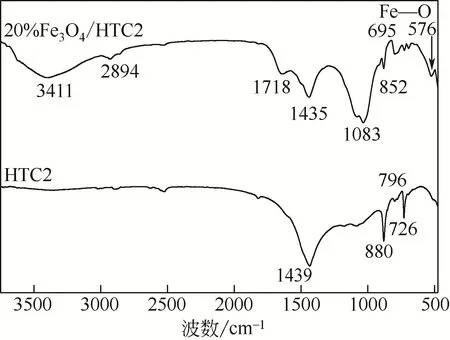
图2 样品的FTIR图谱

图3 Fe3O4、未改性水热炭和Fe3O4/水热炭扫描电镜图
图3(a)为Fe3O4的SEM 图,可知Fe3O4呈球形,粒径约为0.2μm,团聚现象较为明显;图3(b)为200℃条件下制备的水热炭,该条件下制备的水热炭呈片状结构;图3(c)为掺杂Fe3O4(质量分数20%)条件下制备的改性水热炭,可知Fe3O4掺杂前后粒径略微变小且较好地分散于水热炭表面。同时,附着在水热炭表面的Fe3O4使得材料表面形成了大量无规则的沟壑,提升了改性水热炭的比表面积,从而有助于提升其对RhB的吸附能力。
2.2 RhB降解影响因素
2.2.1 Fe3O4掺杂量和制备温度对水热炭降解RhB的影响

图4 RhB的降解曲线
取0.1g 的Na2S2O8投加至体积为150mL、浓度为40mg/L的RhB溶液中,添加0.16g水热炭(其中改性水热炭中水热炭为200℃条件下制备),在27℃、160r/min 的恒温摇床培养箱中振荡,每隔20min 取样分析,140min 内RhB 的降解曲线如图4所示。未改性水热炭作为降解剂时,随着水热炭制备温度的升高,RhB 的降解率先增加后减小,200℃下制备的水热炭性能最优,60min内降解率达到了27.4%,分别为180℃和220℃条件下RhB降解率的1.36 倍和1.45 倍,是仅以过硫酸钠作用时的2.03倍,这可能与水热炭的比表面积和表面官能团有关。由表1 可知,200℃条件下制备的水热炭比表面积最大,为水热炭吸附提供了更多的接触位点,促进了水热炭对RhB 的吸附。表面丰富的羟基等官能团能够活化过硫酸钠产生具有较强氧化还原电位的,在水溶液中还能形成具有强氧化性的·OH[33-34],有机污染物在和·OH的共同作用下完成降解。单一Fe3O4对RhB 的降解率仅为24%,这是因为的等电点在6.5 左右,而反应体系pH为6.7左右,此时Fe3O4表面带正电,而RhB 为碱性阳离子,因此不利于RhB 的吸附。不同Fe3O4掺杂改性水热炭活化过硫酸钠对RhB 的降解率先增加后减小,当掺杂量为20%时RhB 的降解率最高,为94.6%,比Fe3O4/PS 条件下RhB 的降解率提高了31.3%,是水热炭单独作用时的3.3倍,过硫酸钠单独作用时的3.9倍。这可能与Fe3O4是磁性材料,在水体中由于磁性偶极矩作用常会发生团聚作用使得磁性、表面积和吸附容量降低,过多或过少的Fe3O4均会对改性水热炭活化过硫酸钠降解RhB 产生一定的影响。后续实验均采用Fe3O4掺杂量为20%的改性水热炭进行。
2.2.2 水热炭投加量对RhB降解率的影响


图5 改性水热炭添加量对RhB降解率

2.2.3 Na2S2O8投加量对RhB降解率的影响

2.2.4 初始pH对RhB降解率的影响

图6 过硫酸钠投加量对RhB的降解率

图7 初始pH对RhB降解率的影响
溶液初始pH 对改性水热炭活化过硫酸钠具有重要影响。采用Babic序批平衡法[21]测得200℃下改性水热炭的等电点在4.6左右,不同pH条件下RhB的降解率如图7所示,当pH为5.6时RhB的降解率达到最高,这可能与以下两个原因有关:①当pH低于4.6 时,改性水热炭表面官能团质子化,带正电,RhB 主要以季铵阳离子基团的形式存在[21],RhB 可以与改性水热炭发生阳离子交换;当pH 大于4.6时,改性水热炭表面带负电,与RhB 产生静电吸附作用和酸碱中和作用,进一步增大了改性水热炭对RhB 的吸附量。而酸性条件下也有利于产生,使得pH 为5.6 时RhB 的降解率达到最大。②当pH 大于5.6 时,水热炭表面仍带有负电,RhB逐渐变为同时含有季铵阳离子和羧基阴离子的两性物质,RhB之间的聚合或沉积会导致改性水热炭对RhB 的吸附困难[39]。同时,OH-与反应产生氧化能力较弱的·OH,从而使得RhB的降解率降低。
2.2.5 共存阴离子对RhB降解率的影响


图8 不同阴离子对RhB降解率的影响

2.3 Fe3O4对水热炭制备升温行为影响分析
Fe3O4除了能作为催化剂活化过硫酸盐,也是一种良好的微波吸收剂。设定反应体系终温为200℃,添加不同质量分数的Fe3O4(10%、15%、20%、25%)来研究其对生物质水热反应升温行为的影响。由图9 可知,随着Fe3O4添加量的增加,反应体系达到200℃所需时间明显缩短,400W 条件下,Fe3O4掺杂量为20%时,14min左右即达到目标温度,较未添加Fe3O4情况下达到预定温度所需时间缩短了约48.1%,较高的升温速率可能加重热滞后现象[44-47],从而对水热炭的性质产生一定的影响。随着Fe3O4掺杂量的增加,体系内部压强也呈现迅速增大直至稳定的变化过程,这进一步证实了高的Fe3O4掺杂促进了脱水还原反应、脱羧反应等的发生,产生CO2、汽化水等[48-50]。较大的压强也能增加分子间碰撞的机会,从而加速反应速率,使得反应体系较快达到预设温度。

图9 Fe3O4掺杂量对反应体系升温速率及内部压强的影响
2.4 改性水热炭回收实验及稳定性分析
图10 为HTC2 和20%Fe3O4/HTC2 在300K 下测得的磁化曲线。由曲线可知HTC2的磁化曲线几乎为一条直线,其饱和磁化强度基本为0,而改性水热炭的饱和磁化强度达到了22.48emu/g,具有超顺磁特性[51],在外加磁场下利于改性水热炭从液相中的分离。将每次活化反应结束后的20%Fe3O4/HTC2 复合催化剂回收、水洗、干燥后再次进行过硫酸钠活化降解RhB实验,6次循环实验结果如图11 所示,RhB 的降解率仍保持在87%以上,表明复合催化材料具有良好的稳定性。

图10 HTC2和20%Fe3O4/HTC2在300K下的磁化曲线

图11 改性水热炭6次重复实验对RhB的降解率
2.5 改性水热炭降解原理分析
研究表明[52-53],过渡金属催化过硫酸盐反应过程中起主导作用的自由基多为,·OH、也起一定的作用。基于Fe3O4掺杂导致复合材料中水热炭表面产生大量的羟基、羧基等含氧官能团,可能对自由基种类和数量产生一定影响,为此,本实验选择甲醇、异丙醇和苯醌分别作为、·OH和的自由基捕获剂加以验证,捕获剂浓度均为0.01mol/L,实验结果如图12 所示,实验结果表明RhB 降解过程中起主导作用的自由基以为主,·OH和⋅为辅。

图12 不同捕获剂对RhB降解率的影响
3 结论
本研究利用微波水热法,以牛粪沼渣为原料,合成了Fe3O4改性微波水热炭,研究了Fe3O4掺杂量对水热反应进程及活化过硫酸钠降解RhB 的影响,得出如下结论。
(1)随着Fe3O4掺杂量的增加,H/C、O/C 和(O+N)/C 原子比均呈现出下降的趋势,使得改性水热炭具有较好的稳定性、较为丰富的表面含氧官能团以及较强的疏水性,利于疏水性物质RhB 的吸附及降解。
(2)XRD、SEM和FTIR分析表明Fe3O4确实负载在了水热炭表面且通过较为稳定的化学键()相结合,使得Fe3O4不易从水热炭表面脱落。
(3)200℃下制备的水热炭活化性能最优,60min 内降解率达到了27.4%,分别为180℃和220℃条件下RhB 降解率的1.36 倍和1.45 倍,是单独以过硫酸钠作为降解材料时的2.03 倍。掺杂20%Fe3O4的水热炭对RhB 降解率最高,为94.6%。共存阴离子、Cl-和均对改性水热炭活化过硫酸钠降解RhB 的影响产生抑制,其中抑制最为明显。
(4)Fe3O4掺杂量为20%时,14min左右即达到设定温度(200℃),较未添加Fe3O4情况下达到预定温度所需时间缩短了约48.1%,反应体系内部压强显著增大。
(5)改性水热炭具有较好的稳定性、重复利用性和超顺磁性,RhB降解过程中起主导作用的自由基为。
