碳球@纳米片状钴镍金属氧化物核壳型复合材料的制备及其电化学性能
2020-07-25冯艳艳李彦杰杨文牛潇迪
冯艳艳,李彦杰,杨文,牛潇迪
(1 桂林理工大学化学与生物工程学院,广西桂林541004;2 桂林理工大学化学与生物工程学院广西电磁化学功能物质重点实验室,广西桂林541004)
能源与人类社会息息相关,能源对经济社会发展的重大作用不亚于粮食、空气、水等对人类的重要性。然而人类所依赖的传统化石能源(石油、煤炭、天然气等)属于不可再生资源,经过长期的开采,已有日渐短缺的趋势,且其带来的污染问题也导致生态环境的不断恶化。面对如此严峻的状况,开发清洁、安全以及高效的可再生新能源是迫切需要解决的问题[1]。超级电容器作为一种可以储存或释放能量的装置,因其能量密度和功率密度大、可逆性好、对环境无污染、充放电速度快、循环寿命长等特点,越来越受到人们的关注[2-6]。
超级电容器电极材料主要包括三类:碳基材料、过渡金属氧化物和氢氧化物、导电高分子聚合物。其中,过渡金属(如钌、锰、钒、钴、镍等)氧化物和氢氧化物为赝电容电极材料[7-18],主要通过法拉第过程进行储能,具有较高的电容性能,但由于在氧化还原反应过程中容易发生结构变化,导致其循环稳定性较差[19-20]。将金属氧化物和氢氧化物与石墨烯或碳纳米管进行复合,能有效提高材料的导电性能和分散性能,进而有效提高电极材料的电容性能和循环稳定性能[21-23]。然而,石墨烯的制备成本较高,而碳纳米管在负载金属氧化物和氢氧化物时需要进一步酸化氧化,在其表面形成含氧官能团后才能进一步负载金属氧化物或氢氧化物,因而制备过程中会形成大量的废酸[24-25]。近年来,碳球的制备引起大量科研工作者的研究。其中,以葡萄糖为碳源,通过水热法制备碳球的方法简单、方便,同时所得碳球表面富有含氧官能团,这为碳球进一步原位生长和负载其他物质提供了便利[26-27]。
因此,本文分别以氯化钴和氯化镍为钴源和镍源,六次甲基四胺为沉淀剂,采用水热法和高温处理的方式在葡萄糖基碳球上原位合成钴镍金属氧化物,形成核壳结构的碳球@钴镍氧化物复合材料,并用于超级电容器电极材料的储能性能研究。
1 实验部分
1.1 试剂和仪器
主要试剂:六水合氯化钴,AR,西陇科学股份有限公司;六水合氯化镍,AR,天津市大茂化学试剂厂;葡萄糖,AR,西陇化工股份有限公司;尿素,AR,西陇科学股份有限公司;六次甲基四胺,AR,天津市华东试剂厂;无水乙醇,AR,广东光华科技股份有限公司;聚偏二氟乙烯,HSV900,太原力源锂电科技中心(有限公司);乙炔黑,平均粒径30~45nm,天津金秋化工有限公司;N-甲基吡咯烷酮,东莞市伟源化工有限公司;实验室用水为蒸馏水。
主要仪器:电化学工作站,CHI660E型,上海辰华仪器有限公司。
1.2 样品制备
依次向烧杯中加入4.0g 葡萄糖、4.0g 尿素和80mL 蒸馏水,搅拌使固体充分溶解。将溶液转移至100mL反应釜中,于180℃下反应6h。待反应结束冷却至室温后,将所得产物离心分离,并用蒸馏水和无水乙醇交替洗涤数次,之后置于80℃烘箱中干燥6h,即得葡萄糖基碳球(CS)。
分别以NiCl2·6H2O 和CoCl2·6H2O 为镍 源和钴源,控制镍钴摩尔比为1∶2(总摩尔数为3mmol)。依次向烧杯中加入0.24g 氯化镍、0.48g 氯化钴、0.28g六次甲基四胺和80mL蒸馏水,搅拌直至固体完全溶解。然后加入0.01g 碳球,搅拌15min 后,将溶液转移至250mL 圆底烧瓶中,于95℃下低速搅拌冷凝回流6h,待反应结束后自然冷却至室温。对所得复合材料离心分离,用蒸馏水和无水乙醇交替洗涤数次,并于80℃下干燥6h。之后将材料置于管式炉中部,在氮气气氛下300℃处理3h,反应结束冷却至室温,收集样品即为碳球@钴镍氧化物复合材料(CS@CoNi)。
作为对比样品,不加入CS,按照上述步骤制备的钴镍金属氧化物命名为CoNi。
1.3 样品表征
利用荷兰帕纳科公司生产的X’Pert Powder型X射线衍射仪、美国赛默飞世尔科技公司的Thermo ESCALAB 250XI 型X 射线光电子能谱仪、日本日立公司生产的SU5000 型扫描电子显微镜和中国北京金埃谱科技有限公司生产的V-Sorb 2800TP 比表面积及孔径分析仪对材料的结构、表面元素和形貌特征进行分析。
1.4 电化学性能测试
将所制备的样品、乙炔黑、黏结剂(PVDF)按照质量比为85∶10∶5进行混合,加入少量的氮甲基吡咯烷酮,研磨均匀后涂于泡沫镍上,保持涂抹面积为1.0cm2,干燥后于10MPa压力下压片,称量,即得到所需样品电极。其中,CoNi 电极片的面负载量为0.0033g/cm2,CS@CoNi 电极片的面负载量为0.0032g/cm2。
以所制备的样品电极为工作电极,石墨片为对电极,Hg/HgO 电极为参比电极,采用上海辰华CHI660E电化学工作站在2mol/L氢氧化钾溶液中分别进行循环伏安、恒电流充放电、交流阻抗及循环稳定性测试。样品的比电容是根据恒电流充放电所获得的参数来计算的,其表达式为式(1)。

式中,I 为放电电流,s;Δt 为放电时间,s;ΔV为放电电位窗口,V;m为活性物质的质量,g。
2 结果与讨论
图1 为样品CoNi 和CS@CoNi 的X 射线衍射图。可以看出,样品的主要组成成分为NiO、CoO。一般来说,CoO的特征峰出现在衍射角大约为36.68°、42.80°、61.94°、74.31°(JCPDS,No. 43-1004),分别对应(111)、(200)、(220)、(311)晶面,而NiO的特征峰则出现在衍射角大约为37.25°、43.29°、62.85°、75.40°处(JCPDS,No.44-1159),分别对应(101)、(012)、(110)、(113)晶面。由于其具有相近的衍射峰,所以很难区分开。此外,样品CS@CoNi在衍射角22°附近出现碳的衍射峰。

图1 样品的X射线衍射图

图2 样品的XPS谱图
图2为样品中Ni 2p和Co 2p的XPS谱图。从图2(a)可以看出,结合能780.7eV和795.8eV处对应为二价钴;同时,结合能779.4eV 和794.3eV 处对应三价钴[28-29]。样品CoNi 中钴元素主要以二价钴存在,同时存在少量的三价钴;而CS@CoNi 则主要以二价钴存在。从图2(b)可以看出,结合能855.7eV 和873.1eV 处的峰对应二价镍;同时,结合能854.2eV 和871.7eV 处的峰对应三价镍[28,30]。样品CoNi 和CS@CoNi 主要以二价镍存在,同时伴有一定量的三价镍。通过对比可以发现,碳球的加入能有效抑制三价钴和三价镍的形成。
图3 为样品CS、CoNi 和CS@CoNi 的扫描电镜图。可以看出,所制备的碳球粒径分布不均匀;样品CoNi 呈不规则的纳米薄片状结构,且片与片之间存在间隙。当反应体系中引入碳球后,材料的形貌发生了很大的变化,如图3(e)和(f)所示,样品CS@CoNi 中的钴镍金属氧化物被分散成微小的片状结构生长在碳球表面,形成以钴镍金属氧化物纳米片为壳、葡萄糖基碳球为核的核壳式结构,这是由于碳球表面含有大量含氧官能团导致的,在加热条件下,金属离子附着在碳球表面,从而形成核壳式结构。通过对比复合碳球前后CoNi 电极材料形貌的变化,可以发现:钴镍氧化物由无序的片状堆积形成核壳式结构均匀地分散在碳球表面;碳球的加入能够提高钴镍氧化物的分散性,碳球@钴镍金属氧化物核壳式结构可以提供丰富的反应活性位点,从而有助于改善电极材料的电容性能。

图3 样品的扫描电镜图
图4 为样品的低温氮气吸附/脱附等温曲线。从图4 可以看出,两个样品的氮气吸附/脱附曲线在较高的相对压力下出现毛细凝聚现象并产生回滞环,表明两个样品均具有介孔结构。样品的比表面积、孔容和平均孔径如表1所示。样品CS@CoNi的BET(Brunauer-Emmett-Teller)比表面积为24.50m2/g、总孔体积为0.182cm3/g。与样品CoNi 相比,样品CS@CoNi的比表面积和孔体积均略有增加。

表1 样品的孔隙结构参数
图5 给出了样品在10mV/s、20mV/s、30mV/s和50mV/s 扫速下的循环伏安(CV)曲线。从图5中可以看出,两个样品均出现了一对氧化还原峰,这可能是由于CoO 和NiO 具有相近的氧化还原电势,其包括Ni2+/Ni3+和Co2+/Co3+的氧化还原对,其法拉第反应如式(2)和式(3)[31-32]。


图4 样品的氮气吸附/脱附曲线
随着扫描速度的增加,氧化峰和还原峰发生移动,其中,氧化峰向高电势移动,而还原峰向低电势移动,其原因在于电极发生极化[33-34]。在同一扫描速度下,复合材料CS@CoNi 的氧化峰电流和还原峰电流明显高于样品CoNi,说明复合材料CS@CoNi具有更好的电容性能。
图6 为样品在电流密度分别为1A/g、2A/g、3A/g、5A/g、7A/g、10A/g 时的恒电流充放电曲线。从图6中可以看出,样品均存在充放电平台,这对应于循环伏安曲线中的氧化还原峰,表明材料均以赝电容形式储能。在相同电流密度下,相对于样品CoNi,复合材料CS@CoNi 表现出更长的充放电时间,说明CS@CoNi 的氧化还原反应进行得更加充分。原因可能在于碳球的引入提高了钴镍氧化物的分散性,提供了更多的活性位点,从而使得材料的赝电容性能有很大的提升。
图7(a)展示了不同电流密度下样品的比电容。在同一电流密度下,复合材料CS@CoNi 具有更高的电容性能;随着电流密度的增加,两个样品的比电容值均呈减小的趋势,这是因为电流密度增大后,电极活性物质氧化还原反应不充分导致的。其中,样品CoNi 的比电容从767.6F/g 降至568.0F/g,而样品CS@CoNi 的比电容由984.8F/g 降至850F/g。图7(b)为样品的比电容剩余率与电流密度的关系。当电流密度增大到10A/g时,CS@CoNi 的比电容剩余率为86.3%,而样品CoNi 的比电容剩余率仅为74.0%。这说明,碳球的加入使得CS@CoNi复合材料的倍率性能提高。

图5 样品在不同扫描速度下的循环伏安曲线

图6 样品在不同电流密度下的恒电流充放电曲线

图7 比电容和比电容剩余率与电流密度的关系
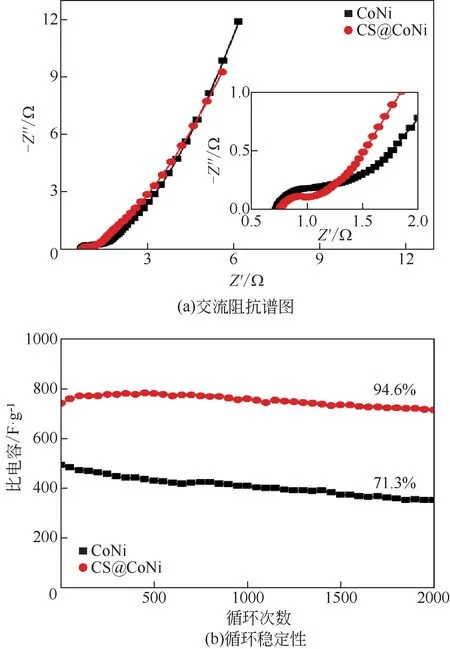
图8 样品的交流阻抗谱图及其在电流密度15A/g时的循环稳定曲线
图8(a)为样品的交流阻抗谱图,其包含了高频区域的半圆和低频区域的直线两部分,而高频区域的半圆直径越小,表明材料的电子转移阻力越小。从图8(a)可以看出,复合材料CS@CoNi在高频区的半圆较小;用Zview 软件对高频区的半圆进行拟合得到电子转移阻力,CS@CoNi 和CoNi 的电子转移阻力分别为0.34Ω、0.54Ω,说明碳球的加入降低了电子转移阻力。图8(b)为样品在电流密度15A/g时的循环稳定曲线。经2000 次恒电流充放电循环后,复合材料CS@CoNi 的比电容保持率为94.6%,而CoNi的比电容则下降至初始值的71.3%。这说明与碳球复合后,材料的稳定性能有了很大的改善。
图9为循环前后样品的交流阻抗谱图。可以看出,经过2000 次循环后,样品的电子转移电阻均有不同程度的增大。其中,样品CoNi 的电子转移电阻增加较为明显,这可能是由于钴镍氧化物是以赝电容的方式进行储能的,电极经过2000 次恒电流充放电,即电极材料经过了2000 次的氧化还原反应。多次氧化还原反应可能引起材料结构发生变化,使得其电容性能降低[35-36],同时也表现出电阻的增加。
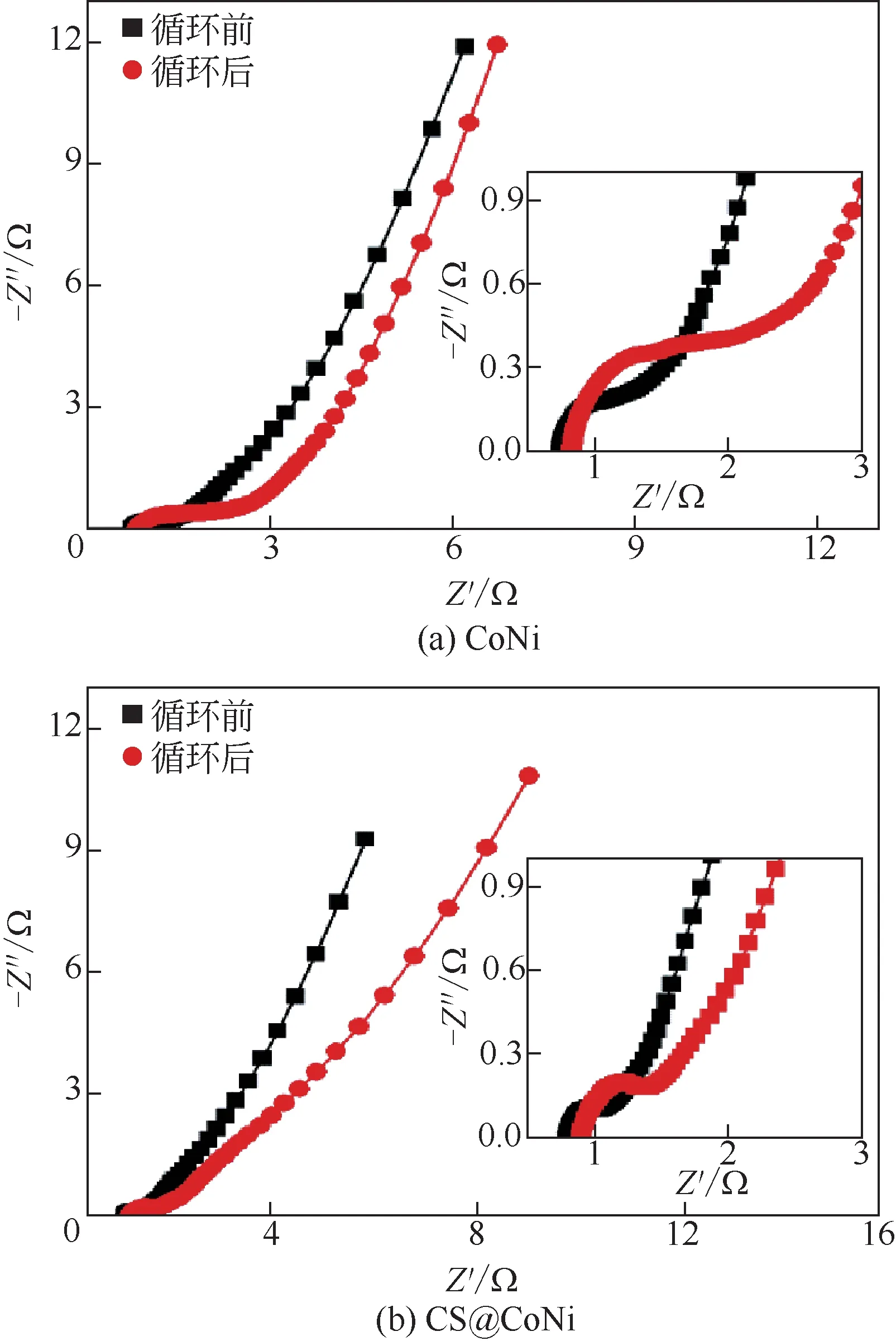
图9 样品循环前后的交流阻抗谱图
3 结论
以氯化钴和氯化镍为钴源和镍源,六次甲基四胺为沉淀剂,采用水热法在葡萄糖基碳球上原位生长钴镍氢氧化物,然后经高温热处理,最终合成一种具有核壳结构的碳球@钴镍金属氧化物纳米复合材料。通过对材料的结构、形貌和电化学性能进行分析,结果表明:碳球的加入使得钴镍金属氧化物的分散性和导电性有所改善,进而提高材料的电容性能以及循环稳定性能。
