基于氢化分解法的粗碳酸锂制备电池级碳酸锂工艺研究
2020-07-25王人杰李明兴李新义
王人杰,李明兴,李新义
(安徽科达新材料有限公司,安徽马鞍山 243041)
近年来,随着汽车业电动化变革大潮的来临,“油电平价”和动力电池行业“学习曲线”要求至2025年动力电池价格将在目前水平下降一半[1]。作为生产锂离子动力电池正、负极材料以及电解液的关键原料,电池级碳酸锂生产的降本增效变得极为重要。
目前,虽然来源于矿石的碳酸锂仍是主流,但是,在世界范围内,盐湖卤水锂资源储量占总储量的70%~90%,从资源角度来说,盐湖卤水碳酸锂具有更大的降本潜力[2-3]。 随着盐湖锂资源开发力度的不断加强,锂盐提纯工艺技术的不断进步,采用成本更低的卤水粗碳酸锂作为原料生产电池级碳酸锂逐渐成为可能。目前,碳酸锂提纯的方法主要有氢化分解法、氢化沉淀法、苛化法、电解法等[2]。其中,氢化分解法去除杂质的能力较全面,且具有工艺流程短、操作方便、成本较低、对环境污染小、热解母液可重复利用等优点[4-5],但是除杂效果无法稳定达到电池级碳酸锂的水平,需结合一定的改进措施[6-8]。改进方法主要有络合法[8]、离子交换法[1]、饱和洗涤法[11]等。其中络合法可用于深度去除二价金属离子,但是会在母液中引入有机络合物[8-9],影响循环使用;离子交换法也具有去除特定离子的深度除杂效果,且不会引入有机物,其中,氨基磷酸型螯合树脂对二价金属离子选择性好,适用于从有害金属离子与大量碱金属离子共存的溶液中将有害金属离子选择除去,其树脂用量少,设备小型化,是除去有害金属的经济有效的方法[10];饱和洗涤法对去除易溶性杂质具有独到优势。
本文以卤水粗碳酸锂为原料,基于氢化分解法进行工艺优化,以制备电池级碳酸锂。通过对比四种实验方案的结果,研究离子交换及饱和洗涤的联用对产品品质及收率的影响,以期获得一种可行的基于氢化分解法的粗碳酸锂制备电池级碳酸锂工艺方案。
1 实验部分
1.1 原料、药品与器材
卤水粗碳酸锂(品质指标见表1),CO2(工业纯),D402-II螯合树脂,HCl(AR),去离子水,烧杯,电动搅拌器,平板离心机,氢化塔,恒温水浴锅,离子交换柱,电子秤、马弗炉。

表1 粗碳酸锂原料的品质指标
1.2 实验方法
通过对氢化分解、离子交换、饱和洗涤的分步组合,形成四种提纯卤水粗碳酸锂的实验方案,如表2所示。其中涉及的工序包括氢化、热解、饱和洗涤、离子交换、离心等。

表2 分析方法
1.2.1 氢化
将粗碳酸锂(或洗涤预处理产品)与去离子水按一定比例混合成料浆后倒入氢化塔,向氢化塔中通入CO2气体,控制适当的温度、气体流速和时间,使碳酸锂浆液与CO2的充分反应生成LiHCO3溶液(实验装置见图1c)。为除去无法被氢化的不溶性杂质,还需结合离心工序。化学反应如下:

操作参数:固液比1∶20;反应温度20℃;反应压力0.1MPaG;CO2流量1.0m3/h;反应时间20min。
1.2.2 热解
将除杂后的氢化液在一定的搅拌速度下加热至适当温度,并保持一定时间。期间LiHCO3重新分解并析出更纯净的Li2CO3晶体(实验装置见图1a)。为将热解母液与晶体分离,得到纯度较高的碳酸锂,还需结合离心工序。化学反应如下:

操作参数:搅拌速度500r/min;反应温度95℃;反应时间90min。
1.2.3 饱和洗涤
将粗碳酸锂与氢化分解法产生的饱和碳酸锂母液按一定比例混合,在适当的温度与搅拌速度下洗涤一定时间(实验装置见图1a),从而使可溶性杂质溶解于水中。为将洗涤母液与固体分离,从而获得品质更好的碳酸锂,还需结合离心工序。
操作参数:固液比1∶2;搅拌速度3 000r/min;洗涤温度80℃;洗涤时间20min。
1.2.4 离子交换
先将一定量的D402-II树脂进行预处理,把Na型树脂转化成Li型树脂,然后将氢化工序得到的澄清溶液流经处理好的离子交换树脂。通过控制氢化液在树脂柱中的流速,可获得有效除去钙镁等杂质离子的深度除杂氢化液(实验装置见图1d)。除杂机理如下(R为树脂骨架):

操作参数:树脂柱体积1L;液体流速10BV/h。
1.2.5 离心
悬浮液在离心力场下产生离心压力,使液体通过过滤介质成为滤液,而固体颗粒被截留在过滤介质表面,从而实现固液分离。(实验装置见图1b)。
操作参数:过滤精度1 000目;过滤时间5min。
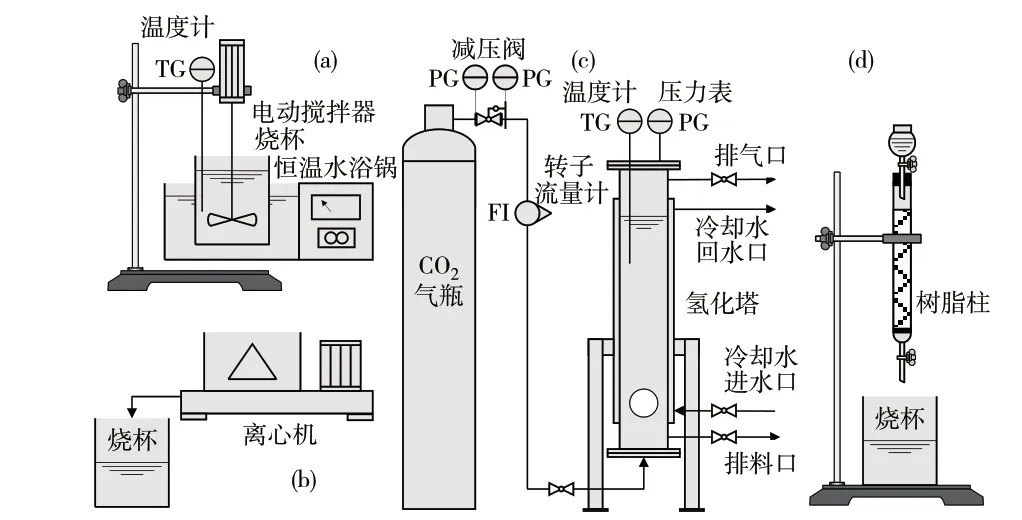
图1 实验装置
1.3 分析方法
产品及中间产物的分析方法如表3所示。

表3 实验方案规划
2 结果与讨论
2.1 方案A:氢化分解
称取500g卤水粗碳酸锂与10L去离子水混合成浆液,采用方案A的工序提纯。获得的产品经干燥后测定其Li2CO3主含量与杂质含量,并计算各种杂质的去除率,结果如表4、图2所示。

表4 各方案提纯产品化验结果
从表4、图2可知,氢化分解法提纯卤水粗碳酸锂,虽能降低各种杂质的含量,但仍达不到电池级碳酸锂行业标准YS/T 582—2013的要求,主要原因是Ca、Mg等难溶性杂质的去除率不理想。
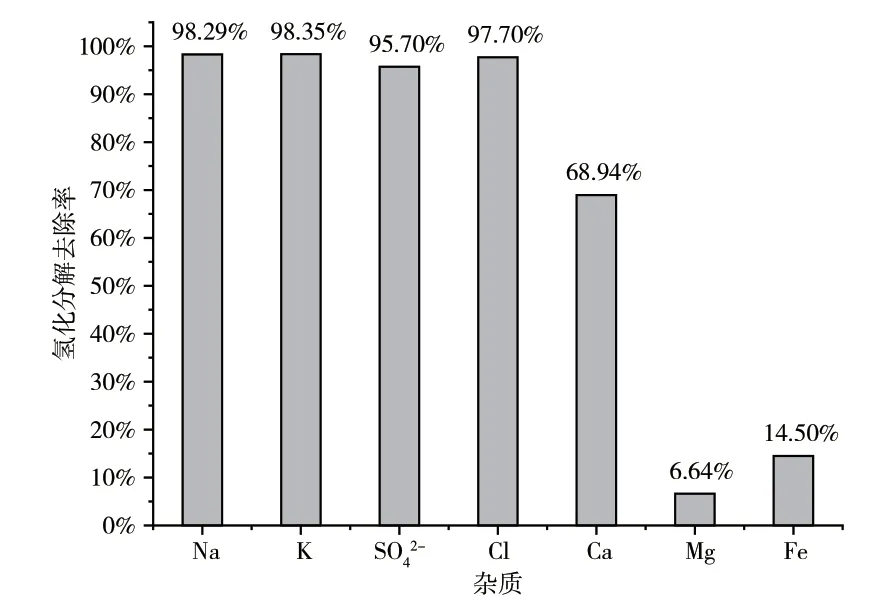
图2 氢化分解法的杂质去除率
2.2 方案B:氢化分解-离子交换联用
称取500g卤水粗碳酸锂与10L去离子水混合成浆液,采用方案B的工序提纯。对获得的产品经干燥后测定其Li2CO3主含量与杂质含量。为单独考察离子交换的效果,对离子交换前后的氢化液进行杂质含量分析,并计算各种杂质的去除率。结果如表4、图3所示。

图3 离子交换的杂质去除率
从表4、图3可知,叠加了离子交换的氢化分解法可以获得合格的电池级碳酸锂,其中离子交换对Ca、Mg等难溶性杂质的深度去除效果十分明显。而K和Cl等易溶性杂质虽然能够达标,但已经接近上限。此外,这些杂质全部进入了热解母液中,并随着母液的循环不断富集,最终导致母液的可循环次数极为有限(不超过1次)。由于提纯收率与母液的循环次数有图4所示的关系,因此本工艺方案的收率很低,不具备经济可行性。
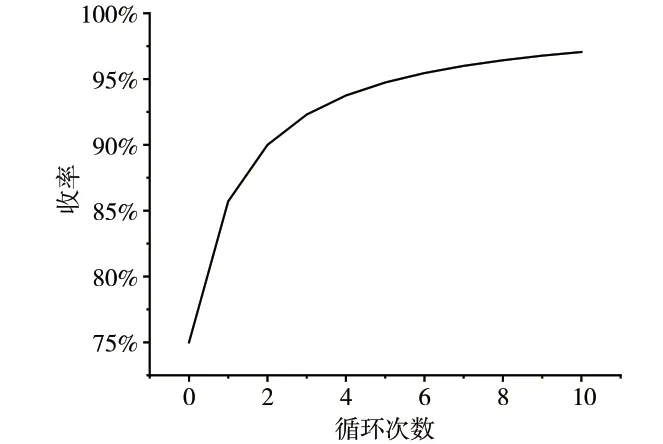
图4 提纯收率与母液循环次数的关系
2.3 方案C:氢化分解-饱和洗涤联用
称取500g卤水粗碳酸锂与10L去离子水混合成浆液,采用方案C的工序提纯。为避免洗涤液溶解碳酸锂而造成锂损,饱和洗涤法取用部分方案A的热解母液(饱和碳酸锂溶液)作为洗涤液,对获得的产品经干燥后测定其Li2CO3主含量与杂质含量。为单独考察饱和洗涤的效果,对饱和洗涤后的碳酸锂进行杂质含量分析,并计算各种杂质的去除率。结果如表4、图5所示。
从表4、图5可知,叠加了饱和洗涤的氢化分解法无法获得电池级碳酸锂,原因是两种方法都难以去除Ca、Mg等难溶性杂质。对SO42-的去除率也不理想,原因可能是粗碳酸锂在沉锂阶段形成了含硫酸盐的包晶,通过洗涤难以去除[12]。但是,饱和洗涤法对Na、K、Cl等可溶性杂质具有不错的去除率,可以有效降低这些杂质进入后工序,从而减轻了氢化分解的负担,非常有利于提高母液的可循环性。

图5 饱和洗涤的杂质去除率
2.4 方案D:氢化分解-离子交换-饱和洗涤联用
从图2、图3、图5的对比可知,三种方法对杂质的去除效果各有优劣,若将它们组合在一起,有望互相取长补短,实现更好的提纯效果。
称取500g卤水粗碳酸锂与10L去离子水混合成浆液,采用方案D的工序提纯。其中饱和洗涤环节取用部分方案A的热解母液作为洗涤液,对获得的产品经干燥后测定其Li2CO3主含量与杂质含量。并计算各种杂质的去除率。结果如表4、图6所示。

图6 改进后氢化分解法的杂质去除率
从表4、图6可知,叠加了离子交换与饱和洗涤的氢化分解法能实现将粗碳酸锂提纯为电池级碳酸锂,各种杂质的去除率与方案A相比均获得了显著的提升。同时,产品中的K、Cl等可溶性杂质大大减少,意味着热解母液可循环性的显著提升(至少3次),收率可观。
3 结语
实验结果表明,氢化分解法提纯粗碳酸锂无法获得合格的电池级碳酸锂;离子交换可以实现深度去除Ca、Mg,提升产品的品质;饱和洗涤可以在避免锂损的同时,有效降低可溶性杂质进入后工序,减轻氢化分解的负担并提高母液的可循环性;叠加了离子交换与饱和洗涤的氢化分解法能实现将粗碳酸锂提纯为电池级碳酸锂,同时具有可观的收率。
通过对四种方案的研究,获得了一种可行的基于氢化分解法的粗碳酸锂制备电池级碳酸锂工艺方案。
