CT引导下经皮穿刺肺活检术致肺出血死亡1例
2020-07-23任洧枢董志斌谭亚晴姚辉任兴华丁润涛温歌华赵锐官大威吴旭
任洧枢,董志斌,2,谭亚晴,姚辉,任兴华,丁润涛,温歌华,赵锐,官大威,吴旭
(1.中国医科大学 法医学院法医病理学教研室,辽宁 沈阳 110013;2.南京市公安局栖霞分局,江苏 南京 210046)
1 案 例
1.1 简要案情和病史摘要
某女,66岁,自觉喘息气短,伴间断咳嗽咯痰,某年12月24日,在当地医院行胸部CT示:右肺门占位性病变伴肺不张,双肺多发结节,右侧胸腔少量积液。次年1月13日,以“发现右肺肿物增大1月,发热1周”入院就诊。查体:脉搏88次/min,呼吸20次/min,血压17/10 kPa(133/72 mmHg)。入院行胸部增强CT示:右肺中、下叶及左肺下叶见不规则片状实变影,增强各期见不均匀强化,实变影内可见明显较粗大血管影,右肺门增大,右肺中叶支气管狭窄,远端闭塞,余肺内散在斑片、索条、结节状高密度影。纵隔内淋巴结增大、融合成团。右侧胸腔见弧形液体密度影。1月16日10:10,行CT引导下经皮穿刺肺活检术:通过CT扫描确定右侧胸腔穿刺部位,垂直床面进针后,再次行CT扫描,见针尖位于病灶边缘,拔出针芯送入活检枪,微调角度后取4块组织(每块为0.5 cm×0.4 cm×0.1 cm)。患者术后即咯血,累计约100 mL。术后35min,患者血压下降至12/8kPa(90/62mmHg),呼吸17次/min,心率89次/min,血氧饱和度68%,随后迅速进展为意识障碍。先后行气管插管,持续心肺复苏,补液支持治疗,12:38患者临床死亡。
肺穿刺活检免疫组织化学结果显示:B细胞淋巴瘤因子-2(B-cell lymphoma-2,Bcl-2)阳性,CD20阳性,CD5阳性,Ki-67约50%,白细胞共同抗原(leucocyte common antigen,LCA)阳性,支持非霍奇金淋巴瘤,倾向于B细胞淋巴瘤。既往史:高血压病3年。
1.2 尸体检验
死后31d进行尸体检验。
尸表检查:尸体中度腐败,尸斑浅淡。右背正中可见一处直径0.3cm穿刺针痕。
尸体解剖:右侧胸腔8、9肋间脊柱旁5cm处与体表穿刺部位相贯通,直径0.3 cm,周围肋间肌浅层少量出血。右侧胸腔见暗紫红色积液,内有块状凝血,共1550mL。右肺下叶背内侧浆膜下灶状紫红色变,可见3处浆膜破裂、组织缺损,由内向外大小分别为0.2 cm×0.1 cm、0.4 cm×0.2 cm、0.5 cm×0.3 cm,为穿刺活检部位。沿支气管分支向下剪开右肺下叶,穿刺部位下方右肺下叶组织内见出血灶,大小11.5cm×8.2cm(图1),其中可见多根血管样结构(管腔最大0.5cm×0.1 cm)分布在穿刺部位深层的淡灰褐色、黄白色肿物周围(图2)。右肺下叶支气管分支与出血区相延续,气管中、下段及气管杈处可见暗红色冰晶样物充塞管腔。左肺下叶、右肺中下叶可见灰褐色占位病变,横截面分别为5.8cm×3.5cm、9.5cm×5.6cm。右肺门及下叶后侧近中线处见灰褐色实变,大小12.5cm×5.2 cm。气管杈处可见较多实变、液化的灰褐色组织,与右肺门肿块相延续。各器官含血量少;冠状动脉粥样硬化,其中左冠状动脉前室间支中下段管腔Ⅱ~Ⅲ级狭窄。余未见异常。
组织病理学检验:心外膜下和心肌间质静脉扩张,管腔空虚,冠状动脉内膜增厚,粥样硬化斑块形成,胆固醇结晶形成,钙盐沉积,管腔狭窄。肺泡腔内可见散在片状出血,肺内小静脉和肺泡壁毛细血管扩张,管腔空虚。肺实质内大量小圆形瘤细胞呈弥漫浸润性生长,其间可见管腔粗细不等血管,纤维组织增生,散在分布的坏死肿瘤组织。脑、心、脾、肾等多器官小动脉硬化。
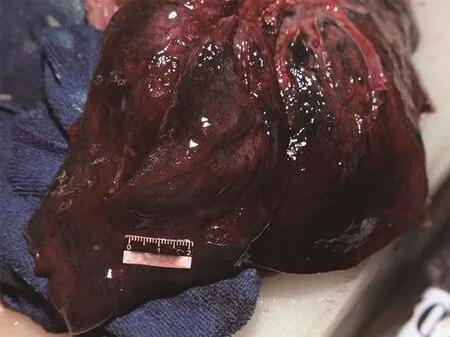
图1 右肺下叶出血灶(箭头所示)Fig.1 Right lower lobe hemorrhage(arrow)

图2 右肺内肿物及其周围的血管样结构(箭头所示)Fig.2 Right pulmonary tumor and its surrounding vascular structure(arrow)
1.3 法医病理学诊断
左肺下叶、右肺中叶及下叶非霍奇金淋巴瘤;右肺下叶穿刺活检下方肺出血,右侧胸腔积血伴凝血块;尸斑浅淡,各器官含血量少;冠状动脉粥样硬化;脑、心、脾、肾等多器官小动脉硬化。
2 讨 论
本例通过系统尸体解剖及组织病理学检验发现:尸斑浅淡,各器官含血量少,呈大量失血的病理形态学改变;左肺下叶、右肺中下叶非霍奇金淋巴瘤(倾向于B细胞淋巴瘤);右肺下叶穿刺活检下方组织出血,右侧胸腔1550mL积血,内可见凝血块。结合病情经过及临床诊疗过程,认为本例符合因患有肺部恶性肿瘤,在经皮穿刺肺活检术中,造成肺组织出血、右侧胸腔积血,导致失血性休克死亡。尸体解剖见肺部肿瘤组织富含血管样结构,以外周部血管较为粗大,最大管腔达0.5cm×0.1cm。穿刺部位在肿瘤组织周围,该区域存在大量肿瘤新生血管,穿刺时可被刺破,短时间内造成大量出血,形成肺出血及血胸。由于穿刺针较细及死后变化的影响,出血点不易寻找。此外,肺出血区与右肺下叶支气管分支相延续,这也是临床上患者咯血的来源。
经皮穿刺肺活检术是一种介入性诊疗手段,通常在CT引导下完成,用于肺周边部病变或弥漫性肺部疾病的诊断和鉴别诊断,通过获取小块肺组织用于镜下形态学观察、特殊染色或组织培养等。气胸是CT引导下经皮穿刺肺活检术最常见的并发症,其他并发症还包括出血(包括肺内出血、血胸、针道出血等)、空气栓塞、皮下气肿、肺内感染、血管迷走神经综合征和针道恶性肿瘤转移等[1]。日本一项9783例关于CT引导下经皮穿刺肺活检术的调查中,0.75%的患者发生严重的术后并发症,严重的肺出血和咯血发生率为0.061%,血胸发生率为0.092%[2]。美国一项研究[3]报道的15865例经皮肺活检中,术后出血发生率为1%,其中17.8%的患者需要输血治疗,且老年人、女性、伴发肺部疾病(慢性阻塞性肺疾病、胸腔积液)等都是与出血相关的重要因素。此外,CT引导下经皮穿刺肺活检术在对于深部的小病灶进行穿刺时更易导致出血[4-5]。可见就穿刺活检本身而言,造成的肺出血大多呈自愈性,无需特殊处理,少数情况下并发严重出血经适当临床手段也可缓解。非霍奇金淋巴瘤是一类淋巴组织的恶性肿瘤,其区别于霍奇金淋巴瘤之处在于缺少典型的里-施细胞(Reed-Sternberg细胞,R-S细胞)。非霍奇金淋巴瘤的生长和发展依赖于肿瘤新生血管,新生血管的机制包括:肿瘤细胞分泌血管内皮生长因子(vascular endothelial growth factor,VEGF)作用相应受体而激活相应信号通路促血管生成;肿瘤微环境促进新生血管转化成熟,并招募循环中的骨髓源性祖细胞[6],如在淋巴瘤患者活检淋巴结中内皮祖细胞的含量显著升高[7]。本例中,肿瘤累及左肺下叶、右肺中下叶及肺门,体积较大,随肿瘤的进展,形成大量较大的血管结构,混杂于肿瘤组织中,CT扫描不易发现。病历记载穿刺结束后重新CT扫描,发现右肺内沿针道新发的渗出影,提示肺活检穿刺造成血管破裂。
对于肺组织穿刺活检术后死亡的法医学鉴定,应充分了解案情资料和临床诊疗过程,注意对穿刺相关致死性并发症的检查,注意是否存在失血征象,如有发现,认真寻找出血部位,统计出血量。同时,应注意排除心、脑等器官原发性致死性疾病等。
