碘催化烯烃双官能团化反应合成新型β-羟基硫醚
2020-07-15贺云鹏钮腾飞倪邦庆
贺云鹏, 钮腾飞, 倪邦庆
(江南大学 化学与材料工程学院,江苏 无锡 214000)
β-羟基硫醚是合成杂环化合物、天然产物和药物的一种重要原料,在有机合成中常作为重要的目标分子或骨架[1-3]。目前,制备此类化合物的方法主要有环氧化物和硫醇的开环反应以及烯烃和硫醇的共氧化反应(TOCO)等。但这些反应往往涉及硫醇、硫酚等剧毒、恶臭化学品的使用,与当今绿色化学的主题不符。因此,在过去的十多年中,研究人员已经开发出使用二硫化物代替硫醇制备β-羟基硫醚的方法。二硫化物和烯烃间的氧化硫化作用引起了人们极大关注[4-24]。
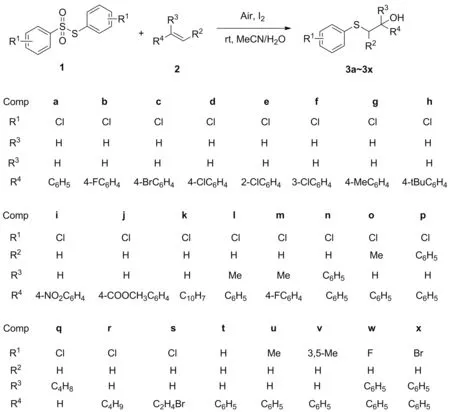
Scheme 1
例如,Movassagh团队报道了以芳基烯烃和二硫化物为原料,用Zn/AlCl3作为催化剂一锅法合成β-羟基硫醚[25]。Yadav等[26]发展了一种非金属催化的自由基途径,通过在有氧条件下使用Rongalite©(甲醛次硫酸钠,Na(HOCH2SO2)·2H2O)作为促进剂制备β-羟基硫醚。最近,Yan研究小组公开了以HBr/H2O2介导的苯乙烯硫化反应,制备β-羟基硫醚的方法[27]。虽然以上方法均可以有效的制备β-羟基硫醚,但是均存在一些缺点,如涉及有毒试剂、过量氧化剂以及金属催化剂。此外,这些方法大多只能应用于末端芳基烯烃,无法应用于脂肪族烯烃。因此,探索一种简单、高效、且对环境友好的β-羟基硫醚的合成方法具有重要意义。
碘是一种经典的非金属元素催化剂,碘催化的氧化反应在对环境保护和降低反应成本方面有重要意义[28-37]。最近,Peddinti课题组[38]开发了一种具有区域选择性的方法合成β-羟基硫醚,通过碘元素催化苯乙烯和苯硫酚反应,但该反应以DMSO作为氧化剂,不符合绿色化学的要求。
本文以空气(氧气)为氧化剂,以乙腈水溶液[V(MeCN)/V(H2O)=3/1]为反应溶剂,以单质碘为催化剂,以硫代磺酸酯作为硫源与烯烃发生氧化双官能团化反应,合成了β-羟基硫醚化合物3a~3x(Scheme 1,其中3i,3k,3r,3s为新化合物),收率51%~86%,其结构经1H NMR,13C NMR, MS(ESI)和元素分析确证。
1 实验部分
1.1 仪器与试剂
Brucker AVANCE 400 MHzⅢ型核磁共振仪(CDCl3为溶剂,TMS为内标);Finnigan TSQ Quantum Ultra AM型质谱仪;Yanagimoto MT3CHN型元素分析仪。
化合物1按文献[39]方法合成;碘单质(99.8%),苯乙烯(99.5%),安耐吉化学;其余所用试剂均为分析纯。
1.2 3a~3x合成(以3a为例)
称取S-(4-氯苯基)-4-氯硫代苯磺酸酯0.159 g(0.5 mmol)和催化剂碘单质0.0254 g(0.1 mmol),加入带有搅拌子的25 mL Schlenk反应管中,在充满空气的反应管中用注射器依次加入苯乙烯0.12 mL(1 mmol),去离子水0.5 mL和乙腈1.5 mL,搅拌下反应2 h[TLC检测,展开剂:V(正己烷)/V(乙酸乙酯)=4/1]。分液,有机相加入Na2S2O3溶液(10 mL),用二氯甲烷(3×4 mL)萃取,合并有机层,用无水硫酸钠干燥,抽滤,滤液旋蒸除溶,残余物经硅胶柱层析[洗脱剂:V(正己烷)/V(乙酸乙酯)=12/1]纯化得无色油状液体3a108.2 mg,收率82%。
用类似方法合成化合物3b~3x。
2-(4-氯苯巯基)-1-苯基-1-乙醇(3a): 无色油状液体, 收率82%;1H NMRδ: 7.38(dd,J=6.2 Hz, 4.5 Hz, 4H), 7.35(s, 2H), 7.30(dd,J=8.8 Hz, 2.2 Hz, 3H), 4.84~4.62(m, 1H), 3.31(dd,J=13.8 Hz, 3.7 Hz, 1H), 3.14(dd,J=13.8 Hz, 9.2 Hz, 1H), 2.76(d,J=2.3 Hz, 1H);13C NMRδ: 142.0, 141.2, 133.6, 132.9, 131.5, 129.3, 128.7, 128.4, 128.1, 125.8, 71.9, 44.1; MS(ESI)m/z: 265{[M+H]+}; Anal. calcd for C14H13OSCl: C 63.51, H 4.95, found C 63.63, H 5.08。
2-(4-氯苯巯基)-1-(4-氟苯基)-1-乙醇(3b): 无色油状液体,收率72%;1H NMRδ: 7.49~7.20(m, 5H), 7.07(dt,J=17.4 Hz, 8.7 Hz, 2H), 4.96~4.60(m, 1H), 3.58~3.27(m, 1H), 3.27~3.01(m, 1H), 2.80(d,J=2.3 Hz, 1H);13C NMRδ: 163.7, 161.3, 137.7, 133.4, 133.1, 131.7, 129.3, 127.53, 115.5, 71.2, 44.3; Anal. calcd for C14H12OSFCl: C 59.47, H 4.28, found C 59.30, H 4.39。
2-(4-氯苯巯基)-1-(4-溴苯基)-1-乙醇(3c): 白色固体,收率75%, m.p.81~83 ℃;1H NMRδ: 7.51(dd,J=12.4 Hz, 8.5 Hz, 2H), 7.36(d,J=8.8 Hz, 1H), 7.32(s, 1H), 7.31~7.29(m, 1H), 7.26(t,J=5.1 Hz, 2H), 7.23(d,J=1.5 Hz, 1H), 4.76(dd,J=47.7 Hz, 8.7 Hz, 1H), 3.44(ddd,J=18.9 Hz, 10.3 Hz, 6.1 Hz, 1H), 3.29~3.04(m, 1H), 2.80(d, J=2.6 Hz, 1H);13C NMRδ: 141.0, 133.2, 132.1~131.6, 129.4, 127.5, 122.3, 121.9, 71.2, 44.3; MS(ESI)m/z: 343{[M+H]+}; Anal. calcd for C14H12OSClBr: C 48.93, H 3.52, found C 50.05, H 3.47。
2-(4-氯苯巯基)-1-(4-氯苯基)-1-乙醇(3d): 无色油状液体,收率80%;1H NMRδ: 7.65(dd,J=82.8 Hz, 11.0 Hz, 1H), 7.41~7.35(m, 2H), 7.35(d,J=1.3 Hz, 2H), 7.33(s, 1H), 7.31(d,J=4.9 Hz, 1H), 7.28(s, 1H), 4.84~4.67(m, 1H), 3.50~3.36(m, 1H), 3.17(ddd,J=23.0 Hz, 13.8 Hz, 6.5 Hz, 1H), 2.56(s, 1H);13C NMRδ: 140.4, 139.6, 134.1, 133.8, 133.2, 131.8, 129.3, 128.8, 127.2, 71.2, 44.3; MS(ESI)m/z: 299{[M+H]+}; Anal. calcd for C14H12OSCl2: C 56.20, H 4.04, found C 56.29, H 4.11。
2-(4-氯苯巯基)-1-(2-氯苯基)-1-乙醇(3e): 无色油状液体,收率51%;1H NMRδ: 7.65(d,J=7.3 Hz, 1H), 7.46~7.36(m, 2H), 7.35(d,J=1.2 Hz, 1H), 7.32(d,J=5.9 Hz, 2H), 7.29~7.18(m, 2H), 5.17(dd,J=32.7 Hz, 9.1 Hz, 1H), 3.67(dd,J=10.4 Hz, 2.9 Hz, 1H), 3.51~3.29(m, 1H), 3.03~2.86(m, 1H);13C NMRδ: 139.3, 138.6, 133.0, 131.8, 131.6, 129.7, 128.9, 127.2, 68.3, 42.3; MS(ESI)m/z: 299{[M+H]+}; Anal. calcd for C14H12OSCl2: C 56.20, H 4.04, found C 56.41, H 4.15。
2-(4-氯苯巯基)-1-(3-氯苯基)-1-乙醇(3f): 无色油状液体,收率72%;1H NMRδ: 8.00~7.43(m, 2H), 7.43~7.38(m, 1H), 7.37(d,J=8.8 Hz, 1H), 7.34~7.30(m, 2H), 7.28(s, 2H), 4.85~4.69(m, 1H), 3.51(dd,J=10.4 Hz, 3.6 Hz, 1H), 3.39(dd,J=10.4 Hz, 8.7 Hz, 1H), 2.58(s, 1H);13C NMRδ: 143.1, 134.6, 133.2, 131.8, 123.0, 129.4, 128.5, 126.0, 124.0, 71.2, 44.2; MS(ESI)m/z: 299{[M+H]+}; Anal. calcd for C14H12OSCl2: C 56.20, H 4.04, found C 56.37, H 4.19。
2-(4-氯苯巯基)-1-(4-甲苯基)-1-乙醇(3g): 无色油状液体,收率86%;1H NMRδ: 7.36(d,J=8.7 Hz, 2H), 7.33~7.26(m, 3H), 7.25(s, 1H), 7.18(d,J=8.0 Hz, 2H), 4.72(d,J=8.7 Hz, 1H), 3.29(dd,J=13.7 Hz, 3.9 Hz, 1H), 3.14(dd,J=13.7 Hz, 9.1 Hz, 1H), 2.70(d,J=2.5 Hz, 1H), 2.37(s, 3H);13C NMRδ: 139.1, 137.9, 133.8, 132.8, 131.5, 129.3, 125.8, 71.8, 44.0, 21.1; MS(ESI)m/z: 279{[M+H]+}; Anal. calcd for C15H15OSCl: C 64.62, H 5.42, found C 64.51, H 5.56。
1-(4-叔丁基苯基)-2-(4-氯苯巯基)-1-乙醇(3h): 无色油状液体,收率73%;1H NMRδ: 7.43~7.37(m, 2H), 7.36~7.32(m, 2H), 7.32~7.26(m, 4H), 4.74(d,J=8.8 Hz, 1H), 3.31(dd,J=13.7 Hz, 3.9 Hz, 1H), 3.17(dd,J=13.7 Hz, 9.0 Hz, 1H), 2.80(s, 1H), 1.35(s, 9H);13C NMRδ: 151.2, 139.1, 133.9, 132.7, 131.4, 129.2, 125.6, 71.9, 43.8, 34.6, 31.4; MS(ESI)m/z: 321{[M+H]+}; Anal. calcd for C18H21OSCl: C 67.38, H 6.60, found C 67.55, H 6.52。
2-(4-氯苯巯基)-1-(4-硝基苯基)-1-乙醇(3i): 黄色油状液体,收率71%;1H NMRδ: 8.22(dd,J=13.7 Hz, 8.8 Hz, 3H), 7.56(dd,J=20.2 Hz, 8.5 Hz, 3H), 7.38(d,J=8.7 Hz, 1H), 7.33~7.28(m, 1H), 4.94~4.81(m, 1H), 3.55(dd,J=10.5 Hz, 3.8 Hz, 1H), 3.41~3.28(m, 1H), 3.07(dd,J=13.9 Hz, 9.1 Hz, 1H);13C NMRδ: 149.2, 148.2, 147.6, 133.5, 132.7, 132.1, 129.5, 126.8, 123.9, 70.8, 44.3; MS(ESI)m/z: 310 {[M+H]+}; Anal. calcd for C14H12NO3SCl: C 54.28, H 3.90, found C 54.19, H 3.83。
4-(2-(4-氯苯巯基)-1-羟乙基)苯甲酸甲酯(3j): 无色油状液体,收率75%;1H NMRδ: 8.04(dd,J=11.3 Hz, 8.4 Hz, 2H), 7.47(d,J=8.2 Hz, 1H), 7.44(s, 1H), 7.42~7.37(m, 1H), 7.36(d,J=2.1 Hz, 1H), 7.31(d,J=2.1 Hz, 1H), 7.30~7.25(m, 1H), 4.84(dd,J=44.5 Hz, 8.0 Hz, 1H), 3.94(d,J=1.6 Hz, 3H), 3.54~3.36(m, 1H), 3.33~3.06(m, 1H), 2.95(s, 1H);13C NMRδ: 166.8, 147.0, 146.0, 133.2, 131.8, 130.2~129.7, 129.4, 125.8, 71.3, 52.2, 44.2; MS(ESI)m/z: 323{[M+H]+}; Anal. calcd for C16H15O3SCl: C 59.53, H 4.68, found C 59.34, H 4.83。
2-(4-氯苯巯基)-1-(萘-2-基)-1-乙醇(3k): 无色油状液体,收率72%;1H NMRδ: 7.88~7.83(m, 3H), 7.81(d,J=0.4 Hz, 1H), 7.54~7.49(m, 2H), 7.46(dd,J=8.5 Hz, 1.7 Hz, 1H), 7.39~7.34(m, 2H), 7.32~7.27(m, 2H), 4.91(dd,J=9.0 Hz, 3.6 Hz, 1H), 3.37(dd,J=13.8 Hz, 3.8 Hz, 1H), 3.28~3.14(m, 1H), 3.00(s, 1H);13C NMRδ: 139.3, 138.5, 133.6, 133.2, 132.9, 131.7, 129.3, 128. 6, 128.0, 127.8, 126.3, 124.9, 123.7, 123.4, 72.0, 44.1; MS(ESI)m/z:315{[M+H]+}; Anal. calcd for C18H15OSCl: C 68.67, H 4.80, found C 68.82, H 4.94。
1-(4-氯苯巯基)-2-苯基-2-丙醇(3l): 无色油状液体,收率74%;1H NMRδ: 7.49~7.45(m, 2H), 7.36(dd,J=8.2 Hz, 6.7 Hz, 2H), 7.28(dd,J=13.6 Hz, 8.0 Hz, 3H), 7.21(d,J=8.8 Hz, 2H), 3.54(d,J=13.3 Hz, 1H), 3.35(d,J=13.3 Hz, 1H), 2.90(s, 1H), 1.66(s, 3H);13C NMRδ: 146.0, 144.3, 135.1, 132.4, 131.4, 129.0, 128.4, 127.5, 127.2, 124.8, 72.7, 49.8, 24.2; MS(ESI)m/z: 279{[M+H]+}; Anal. calcd for C15H15OSCl: C 64.62, H 5.42, found C 64.71, H 5.36。
1-(4-氯苯巯基)-2-(4-氟苯基)-2-丙醇(3m): 无色油状液体,收率65%;1H NMRδ: 7.31(dd,J=8.7 Hz, 5.3 Hz, 2H), 7.24~7.06(m, 4H), 6.91(t,J=8.7 Hz, 2H), 3.39(d,J=13.4 Hz, 1H), 3.21(d,J=13.4 Hz, 1H), 2.76(s, 1H), 1.52(s, 3H);13C NMRδ: 141.7, 134.8, 132.6, 131.4, 129.1, 126.6, 115.0, 73.8, 49.9, 30.4~27.7; MS(ESI)m/z: 297{[M+H]+}; Anal. calcd for C15H14OSFCl: C 60.71, H 4.75, found C 60.54, H 4.59。
2-(4-氯苯巯基)-1,1-二苯基-1-乙醇(3n): 无色油状液体,收率76%;1H NMRδ: 7.38~7.32(m, 1H), 7.23(d,J=6.9 Hz, 1H), 7.21~7.14(m, 1H), 7.11(d,J=8.7 Hz, 1H), 3.75(s, 1H), 3.36(s, 1H);13C NMRδ: 146.0, 136.7, 131.3, 130.7, 128.4, 127.6, 126.6, 126.1, 77.4; MS(ESI)m/z: 341{[M+H]+}; Anal. calcd for C20H17OSCl: C 70.47, H 5.03, found C 70.25, H 5.13。
2-(4-氯苯巯基)-1-苯基-1-丙醇(3o): 无色油状液体,收率66%;1H NMRδ: 7.47~7.41(m, 2H), 7.36(d,J=1.1 Hz, 2H), 7.33(d,J=8.7 Hz, 4H), 7.29(d,J=2.7 Hz, 1H), 4.77(s, 1H), 3.52(dd,J=7.0 Hz, 3.3 Hz, 1H), 2.75(d,J=2.1 Hz, 1H), 1.18(d,J=7.0 Hz, 3H);13C NMRδ: 140.7, 133.7, 132.7, 129.3, 128.3, 127.6, 126.0, 73.6, 51.7, 13.4; MS(ESI)m/z: 279{[M+H]+}; Anal. calcd for C15H15OSCl: C 64.62, H 5.42, found C 64.88, H 5.65。
2-(4-氯苯巯基)-1,2-二苯基-1-乙醇(3p): 无色油状液体,收率58%;1H NMRδ: 7.41(dd,J=4.6 Hz, 0.6 Hz, 1H), 7.32~7.28(m, 3H), 7.27(dd,J=3.8 Hz, 1.7 Hz, 3H), 7.26(s, 1H), 7.21(dd,J=6.9 Hz, 2.9 Hz, 2H), 7.15(s, 4H), 5.06(dd,J=6.3 Hz, 2.3 Hz, 1H), 4.41(t,J=4.7 Hz, 1H), 2.44(d,J=3.0 Hz, 1H);13C NMRδ: 140.5, 137.6, 133.7, 129.0, 128.4, 128.1, 127.8, 126.8, 76.3, 61.6; MS(ESI)m/z: 341{[M+H]+}; Anal. calcd for C20H17OSCl: C 70.47, H 5.03, found C 70.34, H 5.11。
2-(4-氯苯巯基)-1-环己醇(3q): 无色油状液体,收率51%;1H NMRδ: 7.33(d,J=8.7 Hz, 2H), 7.26(d,J=8.7 Hz, 2H), 4.43~3.63(m, 2H), 3.37(d,J=4.3 Hz, 1H), 2.26(s, 2H), 2.23~2.03(m, 2H), 1.81(dd,J=12.8 Hz, 5.0 Hz, 2H), 1.63~1.54(m, 2H);13C NMRδ: 134.3, 132.5, 131.9, 129.1, 82.1, 78.4, 54.1, 35.7, 34.2, 33.4, 31.0, 22.1, 21.9; MS(ESI)m/z: 243{[M+H]+}; Anal. calcd for C12H15OSCl: C 59.37, H 6.23, found C 59.52, H 6.36。
1-(4-氯苯巯基)-4-甲基-2-丁醇(3r): 无色油状液体,收率65%;1H NMRδ: 7.42~7.30(m, 2H), 7.28(t,J=4.4 Hz, 2H), 3.86~3.69(m, 1H), 3.39(d,J=3.4 Hz, 1H), 3.26~3.08(m, 1H), 2.85(dd,J=13.6 Hz, 8.6 Hz, 1H), 1.50(dd,J=13.0 Hz, 4.3 Hz, 1H), 1.34(dd,J=11.3 Hz, 2.6 Hz, 2H), 0.95~0.89(m, 6H);13C NMRδ: 134.1, 132.6, 131.3, 129.2, 69.2, 67.7, 45.7, 45.3, 43.0, 24.9, 23.2, 22.1, 17.4; MS(ESI)m/z: 245{[M+H]+}; Anal. calcd for C12H17OSCl: C 58.88, H 7.00, found C 59.09, H 69.85。
4-溴-1-(4-氯苯巯基)-2-丁醇(3s): 无色油状液体,收率66%;1H NMRδ: 7.34~7.31(m, 2H), 7.31~7.27(m, 2H), 4.12~4.07(m, 1H), 3.97(d,J=7.2 Hz, 1H), 3.89(d,J=2.1 Hz, 1H), 3.87(s, 1H), 3.80~3.71(m, 1H), 3.69(dd,J=9.2 Hz, 5.3 Hz, 1H), 2.34(dd,J=13.0 Hz, 6.7 Hz, 1H), 1.92(dd,J=13.0 Hz, 7.5 Hz, 1H);13C NMRδ: 134.1, 132.9, 132.0, 129.2, 73. 5, 67.6, 45.1, 33.1; MS(ESI)m/z: 295{[M+H]+}. Anal. calcd for C10H12OSClBr: C 40.63, H 4.09, found C 40.54, H 4.17。
1-苯基-2-苯巯基-1-乙醇(3t): 无色油状液体,收率76%;1H NMRδ: 7.46(dd,J=8.3 Hz, 1.2 Hz, 2H), 7.41~7.37(m, 5H), 7.35(d,J=1.5 Hz, 1H), 7.34(dd,J=3.0 Hz, 1.5 Hz, 1H), 7.28(d,J=7.4 Hz, 1H), 4.76(dd,J=9.4 Hz, 3.6 Hz, 1H), 3.36(dd,J=13.8 Hz, 3.6 Hz, 1H), 3.14(dd,J=13.8 Hz, 9.4 Hz, 1H), 2.98(s, 1H);13C NMRδ: 142.2, 135.0, 130.2, 129.2, 128.6, 128.0, 126.8, 125.9, 71.8, 44.0; MS(ESI)m/z: 231{[M+H]+}; Anal. calcd for C14H14OS: C 73.01, H 6.13, found C 73.21, H 6.24。
1-苯基-2-(4-甲苯巯基)硫基-1-乙醇(3u): 无色油状液体,收率80%;1H NMRδ: 7.41~7.40(m, 1H), 7.38(d,J=4.2 Hz, 5H), 7.34(dd,J=5.1 Hz, 3.6 Hz, 1H), 7.18(d,J=7.9 Hz, 2H), 4.72(dd,J=9.5 Hz, 3.5 Hz, 1H), 3.31(dd,J=13.8 Hz, 3.5 Hz, 1H), 3.14~3.08(m, 1H), 3.06(s, 1H), 2.39(s, 3H);13C NMRδ: 142.3, 137.1, 131.1, 130.0, 128.6, 128.0, 125.9, 71.6, 44.8, 21.1; MS(ESI)m/z: 245{[M+H]+}; Anal. calcd for C15H16OS: C 73.73, H 6.60, found C 73.91, H 6.44。
2-(3,5-二甲基苯巯基)-1-苯基-1-乙醇(3v): 无色油状液体,收率78%;1H NMRδ: 7.39~7.18(m, 1H), 6.98(d,J=19.7 Hz, 1H), 6.83(s, 1H), 4.73(t,J=6.5 Hz, 1H), 3.34~3.31(m, 1H), 3.22(d,J=1.4 Hz, 1H), 3.19(t,J=4.0 Hz, 1H), 2.26(s, 1H);13C NMRδ: 143.3, 138.3, 135.8, 127.9, 127.5, 127.3, 126.9, 125.9, 72.4, 42.2, 19.9; MS(ESI)m/z: 259{[M+H]+}; Anal. calcd for C16H18OS: C 74.38, H 7.02, found C 74.50, H 7.11。
2-(4-氟苯巯基)-1,1-二苯基-1-乙醇(3w): 无色油状液体,收率52%;1H NMRδ: 7.43(dt,J=6.0 Hz, 5.3 Hz, 1H), 7.34(dd,J=4.6 Hz, 2.5 Hz, 1H), 7.31(dd,J=5.3 Hz, 3.3 Hz, 1H), 7.27(d,J=1.3 Hz, 1H), 7.25(t,J=1.4 Hz, 1H), 7.23~7.20(m, 1H), 7.00~6.84(m, 1H), 3.81(s, 1H), 3.56(d,J=8.7 Hz, 1H);13C NMRδ: 163.6, 159.7, 145.1, 133.2, 133.1, 128.3, 127.4, 126.2, 116.3, 116.0, 77.7, 50.3; MS(ESI)m/z: 325{[M+H]+}; Anal. calcd for C20H17OSF: C 74.05, H 5.28, found C 73.87, H 5.12。2-(4-溴苯巯基)-1,1-二苯基-1-乙醇(3x): 无色油状液体,收率74%;1H NMRδ: 7.49~7.39(m, 1H), 7.38~7.34(m, 1H), 7.32(dt,J=3.9 Hz, 1.7 Hz, 1H), 7.28(d,J=1.5 Hz, 1H), 7.27~7.25(m, 1H), 7.24(dd,J=3.3 Hz, 2.0 Hz, 1H), 7.22(d,J=2.6 Hz, 1H), 7.19(t,J=2.2 Hz, 1H), 3.84(d,J=5.0 Hz, 1H), 3.42(s, 1H);13C NMRδ: 145.0, 135.7, 131.9, 128.4, 127.5, 126.1, 120.6, 77.7, 49.1; MS(ESI)m/z: 385{[M+H]+}; Anal. calcd for C20H17OSBr: C 62.34, H 4.45, found C 62.22, H 4.32。
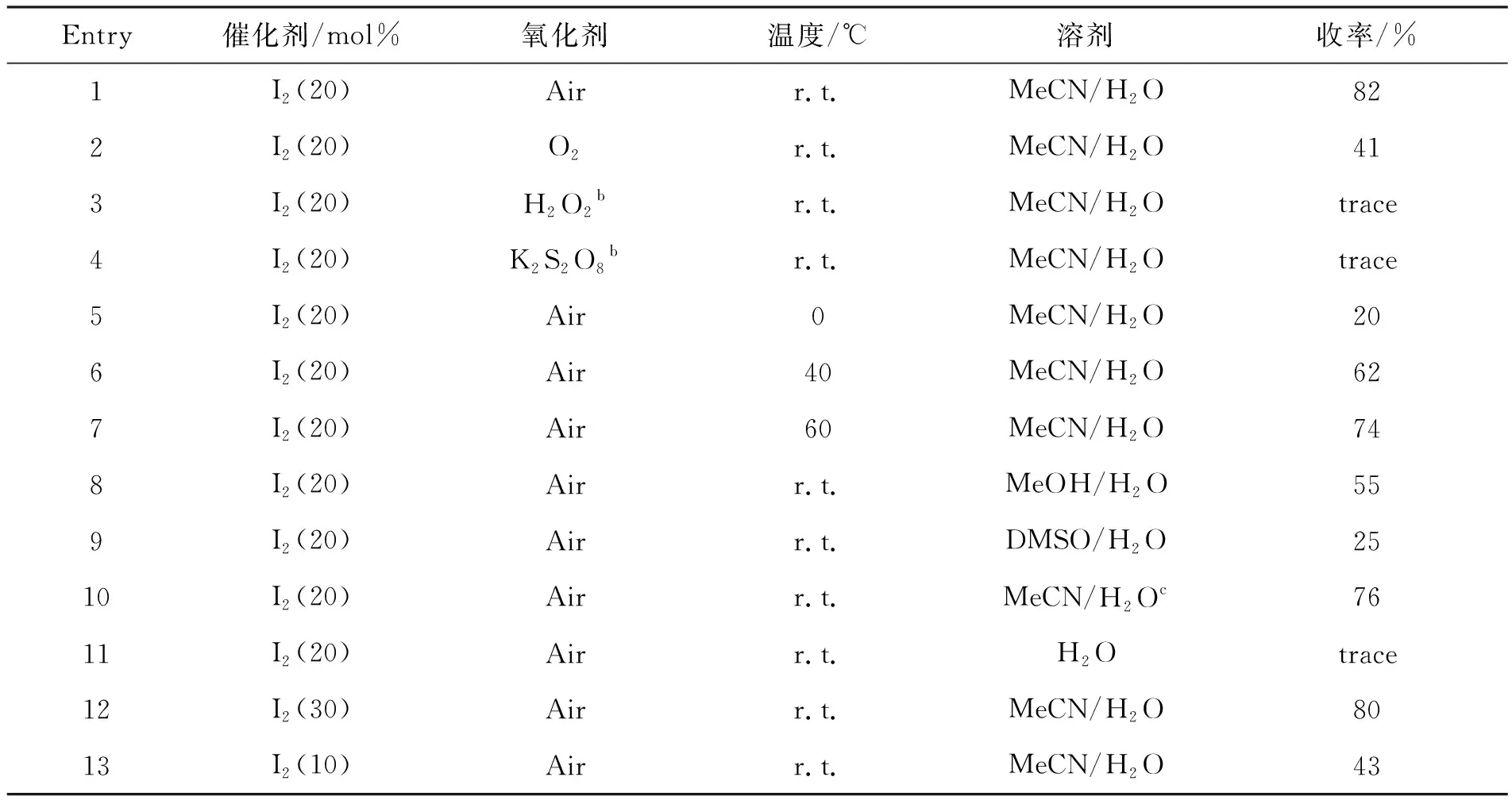
表1 反应条件对 3a 收率的影响
aReaction conditions:1a(0.5 mmol),2a(1 mmol),V(solvent)/V(H2O)=3/1(2 mL), 2 h;b1 mmol;cV(MeCN)/V(H2O)=1/1
2 结果与讨论
2.1 反应条件优化
以3a为例,对反应条件进行了优化,结果见表1。首先对不同氧化剂进行了筛选。当氧气作为氧化剂时,收率比空气做氧化剂时降低(Entry 2)。其他氧化剂如H2O2和K2S2O8均不能有效氧化该反应体系,只检测到微量反应产物(Entry 3, 4)。因此反应在空气中进行。接下来对反应温度进行筛选,结果表明反应温度为室温时,目标产物收率最高(Entry 5~7)。然后再对溶剂和催化剂的用量进行了筛选,当使用V(MeOH)/V(H2O)=3/1混合溶液和V(DMSO)/V(H2O)=3/1混合溶液时反应收率均有所下降(Entry 8, 9),采用V(MeCN)/(H2O)=1/1混合溶液反应时,收率较高(Entry 10),但仅以H2O为溶剂时,只检测到微量反应产物(Entry 11)。通过改变催化剂的用量发现:将催化剂用量增加至30 mol%时,反应收率无明显变化;将催化剂用量降低至10 mol%时,反应收率显著降低(Entry 12, 13)。
综上,最优的反应条件为:S-(4-氯苯基)-4-氯硫代苯磺酸酯(0.5 mmol),苯乙烯(1 mmol,),I2(0.1 mmol, 20 mol%),室温条件下,在充满空气的反应管中反应2 h。
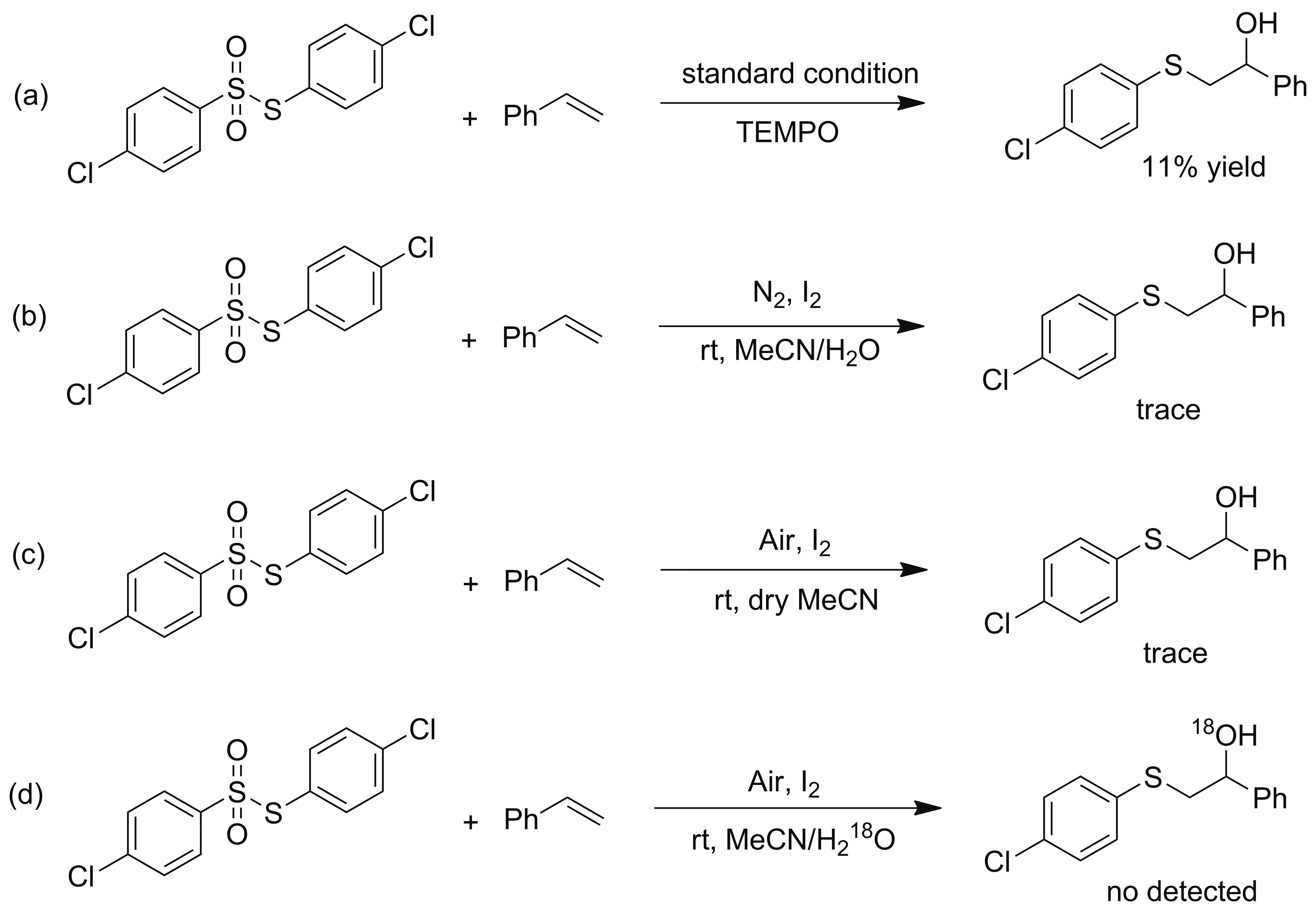
Scheme 2
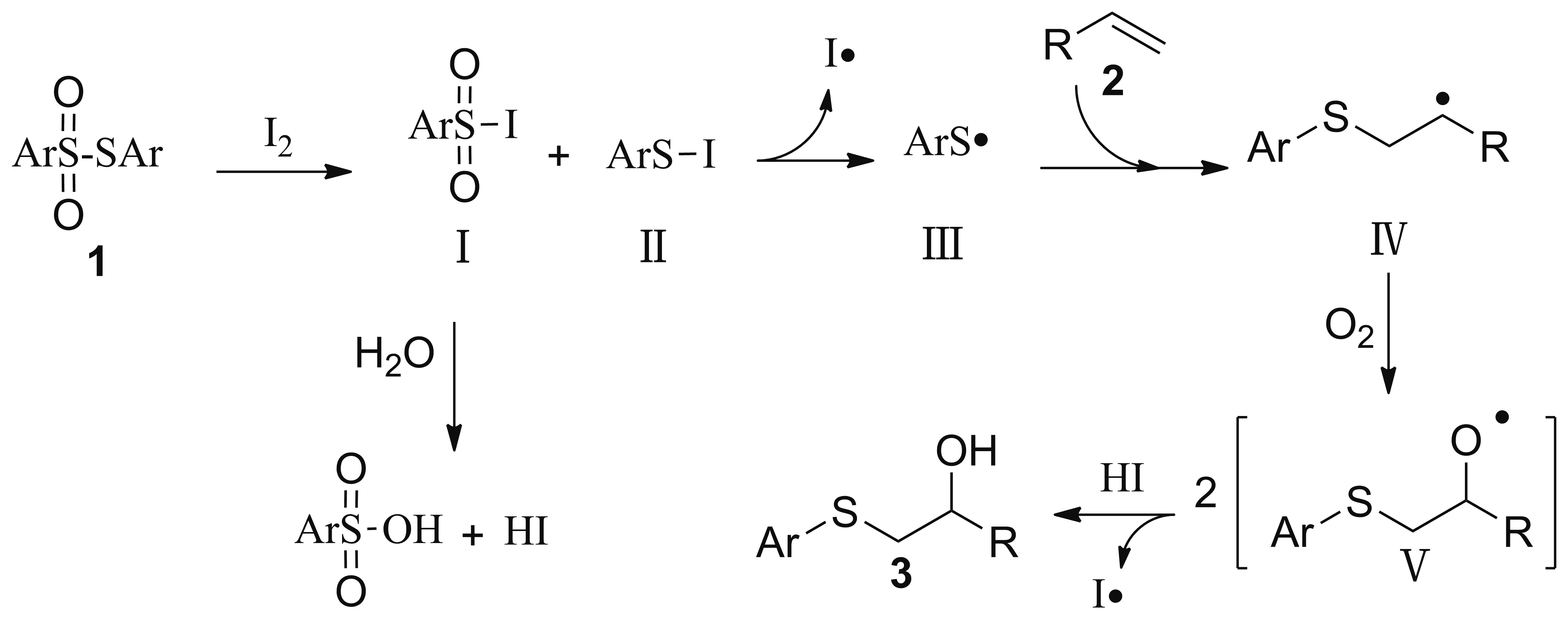
Scheme 3
2.2 底物适应性
在最优条件下,考察了底物的适应性。结果表明:使用带有不同取代基的芳基烯烃进行反应均可生成对应目标产物,并得到51%~86%的收率。烯烃芳环取代基的电子性质对反应影响不大,供电子基和吸电子基均可得到较高的收率(3g~3j)。值得注意的是,烯烃取代基的空间位阻效应对反应收率影响较大,空间位阻越大收率越低(3d~3f)。然而α,α-取代的烯烃在最优反应条件下得到了较高的收率(3l~3n),α,β-取代的烯烃也可以参与该反应,可能是空间位阻的原因,仅获得中等的收率(3o,3p)。除芳基烯烃外,烷基烯烃如环己烯(2q)、 4-甲基-1-戊烯(2r)和4-溴-1-丁烯(2s)在该反应体系中也能生成相应的β-羟基硫醚,并得到中等收率51%~66%(3q~3s)。此外,带有不同取代基的含硫化合物,如带有氟、氯、溴、甲基的含硫化物均可得到对应的β-羟基硫醚(3t~3x)。
2.3 机理探究及反应机理
为了进一步探究反应机理,进行了控制实验(Scheme 2)。以3a的合成为模板反应,在最优条件下探究该反应的反应机理。首先,通过使用2,2,6,6-四甲基-1-哌啶氧基(TEMPO)进行自由基捕获实验,仅获得11%收率的目标产物(2a),表明该反应可能经历自由基途径。接下来,当在没有O2的情况下进行反应时,获得微量的3a(2b)。当反应在没有H2O的情况下进行时,反应被完全抑制(2c)。此外,在最优条件下用H218O代替H2O时,分离产物3a并且未检测到18O标记的产物(2d)。这些结果表明产物中的氧原子不是来自H2O,它可能来自O2。
根据之前的相关报道和实验结果,提出一个可能的实验机理(Scheme 3)[11,40-41]。首先,I2活化硫代磺酸酯1形成中间体Ⅰ和Ⅱ;然后中间体Ⅰ优先和水反应生成磺酸以及HI,而中间体Ⅱ优先释放出巯基自由基Ⅲ和碘自由基[38];接下来巯基自由基Ⅲ和烯烃发生自由基加成反应生成自由基Ⅳ;之后自由基Ⅳ与一分子分子氧反应生成两分子过氧基V[42];最后自由基中间体V进一步攫取HI中的H生成最终产物3,同时生成碘自由基,两分子碘自由基互相反应生成I2分子,完成催化剂的循环。
以碘单质催化烯烃和硫代磺酸酯反应,合成了24个β-羟基硫醚化合物,并优化了反应条件。此反应选用碘单质作为催化剂在乙腈溶液中进行,用硫代磺酸酯代替了有强烈刺激性气味和毒性的硫醇作为反应物,以空气中的氧气作为氧源,反应效率高、条件温和、后处理简单。不同的芳基烯烃和脂肪族烯烃在该转化中的收率均较高。
