植入式心脏监护仪远程监护的应用与发展
2020-07-13赵亚楠丁立刚
赵亚楠 丁立刚
植入式心脏监护仪(insertable cardiac monitor,ICM),亦被称为植入式循环记录器,是一种皮下植入设备,可以在较长时间内连续记录心电信号,存储关于心律失常发作频率、持续时间和其他相关数据,并远程传输以供临床医生回顾。当需要对心律失常进行长期监测时,ICM是有用的。根据当前设备的电池寿命能够进行长达3年的持续监测,从而帮助克服短期心电监测的局限性[1]。
ICM是在20世纪90年代为诊断不明原因晕厥而设计的,在过去的15~20年间,ICM的商业化应用使得心脏监测有了很大的进步。随着近年来ICM技术的改进,如自动心律失常检测算法的增加、记录节律的远程传输、设备的小型化和植入技术的简化等,ICM的应用场合逐渐增多[2]。目前可用的植入式监护仪包括美敦力公司的Reveal XT和Reveal LINQ,雅培公司的Confirm和Confirm Rx,以及德国柏林Biotronik公司的BioMonitor 2型。Reveal XT(美敦力)增加了自动房颤检测算法的功能,通过使用Lorenz曲线图评估2 min内心脏节律变化来检测房颤。Reveal LINQ(美敦力)是目前市场上最小的ICM,尺寸只有7 mm×45 mm×4 mm,可以极大地简化植入过程,具有3年电池续航时间,可行磁共振和自动心律失常检测,包含改进的房颤检测算法,以及名为“P波感知”的额外专利功能,旨在降低假阳性房颤检出率。P波感知算法显示,加入标准的房颤检测算法后,房颤的假阳性检出率降低46%[3-4]。目前已确定的ICM使用适应证包括不明原因的晕厥、心悸和房颤的治疗[5-6]。
1 不明原因性晕厥
晕厥是一种常见的临床症状,是由脑灌注不足引起的短暂性意识丧失,持续时间短,可迅速而自发地恢复。Framingham研究数据显示晕厥的发生率为每年每1000例中发生6.2例,终生累积发病率为30%~40%,占所有急诊就诊患者的3%~6%[7-9]。晕厥的病因可分为神经反射性晕厥、心源性晕厥和直立性低血压等。神经反射性晕厥是最常见的类型,通常预后较好,而心源性晕厥患者与未发生晕厥的患者相比死亡风险增加1倍[7]。常规的晕厥评估包括询问病史、体格检查、24 h动态心电图、直立倾斜试验,部分可能需要行心电生理检查进一步明确。然而,经过一系列的晕厥评估后,仍有超过1/3的晕厥患者未能明确诊断[8]。研究表明,大多数不明原因晕厥的病因可能为心源性晕厥[10]。由于晕厥发作之间可能要经过很长一段时间,因此,ICM提供的长期监测,可能是捕获晕厥发作期间心律的唯一手段。
2017 ACC/AHA/HRS晕厥指南推荐ICM用于部分疑似心律失常所致晕厥(Ⅱa,B-R类)[11]。2009 ESC/EHRA晕厥指南推荐ICM用于下列情况(ⅠB):① 无高风险特征患者的早期评估;② 初步评估结果为阴性的高风险患者[12]。
Krahn等[13]于1995年首次报道了ICM在不明原因晕厥评估中的作用,结果显示在反复不明原因晕厥的患者中,与常规检查相比,ICM最终所需诊断费用更低。多个随机对照试验和观察性研究已经证明了ICM在不明原因晕厥诊断中的有效性。ISSUE研究是另一项对ICM的早期研究[14],研究表明无论何种人群ICM都能够帮助大多数监测期间出现反复晕厥的患者诊断晕厥原因,该研究帮助确立ICM为诊断不明原因晕厥的重要工具。ISSUE2研究证实了在疑似神经介导的反复性晕厥患者中使用ICM的重要性[15]。在监测期间复发的晕厥患者中,大约3/4的患者获得心电图诊断。在试验的第二阶段,接受ICM指导治疗的患者与未接受特殊治疗的患者相比,晕厥复发的发生率明显降低(10%vs.41%),表明接受ICM指导治疗的患者晕厥的相对风险大幅度降低。ISSUE3研究表明尽管被诊断为神经介导性晕厥,但实际上13%的患者晕厥原因为心律失常[16]。RAST研究将60名不明原因晕厥患者随机分为ICM组和常规检查组(包括体外循环记录仪、倾斜试验和电生理检查),并进行平均10.5个月的随访,研究结果表明ICM组的诊断率为55%,而对照组为19%(P=0.0014)[17]。PICTURE研究为多中心前瞻性研究[10],该研究对570名不明原因晕厥患者植入ICM,进行平均10个月的随访,结果ICM诊断晕厥的比例为78%。EaSyAS研究显示了ICM在评估不明原因晕厥方面的有效性[18],患者被随机分为ICM监测组或标准治疗组,经过17个月的中位随访,ICM组88%的反复晕厥患者基于心电图得出诊断,而常规组只有19%的患者得出诊断。EaSyASⅡ研究为前瞻性随机研究[19],结果证实接受ICM植入患者与经过常规评估的患者相比,不明原因晕厥诊断率更高且所需时间显著缩短。
2 不明原因卒中和无症状房颤
虽然评估不明原因晕厥仍然是ICM最常见的适应证,但它正越来越多地被用于检测房颤。房颤是最常见的持续性心律失常,与房颤相关的主要问题是卒中风险的增加。Framingham研究表明房颤使卒中风险增加5倍,死亡风险增加2倍[20-21]。然而,多达40%的房颤患者完全无症状[22]。无症状房颤定义为在无症状的人群中检测到的房颤,既往无心电图能够诊断。由心电监测检测到的无症状房颤也与卒中的风险增加有关,约25%无症状房颤患者卒中可能是唯一的临床表现[22]。不明原因卒中是指有症状的脑梗死患者经过充分诊断评估后仍未确定卒中的原因[23]。由于阵发性房颤的特点,症状和房颤发作之间的相关性不高,因此无症状房颤很难被发现和诊断。随着动态心电图监测的改进,无症状房颤与不明原因卒中的关系日益明显。
几项小型的前瞻性研究证实,延长ICM监测可以在不明原因卒中患者中检测到房颤[24-26]。Ritter等[24]发现卒中2周后植入ICM,17%的不明原因卒中患者可以检测到房颤,平均检测时间为64 d。在同一组患者中,他们还发现在植入ICM同时佩戴7 d Holter监护仪患者中房颤检出率仅为1.7%。Cotter等[26]的研究结果显示房颤检出率为25.5%,平均诊断时间为48 d。Etgen等[25]的研究结果显示房颤检出率为27.3%,平均诊断时间为153 d。值得注意的是,在所有报告的患者中,首次发现房颤的平均时间超过1个月,这支持短期体外心电监测可能不足以满足检测高危患者的观点。这些观察性研究为在不明原因卒中患者中使用ICM检测房颤的更大规模的随机对照研究奠定了基础。这些结果汇总见表1。
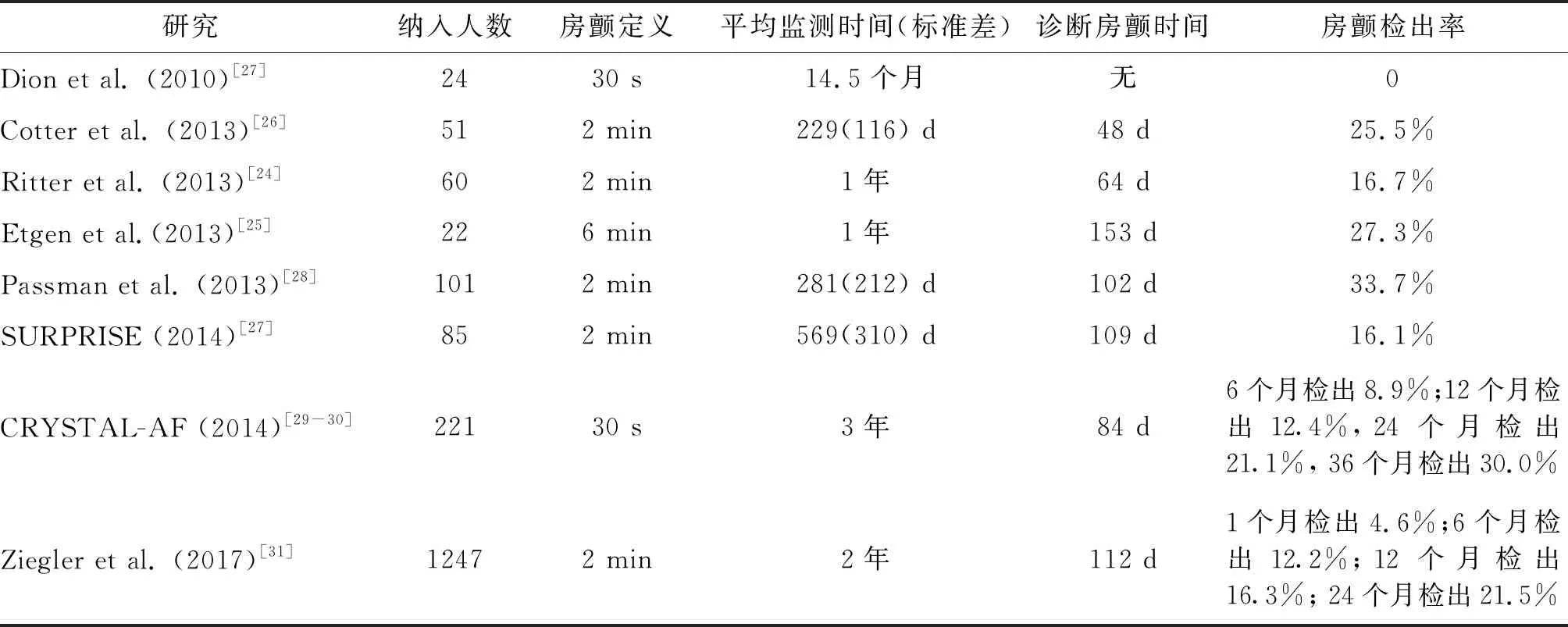
表1 植入式心脏监护仪对不明原因卒中患者中房颤的诊断率
Crystal-AF研究是首个研究不明原因卒中患者中无症状房颤的随机对照试验,也是当时规模最大的ICM研究[29]。该研究将441名患有不明原因卒中或短暂性脑缺血发作(TIA)的患者按照1 ∶1比例随机分为ICM组和对照组来检测房颤。主要和次要终点为在6个月和12个月内发现持续时间30 s或更长的房颤。ICM组在6个月和12个月时分别检测到8.9%和12.4%的房颤患者,而对照组分别为1.4%和2.0%。随访研究发现,ICM组24个月和3年的累计房颤检出率分别为21.1%和30.0%,而对照组分别为3.0%和3.0%[30]。在最初的研究中,ICM组房颤检测的中位时间为84 d,在3年的随访研究中,中位时间为8.4个月。
Ziegler等[31]报道一项研究不明原因卒中患者中无症状房颤发生率的前瞻性观察研究,该研究使用一个包含1200多名患者的数据库,这些患者接受ICM植入,并接受长达2年的随访。主要终点为房颤持续时间超过2 min。房颤检出率在1、6、12和24个月分别为4.6%、12.2%、16.3%和21.5%,中位房颤检出时间为112 d。Crystal-AF和Ziegler等的研究结果表明,不明原因卒中患者中无症状房颤发生率比之前认为的更高。这两项研究的房颤检出率非常相似,检测到房颤的中位时间(原始Crystal-AF研究为84 d,Ziegler等的研究为112 d)已超过当前ASA/AHA指南建议的30 d监测期限。如果只进行长达30 d的监测,Crystal-AF研究及Ziegler等的研究分别有88%和79%的房颤患者将会被遗漏[29-31]。根据这些研究结果,专家小组建议,如果最初30 d的监测结果为阴性,则考虑使用ICM进行较长期的监测[1]。
3 抗凝治疗
虽然多项研究证实了ICM在检测房颤方面的有效性,但ICM的心律监测对于阵发性房颤患者的抗凝治疗指导意义可能更大。无论阵发性房颤患者是否维持窦性心律,目前指南建议对卒中高危患者均要持续抗凝。因为服用抗心律失常药物的患者仍然极有可能发生房颤复发和卒中,而且体外监护仪对于检测房颤复发的敏感性很低,并且房颤复发通常是无症状的[32]。长期抗凝在降低患者缺血性卒中风险的同时,也使患者暴露在出血风险中。为了降低出血风险,理想的做法是只对持续房颤且有卒中风险的患者提供抗凝治疗,而对长时间保持窦性心律的患者停止使用口服抗凝治疗。由于目前ICM提供了长期的监测和极高的房颤检测准确性,临床医生是否可以对通过ICM监测长时间保持窦性心律的房颤患者停用抗凝药物,这是最近研究的主题。
最近两项研究表明,窦性心律后停用抗凝药物是安全的。Mascarenhas等[33]的研究表明阵发性房颤和高出血风险患者中使用ICM指导停用抗凝是安全的。本研究纳入70名经抗心律失常药物治疗的阵发性房颤患者,这些患者既有较高的卒中风险(CHA2DS2-VASc≥2分),又有较高的出血风险(出血≥3分),在恢复窦性心律后植入ICM。连续3个月维持窦性心律或低房颤负荷(定义为<1%房颤)的患者选择停用抗凝。在平均23.5个月的随访期间,76%的患者停用抗凝治疗,这些患者未发生包括卒中或短暂性脑缺血发作在内的不良事件。停用口服抗凝药物的患者中无出血事件,而服用抗凝药物的患者中有1/4出现严重出血事件,需要住院治疗。同样,Zuern等[34]对65例房颤消融3个月后CHADS2评分为1~3的患者植入ICM,ICM植入后停用口服抗凝药物,在平均32个月的随访中,63%的患者房颤负荷每天<1 h,未观察到卒中或其他血栓栓塞事件。
当ICM的持续远程监测能力与新型口服抗凝药的使用相结合时,另一种口服抗凝药物管理“口袋药”方法成为阵发性房颤患者的选择,仅在房颤发作时才服用新型口服抗凝药物,而在窦性心律期间停止抗凝。这种方法可以潜在地减少口服抗凝药物的使用并可降低与持续抗凝相关的出血风险,同时通过在阵发性房颤发作期间进行抗凝来提供对阵发性房颤相关卒中的保护。REACT.COM试点研究证明了该方法的安全性和可行性[28],该研究纳入59名非永久性房颤患者,CHADS2评分为1~2分,既往植入过ICM,可以服用新型口服抗凝药。60 d内未检测到持续≥1 h的房颤,停止抗凝。每日远程传输检查是否有房颤复发,只有在检测到持续≥1 h的房颤发作时,才重新启动抗凝治疗。在14个月的中位随访时间内,69%的患者为无房颤复发和未服用抗凝药物,仅有31%的患者有持续≥1 h的房颤复发。使用该方法,抗凝时间缩短了94%。在研究期间,未观察到卒中或死亡。REACT.COM的研究结果表明ICM指导的个体化新型口服抗凝治疗的方法为非永久性房颤患者的慢性抗凝提供了一种可行的替代方案,但仍需更多的随机对照试验进一步验证。
4 总结
ICM的应用是临床医生评估潜在心律失常的理想方法。诊断不明原因晕厥是植入ICM最常见的原因,目前ICM正越来越多地被用于检测房颤。多项研究表明不明原因卒中患者中检测房颤可能需要监测比当前指南建议更长的时间,因此ICM长期持续监测能显著提高无症状房颤的检出率,未来需要更多研究为该类患者植入ICM的指南提供更多证据。近年来多项研究表明,ICM监测指导新型口服抗凝药物应用,可能会潜在降低房颤患者出血风险而同时卒中风险并未增加,为远程监测指导的个体化抗凝开辟新的可能,但需要进一步的研究证实其有效性。
