五唑非金属盐的氢键作用规律
2020-07-11王鹏程姜振明周新利林秋汉
王鹏程,姜振明,周新利,林秋汉,陆 明
(1. 南京理工大学化工学院,江苏 南京 210094;2. 甘肃银光化学工业集团有限公司,甘肃 白银 730999)
1 引言
五唑阴离子(N5-)是近年来报道的一种新型全氮结构单元[1-3]。理论研究表明,五唑阴离子的能量比全氮阴离子叠氮离子(N3-)高出近一倍,因此,通过离子匹配组装制备的金属、非金属衍生物有望开发成一类高能量密度的含能材料[4-5]。最早报道的五唑衍生物是五唑金属盐,包括碱金属、碱土金属以及过渡金属。五唑金属盐易于制备的原因在于两个方面,一是金属阳离子的电正性强,有利于形成稳定的阴阳离子对;二是金属阳离子,特别是过渡金属类,能够提供可配位的空轨道,形成配位化合物[6-8]。五唑金属盐具有一定的爆炸威力,理论上高于叠氮金属盐[4]。然而,构成这些盐的主要部分是金属阳离子,金属对总体爆炸能量的贡献很小,因此目前的五唑金属盐所储存的能量是有限的。但从另一个角度,无机的金属阳离子与有机离子的物化性质存在较大差异,利用好这种差异,利用离子交换的手段,金属盐可以作为制备非金属盐的很好的前驱物[9-10]。
已报到的用于制备非金属盐的金属盐前驱物可分为两类。第一类是以五唑钠为基础的离子交换。Na—N 键是弱配位键,易被其他相互作用所取代,如强配位键、N—H 氢键或N—O 配位键。采用这种方法制备出了3,9-二氨基-6,7-二氢-双([1,2,4]三唑)[4,3-e:3′,4′-g]并[1,2,4,5]四氮杂环庚烷(1)、N-氨基甲酰胍(2)、草酰肼(3)和4,4′,5,5′-四氨基-3,3′-双-1,2,4-三唑(4)六种非金属盐[11-12]。第二类是以五唑银或五唑钡为基础的离子交换。氯化银、硫酸钡在水溶液中的溶解性非常小,将有机盐酸盐、硫酸盐分别与五唑银、五唑钡进行置换反应,可以简单快捷的得到非金属盐。这种方法普适性好,对有机阳离子无结构要求。笔者采用这种方法制备了铵(5)、羟胺(6)、肼(7)、氨基胍(8)、二氨基胍(9)、双胍(10)、3,5-氨基-1,2,4-三唑(11)和3,6,7-三氨基-7H-[1,2,4]三唑[4,3-b]并[1,2,4]三唑(12)、氨氧基乙酸(13)、O-(4-硝基苄基)羟胺(14)、乙二胺(15)[13-14]。
约化密度梯度(RDG)分析是一种研究弱相互作用的方法,可以反映范德华力、氢键和静电等弱相互作用。杨文升等[15]利用RDG 分析HMX/NQ 共晶分子间中的氢键作用,所得氢键强度变化规律与共晶稳定性、感度一致。朱双飞等[16]研究了3,4-二硝基吡唑(DNP)与CL-20之间的相互作用,基于RDG 方法发现分子间氢键影响了CL-20 分子的电荷分布和电子密度分布,改变CL-20 引发键稳定性。可以认为,RDG 在含能材料的氢键作用分析中,准确性非常高,且具有很好的适用性。
在上述制备的非金属盐中,可以找到阳离子的一个共同点是都存在NH2结构,存在N—H…N 的氢键作用。这些氢键对组装过程中的影响,是否存在规律,尚无较为深入的研究。因此,本工作从五唑与非金属阳离子之间的氢键作用数量和强弱出发,研究非金属盐晶体结构中的氢键作用规律,为探寻其他适合的阳离子,开发新型含能离子盐提供理论依据。
2 计算方法
从文献[9-14]已报道的单晶结构中,取某一N5-离子及其周围阳离子为研究对象,进行密度泛函理论(DFT)分析。DFT 计算采用Gaussian 09 软件进行[17]。结构的优化和频率分析在B3LYP方法6-311++G(d,p)基组下获得。几何优化在默认收敛标准下进行,所有优化的结构是势能面局部能量极小值,没有虚频。总能量(E0)和零点能(ZPE)通过振动计算频率分析。氢键相互作用由Gaussian输出的波函数文件,采用Multiwfn软件由RDG 分析方法拟合得到[18-19],认为sign(λ2)ρ值小于-0.05 a.u.,为强氢键,在[-0.05,-0.02]a.u.范围为中氢键,[-0.02,0.02]a.u.为弱氢键,并与范德华原子半径(rw(N)+rw(N)-3.20 Å)相参考。
3 结果与讨论
本研究中的15 种非金属盐均为已有单晶结构报道。晶体1-4 的制备以Na+N5-为原料,与多种非金属阳离子的盐酸盐分别溶于甲醇溶液进行挥发,非金属阳离子依靠N—H 氢键的作用与N5-离子组装,从而在饱和溶液中形成晶体1-4 析出。晶体5-15 的制备是以 五 唑 银AgN5和 五 唑 钡Ba(N5)2为 原 料,利 用 氯 化银、硫酸钡在绝大多数溶剂中溶解性都非常小的特性,将AgN5和Ba(N5)2分别与不同非金属盐进行复分解反应,合成如图1 所示。
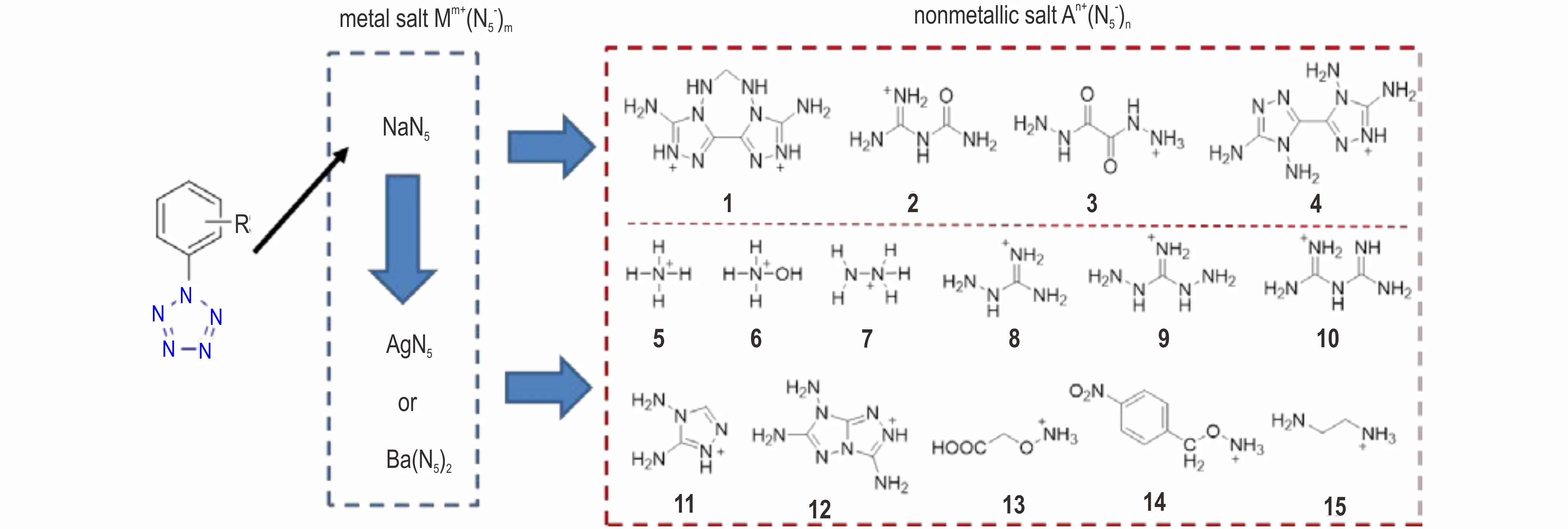
图1 五唑含能盐的合成图Fig.1 Synthesis route of pentazole salts
3.1 含氮氢阳离子的氢键作用
化合物5 和7 的阳离子为NH4+和N2H5+,整体离子盐不含有碳原子,只可能存在N—H…N 型氢键。从图2 中可以看出,对N5-离子而言,每个五元环所形成的氢键具有很好的对称性,呈轴对称分布,与单晶读取的N—N 键的对称性相一致。两种离子盐中的N—H…N 氢键键长分别为2.11 Å 和2.14 Å,按氢键强度计算公式计算后属于中等强度氢键作用(mHB),这种弱氢键作用对五唑环键长的影响较小。值得注意的是,化合物7 是目前非金属盐中等氢键作用和数量均最弱的分子,其N—N 键长平均键长为1.322 Å,与未受外界作用的键长接近。
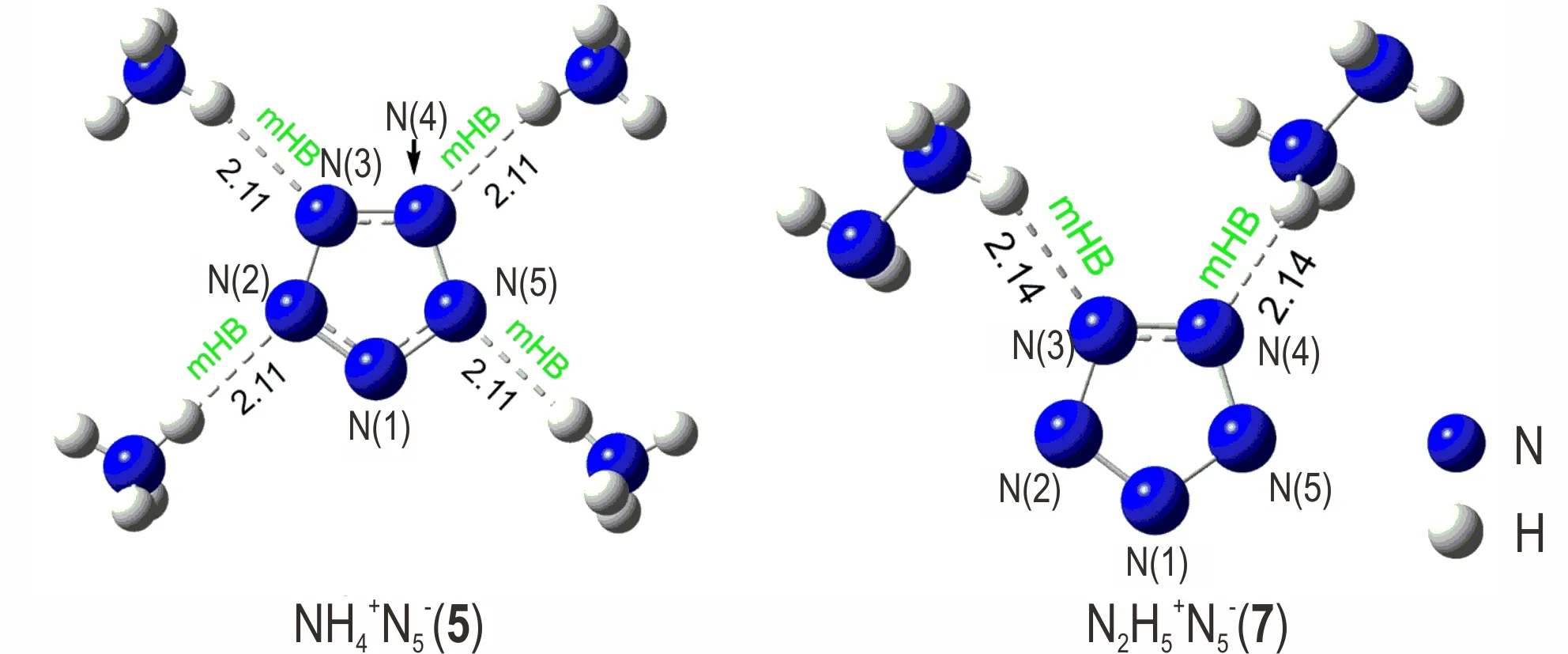
图2 化合物5 和7 的氢键作用(键长单位Å)Fig.2 Hydrogen bonding of compounds 5 and 7(unit of bond length is Å)
3.2 含碳氮氢的胍类阳离子的氢键作用
当分子结构较小时,氮氢化合物以氮元素为基础进行构建,如胺和肼有良好的稳定性,但是随着氮元素增加,多氮长链骨架的稳定性会急剧下降,必须依靠碳元素为骨架进行构建,形成胍等分子。化合物8、9、10分别基于氨基胍、二氨基胍、双胍阳离子进行构建。胍类阳离子提供氨基(—NH2)与N5-离子形成氢键(图3),其作用普遍属于弱氢键作用(wHB),存在大量键长>2.30 Å的氢键。化合物8 和9 中各存在一对强氢键作用(sHB),该强氢键作用明显降低了N—N 键键长。与化合物10 的N—N 平均键长1.317Å 相比,化合物8 和9的N—N 平均键长分别降至1.314 Å 和1.313Å。并且强弱氢键的作用强度不同使得环内部N—N 键长差异增大,化合物10 的N5-离子N—N 键长分布为1.316~1.318 Å,五唑环的均一性和对称性都保持良好,而化合 物8 和9 的 键 长 分 布 为1.304~1.319 Å 和1.308~1.317 Å,五唑环中个别键长明显变短,均一性变差,且已不具有对称性结构。由于N5-离子自身为共轭大π环,良好的均一性和对称性可显著提升含能化合物的稳定性,因此化合物10 的分解温度达到124.8 ℃。

图3 化合物8-10 的氢键作用(键长单位为Å)Fig.3 Hydrogen bonding of compounds 8-10(unit of bond length is Å)
3.3 含碳氮氢的氨基唑类阳离子的氢键作用
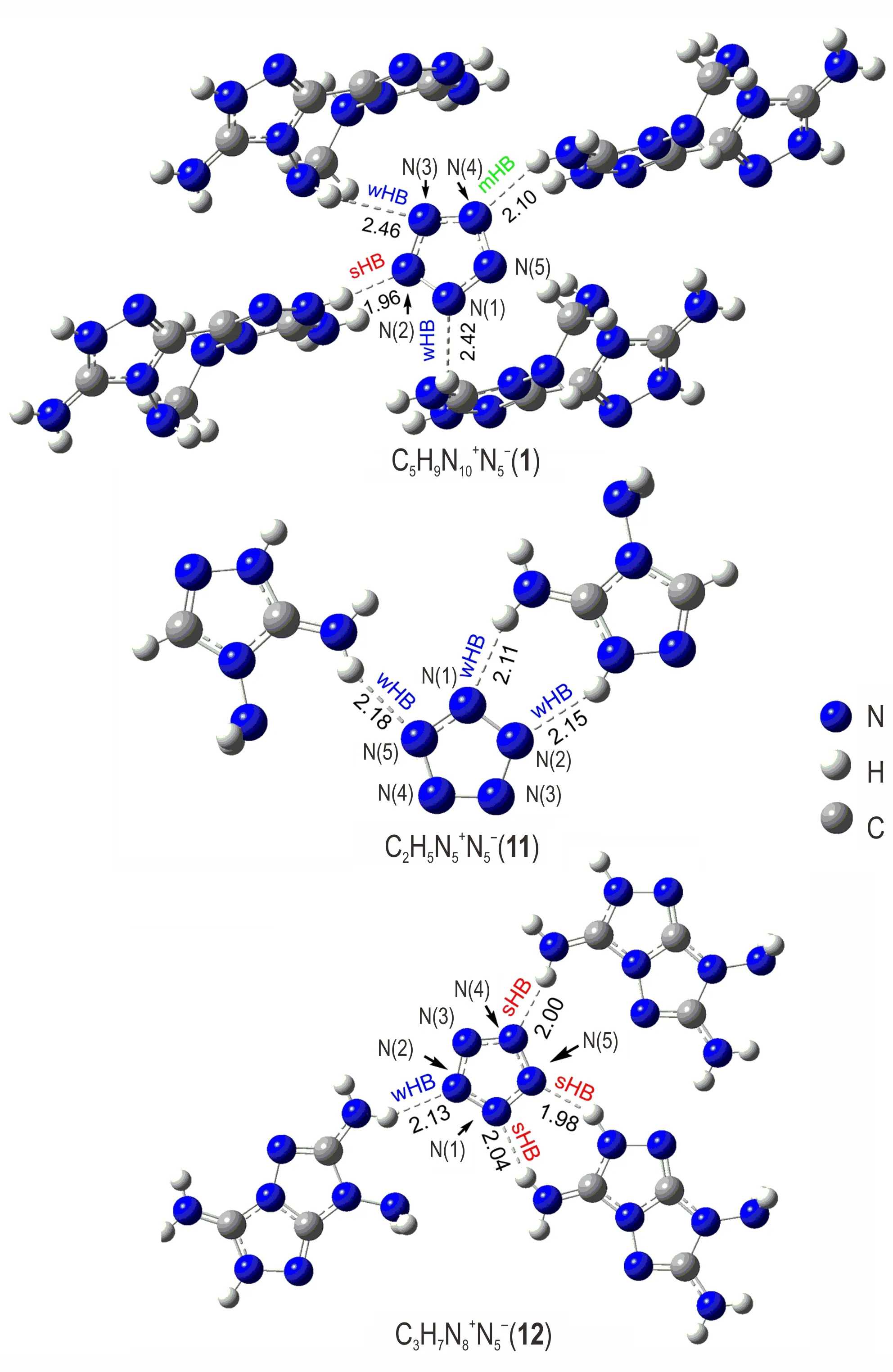
图4 化合物1,11 和12 的氢键作用(键长单位Å)Fig.4 Hydrogen bonding of compounds 1,11 and 12(unit of bond length is Å)
形成多氮唑环是碳氮氢体系的另外稳定方式,选取单三唑环、联三唑环、并三唑环三种阳离子进行构建,如图4 所示。从图4 可以看出,三唑环上的氨基仍能有效的形成氢键。除此以外,三唑环上的N—H 具有明显的电正性,也可参与形成氢键。从结构分析,化合物1 联三唑阳离子的两个三唑环完全不在同一平面,存在较大的唑环错位,两个三唑环平面夹角达54°,三唑环与N5-离子也只能以非平面的3D 空间网络结合。而化合物11 和12 中单唑阳离子和并唑阳离子是平面构型,通过氨基或唑环N—H 与五唑环形成氢键时也能基本保持平面构型,化合物11 中三唑环与离子夹角小于5°,化合物12 中并三唑环则与N5-离子完全公平面。从氢键数量和类型分析,化合物1 和12 中离子均形成了4 个氢键,化合物11 中则形成了3 个氢键,所有氢键键长和强度存在明显差异,强弱无呈现明显规律性。推测其原因在于不仅有氨基的氢键,还有三唑环的N—H 的参与,形成了两类氢键。而且由于分子内存在不止一种氨基,形成氨基氢键的取代氨基化学环境和位置不同,这也导致了氨基氢键性质的不同。在氢键的影响下,离子中N—N 键均一性受到影响,以至于化合物11 和12 中五个N—N 键均不等长,使五唑环不再具有良好的对称性。尽管如此,化合物12 的分解温度仍达到了120 ℃,在表1 中所合成非金属盐中分解温度排第二。笔者推测由于化合物12 具有非常完美的平面结构,使得整体结构形成类石墨烯的大共轭体系,而大共轭体系可有效提高化合物的稳定性。
3.4 含碳氮氧氢的酰类阳离子的氢键作用
在上述CHN 类阳离子中引入氧,形成不同的含氧官能团,对氢键也存在明显的影响。羧基是一种吸电子官能团,引入后可明显增加邻位的电正性,例如酰胺中的N—H 受到羧基的影响,电正性会明显增强,易于形成强氢键。从图5 中化合物2 和3 来看,酰铵的N—H 与离子成氢键普遍为强氢键和中等氢键。化合物2中胍基的N—H 与离子成氢键大多数为弱氢键以及少量的中等氢键,化合物3 中肼基的远端N—H 与5离子成氢键也是中等氢键和弱氢键,与前面图1 和2 中胍和肼阳离子普遍的形成中/弱氢键规律一致。同样由于离子中各个氮原子所形成氢键种类和强度差异较大,五唑环不具有对称性。化合物2 中酰基胍与离子共平面,虽然缺乏大共轭体系,但是平面层状堆积的结构使得化合物2 保持有110.5 ℃的分解温度。而化合物3 则即缺乏良好的对称性,也没有共平面结构,因此其分解温度(95.2 ℃)在所合成非金属盐中最低。
化合物13 和14 中,氧分别形成了氨氧基、羧酸、硝基等含氧官能团。硝基结构自身为氢键受体,与离子不可能形成氢键。羧酸中由于—OH 的存在,形成了O—H…N 型氢键。该氢键为强氢键,键长仅1.86 Å。氨氧基中氨基本身为电正性,因此形成的氢键也是强氢键。化合物13 和14 中等氢键种类或强度不同,且缺乏平面结构,理论上稳定性会较差。很巧合的是,由于两个化合物分别与离子形成的两个氢键是对称的且强度都不低,使得五唑环从N—N 键长看都基本保持了良好的轴对称结构,因此其分解温度仍有98.5 和107.8 ℃。另外,值得注意的是,化合物13 和14 中均存在C—H 键,但是C—H 并不是很好的质子给予体,所以没有与离子形成C—H…N 氢键。
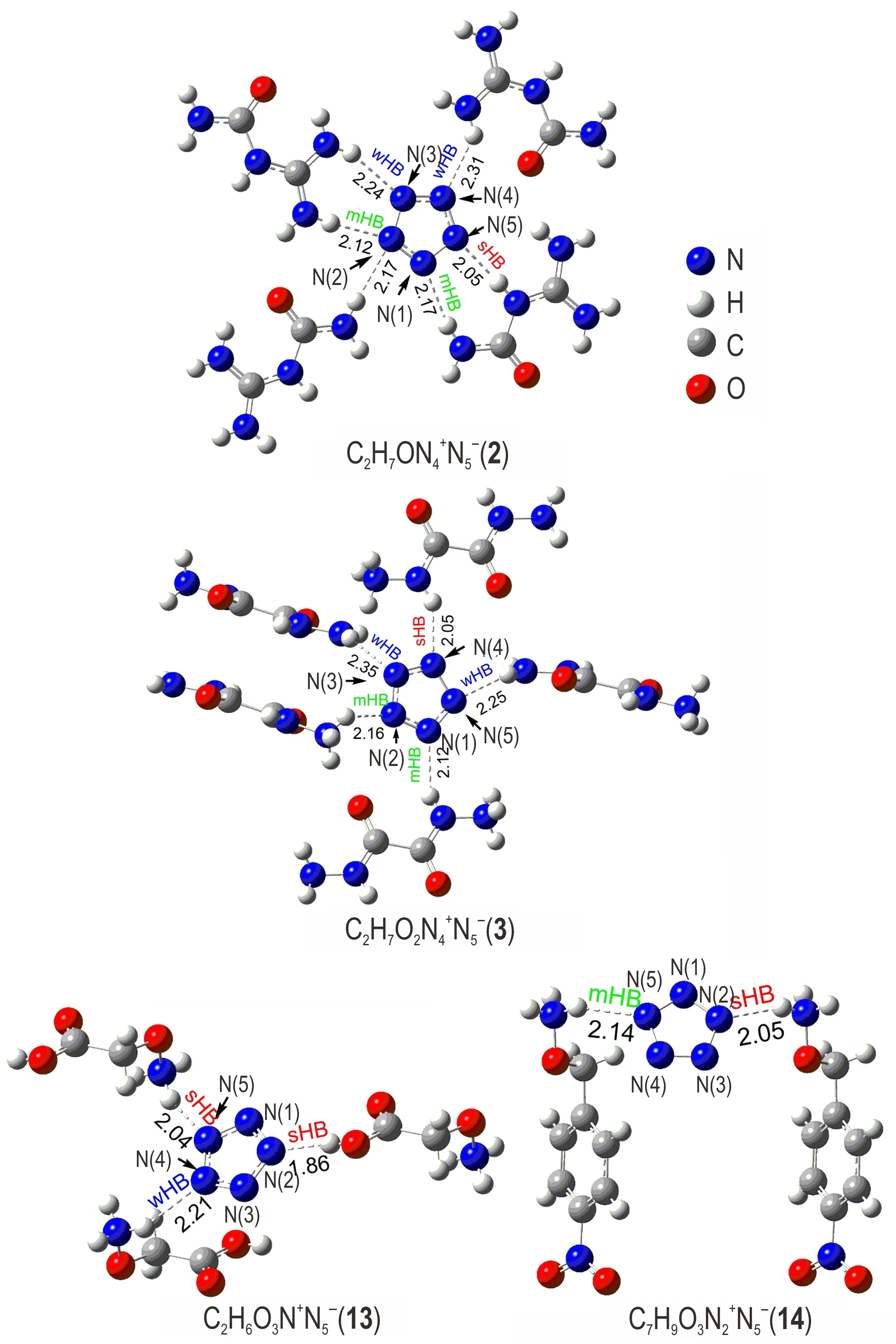
图5 化合物2,3,13 和14 的氢键作用(键长单位Å)Fig.5 Hydrogen bonding of compounds 2,3,13 and 14(unit of bond length is Å)
3.5 含水分子的氢键作用

图6 含水化合物4,6,15 的氢键作用(键长单位为Å)Fig.6 Hydrogen bonding of compounds 4,6 and 15(unit of bond length is Å)
合成过程特别是晶体生长为敞开环境,并且晶体生长时有时会采用含水溶剂,这两个原因导致了部分晶体中含有结晶水。如图6 所示,结晶水会与N5-离子形成氢键,且基本都是强氢键作用。化合物4 中四氨基联三唑阳离子,与化合物1、11、12 三唑类阳离子相比,形成氢键数量减少至仅一个,其余N5-离子中的N原子的氢键均被水分子占据。化合物6 中的羟胺阳离子既可以利用氨氧基电正性形成氢键,也可以利用—OH 羟基形成氢键,氢键强度均为中等氢键,剩下离子中的两个N 原子则与水分子形成强氢键。化合物15 中乙二胺阳离子显电正性一端的N—H 能与离子形成强氢键,另一端不显电正性的N—H 则无氢键,而且水也参与形成了氢键。这三个含水化合物表明,水极易与离子发生氢键作用,形成水合物,而这类水合物中的水较难除去,会对含能材料的爆轰性能会有较大的影响。而且这些氢键使得离子的对称性完全破坏(N—N 键长不均一),键长分布范围大(化 合 物4、6、15 分 别 为1.305~1.324、1.312~1.318、1.295~1.337 Å),同时也不具有平面结构,这也导致了离子的热稳定性较差。化合物4 热分解温度仅为95.2 ℃,还未开始失水离子即已开始分解,在目前已报道的非金属盐中热稳定性最低;而化合物6 和15 热分解温度分别为105.5 ℃和101.8 ℃,随着失水,离子也迅速分解,热稳定性低于已合成的十五种非金属化合物的平均值(105.6 ℃)。这种情况与常见的氢键作用提高化合物稳定性完全不同[20]。
十五种非金属盐的键长、平均键长以及热分解温度列于表1。一般认为,硝胺类含能化合物中最弱的化学键,通常为N—N 键,是影响其热稳定性的关键因素。但是从表1 可以看出,对于五唑离子型化合物,五唑环的最长键长(即最弱键)、平均键长与热分解温度无明显关联性,这表现出了与硝胺类含能材料不同的规律性。由前面分析可知,其原因有二,第一,五唑的N—N 键与硝胺的N—N 键相比,还受到氢键的影响;第二,五唑作为共轭环状结构,其对称性、平面性也对共轭特性有影响。因此对于全氮化合物,其稳定性需要考虑更多因素。
4 结论
对五唑非金属盐的氢键作用规律进行了研究,通过氢键键长、强度、数量以及离子中N—N 键长的分析,结合热分解温度作为稳定性判断依据,得出如下结论:
表1 离子中N—N 键长及含能盐的分解温度Table 1 N—N bond length in pentazole anion and decomposition temperature of energetic salts
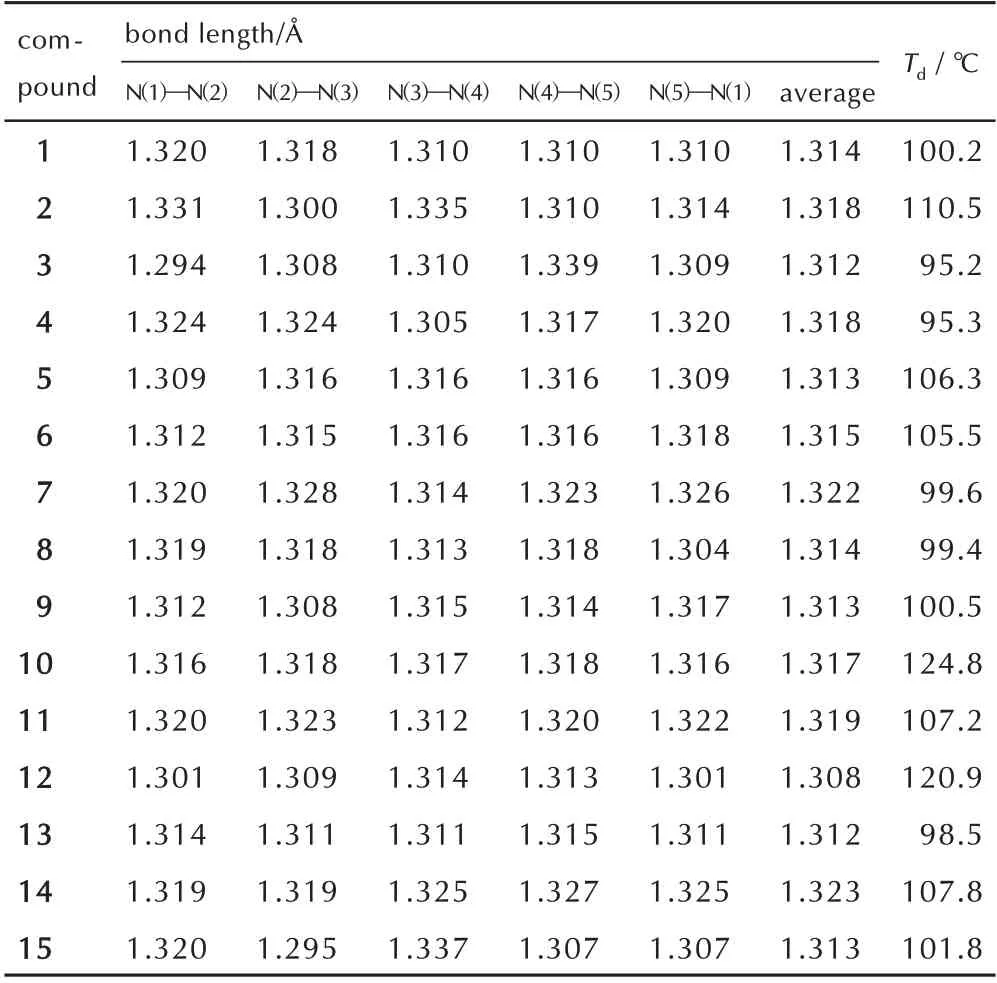
表1 离子中N—N 键长及含能盐的分解温度Table 1 N—N bond length in pentazole anion and decomposition temperature of energetic salts
compound bond length/Å N(1)—N(2)N(2)—N(3)N(3)—N(4)N(4)—N(5)N(5)—N(1)Td / ℃1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 1.320 1.331 1.294 1.324 1.309 1.312 1.320 1.319 1.312 1.316 1.320 1.301 1.314 1.319 1.320 1.318 1.300 1.308 1.324 1.316 1.315 1.328 1.318 1.308 1.318 1.323 1.309 1.311 1.319 1.295 1.310 1.335 1.310 1.305 1.316 1.316 1.314 1.313 1.315 1.317 1.312 1.314 1.311 1.325 1.337 1.310 1.310 1.339 1.317 1.316 1.316 1.323 1.318 1.314 1.318 1.320 1.313 1.315 1.327 1.307 1.310 1.314 1.309 1.320 1.309 1.318 1.326 1.304 1.317 1.316 1.322 1.301 1.311 1.325 1.307 average 1.314 1.318 1.312 1.318 1.313 1.315 1.322 1.314 1.313 1.317 1.319 1.308 1.312 1.323 1.313 100.2 110.5 95.2 95.3 106.3 105.5 99.6 99.4 100.5 124.8 107.2 120.9 98.5 107.8 101.8
(1)N5-离子作为阴离子,易于与具有电正性的片段,即优秀的质子给予体形成N—H…N 和O—H…N两大类氢键。
(2)氢键越多越强,并不意味着N5-离子越稳定。离子受氢键作用后能否保持较好的结构对称性,是影响稳定性的关键因素之一。氢键的强弱不直接决定离子的稳定性。
(4)从已合成的非金属化合物来看,水对N5-离子的稳定性起负面作用。
