外科大手术老年患者发生术后低蛋白血症影响因素的队列研究
2020-07-10李秋萍韩斌如陈曦
李秋萍,韩斌如,陈曦
(首都医科大学宣武医院 护理部,北京100053)
随着人口结构的改变及医学技术的加快发展,老年人手术比例不断增高。 有调查显示美国行手术治疗的患者中,65 岁以上的老年人超过40%[1],我国老年人占全部手术患者的45.6%~52.0%[2]。手术可能导致老年人自主神经、内分泌、代谢及免疫功能失衡[3],外科大手术指创伤大、出血多、涉及重要器官及需要复合麻醉的手术, 由于其难度大、 存在风险高,更容易导致患者术后并发症发生率增高、日常生活能力下降,甚至出现死亡[4-5]。 低蛋白血症是外科大手术后常见的并发症之一,会引起组织、器官水肿致使患者出现胸腔积液、切口愈合延迟等表现,与预后恢复密切相关[6]。 既往研究主要探讨了罹患肺癌、肝癌、胃癌等疾病患者术后低蛋白血症的发生状况[7-8],但对于老年人及外科大手术治疗人群的相关研究较为缺乏。本研究通过前瞻性队列研究,探讨行外科大手术治疗的老年患者术后低蛋白血症的发生现状,分析这类人群低蛋白血症的影响因素, 以期为进一步围术期护理管理提供一定的参考和依据。
1 对象与方法
1.1 研究对象 采用前瞻性队列研究设计, 选取2016 年10 月—2018 年10 月在某三级甲等综合性医院行外科大手术的老年患者作为研究对象。 纳入标准:(1)年龄≥60 岁;(2)行外科择期手术且手术级别为三、四级大手术[5];(3)能配合完成术前评估;(4)知情并同意参与本研究。排除标准:(1)存在严重精神疾病患者;(2)长期卧床、完全失能或不能配合完成资料收集的患者。
1.2 研究工具
1.2.1 研究对象调查表 在参阅相关文献[9-10]及专家咨询的基础上,自行设计研究对象调查表,包括3方面:(1)一般资料调查表:包括性别、年龄、 体质量指数(body mass index, BMI)、既往史、吸烟史、饮酒史、日常生活自理能力、衰弱状态、营养风险。 其中,①日常生活自理能力, 采用Mahoney 等研制的Barthel 指数进行评价[11],该评分包括修饰、如厕、进食、洗澡、穿衣、大便控制、小便控制、床椅转移、平地行走、上下楼梯10 个条目。总分100 分,分数越高自理能力越好,其Cronbach α 系数为0.88[12];②衰弱状态,采用Fried 衰弱表型定义进行评估,包括非自主体质量下降、自述疲乏、肌力弱、行走速度慢、活动量低5 项指标,满足3 项及以上称之为衰弱[13-14],该评估工具为A 级推荐[15];③营养风险,采用住院病人营养风险筛查工具 (Nutritional Risk Screening 2002,NRS 2002)进行评估,含BMI 值、近期体质量变化、膳食摄入情况、疾病严重程度4 方面,总分7 分,评分≥3 分认为存在营养风险,其敏感度、特异度分别为88%、92%,Kappa 系数为0.956[16]。 (2)术前资料:选择研究对象术前最邻近手术开始时的与营养相关的实验室检查指标,包括白蛋白、血红蛋白、前白蛋白。 (3)手术资料:包括美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级[17]、手术类型、手术时间、术中失血量、手术方式。
1.2.2 研究结局指标 本研究结局指标为患者在手术结束后至出院期间发生的术后低蛋白血症。 根据患者术后肝功能生化检查结果, 当白蛋白含量<25 g/L 即认为患者发生了术后低蛋白血症[18],由1 名副主任医师判定,结局观察直至患者出院。
1.3 资料收集方法 由1 名熟悉本研究目的及方法的研究者在患者入院24 h 内对符合纳入、排除标准的研究对象进行问卷调查及评估, 获取患者的一般资料;手术患者在术前常规进行血常规、血生化检验并在电子病历中记录,研究者于术前24 h 内通过电子病历记录患者最临近手术开始的术前资料;于术后24 h 内从电子病历中获取手术相关资料,填写记录表。 患者术后第1 天、第3 天常规复查血常规、血生化检验,有异常指标者会增加检验频次,研究对象术后首次或任意1 次检查结果符合低蛋白症诊断标准则认为结局发生, 研究结局由1 名副主任医师对患者是否发生了院内术后低蛋白血症进行判定,并在记录表上填写。
1.4 统计学方法 采用EpiData 3.1 双人录入数据,系统逻辑检错,采用SPSS 22.0 分析数据。 计量资料采用one sample Kolmogorov Smirnov test 进行正态性检验, 正态分布的计量资料采用均数±标准差描述,组间比较采用两独立样本t 检验;偏态分布的计量资料采用中位数、 四分位数描述, 组间比较采用Mann-Whitney U 检验。 计数资料采用频数、百分比描述, 组间比较采用卡方检验或Mann-Whitney U检验。将单因素分析中P<0.05 的变量进行共线性诊断, 不存在共线性的变量纳入二分类Logistics 回归分析, 分析老年外科大手术患者术后低蛋白血症的影响因素。 以P<0.05 为差异有统计学意义。
2 结果
2.1 外科大手术老年患者术后低蛋白血症发生风险的单因素分析 本研究共纳入363 例外科大手术老年患者,年龄(68.13±6.80)岁,其中男性181 例(49.9%),女性182(50.1%)例。 根据术后低蛋白血症诊断标准[18],术后发生低蛋白血症55 例,术后发生低蛋白血症率为15.2%。 以55 例术后发生低蛋白血症的外科大手术老年患者为低蛋白血症组, 未发生低蛋白血症的308 例患者为对照组, 比较2 组患者一般资料、术前资料及手术资料的差异。 结果显示,低蛋白血症组患者的年龄、性别、饮酒史与对照组相比,差异均无统计学意义(P>0.05);低蛋白血症组患者的吸烟史、日常生活自理能力、营养风险、衰弱状态、术前白蛋白、术前前白蛋白、术前血红蛋白、美国麻醉医师协分分级、手术类型、手术时间、术中失血量、手术方式与对照组比较,差异均有统计学意义(P<0.05)。 见表1。
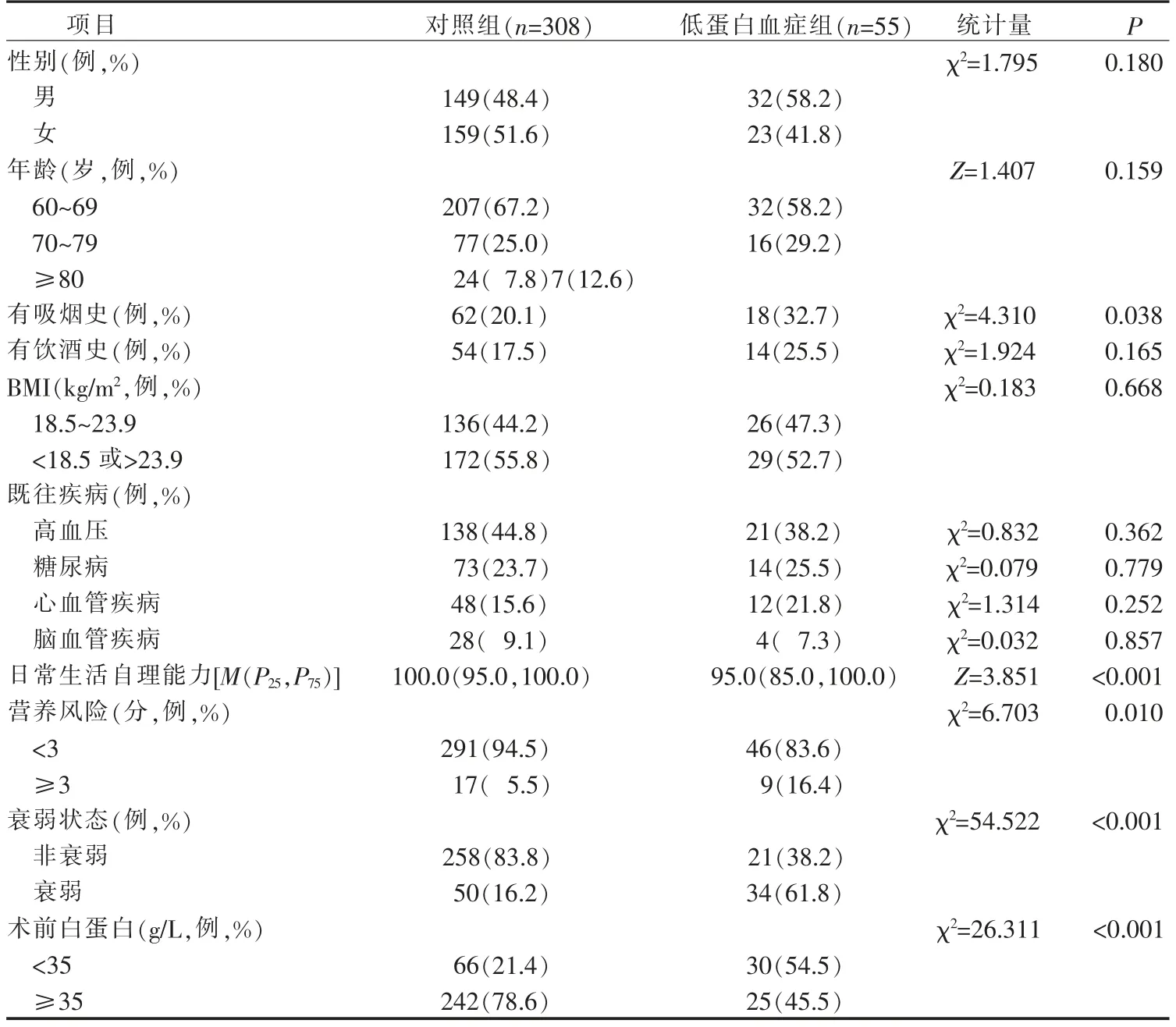
表1 外科大手术老年患者术后低蛋白血症发生风险的单因素分析(n=363)

续表1
2.2 外科大手术老年患者术后低蛋白血症发生的二分类Logistic 回归分析 将组间比较中P<0.05 的变量,即吸烟、日常生活自理能力、营养风险、衰弱状态、术前白蛋白、术前前白蛋白、术前血红蛋白、ASA分级、手术类型、手术时间、术中失血量、手术方式变量进行共线性诊断, 结果显示各变量方差膨胀因子在1.098~2.057,容忍度在0.486~0.911,反映各变量间不存在多重共线性,可纳入Logistic 回归。
以是否发生术后低蛋白血症为因变量(0=未发生,1=发生), 单因素分析有统计学意义的12 个变量为自变量, 采用逐步向前法进行Logistic 回归分析,α入=0.05,α出=0.10。 结果显示,衰弱、术前白蛋白水平、ASA 分级、手术时间是外科大手术老年患者术后低蛋白血症发生的独立危险因素(P<0.05)。 见表2。

表2 外科大手术老年患者术后低蛋白血症影响因素的二分类Logistic 回归分析(n=363)
3 讨论
3.1 本组外科大手术老年患者术后低蛋白血症发生率为15.2% 本研究结果显示,本组行外科大手术的老年患者,术后低蛋白血症发生率为15.2%,略低于李权林在88 例肝癌肝切除术患者研究中的19.32%[7],可能与其将术后低蛋白血症的诊断设定为<30 g/L有关, 而本研究术后低蛋白血症的诊断标准为<25 g/L[18],故其统计出的术后发生白蛋白血症的发生率高于本研究。 既往研究显示腹部手术术后低蛋白血症的发生率为12.5%~69%[19],与本研究结果一致。 究其原因,老年人为特殊群体,其由于免疫力下降,生理储备能力和代谢功能逐步下降,常存在高血压、糖尿病等多病共存的状态, 从而导致老年患者术后不良事件发生率较高[20]。 老年患者常存在胃肠功能减退,合成白蛋白的原料摄入不充足,且多病共存也会增加机体的代谢,增加白蛋白的消耗[9]。 在大手术等应激条件刺激下, 机体易发生炎症反应导致白蛋白渗漏至血管外组织间隙[21],同时术中失血也会造成白蛋白的进一步降低。Norberg 研究也证实在行大手术后血清白蛋白水平会急剧下降33%[22]。
3.2 外科大手术老年患者术后低蛋白血症发生的影响因素
3.2.1 衰弱 本研究结果显示, 衰弱是外科大手术老年患者术后低蛋白血症的危险因素 (OR=6.831,P<0.001)。 沈妍交的研究也显示行髋部骨折治疗的衰弱患者比非衰弱患者低蛋白血症发生风险更高(OR=2.219,95%CI=1.126~4.371)[23]。 衰弱是老年人机体生理储备能力下降、 内环境紊乱导致机体易损性增加的特异性状态[24],衰弱患者在围术期易发生各种负性事件, 是手术不良并发症的首位独立危险因素[25]。 衰弱老年人在经历手术应激刺激后,机体耗损较为严重,机体能量消耗较高,其对于白蛋白的利用率增加;其白细胞介素-6、C 反应蛋白等炎症因子指标常处于较高水平, 这些成分会造成血管内皮屏障完整性丧失,致使血浆白蛋白从体毛细血管渗出[21]。同时衰弱老年人本身易处于营养不良状态, 基础白蛋白水平可能并不高[26],因此在术后更容易出现术后低蛋白症。
3.2.2 术前白蛋白 本研究结果显示, 术前白蛋白是外科大手术老年患者术后低蛋白血症的保护因素(OR=0.457,P=0.042), 即术前白蛋白≥35 g/L 的外科大手术老年患者, 其发生术后低蛋白血症的概率是术前白蛋白<35 g/L 的患者的0.457 倍。 既往研究也表明术后血清白蛋白水平下降幅度与术前白蛋白水平呈明显正相关, 术前低蛋白患者术后低蛋白血症的发生是正常患者的6.163 倍[8],与本研究结果一致。 术前白蛋白浓度反映了患者术前全身营养状况和代谢能力, 被认为是营养不良炎症反应综合征的标志,一方面本身机体白蛋白即处于较低水平,含量不足;另一方面机体长期处于营养不良高危风险中,对能量的消耗易增加, 此时白蛋白的分解会增加以保障代偿性的机体能量平衡[27-28]。 因此,术前白蛋白可作为术前营养和代谢指标预测术后发生低蛋白血症的风险。
3.2.3 ASA 分级 本研究结果显示,ASA 分级是外科大手术老年患者术后低蛋白血症的危险因素(OR=5.414,P=0.001)。 ASA 分级是针对患者疾病严重程度和手术风险进行的术前评估指标, 分级越高意味着并存病情越严重,风险越高[17]。 因此,ASA≥3级的外科大手术老年患者,较<3 级患者的围术期耐受力低,更容易出现术后并发症。本研究纳入的均为行外科大手术的患者,在麻醉与大手术影响下,细胞因子大量释放,致使机体微循环功能障碍、血管内皮细胞损伤、内皮细胞连接破坏,全身毛细血管通透性增加,大量白蛋白从血管腔内漏出组织间隙,导致白蛋白在血管内外的再分布[21],因此术后更容易发生低蛋白血症。 ASA 分级的增加一定程度上反映了手术的创伤和难度的加大, 本研究纳入的均是行胸腹部手术的患者,在手术应激状态下,该类患者肝脏合成白蛋白的功能较易出现下降。基于上述机制,ASA分级能一定程度上影响老年患者术后低蛋白血症的发生。
3.2.4 手术时间 本研究结果显示, 手术时间是外科大手术老年患者术后低蛋白血症的危险因素(OR=1.726,P<0.001),即手术时间较长的患者,其术后低蛋白血症发生风险是手术时间短患者的1.726倍。 手术时间延长, 一方面会导致术后麻醉药物累积,影响患者的呼吸循环系统,同时可能加重术后机体免疫功能的下降,促使术后机体应激反应增强[29],有研究显示手术时间≥2 h 比手术时间<2 h 的应激反应显著[30-31]。 另一方面机体应激激素水平升高,导致体内血糖、炎性介质、细胞因子、免疫功能等发生变化,易引发一系列创伤应激反应,致使白蛋白水平急剧下降。 袁锡裕等[27]调查了159 例行胃肠手术患者术后的白蛋白浓度水平,结果显示术后6~12 h 患者白蛋白水平呈显著下降, 手术时间的延长易形成创伤应激的网络反应加重术后低蛋白的加速下降。
4 对策
术后低蛋白血症会延迟患者组织愈合时间,甚至发生吻合口瘘、脓毒症[32],因此对患者进行围术期低蛋白血症管理具有重要临床价值。 本研究结果中的ASA 分级及手术时间较难从护理角度进行控制及改善,但老年患者的衰弱状态、术前白蛋白水平可在术前进行积极干预。
建议护理人员在患者入院时开展老年综合评估,筛查衰弱患者,对照《亚太平洋地区衰弱管理临床实践指南》[33]、《老年患者衰弱评估与干预中国专家共识》[34]等循证干预措施及流程,开展以护士主导的多学科团队对其进行营养、运动的综合干预,在术前尽早开展衰弱管理以延缓甚至逆转患者衰弱进程[35]。 护理管理者可进一步完善外科大手术老年患者术前护理评估体系及制度,关注其营养状态,强化营养风险筛查的重要性, 将患者营养状况评估作为常态化评估项目。 有研究表明围手术期尽早行肠内营养可使血清白蛋白浓度明显升高, 同时提高肠道耐受力,增强免疫功能[36]。 护士可根据患者术前营养状态将其分级,选择合适的营养补给途径,从营养补充类型及内容方面对不同分级患者给予相匹配的治疗护理措施,改善其术前低蛋白情况。
5 本研究的不足
本研究的不足在于研究设计为单中心、 小样本的研究,在证据级别上仍有待提升;其次研究仅为术后低蛋白血症影响因素的探索, 尚未开展干预性研究,今后将进一步开展多中心、大样本、高质量的研究,并且从因素探索研究迁移至干预性研究,为临床实践提供可借鉴的术后低蛋白血症管理路径, 促使患者受益。
