基于超高效液相色谱-蒸发光散射检测技术优选炒酸枣仁-醋五味子药对最佳配伍比例
2020-07-09吴溪孟楣高家荣
吴溪,孟楣,高家荣
基于超高效液相色谱-蒸发光散射检测技术优选炒酸枣仁-醋五味子药对最佳配伍比例
吴溪,孟楣,高家荣
安徽中医药大学第一附属医院,国家中医药管理局中药制剂三级实验室,安徽 合肥 230031
通过超高效液相色谱-蒸发光散射检测技术测定不同配伍比例炒酸枣仁-醋五味子药对中酸枣仁皂苷A含量,优选最佳配伍比例,为临床用药提供参考。设置不同剂量配比的炒酸枣仁-醋五味子药对(1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1),采用Acquity UPLC BEHC18色谱柱(2.1 mm×50 mm,1.7 μm),蒸发光散射检测器,乙腈-水为流动相梯度洗脱,流速0.3 mL/min,柱温30 ℃,进样量1 μL,酸枣仁皂苷A色谱峰与相邻色谱峰的分离度不低于1.5,测定药对中酸枣仁皂苷A含量。酸枣仁皂苷A在0.010 05~0.100 5 μg范围内呈良好线性关系,回归方程为=1 276 209.888 91-162 396.863 01(=0.999 93),重复性、稳定性和回收率良好。上述9个不同配伍比例炒酸枣仁-醋五味子药对的酸枣仁皂苷A浓度依次为0.015 9、0.015 3、0.016 9、0.011 4、0.013 7、0.013 2、0.018 4、0.014 6、0.010 3 mg/mL。本研究揭示炒酸枣仁-醋五味子配伍比例为7∶3时酸枣仁皂苷A含量最高,可为临床养心安神治法遣方用药提供依据。
超高效液相色谱-蒸发光散射检测法;炒酸枣仁-醋五味子药对;配伍比例;酸枣仁皂苷A
酸枣仁、五味子两药在中医经典安神方剂中多配伍使用,是临床常用药对之一,该药对具有滋阴养血、安神镇惊、消除疲劳、增加耐力等功效,用于治疗神经衰弱、失眠症、消渴、慢性荨麻疹等。本课题前期采用计算机编程及关键词映射法,对以《中医方剂大辞典》为基础的中医方剂数据库进行检索并手工检索2015年版《中华人民共国药典》,发现含有酸枣仁-五味子药对的方剂262首,二者的配伍比例有44种,以1∶1、2∶1、3∶1、1∶2、2∶3居多[1]。通过查阅其他文献得到药对的配伍比例一般按1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1进行研究[2],与统计比例比较接近,因此确定上述9个比例对酸枣仁-五味子药对进行研究。酸枣仁-五味子药对配伍多以酸枣仁为主,故以酸枣仁为主要研究目标。酸枣仁皂苷是酸枣仁中含量高的化学成分,其中达玛烷型三萜皂苷类化合物如酸枣仁皂苷A是酸枣仁中最重要的皂苷。现代药理研究表明,酸枣仁皂苷类是其镇静安神的主要药效成分,与化学类镇静催眠药相比,酸枣仁活性成分有多靶点、多效应器官等特点[3-5]。本研究采用超高效液相色谱-蒸发光散射检测(UPLC-ELSD)技术测定酸枣仁皂苷A含量,从而优选酸枣仁-五味子药对的最佳配伍比例,为临床中医方剂配伍提供参考。
1 仪器与试药
Waters Acquity H-Class UPLC超高效液相色谱仪,Acquity ELSD检测器及Waters Empower2软件(美国Waters公司),Acquity UPLC BEHC18色谱柱(2.1 mm×50 mm,1.7 µm),BP211D电子天平(德国赛多利斯公司)。
酸枣仁皂苷A对照品(批号110734-200509,含量99.9%),中国食品药品检定研究院;乙腈为色谱纯(国药集团化学试剂有限公司),水为屈臣氏纯净水,其他试剂均为分析纯。酸枣仁药材产地为河北赞皇县,五味子药材产地为辽宁丹东市,经安徽中医药大学第一附属医院孟楣主任中药师鉴定,分别为鼠李科植物酸枣Mill. var. spinosa(Bunge)Hu ex H. F. Chou的干燥成熟种子和木兰科植物五味子(Turcz.)Baill.的干燥成熟果实,依据《安徽省中药饮片炮制规范》炒黄方法和醋制方法[6]对酸枣仁和五味子药材分别进行炮制,得到炒酸枣仁和醋五味子。
2 方法与结果
2.1 色谱条件
采用Acquity UPLC BEHC18色谱柱(2.1 mm×50 mm,1.7 μm),ELSD检测器,流速0.3 mL/min,柱温30 ℃,进样量1 μL,流动相A为乙腈、B为水,梯度洗脱程序见表1[7-9]。
表1 流动相梯度洗脱程序(%)
时间流动相A流动相B 0 min 20.080.0 1.5 min 40.060.0 2.5 min 40.060.0 3.5 min 70.030.0 4.0 min100.00 5.0 min 20.080.0 7.0 min 20.080.0
2.2 对照品溶液制备
精密称取酸枣仁皂苷A对照品适量,加甲醇250 mL制成0.020 1 mg/mL的对照品溶液,经0.22 μm微孔滤膜过滤,置5 ℃冰箱备用。
2.3 供试品溶液制备
分别取炒酸枣仁、醋五味子(过2号筛,24目),按1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1比例称量,得到1~9号样品(见表2),分别置于50 mL圆底烧瓶中,将粉末混匀,精密加入60 mL甲醇,加热回流1 h,放冷,过滤,滤液蒸干,分别加入10 mL蒸馏水溶解,倒入离心管中,3000 r/min离心5 min,取上清液,加石油醚(60~80 ℃)萃取3次,每次15 mL,弃去石油醚层,水层加入5%KOH溶液30 mL,用水饱和正丁醇萃取4次,每次20 mL,合并正丁醇层,用正丁醇饱和氨水洗涤2次,每次10 mL,弃去洗液,挥干正丁醇,残渣加甲醇定容至5 mL容量瓶中,即得。
表2 不同配伍比例炒酸枣仁-醋五味子药对样品(g)
编号炒酸枣仁醋五味子 11.0049.008 22.0038.002 33.0037.001 44.0036.001 55.0025.004 66.0024.005 77.0013.000 88.0032.002 99.0021.000
2.4 阴性对照溶液制备
取醋五味子,按供试品溶液制备方法制备,即得。
2.5 方法学考察
2.5.1 系统适用性试验
取对照品溶液、供试品溶液(1号)和阴性对照溶液,按“2.1”项下色谱条件进样,色谱图见图1。在该色谱条件下,酸枣仁皂苷A保留时间为4.1 min,酸枣仁皂苷A色谱峰与相邻色谱峰的分离度>1.5,表明样品中的酸枣仁皂苷A分离度良好,阴性对照及其他成分无干扰。
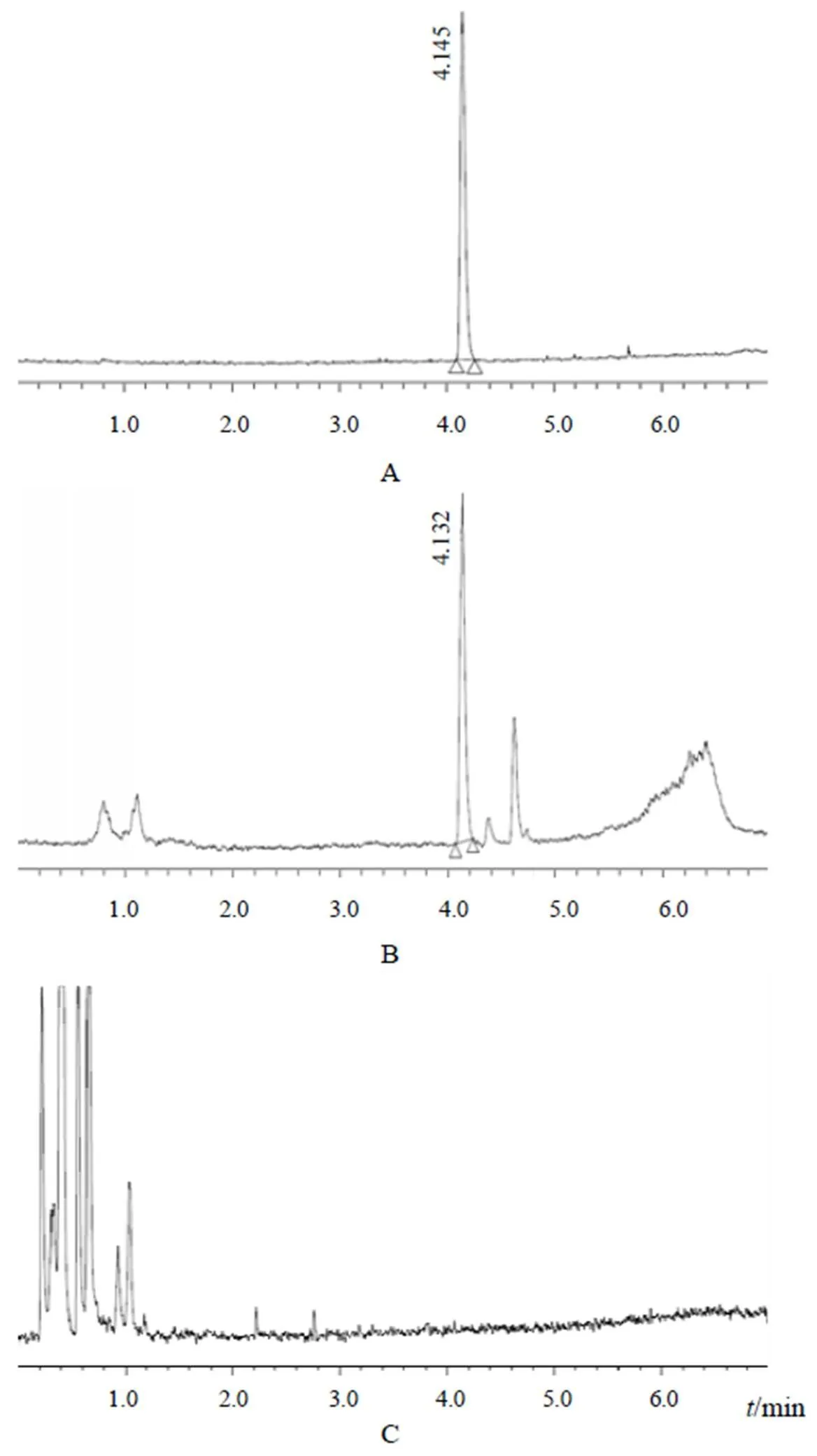
注:A.对照品;B.供试品;C.阴性对照
2.5.2 线性关系的考察
精密吸取对照品溶液,制成酸枣仁皂苷A浓度分别为2.01、4.02、8.04、12.06、16.08、20.1 μg/mL的系列溶液,各进样5 μL。以酸枣仁皂苷A浓度为横坐标,峰面积为纵坐标,绘制标准曲线,得回归方程=1 276 209.888 91-162 396.863 01,=0.999 93。结果表明,酸枣仁皂苷A在0.010 05~0.100 5 μg范围内线性关系良好。
2.5.3 精密度试验
精密吸取对照品溶液,连续进样6次,测定峰面积,结果RSD=0.12%,表明精密度良好。
2.5.4 稳定性试验
取2号供试品溶液,分别于0、2、4、8、12 h按“2.1”项下色谱条件测定酸枣仁皂苷A的峰面积,结果RSD=0.14%,表明溶液在12 h内稳定性良好。
2.5.5 重复性试验
取2号样品6份,按“2.3”项下方法制备,按“2.1”项下色谱条件测定,计算酸枣仁皂苷A含量,结果RSD=0.92%,表明重复性良好。
2.5.6 加样回收率试验
按照2号样品比例分别减半称取样品6份,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样,计算加样回收率,结果平均回收率为96.81%,RSD=1.62%,见表3。
表3 酸枣仁皂苷A加样回收率试验
取样量 /g样品中含量 /mg加入量 /mg测得量 /mg回收率 /%平均回收率 /%RSD /% 1.0010.076 40.060 300.134 1595.8 1.0230.074 70.060 300.132 2995.5 1.0170.075 20.060 300.133 9497.4 1.0200.075 00.075 380.149 4898.8 1.0050.076 10.075 380.150 2398.396.811.62 1.0350.073 90.075 380.145 3794.8 1.0130.075 50.090 450.165 0398.9 1.0050.076 10.090 450.162 3695.4 1.0510.072 80.090 450.160 0396.4
2.6 样品含量测定
分别吸取9个配伍比例的供试品溶液,按“2.1”项下色谱条件进样测定,计算酸枣仁皂苷A含量,结果见表4,酸枣仁皂苷A浓度变化见图2。可见,随着炒酸枣仁配伍剂量增大、醋五味子配伍剂量减小,酸枣仁皂苷A的浓度变化呈波型;当炒酸枣仁与醋五味子配伍比例为7∶3时,酸枣仁皂苷A含量最高。
表4 不同配伍比例炒酸枣仁-醋五味子药对酸枣仁皂苷A浓度
样品编号炒酸枣仁∶醋五味子酸枣仁皂苷A/(mg/mL) 11∶90.015 9 22∶80.015 3 33∶70.016 9 44∶60.011 4 55∶50.013 7 66∶40.013 2 77∶30.018 4 88∶20.014 6 99∶10.010 3

图2 不同配伍比例炒酸枣仁-醋五味子药对中酸枣仁皂苷A浓度变化曲线
3 讨论
本研究预试验中比较了加热回流提取法和超声提取法,结果发现加热回流1 h可使酸枣仁皂苷A充分溶出,因此选择加热回流提取法进行供试品的提取。深入比较样品溶液的预处理方法,对于回流提取后样品直接蒸干定容和样品蒸干后增加一系列处理步骤2种方法进行比较,后者效果较好,通过石油醚萃取除去脂溶性成分,以及其他溶剂的洗涤,可避免杂质的干扰。
酸枣仁皂苷A为三萜皂苷类成分,紫外吸收效果差,不宜采用二极管阵列检测器,而蒸发光散射检测器为质量型通用检测器,可检测挥发性低于流动相的化合物。本试验将超高效液相色谱用于酸枣仁皂苷A的研究,经UPLC-ELSD测定,与普通HPLC采用C18填料的色谱柱(4.6 mm×250 mm,5 μm)比较,分析速度提高了4倍以上,具有较高的分析通量,同时也具有良好的准确度、精密度和耐用性,方法可靠,重复性好。
酸枣仁与五味子从古至今有多种炮制方法,及至现代,酸枣仁的主要炮制方法为清炒,五味子主要为醋制。研究表明,酸枣仁通过炒制能够达到“生效熟增”的目的,主要与药效相关的主要化学成分含量变化有关[10]。中药制剂发挥药理、药效作用与其化学成分含量和配伍比例密切相关,中药量效关系是确定临床用药剂量的依据,也是确保用药有效性和安全性的基础。前期文献研究表明酸枣仁与五味子药对配伍以酸枣仁为主,但最佳配伍比例并不确定。本试验通过考察酸枣仁主要有效成分酸枣仁皂苷A含量变化,结果显示炒酸枣仁与醋五味子的最佳配伍比例为7∶3,在化学成分上为炒酸枣仁与醋五味子的合理配伍提供了依据,可指导临床遣方用药。
[1] 吴溪,高家荣,吴德林.酸枣仁-五味子药对不同配比的中医应用数据分析[J].中国实验方剂学杂志,2011,17(22):273-276.
[2] 朱日然,韩相宁,张亚楠,等.菊花-决明子不同比例配伍药效成分含量变化研究[J].辽宁中医药大学学报,2018,20(6):49-52.
[3] 杜晨晖,崔小芳,裴香萍,等.酸枣仁皂苷类成分及其对神经系统作用研究进展[J].中草药,2019,50(5):1258-1268.
[4] 谭云龙,孙晖,孙文军,等.酸枣仁化学成分及其药理作用研究进展[J].时珍国医国药,2014,25(1):186-188.
[5] 马进杰,刘萍,马百平.酸枣仁化学成分及其镇静催眠作用研究进展[J].国际药学研究杂志,2011,38(3):206-211.
[6] 安徽省食品药品监督管理局.安徽省中药饮片炮制规范[M].合肥:安徽科学技术出版社,2005:394-395.
[7] 国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2015:366.
[8] 李莉,叶晓川,宋小英,等.UPLC-DAD-ELSD切换波长法同时测定复方酸枣仁颗粒中8种成分的含量[J].药物分析杂志,2016,36(10):1722- 1728.
[9] 祝洪艳,张力娜,王国丽,等.高效液相色谱法同时测定人参健脾丸中人参皂苷Rg1、Re、Rb1和酸枣仁皂苷A、B的含量[J].中国药学杂志, 2016,51(9):751-756.
[10] 朱晓钗,刘晓,汪晓莉,等.基于“生效熟增”论探讨酸枣仁炮制方法历史沿革及其镇静催眠作用物质基础[J].中药材,2017,40(8):1991- 1995.
Optimization Compatibility Ratio of Fried Ziziphi Spinosae Semen-Vinegated Schisandra Chinensis Fructus Based on UPLC-ELSD Technique
WU Xi, MENG Mei, GAO Jiarong
To determine the contents of Jujubaside A with different compatibility ratios of fried Ziziphi Spinosae Semen - vinegated Schisandra Chinensis Fructus based on UPLC-ELSD technique; To select the best compatibility ratio; To provide references for clinical medication.Different compatibility ratios of fried Ziziphi Spinosae Semen and vinegated Schisandra Chinensis Fructus were set as 1:9, 2:8, 3:7, 4:6, 5:5, 6:4, 7:3, 8:2, and 9:1. Acquity UPLC BEHC18 (2.1 mm × 50 mm, 1.7 μm) was used as the chromatographic column to detect the contents of Jujubaside A; acetonitrile-water (gradient elution) was used as the mobile phase with 0.3 mL/min flow rate; the detector was ELSD; the column temperature was 30 ℃; the volume was 1 μL. The separation of Jujubaside A chromatographic peak from adjacent chromatographic peaks was not less than 1.5. The contents of Jujubaside A with different compatibility ratios of fried Ziziphi Spinosae Semen - vinegated Schisandra Chinensis Fructus were detected.The regression equation of Jujubaside A was=1 276 209.888 91- 162 396.863 01 (=0.999 93) in the range of 0.010 05–0.100 5 μg, showing a good linear relationship. The repeatability, stability and recovery rate were fine as well. The concentrations of Jujubaside A were 0.015 9, 0.015 3, 0.016 9, 0.011 4, 0.013 7, 0.013 2, 0.018 4, 0.014 6, 0.010 3 mg/mL in the above nine different compatibility ratios of fried Ziziphi Spinosae Semen - vinegated Schisandra Chinensis Fructus.When the compatibility ratio of fried Ziziphi Spinosae Semen - vinegated Schisandra Chinensis Fructus is 7:3, the content of Jujubaside A is the highest, which can provide references for prescribing and medication of clinical method of tranquilizing by nourishing the heart.
UPLC-ELSD; fried Ziziphi Spinosae Semen - vinegated Schisandra Chinensis Fructus; compatibility ratios; Jujubaside A

R284.1
A
1005-5304(2020)06-0065-04
10.3969/j.issn.1005-5304.201904234
安徽高校省级自然科学研究项目(KJ2012Z220);安徽中医学院青年科学研究基金(2013qn009)
高家荣,E-mail:zyfygjr2006@126.com
(2019-04-16)
(2019-05-08;编辑:陈静)
