淀粉基餐勺表征及总迁移检测分析
2020-07-07黄鑫茜余稳稳姚皓程胡长鹰
黄鑫茜,余稳稳,姚皓程,胡长鹰*
1(暨南大学 食品科学与工程系,广东 广州, 510632) 2(广州海关技术中心国家食品接触材料检测重点实验室,广东 广州, 510075)
一直以来,聚对苯二甲酸乙二醇酯(polyethylene terephthalate,PET)、聚乙烯(polyethylene,PE)和聚丙烯(polypropylene,PP)等石油基塑料由于成本低、加工和使用性能良好而被广泛使用。然而,石油基塑料的过度使用和遗弃带来了严重的生态问题[1-3]。因此,可降解的生物基材料的开发和使用成为了人们关注的焦点[4-5]。
淀粉基材料具有来源广泛、无毒、价格低廉以及可生物降解等优点,是一种发展前景良好的生物基材料。目前,我国市场上已有包装薄膜、农用薄膜、一次性餐具和垃圾袋等淀粉基材料[6]。但由于淀粉的疏水性能和机械加工性能较差,食品接触用淀粉基材料(如一次性餐具)通常会以淀粉作为填充材料,与其他高分子材料共混来提高淀粉基材料的使用性能。在实际生产过程中,为提高淀粉与其他聚合物之间的相容性一般会加入一定的增塑剂、增容剂和偶联剂等添加剂[7]。食品接触材料在与食品接触过程中,有意和非有意添加物的迁移会给食品安全性带来一定的风险[8-9],但是目前我国关于淀粉基餐具的安全性研究较少。
总迁移量(overall migration quantity)是食品接触材料到食品或食品模拟物中可迁移的所有不挥发物质的总量,是食品接触材料及制品的质量控制指标之一。因其具有操作简单等特点,通常作为一个整体筛查的指标来初步评估食品接触材料物质的迁移风险。通过考察总迁移量以及蒸发残渣分析,可以帮助判断淀粉基材料在不同食品模拟物中的迁移情况。因此,本文通过对一次性淀粉基餐勺进行总迁移量分析,测定一次性淀粉基餐勺在不同食品模拟物中的迁移总量,并推测其影响机理,这对市售的淀粉基餐具安全评价和控制有一定的参考意义。
1 材料与方法
1.1 材料与试剂
餐勺A和B(利用总淀粉试剂盒测得餐勺A和B的淀粉总含量分别为(40.18±1.03) g/100g、(32.91±5.28) g/100g,江苏某公司;乙酸、无水乙醇、95%(体积分数)乙醇和异辛烷(分析纯),广州化学试剂厂;去离子水,由HHitech和泰纯水机制得;普鲁兰标准品,德国PSS公司。
1.2 仪器与设备
SQP型电子天平,赛多利斯科学仪器有限公司;BON-250型精密鼓风干燥箱,上海三腾仪器有限公司;FW-80型高速万能粉碎机,天津泰勒特科技有限公司;EVO MA15型扫描电子显微镜,德国蔡司公司;iS50型傅里叶变换红外光谱,美国赛默飞公司;TGA-DSC 3+型热综合分析仪,瑞士梅特勒公司;Waters体积排阻色谱,美国怀雅特科技公司。
1.3 实验方法
1.3.1 总迁移实验
参考国家标准GB 31604.1—2015[10]中的规定并结合餐勺预期使用情况,总迁移实验条件为70 ℃,2 h;选取4%(体积分数)乙酸为酸性食品模拟物、10%(体积分数)乙醇为水性食品模拟物、95%(体积分数)乙醇和异辛烷为替代油性食品模拟物。对于油脂类食品未选择植物油作为油性食品模拟物而选择溶剂替代,主要是因为95%乙醇和异辛烷为替代油性食品模拟物更能严苛、真实地反映相应食品模拟物迁移状况。参考SN/T 2824—2011[11],其中油类食品模拟物在70 ℃, 2 h条件相当于95%乙醇(60 ℃,2 h)和异辛烷条件(40 ℃, 0.5 h)。根据GB 5009.156—2016和GB 31604.8—2016[12-13]进行总迁移实验。按照体积比,配制食品模拟液4%乙酸溶液、10%乙醇溶液。由于无法获得实际的S/V或常规S/V(6 dm2接触面积对用1 L或1 kg食品模拟物),因此调整S/V,即采用全浸泡法把2个餐勺浸没在模拟液200 mL进行迁移实验。在预定条件下获得的迁移液200 mL置于已干燥恒重的90 mm玻璃蒸发皿中,在蒸发水浴锅上蒸干,擦去蒸发皿底部水滴,再放入105 ℃干燥箱中2 h,在干燥器中冷却0.5 h后称重。5个平行,并做空白对比。总迁移量的计算如公式(1)所示:
(1)
式中:X,总迁移量,mg/dm2;m1,餐勺测定用浸泡液残渣质量,mg;m2,空白浸泡的残渣质量,mg;V,浸泡液总体积,mL;V1,测定用浸泡液体积,mL;S,餐勺与浸泡液接触的面积是1.5 dm2。
1.3.2 扫描电子显微镜(scanning electron microscopy,SEM)
采用扫描电子显微镜对淀粉基餐勺碎片和从总迁移实验中得到的蒸发残渣进行扫描电镜分析,加速电压为5 kV。样品用导电双面胶粘贴安装在青铜载物台,然后喷涂上一层金(40~50 nm),使样品可视化。
1.3.3 傅里叶变换衰减全反射红外光谱分析(attenuated total reflection Flourier transformed infrared spectroscopy,ATR-FTIR)
采用表面全反射的方法,把淀粉基餐勺碎片和蒸发残渣分别放在FTIR附件晶体表面,调整压力板使样品和晶体表面紧贴,进行数据采集,扫描次数为32,扫描范围450~4 000 cm-1,分辨率为4 cm-1。
1.3.4 热性能分析(thermogravimetric analysis with differential scanning calorimeter,TGA-DSC)
淀粉基餐勺于高速万能粉碎机粉碎得到粉末后,精准称取10 mg于坩埚中,在氮气氛围下以20 ℃/min的升温速率从室温升至600 ℃,得到 TGA-DSC曲线。
1.3.5 体积排阻色谱分析(size-exclusion chromatography,SEC)
参考淀粉分子结构的分析方法[14-15],准确称取10 mg淀粉基餐勺粉末,加入2 mL二甲基亚砜/溴化锂(5 g/L)溶液。混合物放置于thermo mixer(80 ℃,300 r/s)条件下恒温过夜后离心(4 000×g,10 min),得到上清液。加6 mL无水乙醇到上清液,静置10 min后继续离心(4 000×g,10 min),得到含淀粉的下层沉淀在80 ℃、2 h、300 r/s条件下重溶解于约1 mL二甲基亚砜/溴化锂(5 g/L)溶液以进行下一步分析。
SEC根据淀粉的流体力学半径(hydrodynamic radius, Rh)对淀粉进行分离后,经示差检测器检测其浓度,并得到其含量分布。在实验过程中,先根据已知分子质量的普鲁兰标准品建立相应的标准曲线后,将待测物质的洗脱体积换算为其立体力学体积Rh,即是淀粉分子大小。
1.4 数据处理
利用Excel 2013作图,采用SPSS 25统计软件对实验数据进行显著性分析(P<0.05)。所有数据均以平均值±标准差表示。
2 结果与分析
2.1 淀粉基餐勺表征
2.1.1 形貌分析
实验过程中,采用SEM对淀粉基餐勺进行形貌观察,结果如图1所示。由图1-a~图1-d可知,餐勺的表面和断口面呈现出清晰可见的表面光滑且平整淀粉颗粒,说明淀粉与餐勺中其他组分之间没有形成致密的结构,两者界面相容性较差,因此推测研究的淀粉基餐勺是未经过糊化的淀粉作为填充材料与其他材料共同加工而成的一种共混型淀粉基材料[16-17]。
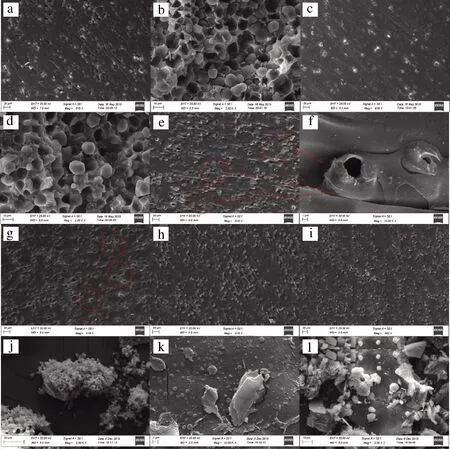
图1 迁移前淀粉基餐勺表面和断口面、迁移后及迁移实验 的蒸发残渣SEM照片
Fig.1 SEM micrographs of the surface and the fracture of starch-based spoons before migration and after the migration experiment as well as the corresponding evaporated residue
2.1.2 热性能分析
不同的聚合物具有不同的裂解温度,热性能分析可以测定聚合物的裂解温度和获得聚合物的失重情况,因此本研究采用热重分析(thermogravimetric analysis,TGA)来确定淀粉基餐勺中除淀粉之外的主要组分,结果如图2所示。餐勺A和B的热分解过程经历了3个阶段,这与CHEN等[18]关于淀粉与聚丙烯共混物的TGA的研究结果相同。在热分解的第一阶段(T≤140 ℃),主要是水等易挥发物质分解的过程;第二阶段(240 ℃≤T≤360 ℃)的质量损失主要是由于淀粉的分解过程[19-20]造成的,这与苑春苗等[21]检测到的玉米淀粉的主要失重峰温度范围266~374 ℃非常相似;第三阶段(360 ℃ 图2 淀粉基餐勺的热重/差示扫描量热曲线 2.1.3 ATR-FTIR分析 ATR -FTIR技术在复合材料中高分子材料成分的分析应用有方法简单、易操作等明显优势[24],因此本文采用ATR -FTIR技术对餐勺A和B表面做进一步定性分析,结果如图3所示。由图3可知,餐勺A和B红外谱图中都有聚丙烯的特征峰和淀粉相关的峰,这一结果与LINARES等采用FTIR和DSC方法对聚丙烯和淀粉的的研究结果相似[25]。因此,结合TGA-DSC和ATR-FTIR的分析结果,本文研究的淀粉基餐勺除淀粉之外的另一种主要成分是聚丙烯。 图3 淀粉基餐勺A和B以及残渣的红外光谱 2.2.1 淀粉基餐勺在4种食品模拟物中总迁移检测 餐勺在4种食品模拟物中总迁移结果如图4-a所示。餐勺A在4%乙酸和10%乙醇的总迁移量分别为(16.05±1.51) mg/dm2和(17.50±1.41) mg/dm2(P>0.05);餐勺B在4%乙酸中的总迁移量为(17.54±1.66) mg/dm2,与餐勺A相比并无显著性差异(P>0.05)。然而,餐勺B在10%乙醇中的总迁移量为(2.21±0.60) mg/dm2,不仅明显地低于餐勺A在相同条件下的总迁移量(P<0.01),还显著性地低于其在4%乙酸中的总迁移量。此外,餐勺A和B在95%乙醇和异辛烷中的总迁移量都小于3 mg/dm2。 2.2.2 温度对淀粉基餐勺在4%乙酸和10%乙醇2种食品模拟物中总迁移的影响 GB 4806.7—2016[26]对塑料制品中总迁移量的限量标准为10 mg/dm2,餐勺A和B在4%乙酸和10%乙醇中的总迁移量都已超过该标准。本研究通过不同温度对餐勺在4%乙酸和10%乙醇2种食品模拟物中总迁移的影响,以进一步揭示淀粉糊化特性是否是导致餐勺A和B在该2种食品模拟物中高迁移量的原因。实验在GB 31604.1—2015基础上,增加了25、40、55 和85 ℃四个温度条件。实验结果如图4-b所示。由图4-b可以看出,总迁移量随着温度的升高而增大。当温度达到85 ℃时,总迁移量迅速增大。但餐勺B在10%乙醇中的总迁移量总是低于10 mg/dm2。 a-食品模拟物;b-温度 2.2.3 迁移后淀粉基餐勺和蒸发残渣形貌分析 结合总迁移实验和餐勺表征结果,猜想总迁移结果主要是受到淀粉的破裂和糊化的影响。因此,通过SEM对迁移后的餐勺表面进行微观形貌观察。图1-e~图1-h是淀粉基勺子A分别在模拟条件4%乙酸(70 ℃,2 h)、10%乙醇(70 ℃,2 h)、95%乙醇(60 ℃,2 h)和异辛烷(40 ℃,0.5 h)迁移实验后的SEM表面图,从图1-e和图1-f中可以明显看到淀粉表面有大量破裂和孔洞现象,这是由于淀粉颗粒在70 ℃高温下浸泡2 h后的破裂和脱落所引起的。但图1-g和图1-h未发现淀粉并脱落和破裂的情况,并与餐勺A表面图没有明显的差异,以上现象与总迁移结果一致。 在此基础上,我们同时利用SEM对总迁移实验收集得到的蒸发残渣进行分析。由于餐勺B在10%乙醇(70 ℃,2 h)总迁移量过小,无法收集得到其蒸发残渣。因此,仅对餐勺A在模拟条件4%乙酸(70 ℃,2 h)、餐勺A在模拟条件10%乙醇(70 ℃,2 h)以及餐勺B在模拟条件4%乙酸(70 ℃,2 h)总迁移实验中得到的蒸发残渣进行分析,结果如图1-h~图1-j所示。由图1-h~图1-j可知,餐勺A和B在食品模拟物中的蒸发残渣都出现了类似于糊化淀粉的团聚物。 2.2.4 蒸发残渣定性分析 为进一步确定残渣的主要成分,还采用了FTIR对残渣进行定性分析,结果如图3所示。通过与关于淀粉FTIR分析的研究[27-30]对比分析,发现残渣FTIR具有淀粉的特征吸收峰,其中包括:1 635 cm-1处由淀粉中H—O—H弯曲振动而产生的峰、3 284 cm-1处附近由于O—H的伸缩振动吸收产生的1个强且宽的吸收峰、2 926 cm-1处亚甲基C—H的不对称伸缩振动而产生的中等强度峰、1 365 cm-1处CH2的弯曲振动而产生的小吸收峰、1 015 cm-1和1 077 cm-1处分别由于C—O和C—C的伸缩振动而产生的吸收峰以及930 cm-1处淀粉由于非对称环模式(α-1,4糖苷键C—O—C)的骨架振动而产生的吸收峰。 因此,根据SEM和FTIR结果,蒸发残渣的主要成分是淀粉。 2.2.5 淀粉基餐勺的淀粉结构分析 通过以上分析,餐勺的总迁移主要是由于淀粉的破裂和脱落引起。考虑到淀粉的糊化过程与淀粉的形状、淀粉的分子结构和体系中的物质等有密切相关性[31-32],推测淀粉的分子结构不同是引起餐勺A和B在10%乙醇食品模拟物中的迁移量具有显著性差异的重要因素。 本研究利用体积排阻色谱法对餐勺A和B中的淀粉分子结构进行分析,结果如图5所示。 图5 餐勺A和B中淀粉分子大小分布 餐勺A淀粉分子主要分布在100 nm内,而餐勺B的淀粉分子分布范围在1~800 nm,可初步推测餐勺A中含有较高含量的直链淀粉或者分子较小的支链淀粉,餐勺B含有较多长链的支链淀粉。餐勺A因其高直链淀粉分子之间主要是通过氢键链接,所以在与水性和酸性食品模拟物的接触过程中更容易受到pH影响,尤其是在碱性条件下其氢键易被破坏。同时由于淀粉分子较小,更有利于水分子渗入,从而加速淀粉糊化。相反,餐勺B的支链分子淀粉比例高、分子较大,容易形成较长的双螺旋结构使得分子之间的作用力增强以阻止水分扩散和渗透,进而导致水分子破坏淀粉结构的能力降低,淀粉糊化速率减慢,需要更高的温度条件来达到淀粉糊化行为。因此在10%乙醇的模拟条件下,餐勺A淀粉更容易糊化以致于餐勺A的总迁移量更高于餐勺B。 淀粉基餐勺在水性和酸性食品模拟物的总迁移量显著大于油性食品模拟物,并已超过GB 4806.7—2016对塑料制品中总迁移量的限量标准10 mg/dm2。淀粉颗粒的破裂和脱落是造成总迁移量增大的主要原因。因此,淀粉基餐勺不适合在高温条件下与水性食品和酸性食品接触,从而也说明食品接触用淀粉基材料与传统食品接触用塑料有所差异,但目前还没有淀粉基食品接触材料的食品安全国家标准。 总迁移实验得到的蒸发残渣主要成分是淀粉,但除淀粉之外是否还有其他物质迁移到食品模拟物(或食品)中,或者由于淀粉的破裂和脱落而增大有意和非有意添加物进入食品模拟物(或食品)的可能性以造成的安全隐患仍不可忽略。 本研究初步判断淀粉基餐勺A和B淀粉分子大小和直链/支链淀粉的比例不同是造成其分别在10%乙醇食品模拟物中的迁移量有显著差异性的重要原因。为扩大淀粉基材料的适用性,减少其在与食品接触时不必要的迁移,原料淀粉的分子结构,如直链/支链淀粉比例、淀粉分子大小等因素对食品接触用淀粉基材料在食品中迁移的影响有待进一步研究。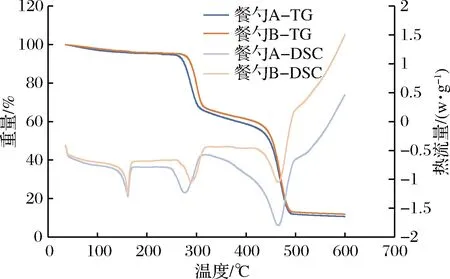
Fig.2 TGA/DSC of starch-based spoons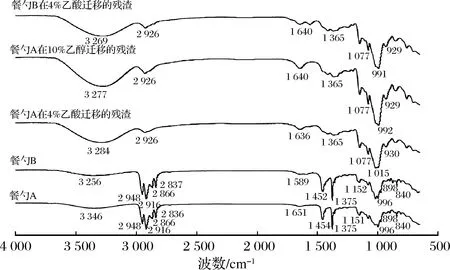
Fig.3 ATR-FTIR of starch-based spoons and the evaporated residue from migration2.2 淀粉基餐勺总迁移检测分析
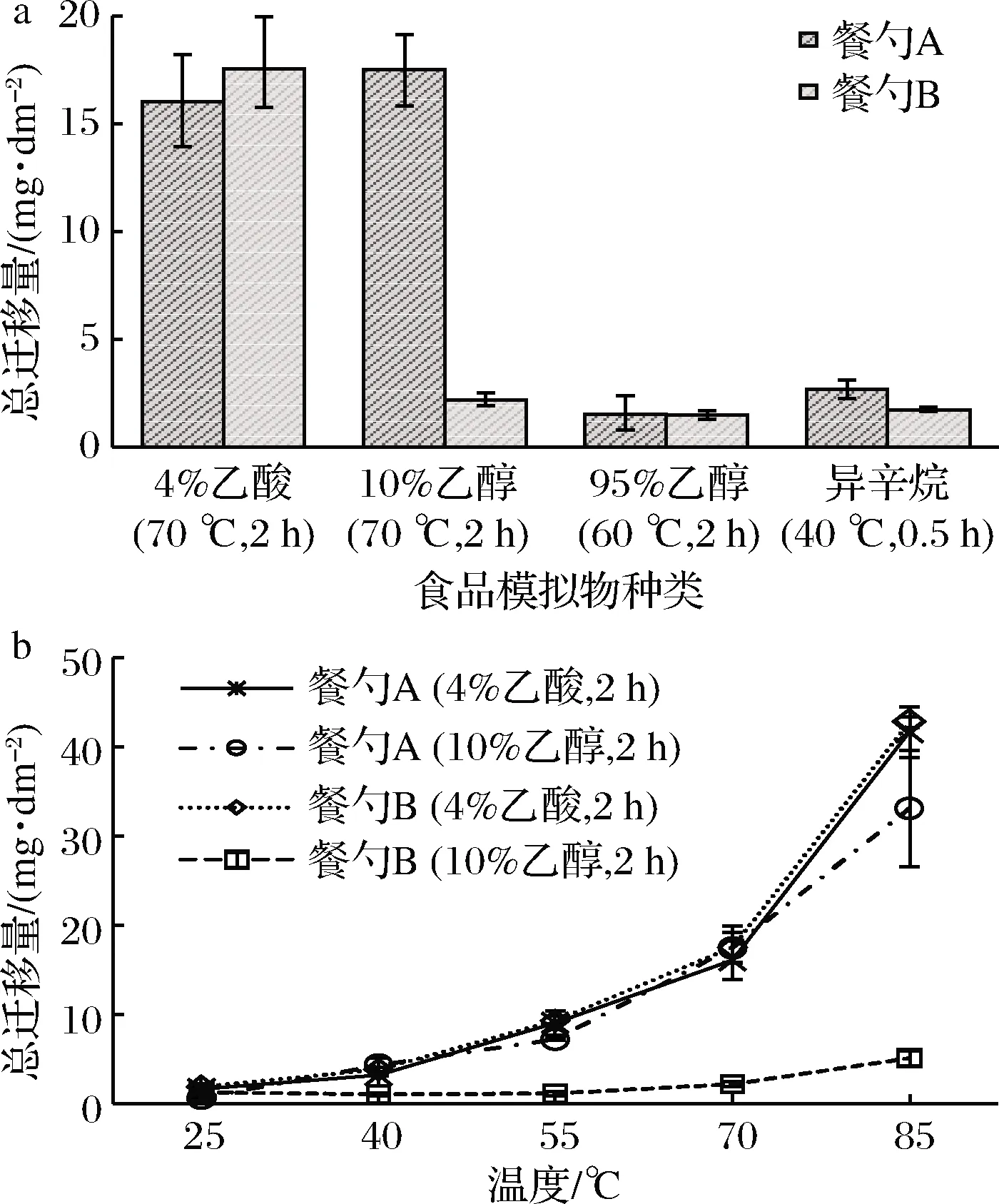
图4 淀粉基餐勺A和B在四种食品模拟物与 不同温度条件下的总迁移
Fig.4 Overall migration from starch-based spoons in four migration conditions, and different temperature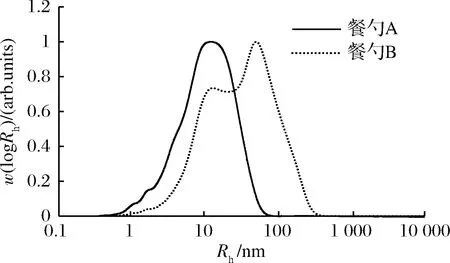
Fig.5 Molecular size distributions of starch from spoons3 结论
