分光光度法测定水中甲醇
2020-07-05张静,郭隽
张 静,郭 隽
(山西省生态环境监测中心, 山西 太原 030027)
甲醇(Methanol,CH3OH) 是结构最为简单的饱和一元醇,沸点为64.8 ℃,为无色、有酒精气味、易挥发的液体。急性甲醇中毒可引起中枢神经损害,表现为头痛、眩晕、乏力、嗜睡和轻度意识障碍等,重者出现昏迷和癫痫样抽搐。甲醇可致视神经损害,重者引起失明或代谢性酸中毒。甲醇是常用的有机溶剂,易溶于水,蒸气压较低;它也是重要的化工原料,主要用于制甲醛,在有机合成工业中用作甲基化剂和溶剂,是制造甲基叔丁基醚的原料,也可直接掺入汽油作为汽车燃料,还是制造某些农药、医药的原料。甲醇的大量生产、应用及其毒害,使之成为环境监测中的一项重要指标。
甲醇的测定有气相色谱法、液相色谱法[1-3]、分光光度法。常用的分光光度法是把甲醇氧化为甲醛,通过羟醛缩合反应生成显色化合物,在可见光条件下通过分光光度法进行测定,预处理后的检测方法主要有乙酰丙酮法[4-5]、酚试剂分光光度法[6]、乙酰乙酸乙酯分光光度法[7]和变色酸氧化法[8]等。
目前环境保护标准中,甲醇的监测分析标准仅有气相色谱法[9-10],但是该方法对仪器及操作人员素质要求较高,而且多为空气中甲醇的测定,目前尚未发布测定水质甲醇的标准方法。本研究采取的分光光度法具有操作简便、易于推广等优点,弥补了水质甲醇监测的空白。
1 实验方法
1.1 实验仪器及主要试剂
分光光度计(上海菁华科技仪器有限公司);50 mL具塞比色管;实验用电炉或恒温水浴锅(上海树立仪器有限公司);万分之一天平(梅特勒电子天平)。
硫酸:ρ(H2SO4)=1.84 g/mL,优级纯。
1%高锰酸钾溶液:称量1.0 g高锰酸钾溶于水中,定容至100 mL,可保存15 d。
0.5%变色酸钠溶液:称量0.5 g变色酸[C10H6Na2O8S2·2H2O或 C10H8O8S2]溶于水中, 定容至100 mL。放入棕色瓶避光,2~8 ℃冷藏,可保存15 d。
5%亚硫酸钠溶液:称量5 g无水亚硫酸钠,溶于水中,定容至100 mL,可保存7 d。
甲醇标准贮备液:于25 mL容量瓶中,先加入10 mL水,准确称量容器和水的总重量m1,然后用微量注射器加入200 μL甲醇(甲醇为色谱纯及以上级别),使用万分之一天平准确称量容器和甲醇水溶液的总重量m2。两次称量之差(m2-m1) 即为甲醇的质量,将该溶液定容至刻度,计算1.00 mL溶液中甲醇的微克数。也可采用市售标准溶液。
甲醇标准使用液:用水将甲醇标准贮备液稀释成5 μg/mL的标准使用液。
1.2 样品采集和保存
用棕色磨口玻璃瓶采集水样,样品密封、避光,2~8 ℃冷藏保存,48 h内完成样品的分析。
1.3 实验步骤
取5 mL水样,加入0.25 mL硫酸和0.5 mL 1%高锰酸钾溶液,及时加盖并摇匀。放置5 min后,滴加5%的亚硫酸钠溶液,直至紫色刚褪去时,再多加一滴。加入0.5 mL 0.5% 变色酸溶液,摇匀。沿管壁缓慢加入6 mL硫酸,加盖,静置约30 s后摇匀,切忌颠倒。将溶液放入沸水浴中加热15 min,取出后于暗处冷却至室温。用20 mm比色皿,以水作参比,在570 nm处测定吸光度,标准系列显色后于暗处放置24 h内吸光度保持稳定。以甲醇的含量(μg) 为横坐标,对应的吸光度为纵坐标,绘制校准曲线,并计算回归线的斜率、截距和相关系数。
2 实验条件的优化
2.1 氧化反应酸度的优化
硫酸提供的酸性环境,影响高锰酸钾的氧化性能。选取不同配比的硫酸进行实验(选取曲线的18 μg中间点作为研究对象),分别加入0.125 mL浓硫酸,0.25 mL(1+1) 硫酸溶液,0.25 mL浓硫酸,0.5 mL(1+1) 硫酸溶液,0.5 mL浓硫酸,进行条件优化,实验结果见表1。

表1 氧化反应酸度条件
由表1的实验结果可见,用0.25 mL的硫酸可以将溶液酸度调整到氧化还原反应所需的范围,实验最终选择加入0.25 mL的硫酸作为氧化还原反应的最佳条件。
2.2 高锰酸钾氧化时间
在酸性环境下,高锰酸钾将甲醇氧化成甲醛。高锰酸钾与甲醇有足够的反应时间,才能保证显色完全并稳定。选取曲线的18 μg中间点作为研究对象,对氧化反应时间进行了优化,实验结果见图1。
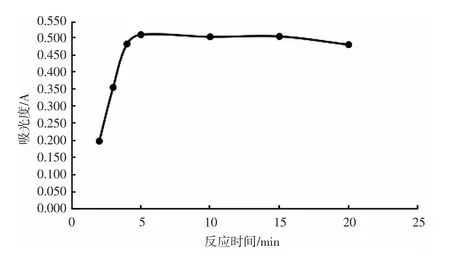
图1 氧化反应时间的选择
由图1可见,加入高锰酸钾5 min后吸光度达到峰值,随后由于反应时间的延长,高锰酸钾将甲醛氧化成甲酸,吸光度下降。实验最终选择10 min为高锰酸钾的氧化时间。
2.3 亚硫酸钠的加入方式
亚硫酸钠用于去除氧化反应剩余的高锰酸钾,亚硫酸钠加入不宜过量,否则会导致浑浊;量不足时,则呈现黄色。《空气和废气监测分析方法》第四版中定量加入0.5 mL亚硫酸钠,不容易判断变色终点,本方法中采用滴管逐滴加入亚硫酸钠溶液,便于判断变色终点,然后多加一滴。两种方法的比对结果见表2(选取曲线的18 μg中间点作为研究对象)。

表2 亚硫酸钠加入方式比对
由表2可见,加入0.5 mL亚硫酸钠时实验空白增大,整体吸光度增大;滴加亚硫酸钠时,空白值低,方法的整体灵敏度大。实验最终选择滴管滴加的方式加入亚硫酸钠。
2.4 加入变色酸后的放置时间
甲醇被氧化成甲醛后,与变色酸钠生成紫色化合物。该显色反应需要在强酸性环境中进行,在加入浓硫酸之前溶液仍然不变色。选取曲线的18 μg中间点作为研究对象,对加入变色酸后的反应时间进行了考察,在每个时间点均进行5次平行测定,实验结果见表3。
由表3可见,加入变色酸后,放置0 min、2 min、5 min、15 min,吸光度没有明显的差别,可以立即加入浓硫酸。
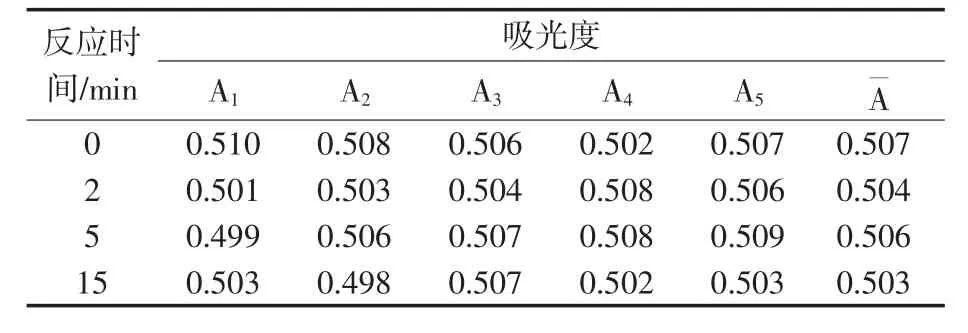
表3 显色反应时间
2.5 显色酸度的优化
甲醛与变色酸的显色反应需在约9M[11]的酸度环境下进行,选取曲线的18 μg中间点作为研究对象,对浓硫酸的加入体积量进行了考察,实验结果见表4。

表4 显色反应酸度条件
由表4可见,硫酸的用量直接影响体系的酸度。酸度不足,导致显色不完全,色度不稳定。在硫酸用量达到6 mL时,可以保证显色完全,吸光度稳定。
2.6 显色后的稳定时间
分光光度法的显色反应需要一定时间才能完成,而且形成的有色配合物稳定性也各不相同,因此必须在显色后一定时间内进行比色。选取曲线的18 μg中间点作为研究对象,进行了显色反应条件实验,实验结果见表5。

表5 显色后的稳定时间
由表5可见,显色后的溶液稳定性好,显色后放置24 h内吸光度保持稳定。显色反应需在暗处避光进行,以避免由于光线照射或散射光引起的色度不稳定。
2.7 本方法与《空气和废气监测分析方法》 第四版中方法的比对
分别按照本方法的实验步骤以及《空气和废气监测分析方法》[12]第四版中的实验步骤进行了校准曲线的测定,结果如图2所示:

图2两种方法校准曲线对比
由图2可见,通过一系列的实验证明,本方法的校准曲线斜率远大于四版书中校准曲线的斜率,即本方法灵敏度高,检出限低,显色反应充分、稳定,便于不同实验室及实验人员操作。
2.8 实际样品的测定
为了验证本方法的实用性,选取地表水实际样品进行了分析,并进行了加标回收实验,结果如表6所示:

表6 实际样品的测定
由表6可见,本方法的加标回收率在85%以上,精密度和准确度均能满足实际工作的需求。
3 结论
本研究对四版书中水质甲醇的测定方法进行了大量的条件优化,各项实验指标均优于四版书,更利于出具准确的环境监测数据,调整后的优点主要体现在:
(1) 根据显色反应的原理,甲醇在酸性溶液中,被高锰酸钾氧化成甲醛,四版书中氧化反应步骤的酸度不足,甲醇未被充分氧化,导致曲线斜率低,灵敏度不足。本方法调整了反应酸度,保证甲醇被最大程度氧化,从而提高了反应效率。变换了试剂加入顺序,先加入变色酸,再加入硫酸,充分利用浓硫酸进入水溶液时的放热反应,使显色反应更加充分,从而提高方法的灵敏度,降低了方法的检出限。
(2) 控制反应酸度、反应时间等关键因素,弥补了原方法标准曲线线性差,准确度、灵敏度不足的缺点。本方法的测定灵敏度高,操作步骤更为简便,为甲醇监测提供了技术支撑。
(3) 水中甲醇的监测工作很重要。然而,目前环境保护标准中,甲醇的监测分析标准仅有气相色谱法,使用气相色谱法设备昂贵、操作复杂,使用成本高,需要实验人员有熟练的技能。与气相色谱法相比,分光光度法仪器设备简单,操作简便,仪器及耗材成本低,人员技术要求相对较低,检出限可以达到与气相色谱法同等浓度水平,精密度、准确度等指标均与气相色谱法无显著性差异。分光光度法具有操作简便、测定快速、可现场分析、易于推广等优点,但目前尚未颁布水中甲醇分光光度法的相关标准,本方法弥补了此空白。
