危重症患者营养评估方法的研究进展
2020-06-24王金宁邱昌翠朱晓萍刘菲于晓丽
王金宁,邱昌翠,朱晓萍,刘菲,于晓丽
(同济大学附属第十人民医院,上海,200072)
ICU 患者由于长期禁食导致营养不良的发生率比一般住院患者高40%~80%[1],而营养不良能明显延长患者在ICU 的滞留时间,增加患者感染和并发症的发生率与死亡率[2]。早期营养支持有助于改善危重患者的临床结局,减轻患者病情,提高患者的生存率,降低致残率,缩短ICU 滞留天数,对患者的治疗和预后具有重要意义[3]。及时、准确地评估患者的营养风险是提供营养支持的前提,然而目前临床上仍有部分存在营养风险的患者未被发现[4]。本文综述了不同类型的营养风险评估方法在危重症患者中的应用,旨在为医护工作者对ICU 患者进行营养评估提供参考。
1 单一测量指标
1.1 实验室评价指标
实验室评价指标包括血红蛋白(hemoglobin,Hb)、白蛋白(albumin,ALB)、前白蛋白(prealbumin,PA)、血尿素、血清肌酐、淋巴细胞总数等。由于危重症患者常出现急性病理生理学上的改变,进而会出现白蛋白以及前白蛋白的减少,因此血浆蛋白质被认为是评估患者营养状况的必要实验室指标[5]。然而,这些指标并不能给临床医生准确的图像判断患者的营养状况,不能准确而全面地反映患者的营养状况。因此,近些年研究者的目光主要集中在探讨复合指标的筛查工具上[6]。
1.2 人体测量学指标
人体测量是一种无创的,简单直接评估患者营养状况的方法。常见的人体测量学指标有体质指数 (body mass index,BMI)、皮褶厚度(skinfold thickness,TSF)、中臂周长 (middle arm circumference,MAC)和小腿周长。由于ICU 患者长期卧床或有水肿,BMI 的测量值可能存在误差,对于危重症的营养评估可能存在一定的局限性。通过TSF 和MAC 的测量可了解患者的皮下脂肪厚度和肌肉情况,较直观地反映患者的营养状况。近几年,有学者[7]提出一种新型的人体测量学指标—拇内收肌厚度(adductor pollicis muscle thickness,APMT)评估患者的营养状况。APMT 是国外的一种新型的营养评估方法,研究表明[8],健康成人的APMT 与体质量、身高、BMI 值有显著的相关性。测量方法:受试者取坐位,五指自然水平伸展平放于同侧大腿,此时拇指与食指形成一个虚拟的三角形,测量虚拟三角形顶点,使用同一皮褶厚度计施以10g/mm2的压力于拇内收肌,连续测量3 次取其平均值[9]。GHORABI 等[7]研究发现,APMT异常的患者与普通人相比,死亡风险增加到5.6 倍,器官衰竭的发展增加到14.5 倍,ICU 停留时间延长到11.3 倍。国外的一项研究发现[8],APMT 的测量是一种有效的检测手术患者和住院患者营养不良的方法,由于它简单、经济、快捷且无创,应作为住院患者的营养风险筛查的一种手段。目前,国内关于APMT 测量应用于营养评估的病例还很少见,希望国内的学者加强这方面的研究,为危重症患者的营养评估找到一种新的方案。
1.3 间接测热法
合理的能量供给是为危重症患者提供个体化营养支持的基础,间接测热法通过测定患者实际的静息能量消耗,从而评估患者的营养状况,并在此基础上为患者制订合理有效的营养支持方案。测量原理是根据能量守恒定律,通过测量患者在一定时间内吸气时O2的消耗量与呼气时CO2的排出量及浓度差,计算出氧耗量(VO2)和二氧化碳释放量(VCO2)[10],并根据Weir 公式计算能量消耗值(metabolic energy expenditure,MEE),MEE=3.9×VO2+1.1×VCO2,从而得到患者每日的热卡平均量。由于危重症患者病种复杂,病情发展快,患者在整个病程中的能量和营养需求一直处在动态的变化之中,间接测热法能够准确评估患者的能量消耗[11],因此在危重症患者营养评估中也起到越来越重要的作用。
1.4 机体成分营养测定评估-相位角(phase angle,PhA)
ICU 患者遭受创伤、脓毒症和大量代谢压力,造成分解状态,严重影响患者的营养状况和身体成分。PhA 是由生物电阻抗技术所衍生的一项评估人体营养状况的指标。PhA 不仅反映了完整细胞膜的电学特性,还反映了水在细胞外和细胞间的空间分布[12]。生物电阻抗分析(bioelectrical impedance analysis,BIA)用50HZ 的电流频率通过测量组织的电阻和电抗,从而计算得到PhA。有学者[13]研究得到以下结果:PhA<2,提示严重营养不良;PhA 介于2~3,提示中度营养不良;PhA>3,提示轻度营养不良。但目前国际上还没有统一的评价标准。研究表明[14],BIA 能够早于人体测量检测到身体的细微变化,并且测量来自BIA 的PhA 值能够客观地筛查营养不良的危重症患者。KYLE 等[15]研究发现,患者的PhA 减少,由NRS2002 或SGA 估计的营养风险增加。也有学者[12,14]研究发现,对于营养状况较好的患者,其PhA 值也较高,并且PhA 值与白蛋白计数呈现明显的正相关。
2 复合指标—营养评估量表
2.1 营养不良通用筛查工具(malnutrition universal screening tool,MUST)
MUST 是英国肠外肠内营养协会多学科营养不良咨询小组开发的营养风险筛查工具,主要用于筛查患者有无蛋白质-热量营养不良[16](proteinenergy malnutrition,PEM)。SKIPPER 等[17]以SGA 为标准测得MUST 对医疗手术住院患者营养不良评估的灵敏度和特异度分别为61%和76%。POULIA等[18]研究表明,MUST 是老年住院患者最适合的营养风险筛查工具,MUST 具有快速、简单、易操作的特点。但此工具内容中的体质量丢失及营养状态皆为患者的主观反映,缺乏客观测量数据,营养评估的结果容易造成较高的假阳性,影响营养干预的准确性和有效性[19]。
2.2 营养风险筛查2002 (nutritional risk screening 2002,NRS2002)
NRS2002 是2002年欧洲肠外肠内营养学会(European society for parenteral and enteral nutrition,ESPEN)以KONDRUP 为首的专家组基于128 个随机对照临床研究制订的[20]。沈玉波[21]对160例ICU患者使用NRS2002 对危重症进行营养评估的灵敏度和特异度分别为86.33%和91.22%。NRS2002 能够动态地判断患者营养状态变化,及时反馈患者的营养状况,为患者调整营养和治疗方案提供依据。JOHANSEN 等[22]研究表明,采用NRS2002 进行临床结局的预测,并对有营养风险的患者进行营养支持能缩短患者住院时间。NRS2002 具有简单、无创,筛查所需时间短的优点,容易被临床医务人员掌握,同时NRS2002 的评分结果还可用来判断住院患者是否存在营养风险[23]。有些医院还在NRS2002 的基础上制订了患者营养风险筛查评估表[24],具体内容见表1。
2.3 微型营养评定法 (mini nutritional assessment short-form,MNA-SF)
MNA-SF 是在20世纪90年代研究提出的营养评价方法[25],MNA-SF 是MNA的简化版,与其他筛查工具相比,MNA-SF 更适合老年患者营养风险评估[26]。KOREN-HAKIM 等[27]研究215例髋部骨折患者的营养评估工具发现,MNA-SF 可以预测36 个月内的再入院率和死亡率。MNA-SF 方法简单、易行、经济、无创,获得了很多国内外学者的肯定。MNA 不仅可用于预测有营养不良风险的患者,也可对已经发生营养不良的住院患者进行综合营养评估,而且还可用于预测健康结局、病死率和住院费用等[28]。韩莹等[29]研究发现,MNA-SF 评分结果不仅与传统营养指标BMI、ALB、Hb 等水平显著相关,还与心功能不全密切相关,可作为诊断心力衰竭严重程度的敏感指标。
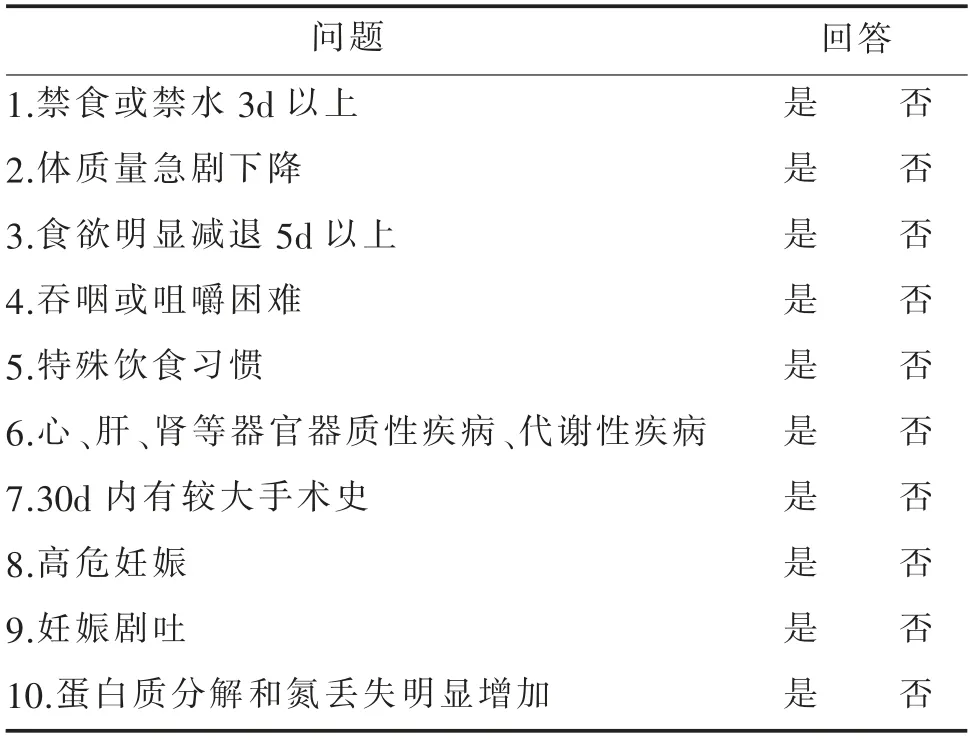
表1 住院患者营养风险筛查表
2.4 主观全面评定法(subjective global assessment,SGA)
SGA 是DETSKY 等[30]于1987年首次提出的一种简便易行的临床营养评估方法,是美国肠外肠内营养学会 (American society for parenteral and enteral nutrition,ASPEN)和欧洲肠外肠内营养学会联合推荐住院患者使用的营养风险筛查工具[31]。张春梅等[32]使用SGA 对271例老年患者进行营养评估得到的灵敏度和特异度分别为71.76%和84.18%。SGA 具有操作简单、快捷、无创、不需要使用其他生化检查等优点。由于SGA 中评估的内容例如病史可由患者本人或家属提供,因此SGA 已被证明可用于评估危重患者的营养状况[33]。
SGA 虽然应用广泛,但它更多反映的是疾病状况或现存的营养不足,不能对患者营养状况的动态变化及时做出反映,因此SGA 在营养筛查方面具有一定的局限性。近些年,有学者[34]对SGA的项目进行调整得到了一种新的评估工具-营养评估分数(nutritional assessment score,NAS),与SGA 相比,NAS 减少了问题的数量,阐明了与住院死亡率、住院时间长度、血清白蛋白和体重等临床变量的关联,与SGA 相比,对于营养状况最差的患者,NAS 更为精确。
2.5 患者自述-主观全面评定量表(patient-generated subjective global assessment,PG-SGA)
PG-SGA 是根据SGA 修正而来的一种应用更广泛的筛查工具[35],是专门为肿瘤患者设计的营养状况评估方法,是一种评估肿瘤患者营养状况的特异性工具。杨眉等[36]使用PG-SGA 量表对61例胃癌患者进行营养评估得到,与NRS2002 相比,PG-SGA 的阳性预测值为78.94%,阴性预测值为78.57%。杨家君等[37]研究发现,消化道恶性肿瘤患者的TNM 分期与患者PG-SGA 评分呈显著正相关,PG-SGA 评分越高的患者所对应的肿瘤TNM 分期越晚,在预测消化道恶性肿瘤患者临床TNM 分期方面,PG-SGA 可以起到一定的作用。FRUCHTENICHT 等[38]研究发现,PG-SGA可用于ICU 病房中的肿瘤患者,以发现肿瘤危重症患者的营养风险。
2.6 危重症营养风险评分(nutric score,Nutric)
Nutric 评分是研究人员针对ICU 住院患者经研究专门推出的营养评分系统[39],主要用于危重症营养风险的评估和筛查。该评分在常用营养筛查工具的基础上,对患者的营养评估内容和方式进行了优化,适用于卧床、病情危重及意识不清患者的营养风险评估[40]。KALAISELVAN 等[2]使用Nutric 评分对678例机械通气的ICU 患者进行营养评估得到的灵敏度和特异度分别为41.5%和73.8%。JEONG 等[41]研究发现,Nutric 评分从急性生理和慢性健康评估(APACHE)II 评分、序贯器官衰竭评估评分、合并症数、入院至ICU 住院天数、血清白细胞介素6(IL-6)水平等多方面对患者进行营养评估,具有比其他工具更好的优越性。但JENS 等[42]研究发现,该评分目前缺乏明确的疾病暴露时间标准,因此对于不同ICU 停留时间的患者,如何提供个体化的营养支持尚需要进一步分析。
3 不同营养评价方法在ICU 的应用现状
3.1 单一营养评估指标的应用现状
实验室测量指标为判断危重症患者营养状况的必查项目,但测量结果较片面,需结合其他指标来判断患者的营养状况。人体测量学指标可直观反映危重症患者的营养状况,但大部分指标易受卧床、水肿等影响,导致测量结果不准、有偏差。APMT 是一种新型的用于评估患者营养状况的方法,水肿对其干扰较小,正在逐渐运用于临床,但在国内重症监护室的应用还较少见。间接测热法可动态地测量患者的能量消耗,评估患者的实际营养需求,从而为患者提供个体化的营养支持方案。间接测热法是测量静息能量消耗的金标准[11],目前广泛地应用于各地医院包括危重症在内的住院患者。PhA 是由生物电阻抗技术所衍生的一项评估人体营养状况的指标。AL-KALALDEHI 等[43]研究证明,来自BIA 的PhA 评分对危重症患者营养不良的筛查是客观有效的,并建议PhA 与MUST一起使用来确认同一危重患者的营养不良状态。该方法因其无创、操作简便、测量数据精确、廉价等优点,在临床上的应用前景广阔。然而,目前尚无统一的PhA 参考值供临床应用,这在一定程度上限制了该技术的应用[44]。笔者认为由于危重症患者病情凶险、病因复杂、并发症多,仅凭单一指标难以全面评估患者的营养状况,还需结合复合指标来综合判断。
3.2 营养评估量表的应用现状
3.2.1 营养评估量表在国内的应用现状 MUST目前在国内主要运用于老年住院患者,对于非老年危重症患者的研究比较少见。安志红等[45]研究发现,重症患者的NRS2002 分值与APACHEⅡ评分、住院费用及并发症发生率呈现明显的正相关。刘新平等[46]对201例重症患者研究发现,对入住ICU 后的患者及时进行营养风险评估,对存在严重营养风险的患者尽早给予营养干预后,患者的病死率总体来说有所下降。沈玉波[21]研究发现,年龄在18 到60 岁之间的危重症患者,NRS2002 的诊断价值优于SGA 及MNA-SF,而在年龄60 岁以上的患者中,MNA-SF 的灵敏度和特异度更高,对于MNA-SF 筛查存在营养不良风险的患者,还可使用MNA 评分量表进一步核实。何超等[47]应用Nutric评分对59例ICU 住院患者进行评估发现,由于Nutric 评分不仅从营养或是热量,而是从多方面对患者的营养状况进行评估,因而比NRS2002 具有更明显的优越性。由于评估方法种类较多,笔者认为国内学者应进行随机对照试验,同时采用多种评估方法评估危重症患者的营养状况,比较其灵敏度及特异度,以寻找最佳证据。
3.2.2 营养评估量表在国外的应用现状 TRIPATHY等[48]研究证明,MUST 在老年危重症患者的营养评估中具有较高的灵敏度和特异度。SGA 虽然可用于危重症患者的营养评估,但具有一定的主观性,PG-SGA 是由SGA 修订而来,比SGA 应用更广泛,对于ICU 中的癌症患者尤为适用,但由于内容中一部分为患者自评,对于病情危重患者具有一定的局限性。NAS 也是在SGA 的基础上发展而来,但对于营养情况较差患者的营养评估,精确性更高[34]。Nutric 评分是最适合危重症患者的营养评估量表,在国际上的应用也十分广泛。ROSA 等[49]将Nutric评分翻译为葡萄牙语,并应用于巴西的危重症患者,根据得分情况给予营养支持,改善了患者的预后。然而,Nutric 评分也存在一些缺点,例如急性生理评分中的IL-6 值在大多数ICU 中并不容易获取,国外部分学者针对这一情况,对Nutric 评分进行了修正,得到mNutric 评分,该评分对于ICU 住院患者28d 死亡率,具有较好的预测效果[41]。但目前该评分在临床上还未普及,需要更多的研究以验证其准确性和实用性。
4 小结及展望
综上所述,目前,没有统一的营养风险评估方法可供ICU 住院患者使用,每种指标和工具都有自己的优点和缺点。总体来看,对于ICU 的患者要在实验室检查和人体测量学指标的基础上,使用合适的营养风险评估量表来对患者进行综合评估,根据评估结果,给予适当地、个体化地营养支持干预,以改善患者的营养状况和预后,降低死亡率。目前,国内对于危重症患者的营养风险筛查工具的使用研究还比较欠缺,医护人员对各评分量表的使用也不够熟练。因此,希望有更多的临床试验来发现并证实适合我国危重症患者的营养风险筛查及评估的工具。
