氧化石墨烯杂化分子印迹复合膜制备及性能研究
2020-06-22毛东阳杨丹范杰平
毛东阳,杨丹,范杰平
(南昌大学资源环境与化工学院,江西南昌330031)
引 言
分子印迹技术(molecular imprinting technique,MIT)又称为分子模板技术,被认为是一种识别与制备“分子钥匙”的人工“锁”技术[1]。MIT 原理类似于生物上的抗原-抗体反应,所以MIT 具有高度的选择性。由于其高选择性特点,MIT 可应用于分子识别、检测、分离和催化等领域[2],尤其是在分离领域更是引起了广泛的研究兴趣[3-7]。由于MIT 作用机理主要是氢键作用力,而水的存在会破坏这种相互作用,所以如何提高分子印迹聚合物在纯水溶液体系中的吸附选择性仍然是一个挑战。
辛弗林具有升高血压、调血脂、收缩血管和促进脂肪分解等作用[8-10]。随着辛弗林的应用越来越广,对其纯度及精度的要求也越来越高。目前,辛弗林的分离纯化方法主要是有机溶剂萃取法、固相萃取法(SPE)、树脂色谱法(离子交换树脂,大孔吸附树脂)、超临界流体萃取技术和分子印迹膜法等[11-13]。分子印迹膜(molecularly imprinted membrane,MIM)是一种结合膜分离技术和分子印迹技术的近代新型分离技术[14-15],它具备特异选择性、构效设定性和长期稳定性特点[1,6,16]。前期研究发现[6-7,15],MIM 存在机械强度不够、易碎的缺点,这也是制约MIM 技术发展的一大因素。
近年,氧化石墨烯(GO)作为石墨烯的衍生物,不仅拥有石墨烯机械强度高的特点,还有很多的亲水基团,如环氧基、—COOH、—OH 等,因此,GO 可与其他物质发生多种相互作用,并拓展其应用范围[17-18]。GO 的特殊网状结构也可提高聚合物的韧性和力学性能[19-20]。
在前期工作中[6],以甲基丙烯酸为功能单体制备了MIM,并考察其在甲醇/水(体积比4/1)溶剂体系中对辛弗林的分离效果。本文以水溶性的丙烯酰胺为功能单体,离子液体(溴代1-丁基-3-甲基咪唑)为致孔剂,通过GO 掺杂制备复合膜(GO-MIM)以提高MIM 的力学性能,并研究其在纯水溶剂体系中对辛弗林盐酸盐的分离性能。
1 实验材料和方法
1.1 主要实验材料及设备
试剂:石墨粉(上海晶纯试剂有限公司,0.03 mm);辛弗林盐酸盐(陕西森弗生物技术有限公司,98.66%);章胺盐酸盐(东科药业,98.5%);酪胺(上海晶纯试剂公司,98%);过硫酸铵(天津市大茂化学试剂厂,98%);N,N'-亚甲基双丙烯酰胺(MBA)(上海晶纯试剂有限公司,97%);N-甲基咪唑(上海晶纯试剂有限公司,99%);溴丁烷(国药集团化学试剂有限公司,化学纯);丙烯酰胺(天津市大茂化学试剂厂,98%);N,N,N,N-四甲基乙二胺(阿拉丁化学试剂有限公司,99%);其他试剂皆为分析纯。
仪器:Agilent 1100 高效液相色谱仪(美国Agilent公司);KQ-600DB数控超声波清洗器(昆山市超声仪器有限公司);KDC-160HR 高速离心机(科大创新股份有限公司中佳分公司);FD-1C真空冷冻干燥机(郑州长城科工贸有限公司);CMT8502 微机控制电子万能试验机(深圳市新三思材料检测有限公司);Quanta200F 环境扫描电子显微镜(荷兰FEI 公司);JEM-2100 透射扫描电子显微镜(日本电子株式会社);FTIRNicolet5700 傅里叶变换红外光谱仪(美国热电尼高力公司);XRD-7000 多功能X 射线衍射仪(英国Bede公司)等。
1.2 GO的制备
参考文献[21]方法,利用改进的Hummers 方法制备GO,具体方法如下。
首先,向500 ml 三口圆底烧瓶中加入135 ml 浓H2SO4(98%),置于冰水浴中,在持续、快速机械搅拌下依次加入3.0 g NaNO3和5.0 g石墨粉,待石墨粉和NaNO3均匀分散后,边搅拌边将18.0 g 的KMnO4缓慢加入反应体系中,并使混合物温度保持在10℃以下,冰水浴搅拌2 h 后,撤去冰水浴,使混合物在室温条件下持续搅拌反应2 d,加入200 ml 的5%H2SO4水溶液进行稀释。室温继续搅拌2 d,再加入200 ml的5%H2SO4水溶液稀释。室温搅拌反应1 d,加入100 ml 的5% H2SO4水溶液后,搅拌反应2 h。随着反应的进行,混合物逐渐由黑色变为淡褐色浆糊状。随后,缓慢加入12 ml的H2O2(30%),混合物变为亮黄色,室温搅拌2 h 后,离心,除去上清液,沉淀物继续用3%稀硫酸和0.5%的H2O2水溶液的混合溶液1000 ml 反复清洗,以除去残留的金属离子,再用去离子水反复洗涤,直至清洗液呈中性,离心后取下层凝胶。
将胶体状的沉淀物分散到2000 ml 的去离子水中,在200 W 和40 kHz 条件下超声剥离2 h,至氧化石墨固体均匀分散到水溶液中。接着,在3000 r/min 下将悬浮液离心25 min,以除去未被剥离的氧化石墨,收集上清液。沉淀物加蒸馏水,继续超声剥离、离心,如此反复,合并上清液。将上清液浓缩,浓缩后的样品呈胶体状,真空冷冻干燥得GO固体。
1.3 GO杂化分子印迹复合膜(GO-MIM)的制备
1.3.1 离子液体的制备 参考文献[22]方法,准确称取0.4 mol N-甲基咪唑和0.48 mol 的溴丁烷混合加入到250 ml 的圆底烧瓶中,在60℃下磁力搅拌回流反应6 h 以上,反应结束后溶液呈淡黄色,用30 ml无水乙醚依次洗涤三次,再用50 ml 二氯甲烷稀释,旋蒸回收溶剂后,在60℃下真空干燥12 h 以上,得到淡黄色的离子液体溴代1-丁基-3-甲基咪唑([Bmim]Br)。
1.3.2 辛弗林盐酸盐GO-MIM 的制备 称取0.2 mmol 辛弗林盐酸盐固体加入50 ml 锥形瓶中,向其中加入10 mmol 丙烯酰胺,再加入4.8 g[Bmim]Br 和不同质量分数的GO 水溶液4 ml,超声混合均匀,静置过夜让其预组装,然后加入4 mmol 交联剂MBA和0.02 mmol 引发剂过硫酸铵,超声处理,得到铸膜液,再加入一定量的催化剂N,N,N,N-四甲基乙二胺;每份铸膜液取1.5 ml加入同样大小的培养皿中,待铸膜液平铺均一后转移至烘箱中于40℃下反应24 h。待印迹膜聚合完成,往培养皿中加入去离子水,浸泡分子印迹膜至其自然脱离培养皿。取出印迹膜,采用索氏提取方法,以醋酸水溶液(体积比,醋酸∶水=1∶9)作为洗脱液,洗涤至洗脱液中检测不到辛弗林盐酸盐,制得氧化石墨烯杂化分子印迹复合膜(GO-MIM)。
采用上述方法,不加GO,制备普通非杂化的分子印迹膜(NGO-MIM);不加辛弗林盐酸盐制备杂化的非分子印迹膜(GO-NIM);不加GO 和辛弗林盐酸盐,制备非杂化的非分子印迹膜(NGO-NIM)。
1.4 色谱条件
参考文献[23]方法,测定辛弗林盐酸盐的高效液相色谱(HPLC)条件为:色谱柱为Hypersil BDS-C18柱(5 μm,4.6 mm×200 mm);流动相为(0.02% H3PO4,0.05% 十二烷基硫酸钠,0.02% 三乙胺)∶甲醇=60∶40;柱温为30℃;流速是1.0 ml/min;检测波长λ 为224 nm。以峰面积和进样量绘制出标准曲线,得到标准曲线方程为y=5.43271316x-5.50252,R2=0.9997,其中,x为进样量,y为峰面积。
1.5 吸附量的测定
取15.0 mg膜材料,放入50 ml磨口锥形瓶中,加入20.0 ml 浓度为0.5 mmol/L 的辛弗林盐酸盐水溶液,将锥形瓶放入30℃的恒温振荡器中振荡数小时,然后用HPLC 检测溶液中辛弗林盐酸盐的浓度,依据吸附前后溶液中辛弗林盐酸盐浓度的变化,按式(1)算出膜材料的吸附量Q

式中,Q 为膜的吸附量,μmol/g;C0为吸附前溶液中模板分子的起始浓度,mmol/L;C 为吸附后溶液中模板分子的浓度,μmol/ml;V为溶液的体积,ml;m为所用膜的质量,g。
1.6 选择性吸附研究
取15.0 mg 的GO-MIM,放入50.0 ml 的磨口三角锥形瓶中,依次加入20.0 ml浓度分别为0.6 mmol/L 的辛弗林盐酸盐、酪胺和章胺盐酸盐水溶液形成的混合溶液,在恒温振荡器中振荡数小时后,用HPLC 检测混合液中各物质的浓度,依据吸附前后混合液中各物质浓度的变化,可计算出MIM(或NIM)对三种物质的吸附量Q。
1.7 膜渗透实验
为考察GO-MIM 对辛弗林盐酸盐分子的印迹及分离效果,参考前期研究工作[6],用膜渗透实验装置(Valia-Chien 渗透池)进行实验。将GO-MIM 或GO-NIM 分别夹在渗透池的中间,一边加入相同浓度的辛弗林盐酸盐水溶液、章胺盐酸盐水溶液、酪胺水溶液或它们的等浓度的混合溶液15.0 ml,另一边的接收池加入等体积的二次水。两边分别放入一个磁力搅拌子,每间隔一定的时间取样。利用式(2)~式(4)分别计算单位面积物质透过量(P,μmol/cm2)、膜渗透印迹因子(TF)和膜渗透选择性因子(SF)。P 值越大,说明该物质渗透速度越大;TF 越大,GO-MIM 印迹效果越好;SF 越大,膜的透过选择性越好。

式中,C 代表接收池中物质的浓度,μmol/ml;V代表接收液体积,ml;A代表膜的有效面积,cm2。

式中,PMIM和PNIM分别代表物质透过单位面积的GO-MIM和GO-NIM的量。

式中,Ptemplate和Panalogue分别代表模板分子和竞争分子透过单位面积膜的量。
2 实验结果
2.1 GO的表征

图1 GO的透射电镜图[(a)、(b)]及选区电子衍射图[(c)、(d)]Fig.1 TEM[(a),(b)]and selected area electron diffraction pattern[(c),(d)]of GO
2.1.1 TEM 检测 如图1(a)、(b)所示,可观察到GO的丝绸般的形态及其褶皱;图1(c)、(d)展示的是GO部分选择区的电子衍射图,可知GO 具有规则的晶型,这些结果都说明成功制备了GO。
2.1.2 红外检测 图2 为GO 的红外光谱图,3443 cm-1处的吸收峰为羟基(—OH)的不对称伸缩振动和弯曲振动吸收,1725 cm-1处的吸收峰为芳基羧酸中羰基()的伸缩振动,1639 cm-1处的吸收峰为未氧化的碳碳双键()的伸缩振动,1279 cm-1处的吸收峰为环氧基中的碳氧键(C—O—C)的对称伸缩振动[24-26],结果说明由氧化石墨成功剥离制备了GO。

图2 GO的IR图Fig.2 IR of GO
2.1.3 XRD 检测 由图3 可以看出,GO 在2θ=10.45°处有非常高特征衍射峰,这表明所制备的GO质量非常好,氧化程度高[27]。通过上述表征可知,本实验成功制备了高质量的GO,产率为79.35%(产率=GO 质量/石墨粉质量),密度约为12.5 mg/cm3,说明冷冻干燥法制得的GO密度很小[28]。

图3 GO的XRD谱图Fig.3 XRD pattern of GO

图4 GO-MIM与NGO-MIM的水接触角Fig.4 Water contact angle of GO-MIM and NGO-MIM
2.2 MIM的表征
2.2.1 接触角检测 如图4,GO-MIM 的接触角为26.4°±0.49°,NGO-MIM 的接触角为22.6°±3.99°,虽然NGO-MIM 的亲水性略大于GO-MIM,但总体变化不明显。这是因为MIM 本身就是聚丙烯酰胺,亲水性很强,故亲水性的GO 加入对GO-MIM 对水的润湿性影响不大。
2.2.2 MIM的SEM检测 图5 为添加不同量GO 的MIM 的SEM 图,由图可看出经洗脱后的MIM 存在明显的孔隙结构,这有利于模板分子的通过。另外,由图可知,随着GO 含量的增加,分子印迹膜表面出现明显的丝绸样的褶皱结构,说明GO 掺杂进入MIM。而未添加GO 的印迹膜[NGO-MIM,图5(a)、(b)]却并无这一结构。这说明添加的GO可掺杂进入MIM 中,将有利于增强MIM 的力学性能。

图5 GO含量不同的MIM洗脱前及相应洗脱后的MIM的SEM图Fig.5 SEM of MIM with different amount of GO before and after washing

图6 GO、GO-MIM和MIM的IR图Fig.6 IR of GO,GO-MIM and MIM
2.2.3 红外检测 如图6,3443 cm-1处为—OH 的不对称伸缩振动吸收峰,2930 cm-1处为C—H 的伸缩振动吸收峰,1639 cm-1处为未氧化的C C的伸缩振动吸收峰,1526 cm-1处为芳环的骨架振动峰,583 cm-1处是苯环的C—H 弯曲振动吸收峰。1113 cm-1为缩醛中和O 相连的C—H 的弯曲振动吸收峰,这个峰只有GO-MIM 才有,GO 与MIM 都没有,说明GO 与MIM 之间已经发生了反应,以化学键的方式结合在一起[24-26],这样使印迹膜各组成部分联系更加紧密和牢固,从而增强了印迹膜的力学性能,拓展了MIM的使用范围。
2.2.4 GO-MIM 机械性的表征 采用微机控制电子万能试验机分别检测洗去模板分子后的辛弗林盐酸盐分子印迹膜的力学性能,检测模式为薄膜拉伸,拉伸速度为1 mm/min,检测结果如图7。随着GO 含量的增加,辛弗林盐酸盐MIM 的机械性表现也随之增强,在印迹膜的GO含量为0.25%时机械性最强,拉伸强度达到2.1 MPa,拉伸率为35.5%。这是因为GO 可以通过氢键及共价键等与聚合物材料连接在一起[29-30],可增强其力学性能。
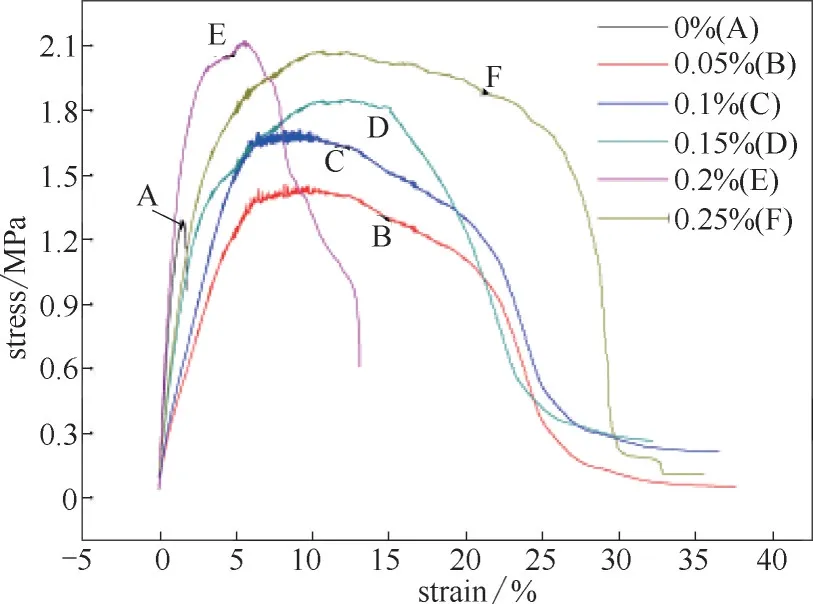
图7 GO-MIM的应力-应变曲线Fig.7 Stress-strain curves of GO-MIM
2.3 MIM吸附性能
2.3.1 吸附动力学曲线 由图8 可以看出,随着吸附时间的不断延长,MIM 对模板分子的吸附量也随之增大,前50 min 的吸附速率很快,之后随着时间的增加,吸附速率趋于平缓,100 min 后MIM 对模板分子的吸附趋于平衡。GO-MIM 和NGO-MIM 对模板分子的吸附量差别不大,NGO-MIM 的吸附量仅略大于GO-MIM。

图8 吸附动力学曲线及拟合曲线Fig.8 Adsorption kinetic data and the fitting curves
为了更好地研究两种MIM 在辛弗林盐酸盐水溶液中的吸附动力学机制,通过Lagergren 的一级动力学方程[式(5)]、二级动力学方程[式(6)]对数据进行拟合。
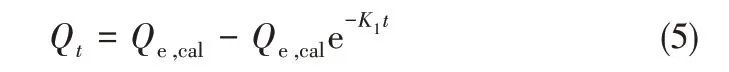
式中,Qt、Qe,cal分别为时间t 及拟合的平衡吸附量,μmol/g;K1是一级动力学方程吸附速率常数。
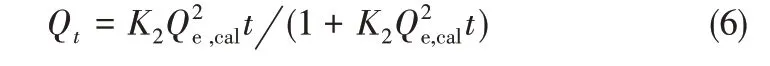
式中,Qt、Qe,cal分别为时间t 及拟合的平衡吸附量,μmol/g;K2是二级动力学方程吸附速率常数。
由式(5)和式(6)拟合出GO-MIM 和NGO-MIM 对辛弗林盐酸盐水溶液吸附的一、二级动力学曲线见图8(a)、(b),拟合出的相应参数见表1。

表1 动力学方程回归参数值Table 1 Regression parameter of kinetic equation
分析拟合曲线和回归参数值可知,两个拟合方程对吸附数据都有较好的拟合效果,但一级动力学拟合相关系数高于二级动力学方程拟合,表明MIM和NIM 在辛弗林盐酸盐水溶液中的吸附行为都更符合一级动力学的吸附机制[31-32]。
2.3.2 吸附热力学 分别配制0.3~1.0 mmol/L 的不同起始浓度的辛弗林盐酸盐水溶液,将15.0 mg的膜分别投入体积为20 ml 不同浓度的溶液中。在40、30、20℃恒温振荡4 h,取样检测。
从图9可以看出,随着温度的增加,平衡吸附量呈下降趋势,说明该吸附过程属于放热过程。而随着辛弗林盐酸盐起始浓度的升高,吸附量也随着增大,但当浓度升高到0.9 mmol/L 左右时,吸附量的增势趋于平缓。
为了进一步研究GO-MIM 和NGO-MIM 对辛弗林盐酸盐水溶液的吸附过程,本实验采用Langmuir方程[式(7)]和Freundlich 方程[式(8)]对这三个温度的等温吸附曲线进行拟合。
Langmuir方程为

Freundlich方程为

式中,Ce表示平衡时辛弗林盐酸盐水溶液浓度;Qe、Qmax分别为平衡时的吸附量和理论上最大吸附量;KL为Langmuir 常数;Qe表示平衡时的吸附量;KF和n都为Freundlich平衡吸附常数。
由图9 及表2 可知,在20,30,40℃这三种温度下,整体上,Langmuir方程表现出的各项拟合度均高于Freundlich 方程,因此它能更好地描述GO-MIM对辛弗林盐酸盐水溶液的吸附行为。对比GO-MIM与NGO-MIM 的吸附平衡常数KL与KF可知,两者的吸附常数都随吸附温度的升高而减小,这表明温度降低有利于吸附进行。

图9 GO-MIM和NGO-MIM的等温吸附数据及拟合曲线Fig.9 Isothermal adsorption data and fitting curves of GO-MIM and NGO-MIM
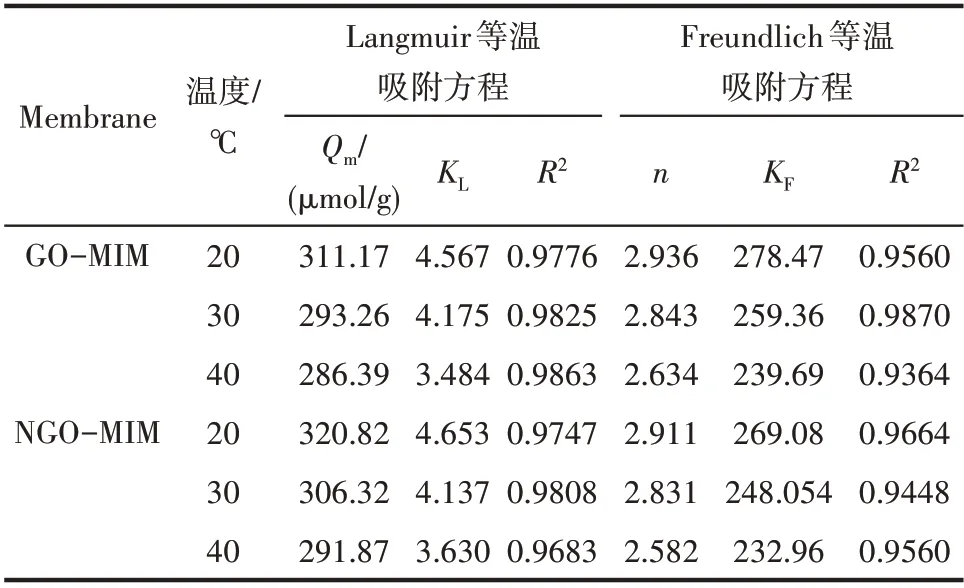
表2 GO-MIM 和NGO-MIM 对辛弗林盐酸盐水溶液的Langmuir和Freundlich回归数据Table 2 Langmuir and Freundlich regression data of GO-MIM and NGO-MIM with synephrine hydrochloride aqueous solution
热力学分析主要是从能量变化的方面来研究MIM 吸附辛弗林盐酸盐的过程。由表2 可知Langmuir 方程对GO-MIM 和NGO-MIM 吸附辛弗林盐酸盐水溶液的拟合效果更好,所以吸附过程的标准Gibbs 能变化ΔG (kJ/mol)、标准熵变ΔS (J/(mol·K))、标准焓变ΔH (kJ/mol)可用式(9)和式(10)进行计算获得[33],相关计算结果列于表3 中。以ΔG°和T 作直线所得截距和斜率的值分别为对应的ΔH°值和ΔS°值。

式中,KL是由Langmuir 方程拟合所得的常数[34],L/mol;R 为常用气体常数,8.314 J/(mol·K);ΔG°为吸附过程的标准Gibbs能变化,kJ/mol;ΔH°为吸附过程的标准焓变,kJ/mol;KL为Langmuir 常数;ΔS°为吸附过程的标准熵变,J/(mol·K);T为吸附温度,K。
由表3 可知,ΔG°在三个温度下均为负值,说明GO-MIM 和NGO-MIM 对模板分子的吸附行为在热力学上是可行的且是自发的过程,ΔG°的绝对值随着温度的升高而减小,说明低温更利于模板分子的吸附。ΔH°的值为负值,说明GO-MIM 和NGO-MIM对模板分子的吸附都为放热过程,这也说明了高温不利于吸附过程的顺利进行。ΔS°的值为正值,说明在吸附过程中,吸附的物质在固液界面上的混乱度增加了[35]。

表3 GO-MIM 和NGO-MIM 吸附辛弗林盐酸盐的热力学参数Table 3 Thermodynamic parameters of synephrine hydrochloride adsorbed by GO-MIM and NGO-MIM
2.3.3 选择性吸附研究 为了考察膜对模板分子的选择性,选取与辛弗林盐酸盐分子结构非常类似的章胺盐酸盐和酪胺为竞争分子,分别测定了它们在20℃下的静态吸附容量,三种物质结构如图10所示。

图10 辛弗林盐酸盐(a)、章胺盐酸盐(b)和酪胺(c)的分子结构式Fig.10 Molecular structural formula of synephrine hydrochloride(a),octopamine hydrochloride(b),and tyramine(c)

表4 不同底物在MIM和NIM上的吸附量Table 4 Adsorption capacity of different substrates on MIM and NIM
由表4 可知,MIM 对辛弗林盐酸盐的吸附量远远高于NIM,说明MIM 对辛弗林盐酸盐有非常好的印迹效果。这是由于MIM 中含有能与辛弗林盐酸盐空间结构互补的特定大小和形状的印迹空穴,同时MIM 表面还含有可与辛弗林盐酸盐相互匹配的官能团,所以GO-MIM 和NGO-MIM 都对辛弗林盐酸盐分子拥有特异选择性吸附能力。另外,MIM 对与辛弗林盐酸盐的吸附量远大于结构相似的酪胺、章胺盐酸盐,而NIM 对三者的吸附量较接近,这同样说明MIM 对辛弗林盐酸盐有较高的选择性识别和吸附能力。此外,由表4 可知,GO-MIM 对辛弗林盐酸盐的吸附容量略低于NGO-MIM,这可能是由于GO 的柔性结构覆盖住了某些有效结合位点导致的。NIM 因其内部没有特异性结合位点,主要凭借聚合物表面上的非特异性吸附来结合底物,所以其对各分子的吸附量都差别不大。
为进一步考察MIM 对辛弗林盐酸盐吸附的选择性,考察了GO-MIM 在0.6 mmol/L 的辛弗林盐酸盐、酪胺和章胺盐酸盐的混合溶液中的吸附性能。如图11 所示,通过比较发现,经过GO-MIM 吸附后[图11(b)],溶液中辛弗林盐酸盐的含量明显大大减少,而酪胺与章胺盐酸盐变化比较小,这说明了GO-MIM 对辛弗林盐酸盐分子具有选择性识别和吸附能力。

图11 GO-MIM吸附前(a)、后(b)混合液的HPLC图Fig.11 HPLC of the mixture before(a)and after(b)adsoption by GO-MIM
2.4 MIM膜渗透实验
为进一步考察不同物质竞争渗透在20℃下通过GO-MIM 和GO-NIM 的能力,以具有相同浓度的三种生物碱的混合溶液作为供给液体,分时段采集接收池溶液,其HPLC 图列于图12 中。从图12 可知,当GO-MIM 作为渗透膜时,在通过GO-MIM 的渗透池的接收池中,辛弗林盐酸盐的峰值变化显著高于另外两种化合物,说明模板分子(辛弗林盐酸盐)明显比另外两种竞争分子(酪胺和章胺盐酸盐)更快地通过印迹膜。而以GO-NIM 作为渗透膜时,三种物质的渗透速度接近。
图12中的数据经过计算后,可绘制三种物质的混合液透过GO-MIM 和GO-NIM 的时间-透过液浓度图,图13 能更直观地看出GO-MIM 和GO-NIM 的性能的差异。比较图13 中曲线1 和4 可以明显看出,在同等的时间段内,模板分子(辛弗林盐酸盐)透过GO-MIM的速度和透过量明显优于GO-NIM的表现,这是因为GO-MIM 中含有与模板分子在形状和大小上正好互补的孔穴结构,进而形成特定的通道供模板分子顺利通过;而GO-NIM 的内部不存在印迹孔道,最后导致模板分子的通过速度较慢。

图12 供给池中初始样品HPLC图(a)、透过GO-MIM(b)和GO-NIM(c)后接收池混合溶液HPLC相图Fig.12 HPLC chromatograms of the standard mixtures in the initial donor solution(a),receptor solutions through GO-MIM(b)and GO-NIM(c)

图13 三种物质的混合液透过GO-MIM和GO-NIM的时间-透过液浓度图Fig.13 Time-transmission of the mixtures through GO-NIM and GO-NIM
对比图13 中GO-MIM 的三条曲线(1、2 和3)可以看出,在同样的时间段内,模板分子透过GO-MIM的量远远高于另外两种竞争分子,这充分说明,即使酪胺和章胺盐酸盐与模板分子的结构和大小差别不大,但它们的透过速度仍慢于辛弗林盐酸盐,因为它们与GO-MIM 中特定的结合位点不匹配,无法像模板分子那样具有优先通过的驱使力,从而导致它们的透过速度都较小。而模板分子与GO-MIM的孔穴在形状和大小上都能够很好地结合,进而具有优先渗透的动力,直观反映就是它的通过速度更快,渗透量更大。
对比图13 中GO-NIM 的三条曲线(4、5 和6),三种物质透过GO-NIM 速度相差不大,这是因为GONIM 中没有特定的结合位点,这阻碍了模板分子顺利通过膜,从而模板分子的渗透速度都较小。
由式(3)和式(4)可知,MIM 的TF和SF值越大,说明此膜的印迹效果和分离选择性越好[36-37]。各物质透过膜的相关参数列于表5 中,由表中数据可知GO-MIM 对辛弗林盐酸盐有明显的印迹效应(TF=2.06),辛弗林盐酸盐透过GO-MIM 的竞争性强于另外两种生物碱(SF 都接近2),属于“优先透过(facilitated permeation)”机理[38]。
3 结 论
本文利用Hummers 法,结合冷冻干燥法制备了GO。通过混入GO制备了GO杂化的GO-MIM,实验发现,GO 可大大提高MIM 力学性能,拉伸强度达到2.1 MPa,拉伸率达到35.5%,并且对MIM 的吸附性能影响很小。吸附动力学研究表明GO-MIM 吸附辛弗林盐酸盐更符合一级动力学吸附机制。吸附热力学研究表明GO-MIM 吸附辛弗林盐酸盐更符合Langmuir 吸附模型,并且该吸附是热力学自发和放热过程。选择性吸附实验结果表明,GO-MIM 对辛弗林盐酸盐有选择性吸附的能力,体现明显的印迹效果。膜渗透实验结果表明,辛弗林盐酸盐透过GO-MIM 的速度大于透过GO-NIM 的速度,且辛弗林盐酸盐透过GO-MIM 的速度大于结构相似的章胺盐酸盐和酪胺的透过速度,符合“优先透过(facilitated permeation)”机理。综上所述,GO-MIM表现出了较好的力学性能和优异的选择吸附性,有望用于对辛弗林盐酸盐的分离。

表5 三种物质通过GO-MIM 和GO-NIM 的相关参数Table 5 Permeation factors of three substrates through GO-MIM and GO-NIM
符 号 说 明
A——膜的有效面积,cm2
C——接收池中物质的浓度,μmol/ml
Ce——平衡时辛弗林盐酸盐水溶液浓度,mmol/L
ΔG°——吸附过程的标准Gibbs能变化,kJ/mol
ΔH°——吸附过程的标准焓变,kJ/mol
KF——Freundlich平衡吸附常数
KL——Langmuir常数
K1——一级动力学方程吸附速率常数
K2——二级动力学方程吸附速率常数
n——Freundlich平衡吸附常数
P——单位面积物质透过量,μmol/cm2
Panalogue——竞争分子透过单位面积膜的量,μmol/cm2
PMIM——物质透过单位面积的GO-MIM 的量,μmol/cm2
PNIM——物质透过单位面积的GO-NIM 的量,μmol/cm2
Ptemplate——模板分子透过单位面积膜的量,μmol/cm2
Qe——平衡时的吸附量,μmol/g
Qe,cal——时间拟合的平衡吸附量,μmol/g
Qmax——理论上最大吸附量,μmol/g
Qt——时间t的平衡吸附量,μmol/g
R——常用气体常数,8.314 J/(mol·K)
ΔS°——吸附过程的标准熵变,J/(mol·K)
SF——膜渗透选择性因子
T——吸附温度,K
TF——膜渗透印迹因子
t——吸附时间,min
V——接收液体积,ml
