HIV-1感染者抗病毒治疗后耐药情况分析及其基线CD4+T细胞与治疗后CD4+T细胞的相关性
2020-06-21黄丽花陈桂彬
周 明,黄丽花,陈桂彬
(广西壮族自治区龙潭医院中心实验室,广西 柳州 545005)
尽管经过抗病毒治疗,HIV感染者体内的病毒得到有效控制,降低了艾滋病的发病率和死亡率。然而由于依从性、个体自身的抵抗力、胃肠道的吸收不好、呕吐、腹泻及HIV病毒自身的变异产生的抗药性,使一部分患者的病毒得不到有效抑制,依然处于高水平,使抗病毒药物的有效性受到影响[1]。人类免疫缺陷病毒(HIV)是一种逆转录病毒,主要攻击人体的CD4+T细胞并使其数量减少,使机体的抵抗力明显下降。CD4+T细胞水平是机体免疫状态的最好体现 ,CD4+T细胞数快速下降说明免疫力降低。艾滋病的病情进展快速,抗病毒治疗可以使病毒得到有效的控制[2]。因此,除了对接受治疗的HIV感染者开展耐药监测以外,分析其产生耐药的原因,可能为HIV感染者的治疗提供新的思路。
1 资料与方法
1.1研究对象:选取2018年~2019年在我院就诊的HIV-1感染者共112例,纳入标准:HIV-1免疫印迹法确证试验阳性,接受抗病毒时间>6个月,年龄>18周岁,经检测病毒载量>1 000拷贝/ml。根据耐药结果分为耐药组和非耐药组。所有患者能够并愿意提供书面知情同意书。本次研究经过本院医学伦理委员会同意。本次调查纳入分析的患者共112例,其中男75例(66.96%),女37例(33.04%),平均年龄(45.91±13.87)岁。
1.2方法:CD4+T细胞通过美国BD公司流式细胞仪FACSCanto检测。血浆样品中的病毒载量使用COBAS Ampliprep /TaqMan96分析系统(罗氏诊断,瑞士Rotkr uez有限公司)检测。①HIV核酸提取:对病毒载量>1 000拷贝/ml的样本,用美国雅培(Abbott)公司Viroseq HIV-1基因型耐药分析试剂盒提取HIV核酸,进行逆转录(RT),聚合酶链式反应(PCR),具体操作按试剂盒说明书进行操作。②循环测序:HIV-1基因型耐药分析检测试剂盒通过使用7个引物(4个正向引物和3个反向引物)测序HIV-1蛋白酶基因密码子1-99的整个区域和密码子1-335的三分之二区域。耐药分析:Viroseq系统软件从每个样本的7个引物采集测序数据,并将信息合并于一个单一项目中,在引物序列的汇集过程中,产生了一个包含整个蛋白酶基因和到达335个密码子的RT基因共有序列,将这一共有序列与已知的参照株HXB-2进行比较,识别变异的位点。
1.3观察指标:用美国雅培(Abbott)公司测序分析仪3500XL 通过sanger测序方法对HIV感染者进行耐药测序分析,分析耐药情况及抗病毒治疗患者耐药和非耐药组治疗前后CD4+T细胞的变化。
1.4统计学分析:应用SPSS 20.0软件处理数据,使用χ2检验和非参数检验比较各组在性别和年龄方面的差异,使用非参数检验比较耐药组和不耐药组的CD4+T细胞差异。以P<0.05为差异有统计学意义。
2 结果
2.1HIV耐药突变和耐药情况:通过耐药测序分析,本次研究对NRTLs有耐药突变者5 例,对NNRTLs有耐药突变者11 例,对PIs有耐药突变者0例,NRTLs和NNRTLs同时耐药者32例,NRTLs和PIs同时耐药者2例,对NRTLs、NNRTLs和PIs同时耐药者1例,共有51例患者至少对某类药物有耐药突变,病毒抑制失败个体总耐药发生率为45.54%(51/112)。见表1。
2.2HIV-1患者耐药情况与基线、治疗后CD4+T细胞的关系:选取的112例HIV-1患者经过抗病毒治疗大于半年以上,病载>1 000拷贝/ml,通过耐药测序分析,有51例耐药(45.54%),通过非参数检验,与非耐药组相比,两组基线CD4+T细胞差异有统计学意义(Z=-2.948,P=0.003),耐药组和非耐药组的CD4+T细胞四分位数分别为23(12.0-123.0)、92.0(22.5-281.5);通过抗病毒治疗后的CD4+T细胞差异有统计学意义(Z=-2.586,P=0.010),耐药组和非耐药组的CD4+T细胞四分位数分别为77.0(33.0-239.0)、174.0(75.0-318.5)。见表2。
表1 112例患者治疗方案及耐药发生比较[例(%),n=112]
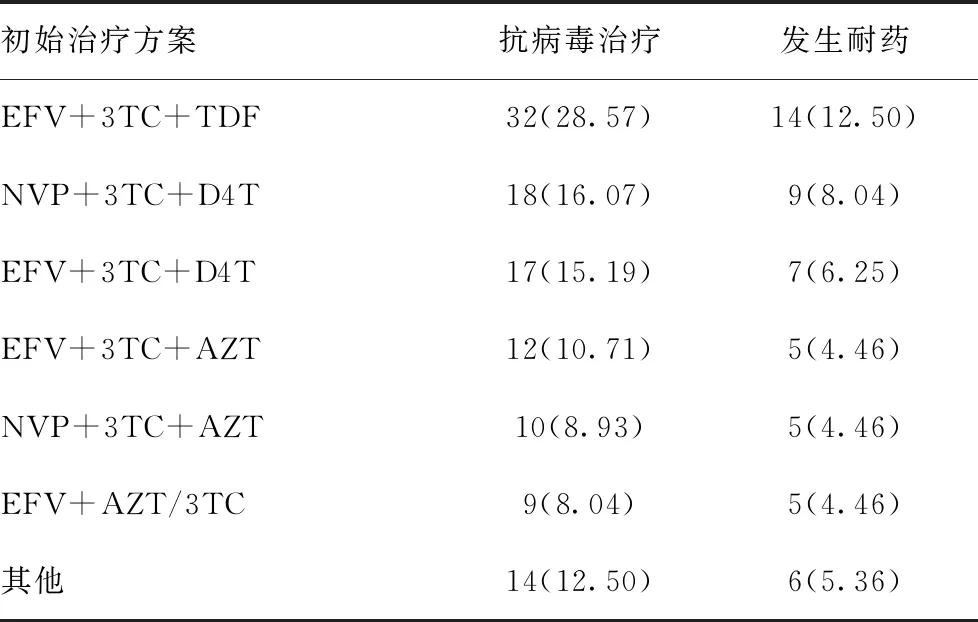
初始治疗方案抗病毒治疗发生耐药EFV+3TC+TDF32(28.57)14(12.50)NVP+3TC+D4T18(16.07)9(8.04)EFV+3TC+D4T17(15.19)7(6.25)EFV+3TC+AZT12(10.71)5(4.46)NVP+3TC+AZT10(8.93)5(4.46)EFV+AZT/3TC9(8.04)5(4.46)其他 14(12.50)6(5.36)
注:其他指克力芝+3TC+AZT 3例,克力芝+AZT/3TC 3例,NVP+AZT/3TC 3例,NVP+3TC+TDF 2例
表2 耐药组和非耐药组一般资料、基线与治疗后CD4+T细胞比较
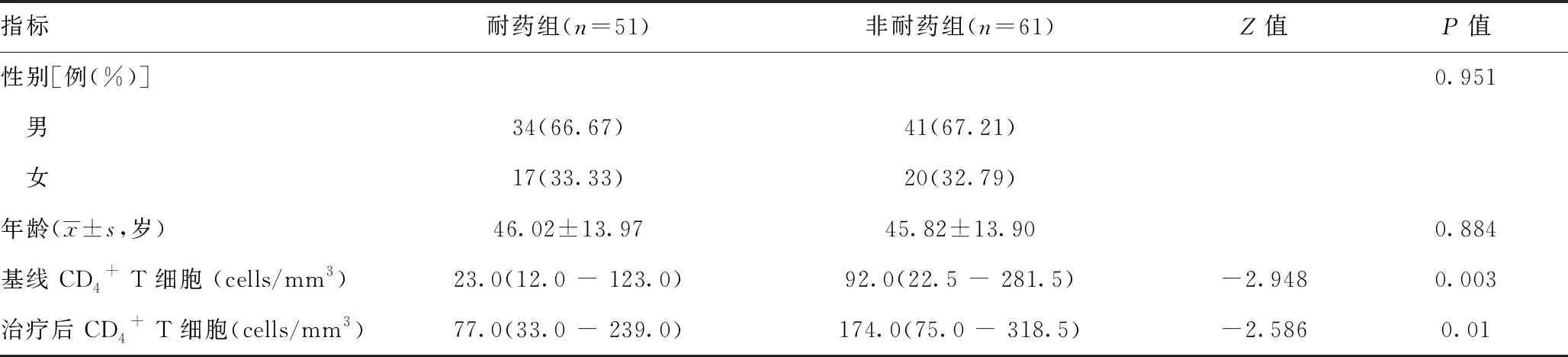
指标耐药组(n=51)非耐药组(n=61)Z值P值性别[例(%)]0.951 男34(66.67)41(67.21) 女17(33.33)20(32.79)年龄(x±s,岁)46.02±13.9745.82±13.900.884基线 CD4+ T细胞 (cells/mm3) 23.0(12.0 - 123.0)92.0(22.5 - 281.5) -2.9480.003治疗后 CD4+ T细胞(cells/mm3) 77.0(33.0 - 239.0) 174.0(75.0 - 318.5) -2.5860.01
3 讨论
抗逆转录病毒治疗(HARRT)能够有效抑制病毒复制,降低艾滋病发病率和死亡率, 然而HIV是反转录病毒的一种,具有高度变异性,在抗病毒药物的选择压力下,HIV基因易发生突变而产生对多种药物的耐药[3]。目前,耐药问题是目前全球的重大公共问题,是感染性疾病防治面临的重大挑战[4]。
本次HIV感染者的耐药以核苷类反转录酶抑制剂(NRTLs)和核苷类反转录酶抑制剂(NNRTLs)同时耐药为主,少数对蛋白酶抑制剂(PIs)耐药,与文献报道的云南和广西的耐药情况相符[5-6]。这可能与云南、广西两省治疗方案中以核苷类反转录酶抑制剂和核苷类反转录酶抑制剂的长期治疗有关。
HIV-1发病机制很复杂,尽管抗逆转录病毒治疗有效,个体对HARRT的疗效存在高度差异。在之前的研究中发现经过抗病毒后的疗效与基线CD4+T细胞水平、性别、年龄、免疫水平、耐药性等都有相关关系[7-8]。CD4+T细胞测量用于了解HIV毒的疾病进展和预防机会性感染,能监测抗病毒治疗后的治疗反应[9]。有研究指出基线CD4+T细胞计数较低和CD4+恢复欠佳与耐药有关[10]。在南非有研究表明,在接受抗逆转录病毒治疗的人群中,早期启动抗病毒治疗者在6个月后比晚期启动者具有更好的病毒抑制能力和更低的耐药性[11]。本次研究中,耐药组和非耐药组的基线CD4+T细胞及治疗后CD4+T细胞相比,差异有统计学意义(P<0.05),耐药组患者不论基线CD4+T细胞还是经过治疗后的CD4+T细胞都明显低于非耐药组,与文献报道结果相符。
总之,耐药检测能及时发现病毒学失败的原因,为临床对药物的选择,提高治疗效果,避免耐药病毒传播及降低死亡率提供可靠依据。分析耐药产生的原因能为HIV患者在治疗方向上提供更多的思路。
