心外膜脂肪组织与经皮冠状动脉介入治疗相关短期并发症的关系
2020-06-18侯小玲付振虹单冬凯张威陈韵岱
侯小玲 付振虹 单冬凯 张威 陈韵岱
心外膜脂肪组织(epicardial adipose tissue,EAT)是一种位于心肌和心包膜脏层之间的内脏脂肪组织。EAT通过分泌大量炎症因子,参与心肌和冠状动脉的生理功能和病理生理进程,与冠心病发生发展密切相关[1-2]。经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)是治疗冠心病的重要手段。最近一些研究表明,EAT与PCI术后无复流、支架内再狭窄等多种并发症相关,提示EAT可能在PCI术后并发症评估中有重要作用[3-6]。本研究拟通过回顾性分析2014年1月至12月于解放军总医院第一医学中心心内科行PCI的冠心病患者的临床资料,探讨EAT对PCI术后短期并发症的预测价值。
1 对象与方法
1.1 研究对象
回顾性分析2014年1月至12月解放军总医院第一医学中心心内科介入手术资料数据库中266例由3名具有丰富介入经验的高级职称医师完成的PCI术临床数据。纳入标准:(1)患者的临床症状、心电图和影像学检查均证实为阻塞性冠心病;(2)术前1周内于解放军总医院第一医学中心完成冠状动脉CT血管造影(computed tomography angiography,CTA)检查。排除标准:(1)既往有PCI及冠状动脉旁路移植术(coronary attery bypass graft,CABG)病史38例;(2)急诊手术11例,临床数据不全8例。最终,共有209例患者纳入本研究中。
1.2 研究方法
1.2.1 EAT体积测定 采用64层螺旋CT对所有入选患者的EAT体积进行测定。方法参照解放军总医院第一医学中心既往发表的文献[5]。简介如下:采用回顾性心电门控方法扫描。扫描参数:准直器宽度1.2 mm,采集螺距0.2,管电压120 kV,管电流自动调节(设定高限为200 mA),球管旋转1圈时间为0.33 s。扫描方法:采用高压注射器以5.0 ml/s的流速在肘前静脉注入370 mg非离子对比剂碘帕醇50~60 ml,同时以相同流速注入50 ml生理盐水,采用对比剂示踪法,在主动脉根部层面选取一兴趣区监测CT值,注射后触发动态同层监测,当感兴趣区内CT值增幅超过100 HU时,再延迟6 s自动触发扫描。使用专用工作站重建EAT图像,图像重建层厚0.75 mm。由有经验的放射科医师使用Volumer软件勾出心外膜边界,设定-180~-30 HU的CT值为脂肪组织,自动计算总EAT体积。
1.2.2 PCI术 PCI术按《中国经皮冠状动脉介入治疗指南2012(简本)》[7]进行,均首选经桡动脉入径。术者根据冠状动脉CTA及术中冠状动脉造影结果决定PCI的术式及支架置入数量。将冠状动脉病变达2支或以上称为多支病变。所有患者在PCI术前分别给予负荷剂量的阿司匹林300 mg和氯吡格雷300 mg,术中动脉内常规给予肝素80 U/kg抗凝。术后继续口服阿司匹林100 mg、每日1次和氯吡格雷75 mg、每日1次,至少维持1年。
1.2.3 短期并发症评估及相关定义 并发症均按照美国心脏病学会国家心血管数据注册系统(The American College of Cardiology-National Cardiovascular Data Registry, ACC NCDR)[8]的定义进行记录。短期并发症定义为PCI术中及术后30 d内所发生的并发症,主要包括冠状动脉夹层、穿孔、心肌梗死、脑血管事件、心原性休克、出血等。冠状动脉夹层定义为靶血管腔内膜撕裂,对比剂出现在腔外并引起血流受限[心肌梗死溶栓治疗试验(thrombolysis in myocardial infarction,TIMI)血流分级0~Ⅱ级],即美国国立心肺血液研究所针对冠状动脉夹层分型中的C~F型夹层。术后心肌梗死定义为PCI术后患者出现心肌缺血的临床症状,同时伴有心肌损伤标志物升高以及心电图的改变。出血按照出血学术研究联合会(The Bleeding Academic Research Consortium,BARC)定义的分类标准[9],重度出血包括BARC 3~5类,即血红蛋白下降≥3 g/dl,或术后输血,或需要经过特殊止血措施进行干预的出血(包括内窥镜下治疗的胃肠道出血,球囊导管压迫止血等),其余则定义为轻度出血,即BARC 1~2类[10]。
1.3 统计学分析
所有数据应用SPSS 17.0统计软件进行分析。计量资料中符合正态分布的采用均数±标准差表示,不符合正态分布的采用中位数(最小值,最大值)表示;计数资料采用例及构成比(%)表示。EAT与其他临床参数的关系采用Pearson相关分析或t检验。并发症的单因素分析采用Fisher确切概率法或χ2检验。将单因素分析中P<0.1的纳入logistic多因素回归分析,应用前进法逐步回归分析确定影响并发症发生的因素。以P<0.05为差异有统计学意义。
2 结果
2.1 患者基线资料情况
209例患者中男性130例(62.2%),平均年龄为(61.7±10.3)岁,平均体重指数(body mass index ,BMI)为(25.1±3.3)kg/m2。术前的平均EAT体积为(129.3±49.7)ml。PCI术中及术后30 d内共有18例(8.6%)患者发生并发症,未发生死亡。冠状动脉夹层为最常见的术后并发症,共有10例(4.8%),其中1例合并冠状动脉穿孔,1例合并术后出血;术后出血6例(2.9%),均为轻度出血;术后脑梗死1例;心肌梗死2例(1.0%),1例发生在PCI术后当日,1例发生在术后21 d因急性心肌梗死合并心原性休克再次入院(表1)。
2.2 EAT与其他临床参数的相关分析。
Pearson相关分析显示,EAT体积与BMI(r=0.433,P<0.001)和总胆固醇(r=0.222,P=0.002)呈正相关,与高密度脂蛋白胆固醇呈负相关(r=-0.235, P=0.001)。高血压病患者较无高血压病患者EAT体积显著增大[(135.6±47.1)ml比(119.3±52.3)ml,P=0.020];吸烟患者较无吸烟患者的EAT体积显著增大[(138.1±45.3)ml比(123.1±51.8)ml, P=0.031](图1)。EAT体积与性别、年龄及糖尿病等无相关性(均P>0.05)。
2.3 并发症的影响因素分析
单因素分析结果显示,高血压病、EAT体积大、多支病变、置入支架数量多的患者,PCI术后并发症发生率显著增高(均P<0.05)。低高密度脂蛋白胆固醇患者,PCI术后并发症的发生率也有所增高,但差异无统计学意义(P>0.05),详见表2。将上述可能的影响因素纳入logistic多因素回归分析,结果显示,EAT体积大(>130 ml)(OR 4.268,95%CI 1.422~12.812,P=0.010)和多支病变(OR 5.113,95%CI 1.786~14.638,P=0.002)是PCI术后并发症的独立危险因素(表3)。
3 讨论
有研究发现,EAT与冠心病的发生、发展及多种不良心血管事件发生风险密切相关[1-2]。 EAT的测量指标主要包括体积和厚度,测量方法主要包括CT、经胸二维超声心动图和心脏磁共振成像,其中CT在临床中应用最为广泛,可从三维全貌上准确测量EAT体积。本研究通过双源螺旋CT测得的209例冠心病患者PCI术前的EAT体积为(129.3±49.7)ml,这与既往的两项研究中报道的国人阻塞性冠心病患者的EAT体积为(125.6±47.1)ml和(140.54±47.09)ml基本一致[11-12]。此外,本研究中EAT体积与高血压病、高密度脂蛋白胆固醇、总胆固醇、吸烟和BMI相关,这与既往的多数研究结果一致,即EAT体积与传统的冠心病危险因素相关[13-14]。本研究通过回顾性分析209例冠心病患者住院期间的并发症情况发现,EAT体积大(>130 ml)和多支病变是PCI术中及术后短期并发症的独立危险因素。

表1 209 例患者临床基线资料
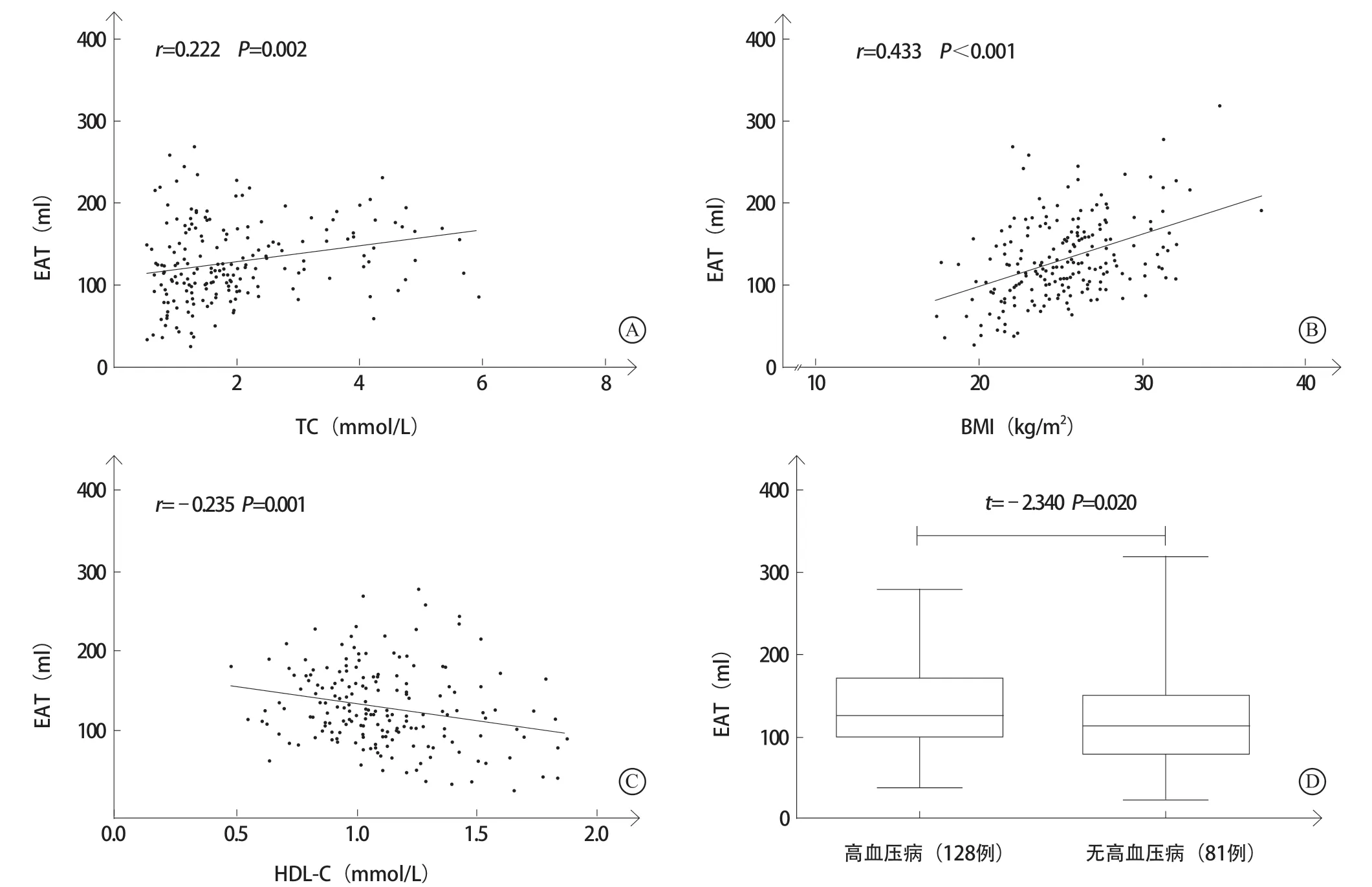
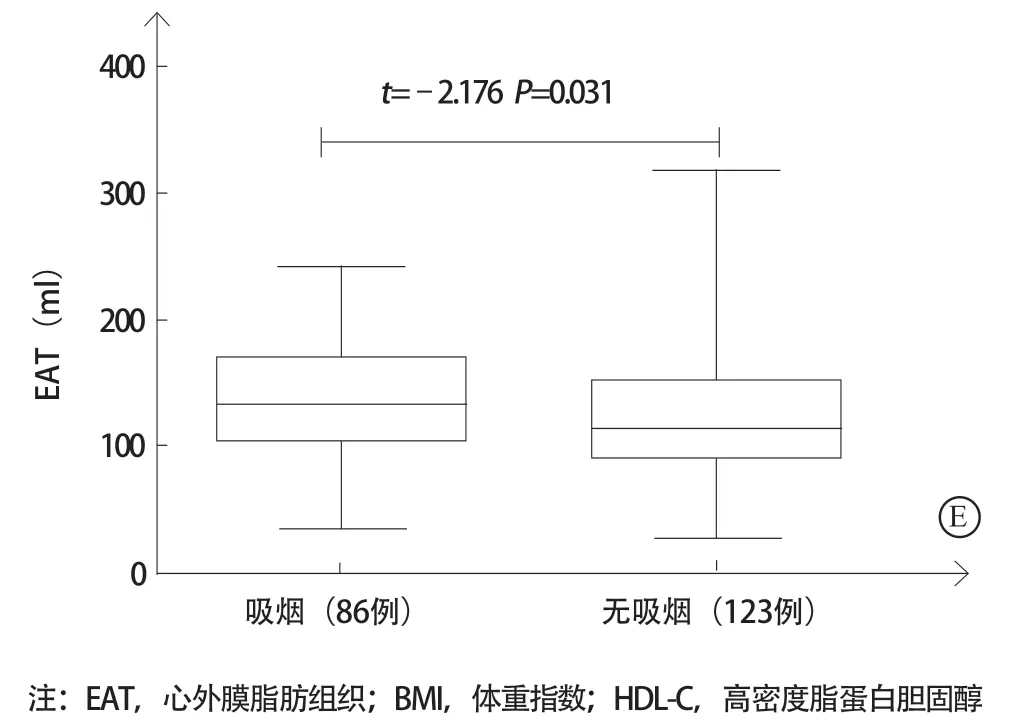
图1 EAT与其他临床参数的相关分析 A.总胆固醇与EAT正相关;B.BMI与EAT正相关;C.HDL-C与EAT负相关;D.高血压病患者较无高血压病患者EAT体积大;E.吸烟患者较无吸烟患者EAT体积大
本研究中,大EAT体积(>130 ml)较小EAT体积(≤130 ml)的阻塞性冠心病患者,首次PCI术相关总并发症的发生风险显著升高(OR 4.628,P=0.010)。近期的研究报道了EAT与PCI术后某些并发症的关系。Park等[4]发现,因支架内再狭窄致再次血运重建患者的EAT厚度明显高于无支架内再狭窄的患者EAT厚度[(3.8±1.8)mm 比(3.2±1.9)mm,P<0.01]。Zhou等[5]发现在PCI术后1年,发生支架内再狭窄组患者的基线EAT体积[(154.5±74.6)ml 比(131.0±52.2)ml,P<0.01]显著大于无支架内再狭窄组患者。Zencirci等[3]发现EAT厚度是PCI术后无复流的独立预测因素(OR 1.43,P=0.003)。这些研究均提示,大的EAT体积可能是PCI术后并发症的重要危险因素。推测支架置入引起冠动脉血管壁内膜的损伤,诱发血管内炎性反应;而过量的EAT释放大量炎性因子加重损伤冠状动脉血管内皮,可能增加了血栓形成、心肌梗死、冠状动脉夹层及穿孔等多种并发症的发生[15]。
既往多项研究提示,BMI可能是PCI术后并发症的重要影响因素[16-18]。Numasawa等[17]发现,低体重(BMI<18.5 kg/cm2)与正常体重(18.5 kg/cm2≤BMI<25.0 kg/cm2)或超重和肥胖(BMI≥25 kg/cm2)患者相比,PCI术后住院期间总并发症(P<0.001)、心原性休克(P=0.018)和重度出血风险(P<0.001)发生率均升高。Gruberg等[18]也发现,低体重(BMI<18.5 kg/cm2)和正常体重(18.5 kg/cm2≤BMI<24.9 kg/cm2)患者PCI术后住院期间的死亡、大出血、肺水肿等重大并发症发生风险较高。本研究中未发现BMI与PCI术后并发症的相关性,原因可能与本组人群中无低体重(BMI<18.5 kg/cm2)患者以及重大并发症发生率低有关。然而既往的这些研究均未纳入EAT进行分析,而在外科手术中发现,与BMI相比,内脏脂肪与术后并发症存在显著相关性[19]。因此BMI与PCI术后并发症发生的关系尚值得进一步探讨。
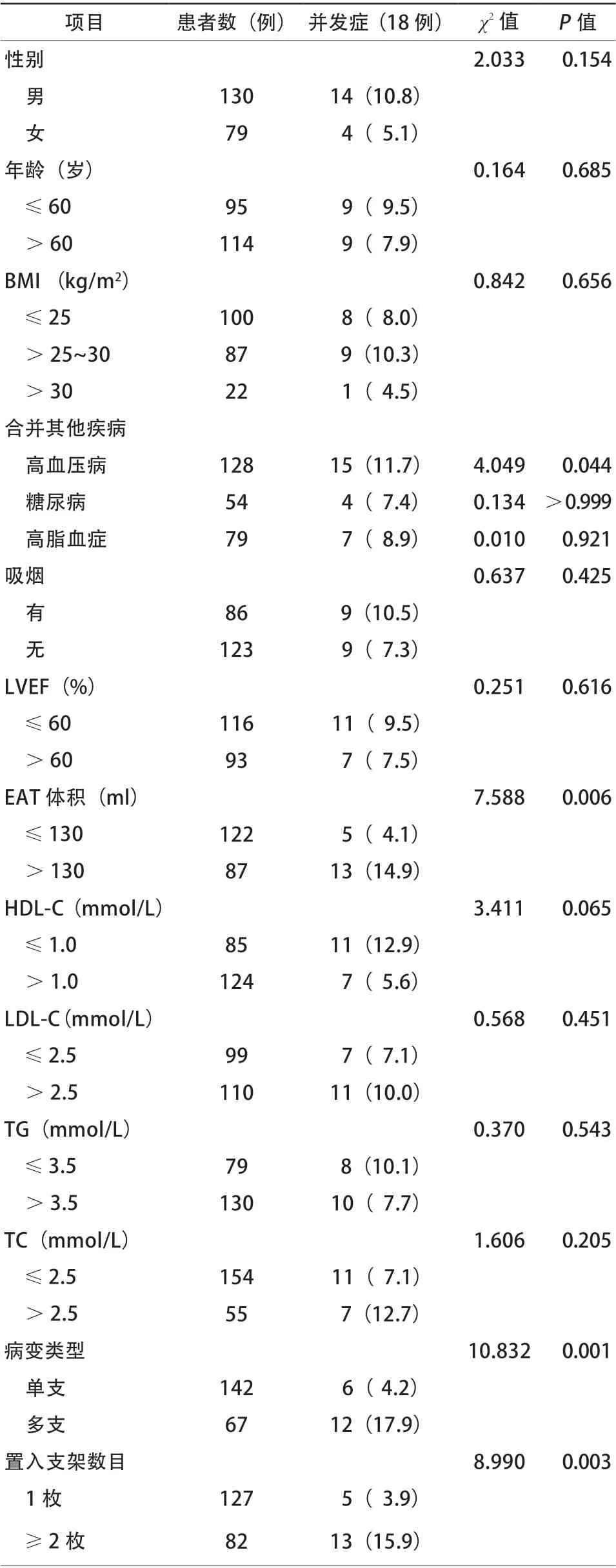
表2 209 例患者PCI 术后并发症相关危险因素的单因素分析[例(%)]

表3 209 例患者PCI 术后并发症相关危险因素的多因素分析
本研究中单因素和多因素分析均发现,多支病变患者行PCI术后短期并发症发生率也较高(均P<0.05)。多支病变患者支架置入数目也较多(P<0.001),客观上增加了术中操作引起相关并发症的风险。单因素分析显示高血压病也是PCI术后并发症发生的重要危险因素,这与既往的研究结论类似[18-20]。本研究中,由于EAT与高血压病显著相关,因此,多因素分析中未发现高血压病与PCI术后并发症的相关性。
本研究尚存在一些缺陷和不足。首先,虽然本研究的数据来源于既往的临床数据库,但为了减少其他因素对EAT评估的影响,本研究只纳入了择期首次PCI术的阻塞性冠心病患者,这部分患者临床症状相对不重,因此术后并发症的发生可能性也受到一定的影响,比如本组人群中重大并发症发生率低。其次,不同的研究对于术后并发症的定义尚存在一定差异[21]。虽然本中心同多数中心一样,主要参照ACC NCDR标准进行记录并发症,但是由于本中心较少发生ACC NCDR定义的出血(BARC定义的重度出血)并发症,所以本研究采取了BARC的标准定义出血并发症,因此,术后总并发症的评估可能受到影响,最后也可能影响了结论的判定。
PCI显著减少了冠心病患者的死亡率,改善了患者的生活质量。然而,PCI相关的一系列并发症可严重影响患者的预后。本研究发现,EAT体积大(>130 ml)是PCI术后短期并发症的独立危险因素,提示术前测定EAT,可能对PCI术后并发症具有一定的预测价值。
