QuEChERS超高效液相色谱-串联质谱法检测中药饮片中黄曲霉毒素
2020-06-17孙夏荣葛晓明王建花
孙夏荣,葛晓明,王建花
(江苏省南京市食品药品监督检验院,江苏 南京 211198)
黄曲霉毒素(aflatoxins)是由黄曲霉和寄生曲霉中某些产菌毒株产生的双呋喃环类毒素,是迄今发现的毒性最大的真菌毒素,常见有 B1,B2,G1,G24 种,其中以黄曲霉毒素B1的毒性最大、致癌性最强,其毒性相当于氰化钾的10倍、砒霜的68倍,已被世界卫生组织(WHO)的癌症研究机构(IARC)划定为Ⅰ类致癌物,是一种毒性极强的剧毒物质[1-4]。中药材及其制剂在储存过程中常会发生霉变,产生很多对人体有害的真菌毒素[5-6],2015年版《中国药典(一部)》已规定了部分中药材品种黄曲霉毒素B1的限量不得超过5 μg/kg、黄曲霉毒素B1,B2,G1,G2的总量不得超过 10 μg /kg[7]。
目前,文献报道的黄曲霉毒素检测方法主要有薄层色谱(TLC)法[8]、酶联免疫(ELISA)法[9]、高效液相色谱(HPLC)法[10-11]、液相色谱 - 串联质谱(LC-MS /MS)法[12-13]等。样品的前处理方面,现行《中国药典》执行的标准为免疫亲和柱净化法联用色谱技术,由于免疫亲和柱填料大多采用进口填料,单根免疫亲和柱售价约为100元,若长期使用则相关检测成本较高。LC-MS/MS法专属性好、灵敏度高、抗干扰强,能有效排除假阳性的干扰,适合在复杂基质下同时筛查痕量的多种黄曲霉毒素。
QuEChERS(quick,easy, cheap,effective, rugged,safe)是由美国农业部的化学家ANASTASSIADAS等于2003年提出的一种快速样品前处理技术[14-15],用于农药残留的检测。该方法具有分析快速、回收率高、精确度和准确度好、使用溶剂量少、污染少、操作简便等优点,近年来主要用于农产品和食品的各项检测中,但在药品的检测中应用较少。本研究中采用基于QuEChERS原理的样品前处理的快速提取方法,结合超高效液相色谱(UPLC)-MS/MS法,建立中药饮片中4种黄曲霉毒素(AFB1,AFB2,AFG1,AFG2)的检测方法,提供一种不使用免疫亲和柱的黄曲霉毒素的检测思路,为药品的监管提供有效的技术支撑。现报道如下。
1 仪器与试药
1.1 仪器
Agilent 6470型三重四极杆串联质谱联用仪,包括电喷雾离子化源(ESI)、MassHunter数据处理系统(美国安捷伦公司);CPA225D型电子天平(德国Sartorius公司,精度为十万分之一);涡旋混匀器(德国维根公司);X-30R型冷冻离心机(德国 Beckman公司);Milli-Q型超纯水系统(美国默克公司);N-EVAP 24型氮吹仪(美国 Organomation公司);KQ-250B型超声波清洗器(昆山市超声仪器有限公司,功率为250 W,频率为 30 kHz)。
1.2 试药
甲醇、乙腈(色谱纯,Honeywell公司);甲酸、乙酸铵(色谱纯,Aladdin公司);无水硫酸镁(分析纯,国药集团化学试剂有限公司);氯化钠(分析纯,南京化学试剂股份有限公司);水为超纯水;黄曲霉毒素混合对照品 ( 批 号 为 610001-201804), AFB1,AFB2,AFG1,AFG2含量分别为 0.93,0.30,0.93,0.35 μg /mL,均购自中国食品药品检定研究院;陈皮、大枣、柏子仁均为市售样品或抽样样品。
2 方法与结果
2.1 液相色谱及质谱条件
2.1.1 液相色谱条件
色谱柱:Agilent Eclipse XDB C18RRHD柱(50 mm×2.1 mm,1.8 μm);流动相:2 mmoL /L 乙酸铵溶液(含0.1%甲酸,流动相A)-乙腈(流动相B),按表1进行梯度洗脱;流速:0.3 mL /min;柱温:30 ℃;进样量:2 μL。

表1 流动相梯度洗脱程序
2.1.2 质谱条件
离子源模式(ESI):正离子模式;毛细管电压4 000;雾化器流速:9 L/min;干燥器温度:325℃;雾化器压力:40 psi(1 psi= 6.89 kPa);鞘气温度:350 ℃ ;鞘气流量:11 L/min;扫描模式:动态多反应离子监测(DMRM)。相关质谱采集参数见表2。
2.2 溶液制备
分别精密量取黄曲霉毒素混合对照品1 mL,置20 mL容量瓶中,用70%甲醇溶液稀至刻度,摇匀,作为标准贮备液。精密量取标准贮备液适量,用70%甲醇溶 液 稀 释 成 每 1 mL 含 AFB1,AFG10.093, 0.465,0.930, 1.860, 3.720, 9.300 ng, AFB20.030, 0.150,0.300, 0.600, 1.200, 3.00 ng, AFG20.035, 0.175,0.350,0.700,1.400,3.50 ng 的混合标准系列溶液。取供试品粉末 2 g(过3号筛),精密称定,置50 mL离心管中,加入 80%乙腈溶液(含 0.1%甲酸)20 mL,超声10 min,离心 5 min(离心速率 10 000 r/min),取上清液,再加入0.5 g氯化钠和2 g无水硫酸镁,充分涡旋振荡2 min,离心 5 min(离心速率 6 000 r/min),取上清液1 mL用50℃氮气吹干,快速加入2 mmoL/L乙酸铵溶液(含 0.1% 甲酸)-乙腈(65 ∶35,V/V)1 mL,过微孔滤膜(0.22 μm),取滤液,供 LC-MS /MS 分析。
2.3 方法学考察
线性关系考察:取6个不同质量浓度的混合标准系列溶液,分别进样,记录峰面积。以质量浓度(X,ng/mL)为横坐标、峰面积为纵坐标(Y)绘制标准曲线。结果见表3。
精密度试验:取同一质量浓度的混合标准系列溶液(AFB1, AFG10.930 ng /mL; AFB20.300 ng /mL; AFG20.350 ng /mL),进样 6 次。测定结果见表 3,各组分峰面积的 RSD均在 1.80% ~3.52%(n=6),表明仪器精密度良好。
重复性试验:精密称取空白样品2 g(过3号筛),共6份,加入标准贮备液0.1 mL,按供试品溶液制备方法制备,按拟订条件进样测定。结果见表3,上述各组分峰面积的 RSD<4.00%(n=6),表明方法重复性良好。
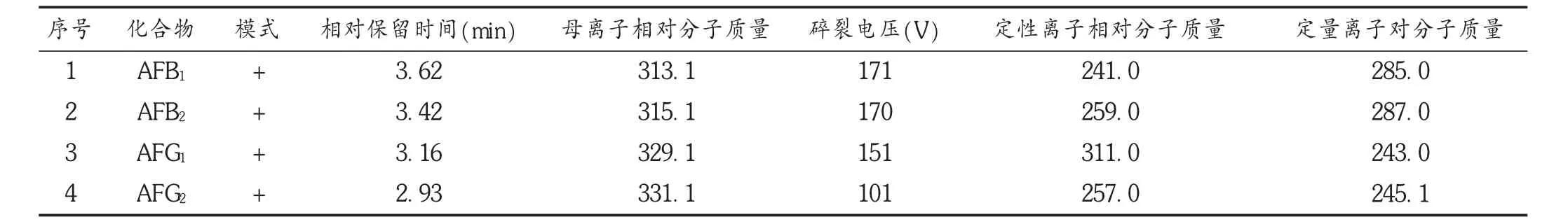
表2 黄曲霉毒素的质谱离子参数
稳定性试验:取重复性试验项下供试品溶液1份,置室温,分别于 0,4,8,12,24 h 时依法进样测定。结果见表 3,各组分峰面积的 RSD <5.00%(n=5),表明供试品溶液在24 h内稳定性良好。
检测限与定量限确定:将混合标准系列溶液加入空白样品溶液中,依法制备供试品溶液并进样测定。以信噪比(S/N)为 3∶1确定各组分的检测限(LOD),当 S/N为10∶1确定各组分的定量限(LOQ)。结果见表3。
准确度试验:取空白样品2 g,精密称定,共18份,每6份按低、中、高3种质量浓度水平分别精密加入标准贮备液 0.05,0.10,0.50 mL,依法制备供试品溶液并进样测定,计算回收率。结果见表3。
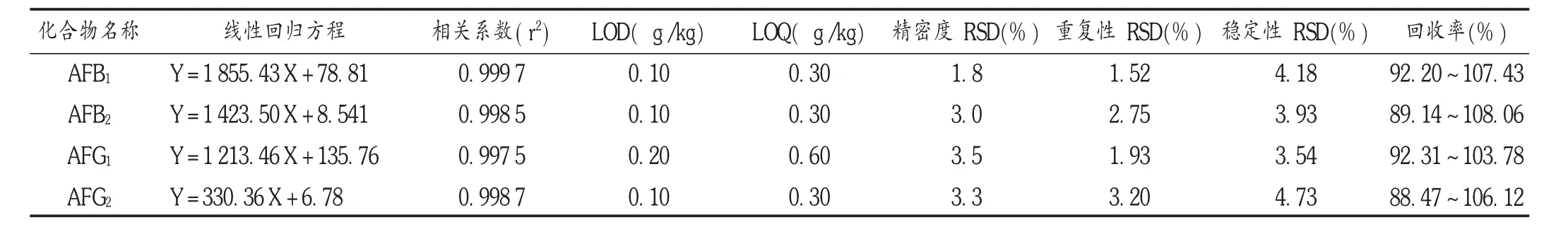
表3 黄曲霉毒素方法学考察结果(n=6)
2.4 样品含量测定
对10批市售样品进行测定,结果在2批样品中检出AFB1,其余均未检出。详见图1和图2。
3 讨论
3.1 色谱条件优化
曾考察不同比例的甲醇-水系统、乙腈-水系统、乙酸铵-乙腈系统等多个流动相体系进行梯度洗脱。结果显示,在2 mmoL/L乙酸铵溶液的流动相体系下,各化合物的响应值最高、峰形较好,且加入一定量的甲酸可进一步提高各化合物的离子化效率,故选取2 mmoL/L乙酸铵溶液(含0.1%甲酸)-乙腈系统为流动相。
3.2 质谱条件优化
本试验中对影响离子化效率的干燥器温度、鞘气温度、鞘气流量、雾化器压力、毛细管电压、碰撞能量等条件均进行了优化,最终选择电喷雾正离子扫描模式,得各化合物最佳的质谱条件。

图1 黄曲霉毒素定性和定量离子对的DMRM图
3.3 样品前处理优化
提取溶剂选择:曾考察不同提取溶剂对4种黄曲霉毒素的提取效率,比较了甲醇、乙腈、不同比例的酸化甲醇水溶液(含0.1%甲酸)、不同比例的酸化乙腈水溶液(含0.1%甲酸),结果发现,不同类型的提取溶剂对黄曲霉毒素的提取效率存在差异。当提取溶剂为80%乙腈溶液(含0.1%甲酸)时,提取效率最高,各化合物回收率均超过85%,且选择高有机相比例的提取溶剂,可明显缩短氮吹时间,节约试验时间。因此,确定80%乙腈溶液(含0.1%甲酸)为提取溶剂。
提取方式选择:曾考察超声波提取、涡旋振荡提取2种方式对提取效率的影响,结果无显著性差异。从试验操作的方便性考虑,宜采用超声波提取。此外,进一步比较了不同超声时间(2,5,10,20,30 min)对提取结果的影响。结果显示,样品超声处理10 min和20 min与30 min相比,回收率无显著差异,故选择超声处理10 min。
盐析剂和复溶溶剂选择:QuEChERS方法中盐析剂对黄曲霉毒素的回收率也有一定影响。经比较发现,0.5 g氯化钠和2 g无水硫酸镁能促进提取液分层,回收效率最高。曾考察样品在氮吹蒸干后不同的复溶溶剂对试验的影响,比较甲醇、乙腈、2 mmoL/L乙酸铵溶液(含 0.1% 甲酸)-乙腈(65 ∶35,V/V)的复溶溶液,结果直接采用甲醇或乙腈作为复溶溶液,会出现溶剂效应。故最终选择2 mmoL/L乙酸铵溶液(含0.1%甲酸)-乙腈(65∶35,V/V)作为复溶溶液,也作为流动相的初始比例溶液。

图2 典型阳性供试品定性和定量离子对的DMRM图
3.4 方法评价
本研究中建立了基于QuEChERS原理的样品前处理方法,结合UPLC-MS/MS技术,建立中药饮片中4种黄曲霉毒素(AFB1,AFB2,AFG1,AFG2)的检测方法。该方法快速简便、操作性强、灵敏度高,为中药饮片中快速检测4种黄曲霉毒素提供了新的研究思路和参考。
