皮克林乳液聚合法制备辣根过氧化物酶印迹材料
2020-06-16马珍珍
马珍珍,赵 涛
(齐鲁工业大学(山东省科学院)食品科学与工程学院,山东济南 250353)
糖蛋白是由寡糖和多肽链共价修饰连接而形成的一类重要生理活性物质。糖蛋白对于增殖的调控、受精、发生、分化以及免疫等生命现象,起着十分重要的作用[1-4]。糖蛋白还是一种重要的诊断标记物,病变的细胞表面的糖蛋白脱落进入体液或血液循环,糖蛋白的异常表现作为疾病诊断重要依据[5-6]。针对糖蛋白的分离材料以及快速检测手段受到了研究者的广泛关注,然而糖蛋白的分离分析研究中存在丰度低以及基质干扰严重等问题[7-8]。在近些年的研究中,苯硼酸作为一种糖类亲和试剂受到了广泛的关注,特别是在大分子糖类物质的分离、分析以及保护方面[9-13]。
苯硼酸的糖类亲和性主要依靠硼酸配体与顺二羟基结构之间形成的可逆共价键,图1展示了苯硼酸与含有顺二羟基结构物质识别的过程。当体系中的pH超过苯硼酸配体的pKa值时,硼酸基团与体系中的羟基络合,形成sp3杂化轨道,呈现四面体结构,这种结构能够特异性的识别糖类的顺二羟基结构,并通过脱水形成五元或者六元环酯。当体系中的pH降低时,硼酸酯之间的共价键通过水解断裂,苯硼酸基团恢复至sp2的平面结构。可逆共价键之间的转换特性赋予了苯硼酸良好的糖类亲和特性以及pH响应特性,可应用于糖类物质的快速分离和检测[14-16]。
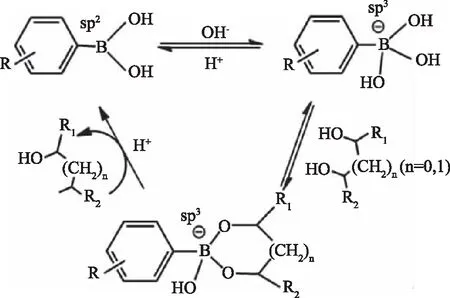
图1 苯硼酸与顺二羟基结构之间的关系Fig.1 Relationship between phenylboronic acidand cis-dihydroxy structure
皮克林乳液是利用固体颗粒代替表面活性剂来稳定两相形成的乳液[17-18]。皮克林乳液聚合法制备分子印迹材料能够避免表面活性剂对于材料结构以及性能的影响,同时提高材料在生物大分子以及活体检测上的应用[19]。皮克林乳液聚合法作为一种制备分子印迹材料的新手段受到了研究者的广泛关注[20-22],特别是在制备蛋白印迹材料方面[23-25]。现阶段大部分研究都是以二氧化硅作为稳定剂来制备分子印迹材料,例如:Zhou等[26]利用二氧化硅为皮克林乳液稳定剂,在水包油体系中通过皮克林乳液聚合的方式制备了人体血红蛋白印迹材料。以二氧化硅为皮克林乳液稳定颗粒制备分子印迹材料存在一个问题,即在合成分子印迹材料的最后阶段需要用氢氟酸去除二氧化硅颗粒,氢氟酸会破坏合成的分子印迹材料的印迹孔穴。
常规的糖蛋白分子印迹材料在水相中制备,苯硼酸功能单体在水相中溶解性差,制备的分子印迹材料为块状结构,印迹位点分布不均匀,材料形貌差。本研究以聚(二乙烯基苯-co-对乙烯基苯硼酸)微球作为糖蛋白识别单元,通过两相界面上的聚合反应,制备高特异性的糖蛋白印迹材料,可以解决苯硼酸功能单体溶解性差,糖蛋白印迹材料识别位点分布不均的问题,利用糖蛋白(辣根过氧化物酶、鸡卵蛋白、转铁蛋白、伴清蛋白)以及非糖蛋白(牛血清蛋白、细胞色素C)对合成的辣根过氧化物酶印迹材料的选择吸附能力、吸附动力学性能以及可重复性能进行了评价。
1 材料与方法
1.1 材料与仪器
二乙烯基苯混合物(DVB) 纯度80%,国药集团;偶氮二异丁腈(AIBN)、4-乙烯基苯硼酸(4-Vinylphenylboronic acid,PBA)、碱性氧化铝(Alkaline alumina、N-异丙基丙烯酰胺(N-Isopropyl acrylamide,NIPAAm) 国药集团;辣根过氧化物酶(Horseradish peroxidase,HRP) 酶活度150 U/mg,美国Sigma-Aldrich公司;鸡卵白蛋白(Ovalbumin,OVA)、伴清蛋白(Conalbumin,CON) 纯度≥97%(HPLC),美国Sigma-Aldrich公司;转铁蛋白(Transferrin,TRF)、牛血清蛋白(Bovine albumin,BSA) 纯度≥98%,美国Sigma-Aldrich公司;细胞色素C(Cytochrome C,Cyt-C) 纯度≥95%,美国Sigma-Aldrich公司;所有使用有机溶剂 均为国产分析纯。
Cary 50-Bio型紫外分光光度计 澳大利亚Victoria公司;Nicolet 6700傅里叶变换红外光谱仪(Fourier Transform Infrared Spectrometer,FTIR) 美国Nicolet公司;SU1510型扫描电镜(SEM) 日本Hitachi公司;ZK-35BS型真空干燥箱 天津三水科学仪器有限公司;PHSJ-3F型pH计 上海雷磁仪器有限公司。
1.2 实验方法
1.2.1 实验药品的处理 采用重结晶法处理引发剂偶氮二异丁腈(2,2-Azobisisobutyronitrile,AIBN)。处理过程如下:将200 mL乙醇加入到500 mL锥形瓶中,80 ℃水浴加热15 min。将20 g偶氮二异丁腈加入到上述溶液中,超声使其完全溶解,趁热立即抽滤,待滤液冷却后,收集析出的白色晶体。将重结晶后的偶氮二异丁腈低温保存在棕色瓶中备用。
二乙烯基苯(Divinylbenzene,DVB,80%)混合物中阻聚剂的去除,其过程如下:取200 mg的碱性氧化铝装填至固相萃取小柱中,取3 mL的二乙烯基苯混合物过柱,将纯化后的二乙烯基苯低温避光储存。
N-异丙基丙烯酰胺(N-Isopropyl acrylamide,NIPAAm)纯化过程如下:正己烷中重结晶3次,室温真空干燥,得白色针状晶体,低温避光储存。
1.2.2 溶剂热法制备聚(二乙烯基苯-co-对乙烯基苯硼酸)微球 将4-乙烯基苯硼酸(1.48 g,10 mmol)和二乙烯基苯(1.30 g,10 mmol)加入到80 mL乙腈中,超声充分溶解后,将上述溶液加入到100 mL反应釜中。加入引发剂AIBN(60 mg,0.37 mmol),超声溶解,充氮气15 min后,置于110 ℃烘箱中反应8 h。将产物通过砂芯漏斗(G5)抽滤,去除反应溶剂,然后用甲醇洗涤三遍,去除未反应的试剂,最后真空干燥。
1.2.3 皮克林乳液聚合法制备辣根过氧化物酶印迹材料 辣根过氧化物酶印迹材料制备:首先将200 mg聚(二乙烯基苯-co-对乙烯基苯硼酸)微球加入到装有15 mL甲苯的螺口试剂瓶中,超声(功率:360 W,频率:40 kHz,)30 min。然后在水相(5 mL)中加入10 mg辣根过氧化物酶,150 mg 丙烯酰胺以及50 mg异丙基丙烯酰胺作为功能单体,10 mg N,N′-亚甲基双丙烯酰胺作为交联剂,孵育20 min。将甲苯与水相混合,大力摇晃3 min,直至形成稳定的皮克林乳液,加入引发剂10 mg过硫酸铵,以及催化剂四甲基乙二胺(20 μL),30 ℃水浴反应24 h。聚合反应结束后,通过倾析去除上层透明油相,然后将乳液倒入G5砂芯漏斗中,用十二烷基硫酸钠(10%,v/v)和乙酸(10%,v/v)洗涤,去除模板分子,直至紫外检测无模板信号,真空干燥得到最终的辣根过氧化物酶印迹聚合物。
非印迹材料的合成方法除不加入模板辣根过氧化物酶外,与上述印迹材料合成方法一致。
1.2.4 材料的表征
1.2.4.1 红外光谱表征 准确称取三份干燥的溴化钾晶体150 mg,分别放入三个研钵中。分别加入2 mg已干燥的聚合物微球。研磨混匀,压片,用傅里叶变换红外光谱仪进行分析测试。
1.2.4.2 扫描电镜 使用扫描电子显微镜对合成的材料进行观察。
1.2.5 辣根过氧化物酶印迹材料的选择性吸附试验 以辣根过氧化物酶(HRP)、鸡卵白蛋白(OVA)、伴清蛋白(CON)和转铁蛋白(TRF)作为糖蛋白对照组,牛血清蛋白(BSA)和细胞色素C(Cyt-C)作为非糖蛋白对照组,进行选择性试验。选择性试验过程如下:称取辣根过氧化物酶印迹材料以及非印迹材料各10 mg分别加入到不同试管中,配制浓度为1 mg/mL的不同类型蛋白的Tris-HCl缓冲液(0.1 mol/L,pH9.0)。取1 mL 样品标准液加入到试管中。放置在摇床上,4 ℃下振荡一段时间后,离心取上清液(4000 r·min-1,15 min)。在波长为403 nm条件下,利用紫外分光光度计进行检测。吸附容量用以下式(1)进行计算:
Q=(Ci-Cf)V/m
式(1)
其中,Ci和Cf分别代表溶液中模板分子吸附前和吸附后的浓度,mg/mL;V为样品溶液的体积,mL;m为合成材料的质量,g。
1.2.6 辣根过氧化物酶印迹材料的等温吸附曲线 配制0.1~1 mg/mL的辣根过氧化物酶标液,称取辣根过氧化物酶印迹材料以及非印迹材料各10 mg分别加入到不同试管中,然后分别加入不同浓度的辣根过氧化物酶标液,置于摇床上,4 ℃下振荡一段时间,离心取上清液。在波长为403 nm条件下,利用紫外分光光度计进行检测。吸附容量用式(1)进行计算,所得的数据利用Origin软件进行拟合。
1.2.7 辣根过氧化物酶印迹材料的吸附动力学试验 将10 mg辣根过氧化物酶印迹材料分散于装有5 mL辣根过氧化物酶Tris-HCl缓冲液(1 mg/mL)的离心管中。将其放置于摇床上,在低温下振荡,取振荡不同时间后的样品,4000 r/min离心15 min进行分离。取分离后的上清液,利用紫外分光光度计进行检测。吸附容量用式(1)进行计算。
1.2.8 辣根过氧化物酶的重复性能评价 为了评价合成的辣根过氧化物酶的重复使用的性能,对合成的材料进行了重复性试验:称取合成的辣根过氧化物酶印迹材料(10 mg),加入1 mL 的1 mg/mL的辣根过氧化物酶的Tris-HCl缓冲液(0.1 mol/L,pH9.0)。放置在摇床上,4 ℃下振荡40 min,离心取上清液,测定吸附容量。回收吸附后的辣根过氧化物酶印迹材料,利用SDS(10%,v/v)和乙酸(10%,v/v)混合液洗涤,去除模板分子,直至紫外检测无模板信号。将洗脱后的材料再次浸入到1 mL的1 mg/mL的辣根过氧化物酶的Tris-HCl缓冲液中,重复上述吸附分离整个过程,重复五次,计算每循环吸附一次后的吸附量。
1.3 数据处理
采用Excel、Origin 8.0和GraphPad Prism 7软件进行数据处理。使用Adobe illustrator和Power point软件绘图。
2 结果与讨论
2.1 材料表征
图2A结果表明,合成的聚合物微球形貌规整,其粒径在1 μm左右,达到了亚微米级别。如图2B所示,3446、1342 cm-1处的峰为硼酸基团的-OH的伸缩振动峰,3018 cm-1处的峰为苯环上的C-H键,1608 cm-1为苯环的C=C键振动,2237 cm-1处为B-O键,1803和1922 cm-1处分别为直链烯烃中的R-CH=CH中C-H和C-C振动,1608 cm-1处为共轭型的C-C振动。红外结果表明成功合成了聚(二乙烯基苯-co-对乙烯基苯硼酸)。
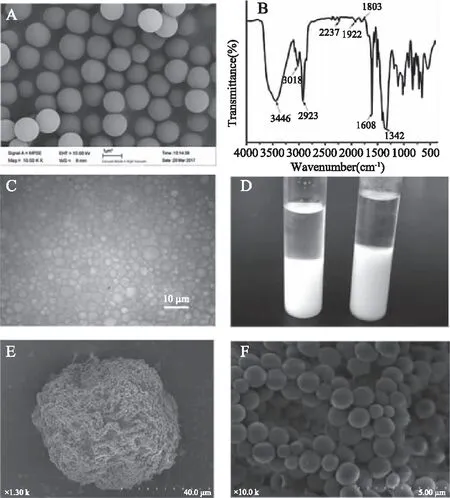
图2 材料的表征Fig.2 Characterization of materials注:聚(二乙烯基苯-co-对乙烯基苯硼酸)微球的扫描电镜图(A)和傅里叶红外图谱(B);皮克林乳液的光学显微图(C)和照片(D);辣根过氧化物酶印迹材料整体扫描电镜图(E)和表面扫描电镜图(F)。
图2C结果表明合成的聚(二乙烯基苯-co-对乙烯基苯硼酸)能够在甲苯和水的两相体系中形成稳定的皮克林乳液。
在油包水体系中,水相以颗粒的形态分散到油相中形成乳液。利用小颗粒来代替表面活性剂作为油水两相的稳定剂是皮克林乳液最主要的特征。要形成稳定的皮克林乳液体系,需要稳定剂既具备一定亲水特性又具备一定的亲油特性。聚(二乙烯基苯-co-对乙烯基苯硼酸)微球的亲油性是因为其聚合单体二乙烯基苯,其亲水性来自其聚合单体4-乙烯基苯硼酸的羟基基团。而常规聚(二乙烯苯-co-苯乙烯)微球由于其太过于亲油,所以难以形成稳定的皮克林乳液。图2D为辣根过氧化物酶印迹材料以及非印迹材料形成皮克林乳液的照片,试验结果表明合成形貌规整的小球包大球的结构需要油相甲苯的量远大于水相的量。原因可能是过量的甲苯使皮克林乳液中水相液滴能够有效的分离,避免了成核过程中聚合反应导致的球体之间粘连。同时,辣根过氧化物酶自身具备良好的乳化效果,在制备辣根过氧化物酶印迹材料时,要控制辣根过氧化物的添加量以及乳化时间。
图2E为辣根过氧化物酶印迹材料的扫描电镜图,疏水性粒子聚(二乙烯基苯-co-对乙烯基苯硼酸)颗粒附着在印迹材料的表面(图2F),而内核为亲水性水凝胶。这种结构赋予了合成材料的两性亲和性。其疏水性的外壳能够有效的抵御外界环境影响,从而阻止内核水凝胶因吸水溶胀而破裂。同时,内部的水凝胶改善了苯硼酸类印迹材料的亲水性,提高了材料在水相中的适用性。
2.2 辣根过氧化物酶印迹材料的选择性试验
由图3可知,印迹材料对于辣根过氧化物酶的吸附量要明显高于其他类型蛋白,该结果表明通过皮克林乳液聚合方式制备的辣根过氧化物酶印迹材料对于模板辣根过氧化物酶表现出良好的选择性。该蛋白印迹材料对辣根过氧化物酶的吸附量是非印迹材料吸附量的5.00倍。同时,聚(二乙烯基苯-co-对乙烯基苯硼酸)作为皮克林乳液稳定剂与印迹材料复合,提高了印迹材料对于糖蛋白的选择性,合成的印迹材料对于糖蛋白(辣根过氧化物酶)的吸附量是对于非糖蛋白(BSA)的吸附量的42.77倍(表1)。
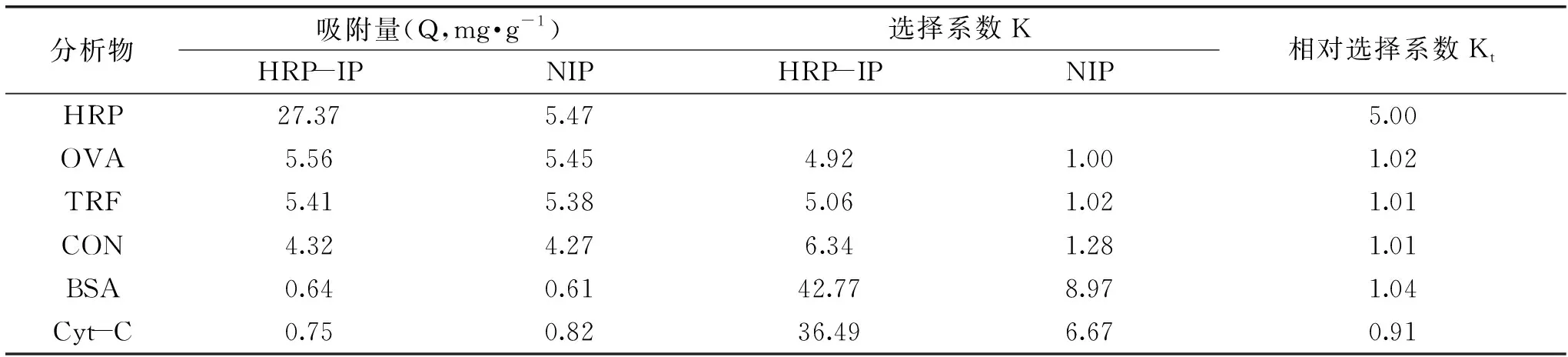
表1 材料对于糖蛋白和非糖蛋白的选择性能Table 1 Selective properties of materials for glycoproteins and non-glycoproteins
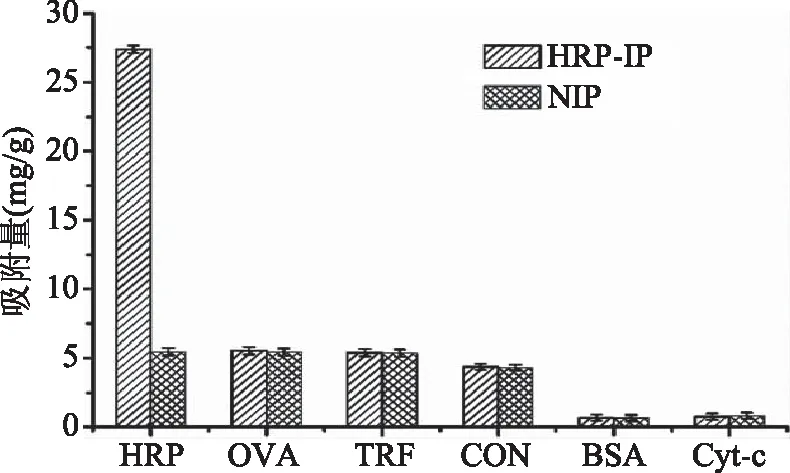
图3 对于糖蛋白和非糖蛋白的吸附能力Fig.3 Adsorption capacity of theglycoproteins and non-glycoprotein
2.3 辣根过氧化物酶印迹材料的等温吸附曲线
等温吸附平衡曲线是指维持温度不变,当达到吸附平衡时,吸附质在固-液两相中浓度的关系曲线,即吸附剂表面的吸附量(qe)与溶液中吸附质平衡浓度(Ce)之间的关系曲线。常用的吸附等温线模型有Langmuir等温线模型[27]、Freundlich等温线模型[28]。Langmuir等温吸附模型是通过大量实验数据归纳而来的经验模型,是实际运用中使用最广泛的吸附等温线方程,其理论模型的提出基于以下假设:吸附剂表面是均匀的,即吸附位点是无差别的、完全相同的;所有吸附粒子具有相同的吸附热和吸附能;吸附质分子之间,吸附质分子与表面活性位点之间不存在相互作用力;吸附为单分子层吸附。其表达式和线性形式分别为:
qe=Ktq0Ce/(1+KtCe)
式(2)
式中,Ce为吸附质平衡浓度,(mg·L-1);qe为吸附剂平衡吸附量,(mg·g-1);q0(mg·g-1)和 Kt(L·mg-1)分别是Langmuir等温模型的最大吸附量和吸附常数。
Freundlich吸附等温模型是多分子吸附,也是一种经验模型。该理论模型的假设为:吸附剂表面不均匀,吸附剂和吸附质之间、吸附质分子之间存在多种相互作用关系。其表达式和线性形式如下所示:
式(3)
式中,q0(mg g-1)为Freundlich等温模型的最大吸附量,KF(mg/g(L/mg)1/n)为Freundlich等温模型的吸附常数,n为Freundlich等温模型的线性指数。
表2的结果表明材料的等温吸附模型更符合Langmuir等温吸附模型,经拟合后得到印迹材料的最大吸附量为38.67 mg/g,非印迹材料的最大吸附量为7.15 mg/g。
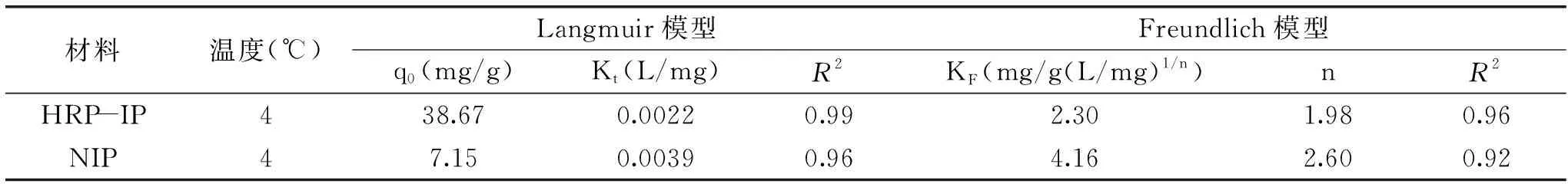
表2 印迹材料和非印迹材料对于辣根过氧化物酶的等温吸附模型拟合参数(Langmuir,Freundlich)Table 2 Parameters of Langmuir and Freundlich model of MIP and NIP
2.4 辣根过氧化物酶印迹材料的吸附动力学
为了评价合成的材料对模板辣根过氧化物酶的吸附速率,进行了吸附动力学实验,测定不同吸附时间下(t)材料对辣根过氧化物酶的吸附量,图4结果表明,印迹聚合物对模板具有较快的吸附速率,在25 min内就可以达到最大吸附量的50%,吸附50 min后基本达到平衡。其原因是合成的材料内部为水凝胶,提高了合成材料的亲水性以及物质传输速度。
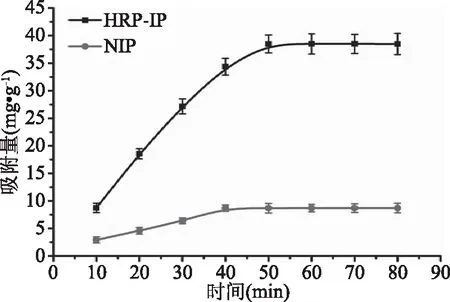
图4 辣根过氧化物酶印迹和非印迹材料的吸附动力学曲线Fig.4 Adsorption kinetic curve of HRPon the HRP-IP and NIP
为了进一步评价辣根过氧化物酶印迹和非印迹材料的传质速率和控制过程,采用准一级吸附动力学方程(pseudo-first-order)和准二级吸附动力学方程(pseudo-second-order)对辣根过氧化物酶印迹材料的动力学数据进行了分析,方程模型用式(4)和式(5)表示。准一级吸附动力学模型的限速步骤是扩散步骤。准二级吸附动力学模型的吸附速率由吸附剂表面未被占有的吸附空位孔穴数的平方值决定,吸附过程受化学吸附机理的控制,这种化学吸附涉及到吸附剂与吸附质之间的电子共用或电子转移。
准一级吸附动力学方程:
Qt=Qe(1-e-K1t)
式(4)
式中,K1(min-1)为准一级吸附速率常数,Qe(mg/g)和Qt(mg/g)分别是平衡时的吸附量和t时间时的吸附量,t为吸附时间(min)。
准二级吸附动力学方程:
式(5)
式中,K2(g/(mg·min))为准二级吸附动力学常数,Qe(mg/g)、Qt(mg/g)、t与准一级吸附动力学一样。由t/Qt与t的线性关系计算出速率常数K2、Qe和相关系数R2。
拟合结果参数如表3所示,准二级吸附动力学方程的R2值(0.9844)高于准一级吸附动力学方程的R2值(0.9346),准二级吸附动力学得到的理论值Qe(cal)(40.24 mg/g)与实际值Qe(exp)(38.31 mg/g)相近。因此,可以用准二级吸附动力学来描述辣根过氧化物酶印迹材的吸附过程,由于准二级吸附动力学的主要限速步骤是化学吸附,因此限制辣根过氧化物酶印迹材料吸附速率步骤的也是化学吸附。

表3 准一、二级吸附动力学方程拟合结果Table 3 Adsorption rate coefficient for two kinetic models
2.5 重复性试验
图5的结果表明合成的辣根过氧化物酶印迹材料具备良好的重复性,经过6次循环后,材料对于模板辣根过氧化物酶的吸附量仅降低了2.5%,说明合成的辣根过氧化物酶印迹材料稳定性能好,能够重复使用。其原因可能是材料表面的聚(二乙烯基苯-co-对乙烯基苯硼酸)颗粒能够有效的阻止外界环境对印迹材料的破坏。
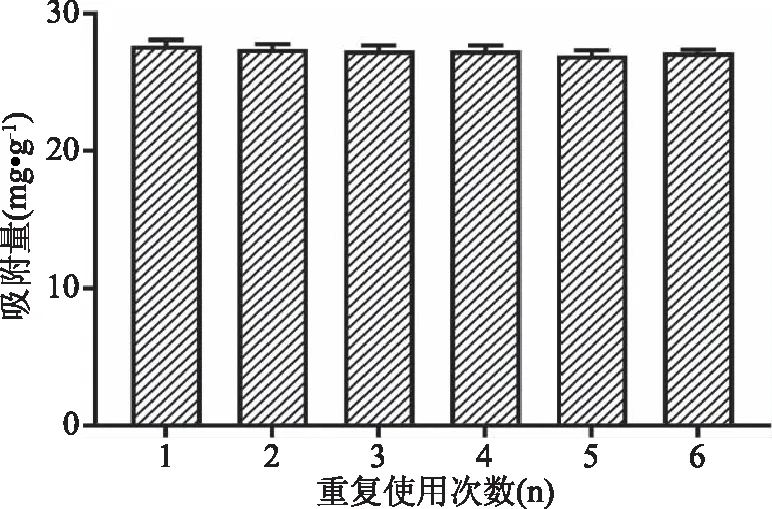
图5 辣根过氧化物酶印迹材料的重复性试验Fig.5 Repeatability test of HRP-IP materials
3 结论
以聚(二乙烯基苯-co-对乙烯基苯硼酸)颗粒作为皮克林乳液稳定剂,在甲苯包水体系中通过皮克林乳液聚合的方式制备了一种核壳结构的辣根过氧化物酶印迹材料。其表面的聚(二乙烯基苯-co-对乙烯基苯硼酸)颗粒能够有效的提高印迹材料对于糖蛋白的选择性,合成的印迹材料对于糖蛋白(辣根过氧化物酶)的吸附量是对于非糖蛋白(BSA)的吸附量的42.77倍;其亲水性的水凝胶内核能够提高合成的印迹材料的传输速度以及水溶性,吸附50 min后基本达到吸附平衡,对于模板辣根过氧化物酶的最大吸附量为38.67 mg/g;且合成的印迹材料具有良好的稳定性,6次循环后对模板辣根过氧化物酶的吸附量仅降低了2.5%。
