大鲵活性肽与低分子量透明质酸组合物抗氧化活性研究
2020-06-13关百婷佟长青
关百婷,佟长青,李 伟
(大连海洋大学食品科学与工程学院,辽宁大连 116023)
0 引言
透明质酸,又称玻尿酸,是一种分布于皮肤表皮与真皮中的酸性黏多糖,由N-乙酰氨基葡萄糖(GlcNAc)与葡萄糖醛酸(GlcA)二糖单位重复聚合形成[1]。低分子量透明质酸平均分子量为1×106Da。柯春林等人[2]的研究表明,低分子量的透明质酸具有小鼠巨噬细胞和T 细胞的免疫调节作用。透明质酸因其具有较好的保水作用,已经成为重要的皮肤友好型化妆品原料,被广泛添加于面膜、乳液、膏霜和化妆水中。同时,利用透明质酸的天然交联特性,研制出多种透明质酸组合物。柳志喆等人[3]通过胶原蛋白和玻尿酸的天然交联强化橡胶性质物性的生体材料物质,将胶原蛋白和玻尿酸混合,利用最佳混合比率和非化学性或物理性交联的天然交联条件,制作出具有橡胶特性的胶原蛋白和玻尿酸交联物。陈海佳等人[4]发明了一种间充质干细胞与透明质酸的组合物,该组合物具有快速起效和间充质干细胞作用时间长的优点。Scott J E 等人[5]利用电子显微镜和计算机模拟等方法进行研究,发现透明质酸具有三级网状结构。透明质酸的这些特性为其开发成活性物质的载体提供了巨大的潜力。
研究表明,大鲵肌肉中含有粗蛋白17.15%,水分84.04%,粗脂肪1.73%,灰分0.66%[6]。因此,大鲵肌肉具有较高的蛋白含量。大鲵肉的深度利用是通过酶解技术来实现。大鲵蛋白质经过蛋白酶水解获得的大鲵肽,往往具有多种生物活性,如增强免疫力、抗氧化、促进细胞增殖等[7-8]。为了探讨在化妆品领域应用大鲵活性肽进行了大鲵活性肽与透明质酸组合物的制备,并对其抗氧化活性进行了评价。
1 材料与方法
1.1 材料与仪器
大鲵活性肽,分子量1 400~2 000 Da,由辽宁省水产品加工及综合利用重点实验室制备;低分子量透明质酸(LMWHA-145 kDa),深圳润朗医药科技有限公司提供;2,2-二苯基-1-苦肼基自由基(2,2-diphenyl-1-picrylhydrazyl, DPPH·)(AR)、2,2'-联氮双(3-乙基苯并噻唑啉-6-磺酸)二铵盐 (2,2'-Azino-bis(3-ethylbenzthiazoline-6-sulphonic acid)diammonium salt,ABTS)(AR),美国Sigma 公司提供。
傅里叶变换红外光谱仪,珀金埃尔默仪器有限公司产品;电热鼓风干燥箱,上海一恒科学仪器有限公司产品;FW-5A 型手动压片机,天津博天胜达科技发展有限公司产品;UV-754 型紫外分光光度计,上海光谱仪器有限公司产品。
1.2 试验方法
1.2.1 大鲵活性肽与LMWHA 组合物的制备
将大鲵活性肽溶于pH 值为6 的浓度为0.01 mol/L PBS 中,制成质量分数10%的溶液。将LMWHA 溶于pH 值为6 的0.01 mol/L PBS 中,制成质量分数10%的溶液;按照1∶1 的体积,将上述2 种溶液混合,经过纳滤膜过滤,将滤液进行冷冻干燥,得到大鲵活性肽与透明质酸组合物。
1.2.2 红外光谱及显微镜观察
称取0.8 g 溴化钾、0.002 g 大鲵活性肽与透明质酸组合物、0.002 g 大鲵活性肽、0.002 g 透明质酸于干燥皿中,置于105 ℃烘箱中烘干至恒质量;称取0.2 g 溴化钾于玛瑙研钵中研磨至超细粉末进行压片,使其成为透明片,放于红外机器中扫描为背景片,然后称取0.2 g 溴化钾与0.002 g 样品,混合后放于玛瑙研钵中研磨至超细粉末,进行压片后放入Frontier FT-IR 光谱仪(Perkin-Elmer)中测定样品的FT-IR 光谱。
将大鲵活性肽与透明质酸组合物溶于ddH2O 中,配制成质量分数10%的溶液,置于光学显微镜下进行观察。
1.2.3 DPPH·清除率的测定
将样品配成质量浓度为5 mg/mL 的混合溶液。称取10 mg DPPH 溶于无水乙醇中,定容至250 mL,配制成DPPH 工作液。分别加入不同浓度的样品溶液3 mL,DPPH 工作液3 mL,混匀,置于避光环境中静置30 min,在波长517 nm 处测定吸光度。按如下公式计算DPPH·清除率:

式中:A0——未加入样品时DPPH 吸光度;
A1——未加入DPPH 时样品的吸光度;
A2——样品与DPPH 混合后的吸光度。
1.2.4 ABTS+·清除率测定
称取0.020 6 g ABTS+·溶于5 mL 蒸馏水中,称取0.003 5 g 过硫酸钾溶于5 mL 蒸馏水中混匀暗反应12 h 后,用蒸馏水稀释到波长734 nm 处吸光度为0.7±0.02,用蒸馏水调零。分别加入不同质量浓度的样品溶液1 mL,ABTS 工作液4 mL,振荡摇匀,室温静置6 min 后,在波长734 nm 处测吸光度。按如下公式计算ABTS+·清除率:
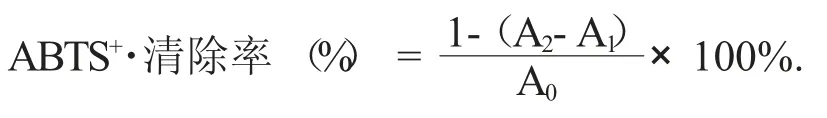
式中:A0——未加入样品时ABTS 吸光度;
A1——未加入ABTS+·时样品的吸光度;
A2——样品与ABTS+·混合后的吸光度。
2 结果与分析
2.1 大鲵活性肽与LMWHA 组合物的分析
将质量分数10%的大鲵活性肽的磷酸盐缓冲液溶液与质量分数10%的LMWHA 磷酸盐缓冲液溶液按照1∶1 的体积进行混合,冷冻干燥后得到大鲵活性肽与LMWHA 组合物。对其进行红外光谱分析,红外光谱的谱带数目、形状、位置及强度都随着被分析物质的结构改变而改变。
红外扫描图谱见图1。
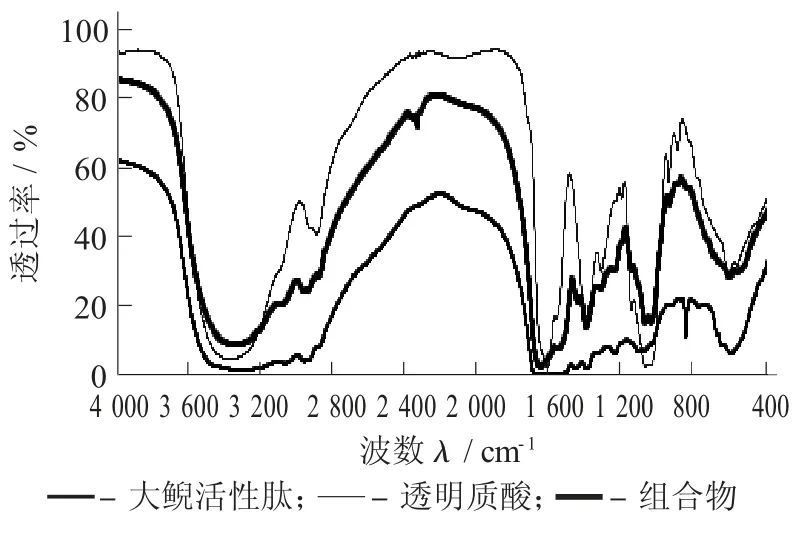
图1 红外扫描图谱
从图1 可以看出,大鲵活性肽与LMWHA 组合物与LMWHA、大鲵活性肽的红外光谱图具有较大的差别。大鲵活性肽的红外光谱在3 528~2 867 cm-1表现出较宽的吸收峰,同时具有1 657,1 457,1 415,1 329,1 256,1 096,1 020,851,605 cm-1的特征峰,1 415 cm-1吸收为CN 伸缩及部分NH 弯曲振动。LMWHA的红外光谱特征吸收为3 408,2 880,1 624,1 508,1 409,1 292,1 240,1 209,1 157,1 065,909,897,622 cm-1的特征峰,其中1 624,1 409,622 cm-1为酰胺特征振动峰,1 157,1 065,909 cm-1表明具有C-O-C 化学键,3 408 cm-1为羟基振动峰。大鲵活性肽与LMWHA 组合物的特征峰为3 385,3 060,2 942,1 675,1 533,1 457,1 409,1 317,1 248,605,589 cm-1,这些特征峰即不同于大鲵活性肽的红外光谱,也不同于LMWHA 的红外光谱。这表明 2 种物质形成组合物时其 O-H,N-H,C-O-C,C=O 都受到相互作用,说明该组合物是一种新的物质。
将10%的溶于ddH2O 中的大鲵活性肽与LMWHA组合物溶液,置于光学显微镜下进行观察。
大鲵活性肽与LMWHA 组合物显微照片(放大40 倍)见图2。

图2 大鲵活性肽与LMWHA 组合物显微照片(放大40 倍)
从图2 可以看出,大鲵活性肽与LMWHA 组合物表现出自然交联形成的结构。
2.2 抗氧化活性测定
DPPH·与ABTS+·是常规使用的基于电子转移原理进行抗氧化活性的方法[9]。利用DPPH·方法测定的大鲵活性肽与LMWHA 组合物抗氧化活性,并与大鲵活性肽、LMWHA。
样品质量浓度对DPPH·的清除率的影响见图3。

图3 样品质量浓度对DPPH·的清除率的影响
从图3 可以看出,在相同质量浓度下,大鲵活性肽与LMWHA 组合物的清除DPPH·的能力与大鲵活性肽清除DPPH·的能力相当。
利用ABTS+·方法测定的大鲵活性肽与LMWHA组合物抗氧化活性,并与大鲵活性肽、LMWHA。
样品质量浓度对ABTS+·的清除率的影响见图4。

图4 样品质量浓度对ABTS+·的清除率的影响
从图4 可以看出,在相同质量浓度下,大鲵活性肽与LMWHA 组合物的清除ABTS+·的能力显著高于大鲵活性肽清除ABTS+·的能力。
溶剂对于DPPH·与ABTS+·方法测定抗氧化活性具有较大的影响。2 种方法的主要差别在于DPPH·需要利用乙醇来进行溶解,而ABTS+·用水溶液来进行溶解。在水溶液的环境下,大鲵活性肽与LMWHA组合物的抗氧化能力显著提高。这也从另一个方面证明了大鲵活性肽利用LMWHA 的有三级网状结构,发挥了更好的抗氧化活性。
3 结论
在pH 值为6 的条件下,等量的大鲵活性肽与LMWHA 在溶液中形成了组合物。该组合物的红外光谱呈现出了其独特的吸收峰。显微镜观察到大鲵活性肽与LMWHA 组合物表现出自然交联形成的结构。在相同质量浓度下,大鲵活性肽与LMWHA 组合物清除DPPH·的能力与大鲵活性肽清除DPPH·的能力相当,大鲵活性肽与LMWHA 组合物的清除ABTS+·的能力显著高于大鲵活性肽清除ABTS+·的能力。因此,在大鲵活性肽与LMWHA 组合物中,大鲵活性肽利用了LMWHA 的有三级网状结构,发挥了更好的抗氧化活性。
