迈瑞CL-6000I化学发光免疫分析仪检测系统性能验证
2020-06-11谢菊红何沛郭炫
谢菊红 何沛 郭炫
[摘要] 目的 验证迈瑞CL-6000I化学发光分析仪检测系统的性能。方法 参照国家临床实验室标准化委员会(NCCLS)等相关文件对迈瑞CL-6000I化学发光免疫分析仪检测系统检测甲状腺激素:三碘甲状腺原氨酸(T3)、四碘甲状腺原氨酸(T4)、游离三碘甲状腺原氨酸(FT3)、游离四碘甲状腺原氨酸(FT4)、促甲状腺素(TSH)5个项目的精密度、准确度、线性范围、生物参考区间进行验证。结果 检测的5个项目批内精密度变异系数CV%在1.837%~4.07%,批间精密度变异系数CV%在2.634%~7.49%,准确度比对偏倚范围为6.289%~9.62%,线性范围斜率在0.981 2~1.013,r2在0.951 7~0.999 2,均满足相关文件的要求;参与生物参考区间验证的样本检测结果均在厂家标注的范围内。结论 迈瑞CL-6000I化学发光分析仪检测系统精密度、准确度、线性范围、生物参考区间验证通过。满足临床诊断与预后监测的需要。
[关键词] 化学发光;性能验证;甲状腺激素
[中图分类号] R446 [文献标识码] A [文章编号] 1672-5654(2020)03(a)-0001-03
[Abstract] Objective To verify the performance of Mindray CL-6000I chemiluminescence analyzer detection system. Methods According to the National Clinical Laboratory Standardization Committee(NCCLS) and other relevant documents, the Mindray CL-6000I chemiluminescence immunoassay detection system was used to detect thyroid hormones: triiodothyronine (T3), tetraiodothyronine (T4), Free triiodothyronine (FT3), free tetraiodothyronine (FT4), and thyroid stimulating hormone (TSH) were tested for precision, accuracy, linear range, and biological reference interval. Results The precision variation coefficient CV% of the five items tested was 1.837%-4.07%, the precision variation coefficient CV% between batches was 2.634%-7.49%, the accuracy comparison bias range was 6.289%-9.62%, and the linear range slope was 0.981 2-1.013, r2 of 0.951 7-0.999 2, all met the requirements of relevant documents; the test results of the samples participating in the biological reference interval verification were within the range marked by the manufacturer. Conclusion Mindray CL-6000I chemiluminescence analyzer detection system precision, accuracy, linear range and biological reference interval have been verified, which meets the needs of clinical diagnosis and prognosis monitoring.
[Key words] Chemiluminescence; Performance verification; Thyroid hormone
在臨床工作中,准确可靠的检测结果是疾病诊断治疗必不可少的依据,也是健康检查的一部分,是检验科工作的核心和基本要求。为了保证检验质量,临床实验室应在正式投入使用前对检验仪器及检验方法进行性能验证。各项指标在生产厂家所标注的范围或有关文件要求范围内即为验证合格,才能应用于临床工作[1-2]。该实验室对CL-6000I(中国)化学发光分析仪检测甲状腺激素:三碘甲状腺原氨酸(T3)、四碘甲状腺原氨酸(T4)、游离三碘甲状腺原氨酸(FT3)、游离四碘甲状腺原氨酸(FT4)、促甲状腺素(TSH)进行了性能验证。验证内容包括精密度、准确度、线性范围、生物参考区间[3],现报道如下。
1 材料与方法
1.1 实验样本
选取2018年5—7月西安交通大学第一附属医院长安区医院就诊和健康体检者不同浓度的新鲜血清样本。空腹静脉采血后,静置待其凝固后3 500 r/min,离心10 min。分离血清,密封-20℃冷冻备用[4]。要求血清外观清亮,无溶血无黄疸,无脂肪血等。依据NCCLSEP5-A2文件对仪器进行性能验证。
1.2 仪器与试剂
迈瑞CL-6000I化学发光免疫分析仪,试剂、校准品、质控品和耗材均为仪器配套产品。实验过程中所有试剂耗材未更换批号。试剂批号:T3 2018040121,T4 2018040121,FT3 2018040121,FT4 2018060111,TSH 2018040121;校准品批号:T3 2018030100,T4 2018060100, FT3 2018060100,FT4 2018050100,TSH 2018060100,迈瑞复合质控品低值批号2018060101,复合质控品高值批号2018020101,发光底物液,清洗液,反应杯均在有效期内。
1.3 验证方法
1.3.1 精密度验证 依据NCCLS EP5-A2文件对待验证仪器进行精密度验证,选取三碘甲状腺原氨酸(T3)、四碘甲状腺原氨酸(T4)、游离三碘甲状腺原氨酸(FT3)、游离四碘甲状腺原氨酸(FT4)、促甲状腺素(TSH)高、低浓度两个水平的患者血清样本在1 d内连续检测20次。计算其均值(x±s),变异系数(CV%),验证其批内精密度[5];利用高值、低值两个水平的室内质控品连续20 d的质控结果,统计其均值(x±s)和变异系数(CV%),验证其批间精密度[6-7]。检测的批内精密度CV%应该≤1/4CLIA88′TEa 允许的总误差(6.25),批间精密度CV%应该≤1/3 CLIA88′TEa(8.25),该检测系统精密度即为验证通过[5-6]。
1.3.2 准确度验证 T3、T4、FT3、FT4、TSH每个项目收集低于生物参考区间、生物参考区间内和高于生物参考区间的血清样本各7份,经待验证仪器迈瑞CL-6000I检测3次,计算平均值为A值。与已通过ISO15189认证的西安交通大学第二附属医院检验科检测结果进行比对[5-6,8-9],每个样本检测3次,计算其平均值B。计算公式:相对偏倚=[(A-B)/B]×100.00%,平均偏倚=21次相对偏倚绝对值的和的平均数。判断标准为平均偏倚≤1/2CLIA88′TEa(12.50)即为准确度验证通过[5-6,9]。
1.3.3 线性范围 参照EP6-A2文件选取T3、T4、TSH 低值高值血清各1份[4]。将高值H和低值L按照5H、4H+1L3H+2L、2H+3L、1H+4L、5L的比例配成6份同体积不同浓度的样本。以预期值Y为纵坐标,每份样本连续检测3次。计算其平均值X作为横坐标,将所有结果数据绘制于X-Y坐标图中,计算回归方程Y=aX+b,斜率 a在0.97~1.03,并且r2≥0.95,即可判断为验证通过[5,10]。
1.3.4 生物参考区间验证 参照行业标准[11]进行生物参考区间的小样本验证,收集男性和女性健康体检者各10名(年龄在18~60岁之间)血清样本及时检测,计算出比率R,R=检验结果在厂家提供的生物参考区间内的样本数/20,若R≥90%,即为验证通过。
1.4 统计方法
采用SPSS 21.0统计学软件进行数据处理。计量资料采用(x±s)表示,相关性检验采用线性分析和回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 精密度验证结果
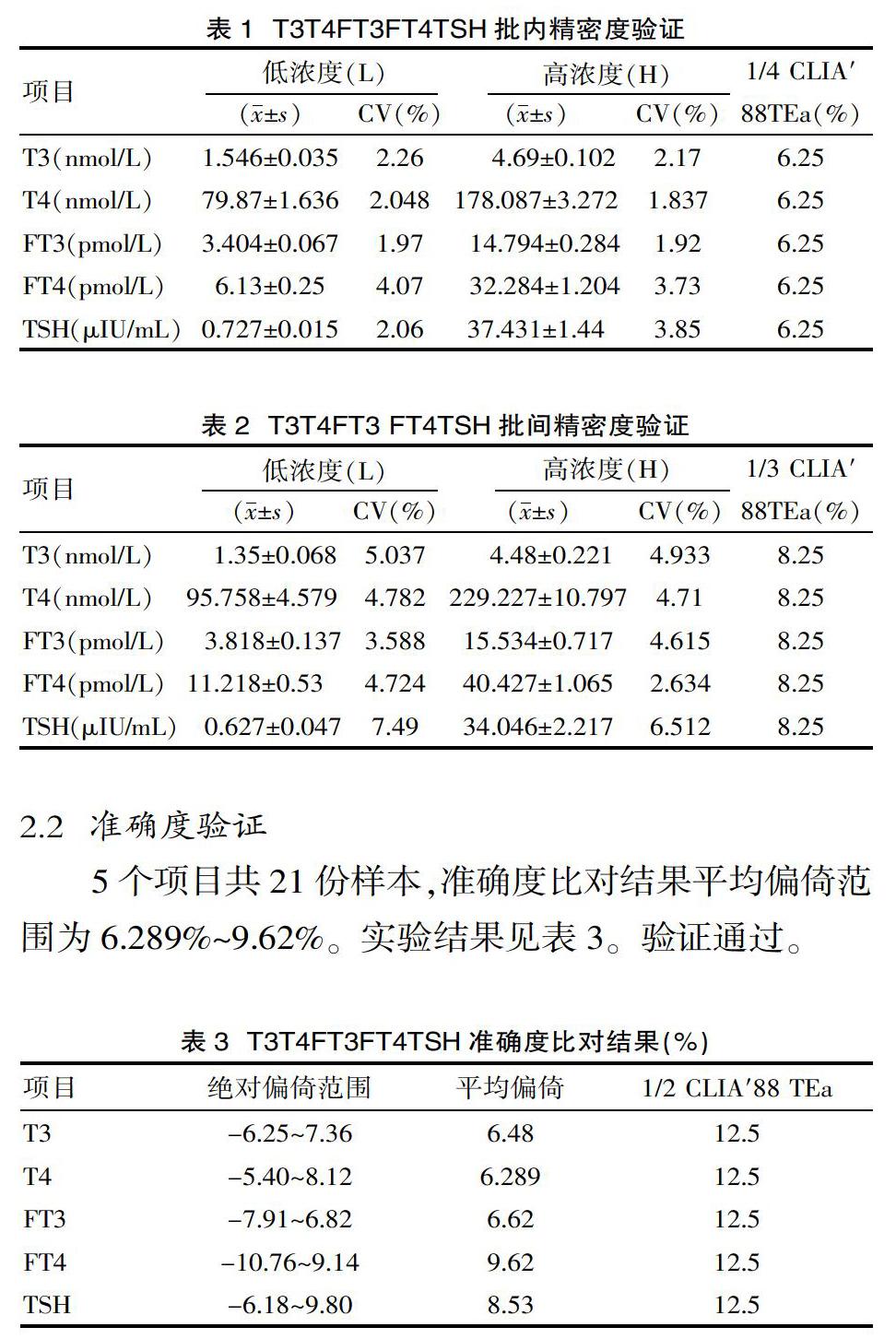
T3、T4、FT3、FT4、TSH共5个项目,批内精密度CV%在1.837%~4.07%,见表1。批间精密度CV%在2.634%~7.49%,见表2。精密度验证符合要求。
2.2 准确度验证
5个项目共21份样本,准确度比对结果平均偏倚范围为6.289%~9.62%。实验结果见表3。验证通过。
2.3 线性范围
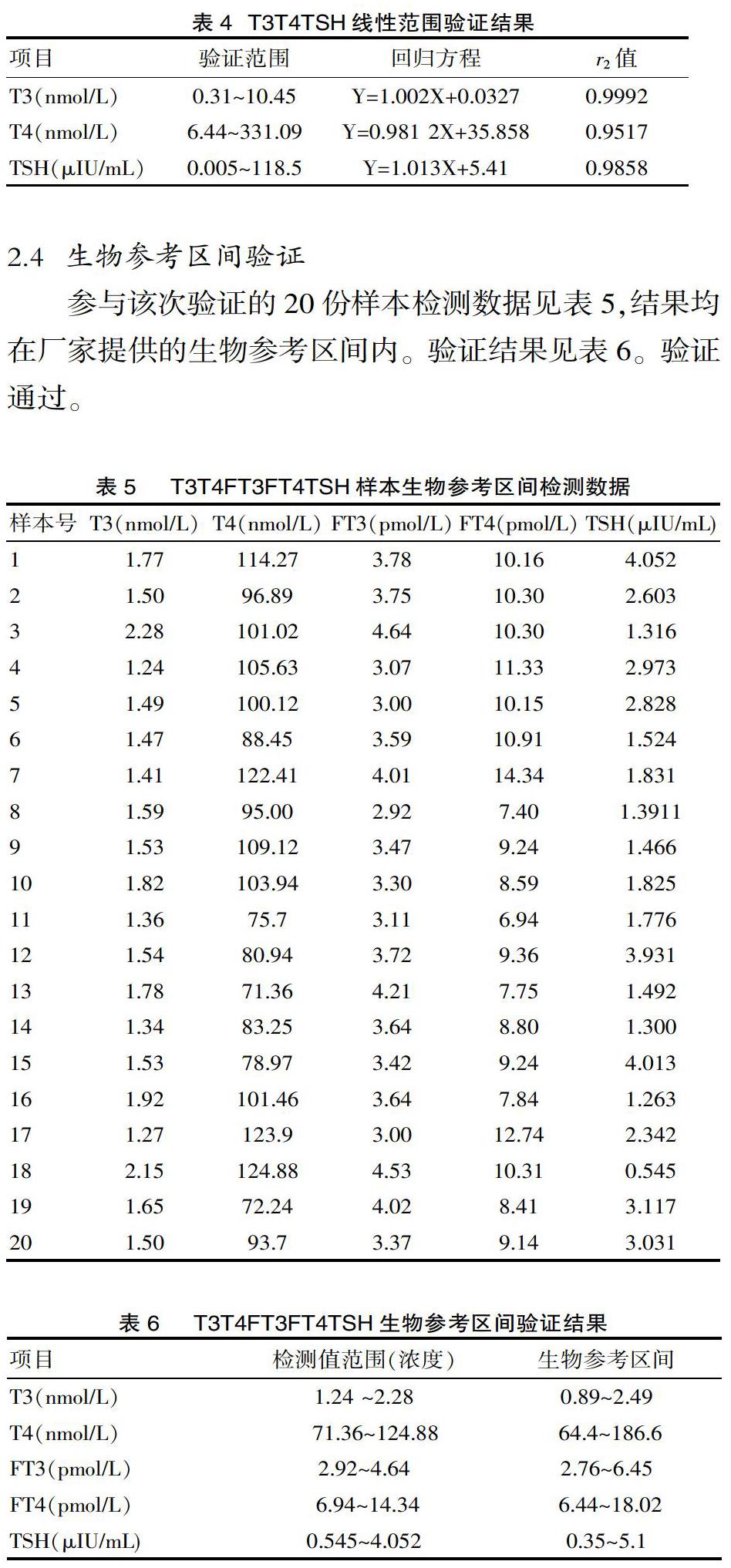
T3斜率为1.002、T4斜率为0.9812、TSH斜率为1.013。T3 r2为0.999 2、T4r2为0.951 7、TSHr2为0.985 8。验证结果见表4。验证通过。
2.4 生物参考区间验证
参与该次验证的20份样本检测数据见表5,结果均在厂家提供的生物参考区间内。验证结果见表6。验证通过。
3 讨论
精密度是在相同条件下对同一样本多次重复检测所得结果的一致性程度,反映检测系统的随机误差,用变异系数CV%来表示。是实验方法、仪器、试剂等性能的重要指标,也是进行性能验证的基础,该次实验T3、T4、FT3、 FT4、TSH的批内精密度CV%为1.837~4.07%,均<1/4 CLIA′88TEa(6.25%)。批间精密度CV%为2.634~7.49%,<1/3 CLIA88′TEa(8.25%)。该次参与验证的5个项目,精密度验证全部合格。
准确度是检测结果与其“真值”之间的差异大小,用“偏倚”表示,反映检测系统的系统误差[6-9],该次参与验证的5个项目其平均偏倚范围为6.289%~9.62%,<1/2 CLIA′88TEa(%)(12.5),准确度验证合格。在实际工作中,重复检测样本的几率很小,因此分析系统的准确度非常关键。精密度和准确度是对检测系统最基本的性能验证。因为FT3和FT4稀释过后的反应不成线性[4],因此,没有进行二者的线性实验。
进行性能验证,必须保证足够的在有效期内的同一批号试剂和耗材,实验过程中忌更换批号,尽量减少可能引起的误差。每一瓶新启用试剂均应先做校准和质控,质控在控的情况下才能进行工作,所有操作均应按仪器及试剂说明操作。参与实验的样本采集者不应服用药物,特别是内分泌系统疾病患者和孕婦应排除。由于孕妇样本收集要求更严格[12],短时间内无法收集到足够的合格样本,此次未进行孕妇生物参考区间的验证,此工作后续进行。通过该次实验,迈瑞CL-6000I化学发光分析仪检测系统在精密度、准确度、线性范围、参考区间四个方面达到相应要求,可用于临床工作。
[参考文献]
[1] 从玉隆,邓新位.实验室ISO15189认可对学科建设的几点启示[J].中华检验医学杂志,2007,30(2):128-131.
[2] 张秀明,阚丽娟.浅析定量检验程序分析性能验证实验方案设计[J].中华检验医学杂志,2015,38(6):428-430.
[3] 任亚萍,胡敏.ISO15189:2012与临床实验室定量检测程序性能评价[J].国际检验医学杂志,2018,39(2):209-213.
[4] 中华医学会检验医学分会,卫生部临床检验中心,中华检验医学杂志编辑委员会.甲状腺疾病诊断治疗中实验室检测项目的应用建议[J].中华检验医学杂志,2012,35(6):484-492.
[5] 张玥,董振芳,鞠瑛,等.ADVIA Centaur XP全自动化学发光免疫分析系统的性能验证及评价[J].国际检验医学杂志,2018,39(3):282-292.
[6] 杨伟明,王小中,刘静,等.Beckm an CoulterAU2700全自动生化仪的性能验证[J].实验与检验医学,2017,35(2):222-245.
[7] 陈兰,邵婧,陈义庆,等.LIAISON化学发光免疫分析仪检测的性能验证[J].国际检验医学杂志,2018,39(2):149-152.
[8] 魏松,陈秋序,李宜珊,等.罗氏电化学发光免疫分析仪检测系统的性能验证[J].国际检验医学杂志,2018,39(2):223-225.
[9] 谢文阁,黄宁,李金星.用室间质评数据评估临床生化检验中的偏倚[J].医学检验与临床,2017,28(9):18-21.
[10] 兰庆站,成士清,刘义庆,等.贝克量AU5800全自动生化分析仪检测血浆脂蛋白磷脂酶A2性能验证[J].国际检验医学杂志,2018,39(18):2249-2252.
[11] 中华人民共和国卫生部.临床实验室检验项目参考区间的制定(WS/T402-2012)[S]:2012-12-24.
[12] 卫蔷,张力,刘兴会,等.妊娠不同时期甲状腺功能指标参考值的临床分析[J].中华妇产科杂志,2018,53(5):299-303.
(收稿日期:2019-12-03)
