C6H11NO/nCF3SO3H型低共熔溶剂氧化脱除模拟油中的二苯并噻吩
2020-06-09刘昊然王韵淇李秀萍赵荣祥
刘昊然,王韵淇,李秀萍,赵荣祥
(1 辽宁石油化工大学化学化工与环境学部石油化工学院,辽宁抚顺113001;2 辽宁石油化工大学化学化工与环境学部化学与材料科学学院,辽宁抚顺113001)
近年来,燃料的深度脱硫已成为世界各国的一个重要研究课题。燃料中的有机硫化物燃烧而产生的硫氧化物(SOx)已成为严重的环境污染和雾霾形成的主要原因之一[1-2]。为此,许多国家制定了严格的环境法规,将燃料油的硫含量限制在10μg/g[3]。目前,传统的加氢脱硫(HDS)工艺是一种去除脂肪族和无环硫化合物的技术,被认为是一项成熟的技术。然而,由于噻吩、苯并噻吩、二苯并噻吩等多环有机硫化物存在空间位阻的影响,常规加氢脱硫难以实现深度去除。作为加氢脱硫工艺的补充,非加氢脱硫技术(NHDS)获得了广泛的关注,如光催化脱硫[4]、萃取脱硫[5]、吸附脱硫[6-7]和氧化脱硫[8-10]等。在这些非加氢脱硫工艺中,氧化脱硫(ODS)以其反应条件温和、高脱硫率和不消耗氢气等优点被认为是最有发展前途的技术之一。离子液体(ILs)是一种全部由离子组成的液体,因其独特的物理化学性质,被广泛应用于材料合成、催化、材料科学、电化学和分离过程中[11]。然而,常规的离子液体存在成本较高、合成过程复杂、生物降解性低、提纯困难等缺点,限制了其工业应用[12]。
低共熔溶剂(DESs)是以氢键供体(酰胺、羧酸和多元醇等化合物)和氢键受体(季铵盐)按照一定的摩尔比混合而成的溶剂。2003年,Abbott等[13]首次提出低共熔溶剂(DESs)的概念,低共熔溶剂具有与离子液体相似的性质,同时具有制备简便、成本低、毒性低、易生物降解等特点,广泛应用于如纳米材料、电化学、催化剂等领域[14]。近年来,许多学者将低共熔溶剂应用到了油品脱硫领域[15-17]。然而,实践表明直接用低共熔溶剂萃取脱硫,其效果并不好,往往需要多级萃取才能实现深度脱硫[18]。研究发现,制备酸性低共熔溶剂,并将其应用到油品中硫化物的去除,可以极大提高脱硫效率。Yin等[19]制备了氯化胆碱/对甲苯磺酸(ChCl/p-TsOH)和四丁基氯化铵/对甲苯磺酸(TBAC/p-TsOH)。在最佳条件下,ChCl/p-TsOH 和TBAC/p-TsOH 对实际燃料的脱硫效率分别高达97.25%和95.90%。Lü等[20]研究了TBAC/2C2H2O4的氧化脱硫性能,最佳条件下,其对DBT的去除率达到了98%。Chen等[21]探讨了[Hnmp]Cl/ZnCl2低共熔溶剂对柴油的氧化脱硫效果,最佳条件下脱硫率高达99.9%。Hao 等[22]合成了C6H11NO/OXA低共熔溶剂,以其作为催化剂和萃取剂,H2O2作为氧化剂,反应3h 后对DBT 的去除率达到98%。Mao 等[23]将ChCl/CF3SO3H 应用于氧化脱除模拟油中的硫化物,对DBT 的去除率达到98.6%。上述催化剂虽然具有较高的脱硫率,但溶剂中的氯会造成环境污染,因此不用或少用含氯的氢键配体合成的低共熔溶剂具有重要意义。研究表明,低共熔溶剂的熔点取决于与氢键供体和受体间形成的氢键数量[24],而具有较低熔点的低共熔溶剂更加适合作为萃取剂和催化剂。三氟甲磺酸是一种很强的有机酸,具有较强的稳定性,其结构中存在1 个氢键供体和6 个氢键受体。己内酰胺属于杂环化合物,其结构中存在1个氢键供体和1个氢键受体。理论上两者可以通过多重氢键作用形成低熔点强酸性的低共熔溶剂。
本文以己内酰胺(C6H11NO)和三氟甲磺酸(CF3SO3H)作为氢键配体通过简单加热合成了一系列新型酸性低共熔溶剂C6H11NO/nCF3SO3H(n=0.25,0.5,1)。该低共熔溶剂较低的熔点和较强的酸性有利于氧化脱硫反应的进行。将其作为萃取剂和催化剂、H2O2作为氧化剂,组成萃取-氧化脱硫系统,并将其应用于模拟油中硫化物的脱除。分别考察了n(CF3SO3H)∶n(C6H11NO)、反应温度、O/S、C6H11NO/0.5CF3SO3H 加入量和不同硫化物对脱硫效果的影响,并分析了此萃取-氧化脱硫过程的反应机理。
1 实验部分
1.1 试剂及仪器
三氟甲磺酸(98%,国药集团化学试剂有限公司);己内酰胺(99%,阿拉丁试剂有限公司);正辛烷(98%,国药集团化学试剂有限公司);四氯化碳(99%,国药集团化学试剂有限公司);二苯并噻吩(98%,阿拉丁试剂有限公司);苯并噻吩(97%,阿拉丁试剂有限公司);4,6-二甲基二苯并噻吩(99%,阿拉丁试剂有限公司);H2O2(30%,辽宁泉瑞试剂有限公司)。
微库仑综合分析仪,WK-2D 型,江苏江分电分析仪器有限公司;傅里叶变换红外光谱仪,NEXUS 870 型,美国尼高力仪器公司;核磁共振仪,AV-400 型,瑞士buker 公司;旋转蒸发器,RE-52型,巩义市予华仪器有限责任公司;旋转黏度计,NDJ-79型,上海平轩科学仪器有限公司。
1.2 低共熔溶剂C6H11NO/nCF3SO3H 的合成及其物理化学性质
将CF3SO3H和C6H11NO按相应的摩尔比(0.25∶1,0.5∶1,1∶1)混合加入到配有冷凝管的三角瓶中,在90℃水浴下,磁力搅拌至固体完全溶解为澄清、黏稠状的液体,即得到C6H11NO/nCF3SO3H型低共熔溶剂,合成反应见图1;测得其相关物理化学性质,结果如表1所示。
图1 C6H11NO/nCF3SO3H的合成反应

表1 C6H11NO/nCF3SO3H的物理化学性质
1.3 萃取-氧化脱硫过程
分别将DBT、4,6-DMDBT、BT 加入500mL 的正辛烷中,配成三种硫含量均为500μg/g 的模拟油。分别将5mL模拟油、一定量的C6H11NO/nCF3SO3H和H2O2加入到100mL 配有冷凝管的三角瓶中,将其放置到集热式搅拌器,并在相应的温度和搅拌速率下进行氧化脱硫反应。利用WK-2D 微库仑综合分析仪测定其硫含量,按式(1)计算脱硫率η。

式中,C0为氧化脱硫反应前油品中硫的质量分数,%;C为氧化脱硫反应后油品中硫的质量分数,%;η为氧化脱硫反应对硫化物的脱除率,%。
2 结果与讨论
2.1 低共熔溶剂的表征结果
C6H11NO、CF3SO3H 和C6H11NO/0.5CF3SO3H 的红外光谱如图2(a)所示,在C6H11NO 的红外谱图中3218cm-1为N H 的伸缩振动吸收峰,2936cm-1为C H 伸缩振动吸收峰,1662cm-1为C O 伸缩振动吸 收 峰[25]。 在CF3SO3H 的 红 外 谱 图 中 可 见,3274cm-1为O H伸缩振动吸收峰;1392cm-1为S O伸缩振动吸收峰;1031cm-1和636cm-1为F C 的伸缩振动和弯曲振动吸收峰[23]。从C6H11NO/0.5CF3SO3H的红外光谱可以看出,相比于C6H11NO,3218cm-1的N H 伸缩振动吸收峰偏移到3252cm-1,C O 伸缩振动吸收峰从1662cm-1偏移到1629cm-1。上述现象表明C6H11NO和CF3SO3H之间形成了分子间氢键[26]。

图2 低共熔溶剂的FTIR和1HNMR表征结果
为了进一步确定C6H11NO 和CF3SO3H 之间是否形成了氢键,分别对C6H11NO、CF3SO3H和C6H11NO/0.5CF3SO3H 进行了1HNMR 分析,结果如图2(b)所示。由图2(b)可知,C6H11NO在δ=1.49、δ=2.32、δ=3.11和δ=4.69 处存在较强的氢峰,CF3SO3H 仅在δ=4.86处存在一个较强的氢峰。在C6H11NO 和CF3SO3H 形成低共熔溶剂后,相比于C6H11NO 和CF3SO3H,其对应的氢键位置均发生了轻微的移动。由此可以证明C6H11NO 和CF3SO3H 之间多重氢键作用[27],这种氢键网络的形成有利于降低低共熔溶剂的熔点[24]。
2.2 n(CF3SO3H)∶n(C6H11NO)对脱硫率的影响
CF3SO3H作为一种较强的有机酸,其含量的高低对低共熔溶剂的酸性有着直接的影响。本实验以CF3SO3H 和C6H11NO 作为原材料,按照不同的比例合成了3 种低共熔溶剂:C6H11NO/0.25CF3SO3H、C6H11NO/0.5CF3SO3H 和 C6H11NO/CF3SO3H, 并 以CF3SO3H 作对比。其酸性顺序为C6H11NO/0.25 CF3SO3H<C6H11NO/0.5CF3SO3H<C6H11NO/CF3SO3H<CF3SO3H。从图3 可以看出,当n(CF3SO3H)∶n(C6H11NO)分别为0.25∶1、0.5∶1、1∶1、1∶0时,其脱硫率分别达到了88%、99.8%、99.2%、82.3%,到达反应平衡的时间分别为100min、60min、120min、140min。这是因为CF3SO3H 作为一种酸性较强的有机酸,可以使低共熔溶剂的酸性显著提高,从而提高低共熔溶剂的催化活性。然而,当CF3SO3H与C6H11NO的摩尔比为1∶1时,脱硫率略微下降,且需要较长的反应时间才达到平衡。另外,相比于C6H11NO/0.5CF3SO3H,纯的CF3SO3H的脱硫率较低。这可能是因为催化剂过高的酸性加速了过氧化氢的分解,从而抑制氧化脱硫的进行[28]。因此,选择C6H11NO/0.5CF3SO3H 作为本实验的最佳低共熔溶剂。
2.3 反应温度对脱硫效果的影响

图3 n(CF3SO3H)∶n(C6H11NO)对脱硫率的影响
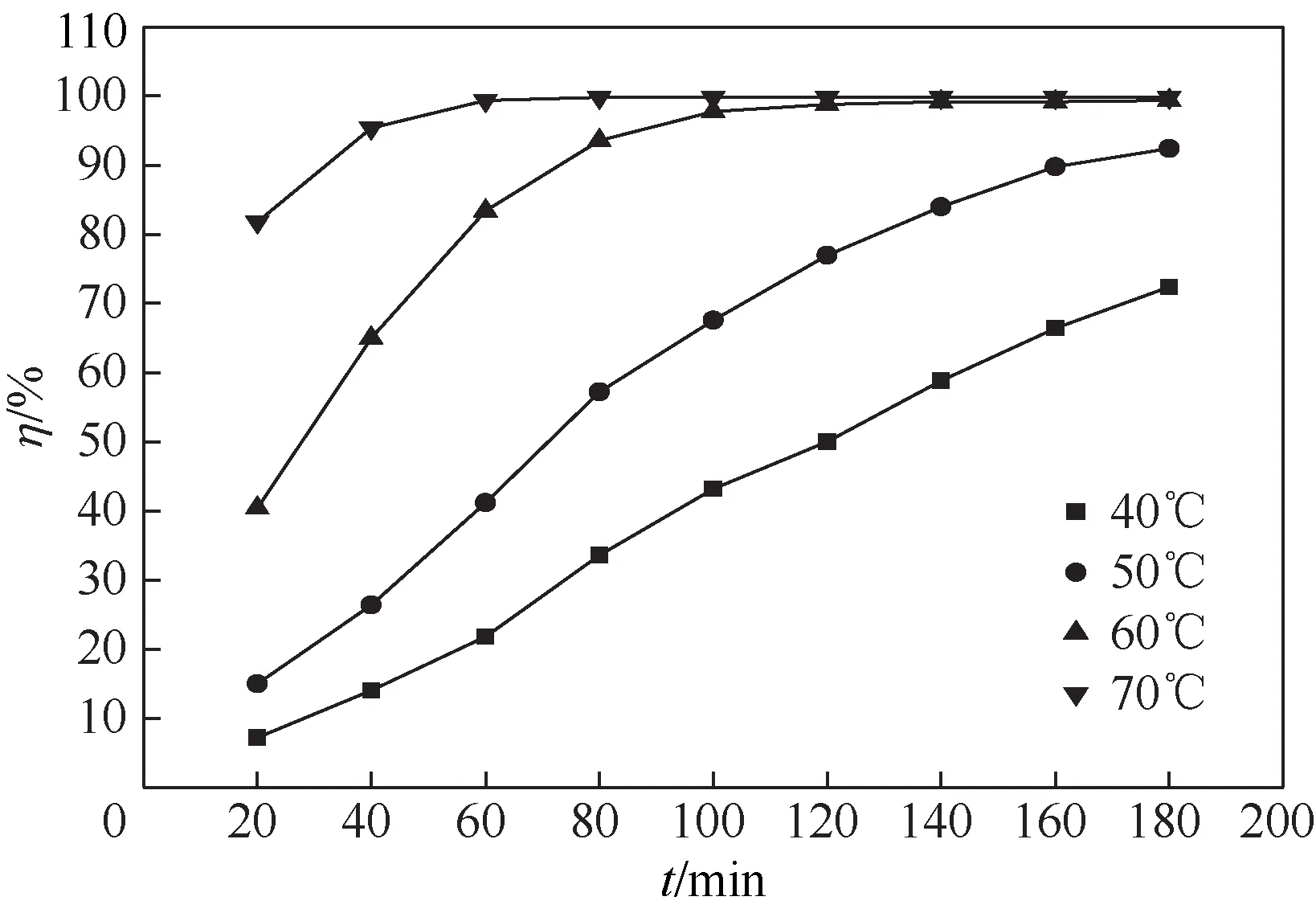
图4 反应温度对脱硫率的影响
C6H11NO/0.5CF3SO3H 在不同温度下的对二苯并噻吩的脱除效果如图4所示。由图4可知,当温度从40℃增加到60℃时,DBT的脱除率由72.4%增加到99.4%。这是因为氧化脱硫是吸热反应,反应温度的增加可促进氧化反应的进行[29]。另外,由于低共熔溶剂的黏度随着反应温度的增加而降低,升高温度有利于提高低共熔溶剂的传质速率,从而增加了DBT 的脱除率[30-31]。当温度进一步升高到70℃时,脱硫率达到99.8%,上升幅度很小。因此,选择60℃作为本实验的最佳温度。
2.4 O/S对脱硫效果的影响
不同的O/S 对体系中DBT 的脱除率见图5。由图5 所示,当O/S 为0 时,反应体系中仅有低共熔溶剂和模拟油,属于萃取脱硫,脱硫率仅为22.4%。当O/S从2逐渐增加到6时,脱硫率从72%增加至99.4%。这是因为增加过氧化氢的量,可以提高反应体系对模拟油中DBT 的氧化效率,从而提高反应的脱硫率[32]。然而,当O/S 继续增加到8时,脱硫率却略降至98.6%。这是因为随着H2O2用量的增加,体系同时会生成较多的水,水的存在会抑制氧化脱硫的进程,导致氧化效率降低[33]。因此,本实验最佳的O/S为6。
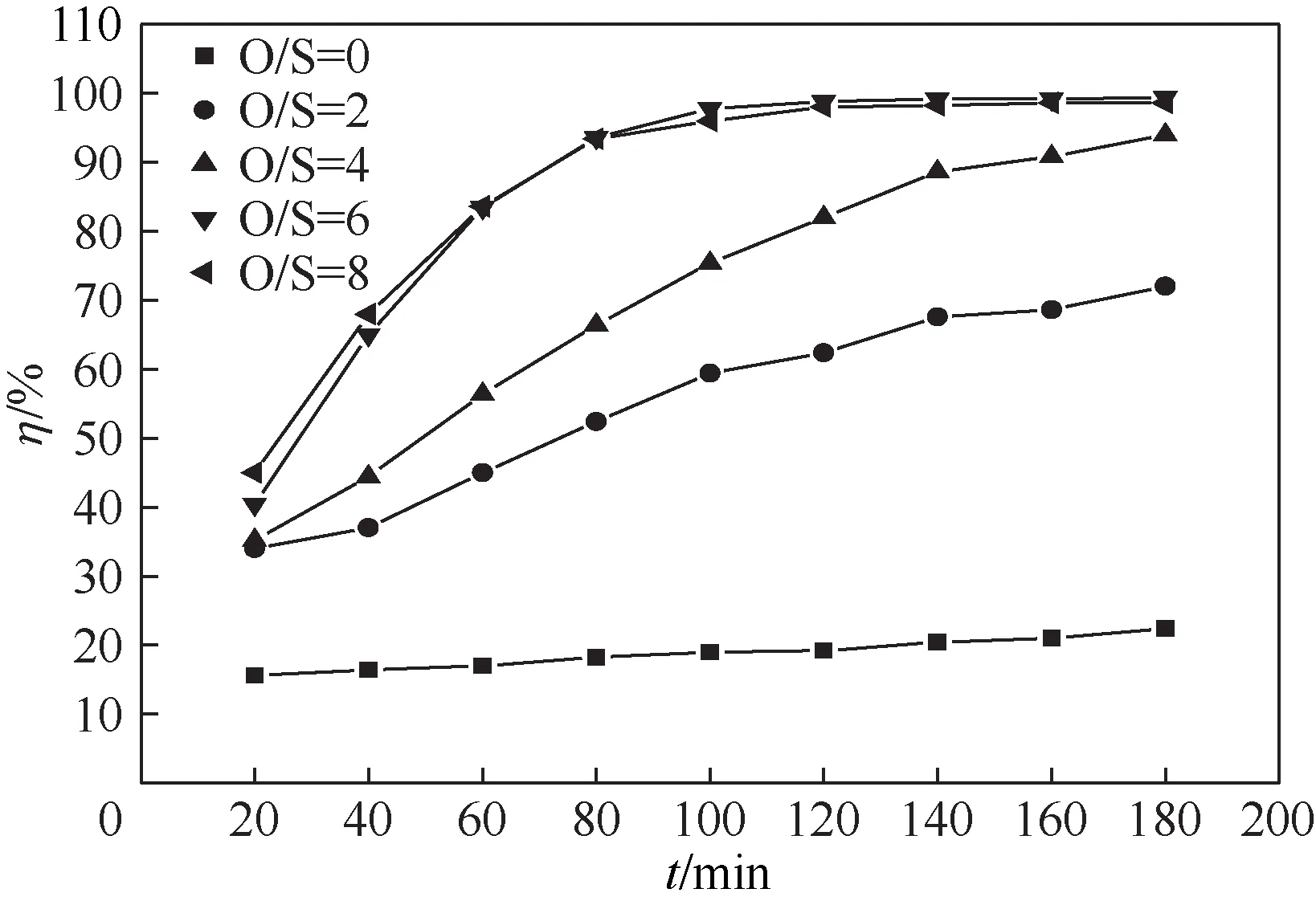
图5 O/S对脱硫率的影响
2.5 C6H11NO/0.5CF3SO3H 的加入量对脱硫效果的影响
低共熔溶剂的加入量对脱硫效果有着至关重要的影响。同时,也影响氧化脱硫的成本。从图6可以看出,当C6H11NO/0.5CF3SO3H 的加入量由0.5mL 升高到1.0mL时,其对DBT的脱除率由95.6%升高到99.4%。这是因为提高低共熔溶剂的加入量,有利于从模拟油中萃取DBT,使更多的DBT 参与到催化氧化反应中,从而提高氧化脱硫反应的效率[34]。然而,当C6H11NO/0.5CF3SO3H 的加入量达到1.5mL 时,其对DBT 脱除率略有下降。这是由于在氧化剂的加入量恒定的情况下,过量的低共熔溶剂会促使更多的DBT 被萃取到低共熔溶剂相中,致使氧化剂相对不足(O/S下降),DBT的脱除率降低[35]。综合考虑,C6H11NO/0.5CF3SO3H的最适宜加入量为1.0mL。

图6 C6H11NO/0.5CF3SO3H的加入量对脱硫率的影响
2.6 不同的硫化物和真实油对脱硫效果的影响

图7 不同的硫化物和真实油对脱硫率的影响
由于实际油品中所含的硫化物复杂多样,因此考察C6H11NO/0.5CF3SO3H对不同硫化物的去除能力具有重要的意义。由图7可知,C6H11NO/0.5CF3SO3H对DBT、4,6-DMDBT 和BT 的去除率分别达到99.4%、98.6%、83.6%。C6H11NO/0.5CF3SO3H 对不同硫化物的去除效果出现了较大的差异,这种现象跟S原子的电子云密度有着很大的相关性,电子云密度越大则活性越高,硫化物越容易被脱除[36]。了解到4,6-DMDBT、DBT、BT 上S 原子的电子云密度分别为5.760、5.758、5.739[37]。然而,C6H11NO/0.5CF3SO3H 对DBT 的脱除却高于4,6-DMDBT,这主要是因为4,6-DMDBT 苯环上的甲基基团增加了空间位阻,增加了氧化脱硫的难度[38]。实验中还测试了实际柴油(抚顺石油二厂催化柴油,硫含量350mg/kg)的脱硫效果。可以看出C6H11NO/0.5CF3SO3H对真实油的脱硫效果一般,脱硫率仅为61.6%。这是因为催化柴油中的硫化物成分较为复杂,含有如苯并噻吩、4-甲基苯并噻吩、二苯并噻吩、4-甲基二苯并噻吩、4,6-二甲基二苯并噻吩等主要硫化物,这些硫化物由于受到S原子电子云密度和空间位阻的影响,具有不同的氧化活性[39-40]。此外,柴油中含有的烯烃对氧化脱硫具有较强的抑制作用[41]。
实验结果表明,C6H11NO/0.5CF3SO3H 具有良好的氧化脱硫活性。表2 显示了不同DESs 和ILs 对DBT 氧化脱除的比较。由表2 可以看出,C6H11NO/0.5CF3SO3H具有较高的脱硫率。相比于先前合成的ChCl/CF3SO3H,C6H11NO/0.5CF3SO3H 在合成过程中不引入氯元素并减少了CF3SO3H的使用量,有利于降低对环境的危害。
2.7 C6H11NO/0.5CF3SO3H的回收利用
萃取-氧化脱硫实验结束后,采用倾倒法分离回收下层C6H11NO/0.5CF3SO3H,然后用相同体积的CCl4对C6H11NO/0.5CF3SO3H 进行3 次反萃取,采用旋转蒸发仪将残留在C6H11NO/0.5CF3SO3H 中的CCl4蒸出,得到的黏稠液体即是回收的C6H11NO/0.5CF3SO3H。对反应前后的C6H11NO/0.5CF3SO3H 进行红外分析,结果如图8所示。由图8可知,反应前后C6H11NO/0.5CF3SO3H 的各吸收峰基本保持一致,说明C6H11NO/0.5CF3SO3H 在萃取-氧化脱硫过程中结构未发生破坏,保持了较好的稳定性。
由表1 可知,DESs 在油中的溶解度较小,所以其对反应体系脱硫率的影响有限。C6H11NO/0.5CF3SO3H低共熔溶剂在完成氧化反应后,用CCl4反萃取氧化脱硫产物得到回收的DESs。在最佳条件下,加入回收的DESs、新鲜的双氧水和模拟油进行氧化脱硫重复使用实验。由表3 可知,5 次重复使用后其脱硫率从99.4%降到91.8%。然而,未经CCl4反萃取的C6H11NO/0.5CF3SO3H 脱硫率下降比较明显。这是因为DESs在萃取-氧化脱硫过程中会有二苯并噻吩砜等杂质不断积累导致脱硫率下降[42]。

表2 DESs和ILs对DBT氧化脱除的比较
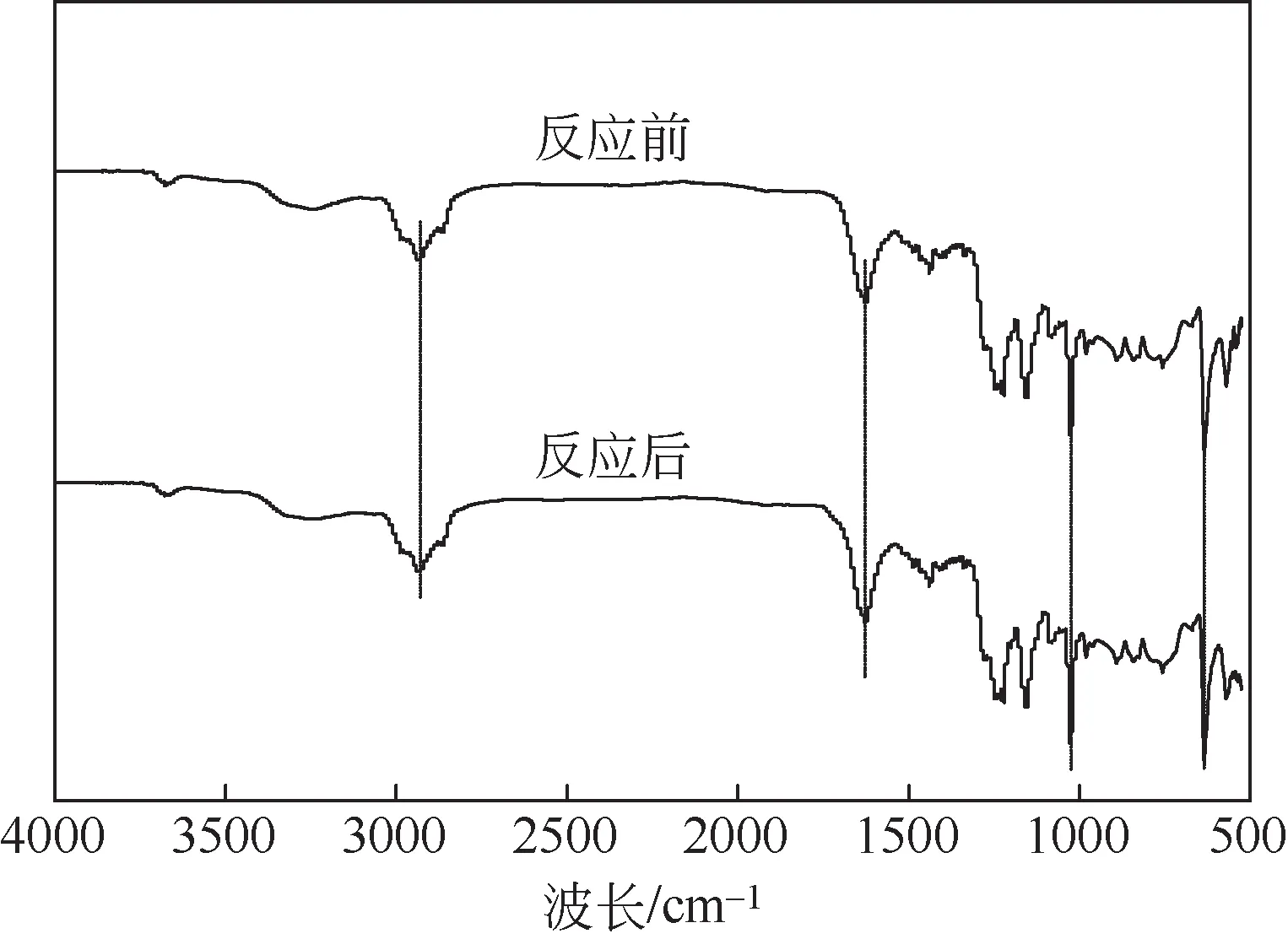
图8 反应前后C6H11NO/0.5CF3SO3H的红外光谱图

表3 低共熔溶剂的回收对脱硫率的影响
2.8 氧化产物的红外表征
为了研究氧化产物的形式,用分离漏斗分离上层油相,保留低共熔溶剂相。水作为副产物会残留在低共熔溶剂相中,可以采用旋转蒸发仪在70℃下将其去除。然后再加入等体积的CCl4在室温下搅拌30min,静置24h 后,采用旋转蒸发仪将体系中的CCl4蒸出,最后得到白色晶体状物质即为氧化产物。分别对DBT 和氧化产物进行红外表征,结果如图9所示,由图9可以看出,相比于DBT的红外谱图,氧化产物分别在1045cm-1,1165cm-1和1289cm-1处形成DBTO 和DBTO2的特征吸收峰[43]。这说明了在此萃取-氧化脱硫体系中,DBT 被氧化成了DBTO和DBTO2。

图9 DBT和氧化产物的红外光谱图
2.9 低共熔溶剂催化氧化脱硫机理
低共熔溶剂氧化脱硫机理对于理解低共熔溶剂催化氧化脱硫的过程是至关重要的。分别对DESs、DESs-DBT(1∶1)和DBT 进行红外表征,结果见图10。由 图10 可 知,DBT 在929cm-1、743cm-1和702cm-1的3个吸收峰在DESs-DBT中发生了不同程度的衰退和消失,表明C6H11NO/0.5CF3SO3H与二苯并噻吩之间发生了强烈的反应,导致二苯并噻吩的结构发生了“畸变”,从而降低了二苯并噻吩的芳香性[44-45]。
由于C6H11NO/0.5CF3SO3H与二苯并噻吩之间的相互相用,降低了二苯并噻吩的芳香性,因此其更容易发生氧化反应。由文献[15,46]的研究可知,对甲苯磺酸的 SO3H 在双氧水的作用下可以氧化为

图10 DESs、DESs-DBT(1∶1)和DBT的红外光谱图

图11 氧化脱硫机理
SO3OH,本实验所用的三氟甲磺酸同样含有SO3H,所以在双氧水的作用下可以被氧化成SO3OH,其具有氧化二苯并噻吩的作用。因此,该萃取-氧化脱硫系统的过程包括二苯并噻吩的萃取、C6H11NO/0.5CF3SO3H 中 SO3OH 的形成和二苯并噻吩的氧化。
基于以上的实验结果与讨论,C6H11NO/0.5CF3SO3H的萃取-氧化脱硫机理如图11所示。首先,由于C6H11NO/0.5CF3SO3H和DBT之间形成π-π共轭效应,C6H11NO/0.5CF3SO3H 将DBT 从油相萃取到DESs 相。被萃取到DESs 相的DBT 进一步与C6H11NO/0.5CF3SO3H 相互作用,并使DBT 的结构发生“畸变”。同时,DESs中的磺酸根 SO3H被H2O2氧化成相应的过氧磺酸根 SO3OH,然后过氧磺酸根 SO3OH将“畸变”的DBT氧化成相应的砜。随着氧化反应的进行,过氧磺酸根 SO3OH还原后会再次被H2O2氧化,直至H2O2完全消耗或硫化物完全被氧化。
3 结论
(1)通过简单加热C6H11NO 和CF3SO3H 合成了不同配比的C6H11NO/nCF3SO3H(n=0.25,0.5,1)型低共熔溶剂。并以C6H11NO/0.5CF3SO3H低共熔溶剂和H2O2组成萃取-氧化脱硫系统,并将其应用于脱除模拟油中的二苯并噻吩(DBT)。红外光谱和氢谱分析表明C6H11NO 与CF3SO3H 之间存在多重氢键作用。
(2) 在 模 拟 油 体 积 为5mL、n(CF3SO3H)∶n(C6H11NO) =0.5、 反 应 温 度 为60℃、 O/S=6、C6H11NO/0.5CF3SO3H 的加入量为1.0mL 的最佳反应条件下,C6H11NO/0.5CF3SO3H对DBT、4,6-DMDBT、BT和真实油的脱除率分别为99.4%、98.6%、83.6%和61.6%。
(3)此低共熔溶剂具有较强的稳定性,循环5次使用后,脱硫率仍高达91.9%。同时,证实了低共熔溶剂与DBT 之间存在相互作用,并促进了氧化脱硫的进程。
