白酒中氰化物的检测
2020-06-08王蕊冉艳瑞
王蕊 冉艳瑞


摘 要:本文采用顶空气相色谱法测定白酒中氰化物的含量。结果显示:氰化物在6~100 ng·mL-1范围内具有良好的线性关系(r>0.99),当标准添加水平为20、40、80 ng·mL-1时,回收率在89.6%~95.2%,方法检出限为15.752 ng·mL-1,相对标准偏差均小于15%。该方法简便、快速、灵敏和准确,适合酒中氰化物的快速检测及定量分析。
关键词:氰化物;检测;白酒
Abstract:In this paper, headspace gas chromatography was used for the determination of cyanide in liquor. The analytes were quantified by matrix -matched standard solution and the calibration curve showed good linearity within the concentrations of 6 to 100 ng·mL-1(r>0.99).The recoveries of the cyanide ranged from 89.6% to 95.2% in the three spiked levels of 20, 40 and 80 ng·mL-1, The relative standard deviation (RSD) were less than 15%. The limits of quantification was 15.752 ng·mL-1, The results indicate that the method is easier, faster, more sensitive,and suitable for the qualitative and quantitative confirmation of the cyanide from liquor.
Key words:Cyanide; Determination; Liquor
人體可通过皮肤和呼吸道快速吸收剧毒物质——氰化物,氰化物释放的氰基(CN-)会与位于线粒体膜上的细胞色素C氧化酶的Fe3+离子结合[1],从而抑制细胞色素C氧化酶的活性,阻断电子传递链使细胞组织缺氧[2]。过量吸入氰化物会导致患者深度昏迷、全身肌肉松弛、反射消失、呼吸浅慢及心跳停止[3]。此外氰化物在消化道中释放出的氢氧离子有腐蚀作用[4],会对胃肠道造成损害。口服氰化钠、氰化钾的致死量为1~2 mg·kg-1[5]。酒中的氰化物主要由原料(如木薯、代用品、豆类及其他果核或混入一些野生植物)中含有的氰甙类配糖体在发酵过程中水解产生[6]。
GB 5009.36-2016规定酒中氰化物的定量测定方法主要有分光光度法、气相色谱法[7]。此外崔鹏[8]采用荧光光谱法测定食品中氰化物含量,董明[9]利用傅里叶变换红外光谱快速检验了氰化物,张玮[10]应用流动注射分析仪测定了饮用水中的氰化物。
1 材料与方法
1.1 材料与试剂
20种随机购买市售白酒;氯胺T;磷酸;氢氧化钠;水中氰标准溶液:浓度:50 μg·mL-1;编号GBW(E)080115,由中国计量科学研究院提供。
1.2 仪器与设备
气相色谱仪(型号Trace1310);万分之一电子天平;离心机;超声波清洗器。
1.3 标准溶液列的配制
氰离子(以CN-计)标准中间溶液:准确移取2.0 mL酒中氰化物成分分析标准物质于10 mL的容量瓶,用0.1%氢氧化钠的溶液定容。
氰离子(以CN-计)标准工作溶液:移取适量氰离子(以CN-计)标准中间溶液用水稀释配制成浓度为:6、8、10、20、40、60、80 ng·mL-1和100 ng·mL-1系列标准工作溶液,现配现用。
1.4 试样制备与保存
按照GB/T 5009.36-2016,取液体试样约500 mL充分混匀,装入洁净容器中,密封,于0~4 ℃条件下保存。
1.5 标准曲线的制作
分别准确移取10.0 mL氰离子标准工作溶液于8个顶空瓶中,加入0.2 mL磷酸溶液,涡旋混合,然后加入0.2 mL氯胺T溶液,立即加盖密封,涡旋混合,待测。
1.6 试样溶液的测定
准确移取0.2 mL试样于顶空瓶中,加入蒸馏水9.8 mL,加入0.2 mL磷酸溶液,涡旋混合,然后加入0.2 mL氯胺T溶液,立即加盖密封,涡旋混合,待测。
1.7 色谱条件
色谱柱:TG-WAXMS,柱长30 m,内径0.25 mm,膜厚0.25 μm;色谱柱温度:初温40 ℃,保持1 min,以4.0 ℃·min-1升到130 ℃,以20℃·min-1升到200 ℃保持5 min;检测器温度:250 ℃;进样口温度:250 ℃;载气流量:1.0 mL·min-1;进样量:1.0 μL;分流比:20∶1。
2 结果与分析
2.1 标准曲线
将标准系列的标准工作溶液进行测定,以各组分的峰面积与对应的浓度绘制标准曲线,得回归方程和相关系数。结果表明,氰化物在6~100 ng·mL-1范围内具有良好的线性关系,线性相关系数大于0.99,可以满足定性、定量分析的需要。实验结果如表1所示,氰化物色谱图如图1所示。
2.2 检出限
取标准储备液配制成低浓度的标准溶液,以3倍信噪比15.752 ng·mL-1为检出限,GB 5009.36-2016《食品安全国家标准 食品中氰化物的测定》中气相色谱法氰化物的检出限为0.02 mg·L-1,因此本方法符合检测需求[7]。
2.3 回收率
在空白样品中添加浓度为20、40、80 ng·mL-1的标准溶液,平行测定6次,计算含量、回收率。
2.4 方法的精密度
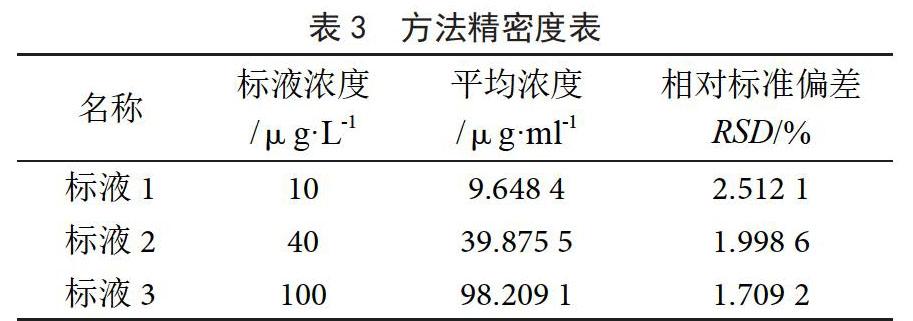
方法的精密度用变异系数即相对标准偏差来衡量,用浓度分别为10、40、100 ng·mL-1的标液分别平行测定6次,计算相对标准偏差,本实验的平均相对标准偏差RSD<15%,其精密度满足含量分析的要求,结果见表3。根据变异系数是标准差与平均数的比值得本次试验所得的数据2.5121%、1.998 6%和1.709 2%均符合GB/T 27404-2008检验方法确认的技术要求和实验室内变异系数≤15%的要求。
2.5 样品的测定及分析
采用本方法对随机从市场购买的白酒进行测定,通过实验结果,均未检出氰化物,说明市售白酒质量较好。
3 结论
通过实验发现,本文采用的氰化物检测方法在6~100 ng·mL-1范围内具有良好的线性关系(r>0.99),当标准添加水平为20、40、80 ng·mL-1時,回收率在89.6%~95.2%,方法检出限为15.752 ng·mL-1,相对标准偏差均<15%。该方法简便、快速、灵敏和准确,适合酒中氰化物的定量分析。通过对20个随机市售白酒样品的检测发现,所有样品均未检出氰化物,提示白酒质量较好。
参考文献:
[1]Logue B A,Hinkens D M,Baskin S I,et al.The Analysis of Cyanide and its Breakdown Products in Biological Samples[J].Critical Reviews in Analytical Chemistry,2010,40(2):122-147.
[2]Cooper C.E,Brown G C.The inhibition of mitochondrial cytochrome oxidase by the gases carbon monoxide,nitric oxide,hydrogen cyanide and hydrogen sulfide:chemical mechanism and physiological significance[J].Journal of Bioenergetics and Biomembranes,2008,40(5):533-539.
[3]戴 寅,陈君石,李悠慧,等.食品安全性毒理学评价程序和方法[J].医学研究杂志,1997(12):9-10.
[4]王明军.氰化物中毒的生化机理[J].黔南民族师范学院学报,2008(3):75-77.
[5]黄光照.法医毒理学[M].北京:人民卫生出版社,1999.
[6]张文德,张光仲,郭 忠,等.酒中微量氰化物的测定研究[J].中国食品卫生杂志,2004(3):232-235.
[7]国家卫生和计划生育委员会,国家食品药品监督管理总局.GB 5009.36-2016 食品安全国家标注 食品中氰化物的测定[S].北京:中国标准出版社,2016.
[8]崔 鹏.荧光法测定食品中氰化物含量的分析探讨[J].青海医药杂志,2006,36(7)70-71.
[9]董 明.利用红外光谱快速检验氰化物[J].刑事技术,2001(3):16.
[10]张 玮.应用Lachat QC8500流动注射分析仪测定水中氰化物[J].科技情报开发与经济,2008,18(35):214-215.
