响应面法优化蛋清蛋白碱法凝胶化条件
2020-06-02张高阳丘佳韵彭佳佳汪学荣
张高阳,丘佳韵,彭佳佳,汪学荣
(西南大学动物科学学院,重庆402460)
皮蛋作为我国传统再制蛋加工制品之一,别名有松花蛋、变蛋、彩蛋等。皮蛋的风味独特,香醇可口,并且营养成分丰富,含有大量的优质蛋白质、维生素和微量元素,具有易吸收、清热解毒等特点,从而受到大众的喜爱[1]。但随着人们食品健康安全意识的逐步提高,传统的皮蛋生产制造工业面临着极大的挑战,同时在生产工艺方面也有很多地方有待改进。例如生产加工中使用的氧化铅(lead oxide,PbO)危害人体健康[2],咸蛋黄生产过程中蛋白过咸,油脂的抗氧化能力下降,不宜食用[3],但如果丢弃在环境中,容易造成蛋白质资源的极大浪费。另外传统皮蛋加工过程中的深加工程度、原料蛋品质、生产技术的先进性等问题也值得大家反思,因此对于如何优化生产流程,提高生产效率,降低生产成本、减少破损率就成为了困扰广大蛋制品生产厂家的“心病”[4-5]。
目前对蛋清蛋白碱诱导的研究主要集中于对蛋白质浓度、pH值、加热温度、加热时间等诸多单一因素的影响[6]。例如一些学者研究了蛋清在酸、碱作用下的凝胶化现象,发现蛋清在pH 2.3以下或pH 12.0以上都会形成凝胶,在pH 2.3~12.0之间则不发生凝胶化[7]。此外,Croguennec等[8]研究发现不同的金属离子pH值对蛋清蛋白质凝胶性能有显著影响;pH值为7时,Fe3+、Ca2+和Mg2+能影响凝胶的粘弹性和微观结构且Fe3+最为显著;而高浓度的氯化钠(sodium chloride,Na-Cl)能降低凝胶的持水力。但直到如今科研人员对通过控制多因素来优化蛋清蛋白碱诱导凝胶,促进凝胶结构的稳定性的研究仍有欠缺[9]。通过一系列预试验和理论分析,拟将蛋清和蛋黄分离,蛋清用作皮蛋的原材料,蛋黄则用来制作咸蛋黄等其他产品。直接向蛋清中加入一定量的可食用碱[10],这样做既能简化工艺流程,缩短生产周期,又能节约成本,与传统皮蛋及其制品的加工工艺相比,生产效率得到了显著提高。本试验以蛋清为原料,将食用碱与蛋清直接混合,通过响应面法优化蛋清蛋白碱法凝胶化工艺条件[11]。算出最佳响应值。以期为提高皮蛋及其系列制品生产效率提供基础数据和有益参考。
1 材料与方法
1.1 材料
新鲜鸡蛋:荣昌地区市售,检验合格;氢氧化钠(sodium hydroxide,NaOH)(食用级):衢州市博特化工有限公司。
1.2 仪器与设备
磁力加热搅拌器(BNCH78-1型):武汉格莱莫检测设备有限公司;凝胶强度测试仪(MD-NJ-5型):临安丰源电子有限公司;电子分析天平(FA1204B型):上海建恒仪器有限公司;离心机(H3-18KR型):湖南可成仪器有限公司;电热恒温干燥烘箱(DGH-9140A型):上海精宏实验仪器有限公司;电热恒温水浴锅(SSY6型):金坛市富华仪器有限公司。
1.3 方法
1.3.1 NaOH用量对蛋清蛋白碱诱导凝胶性质的影响
以蛋清质量为计算基准,分别添加0.6%、0.8%、1.0%、1.2%、1.4%食用级NaOH于蛋清中,置于40℃恒温水浴锅中静置反应3.5 h,冷却至室温(25℃),测定其凝胶强度和持水力。
1.3.2 凝胶化温度对蛋清蛋白碱诱导凝胶性质的影响
以蛋清质量为计算基准,添加1.2%的NaOH,将蛋清蛋白分别置于 36、38、40、42、44℃恒温水浴锅中静置反应3.5h,冷却至室温(25℃),测定其凝胶强度和持水力。
1.3.3 凝胶化时间对蛋清蛋白碱诱导凝胶性质的影响
以蛋清重量为计算基准,添加1.2%的NaOH,将蛋清蛋白置于40℃恒温水浴锅中分别静置反应2.5、3.0、3.5、4.0、4.5 h,冷却至室温(25 ℃),测定其凝胶强度和持水力。
1.3.4 蛋清蛋白凝胶化最佳工艺条件的确定
在单因素试验基础上,以凝胶强度为响应值,通过三因素三水平响应面试验确定蛋清蛋白凝胶化的最佳工艺条件。
1.4 测试指标
1.4.1 持水力(water holding capacity,WHC)
取样品3个不同部位共10g称重,用规格为150×150 mm的滤纸包裹后置于50 mL离心管中,于25℃、3 000 r/min下离心10 min,将称量纸剥离后再次称量,计算公式为:
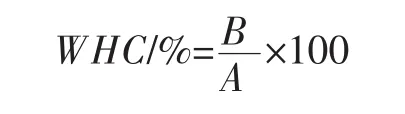
式中:A为离心前重量,g;B为离心后重量,g。
1.4.2 凝胶强度
采用凝胶强度测定仪测定蛋清蛋白凝胶的强度,每个样品测定7次,去除最大、最小值后,取剩余5个值的平均值作为其凝胶强度。
1.5 试验数据收集与处理
2 结果与分析
2.1 NaOH用量对蛋清蛋白碱诱导凝胶性质的影响
固定凝胶化温度和时间,考察NaOH用量对蛋清蛋白凝胶性质的影响,结果见图1。

图1 NaOH用量对蛋清蛋白凝胶强度和持水力的影响Fig.1 Effect of sodium hydroxide on gel strength and water holding capacity of egg albumin
图1表明,随着NaOH用量的增加,蛋清蛋白的凝胶强度和持水力均呈现先增加后减小的变化,当NaOH用量为1.2%时,蛋清蛋白的凝胶强度达到最大值0.88 kgf,明显高于碱添加量较小的样品(P<0.05)当NaOH用量为1.0%时,持水力最大值为90.78%。这是由于蛋清蛋白中加入一定量氢氧化钠后,pH值的增加促进了更多的疏水性氨基酸的暴露,从而促进蛋白链的排斥凝结,进而提高了凝胶性质。当碱添加量高于1.2%时,凝胶强度显著下降(P<0.05),这是由于加入过量的氢氧化钠后,强碱性pH值下加热将会使发生热聚集的蛋白质解折叠或降解,从而降低了凝胶性质[12],在强碱性条件下,凝胶的形成时间短、卵白蛋白更易变性、游离基增加,但是表面疏水性不稳定,先增加而后又缓慢下降,从而降低凝胶强度[13]。综合分析可知,1.2%的NaOH用量为较优添加量,应采用其进行后续优化试验。
2.2 凝胶化温度对蛋清蛋白碱诱导凝胶性质的影响
固定NaOH用量和凝胶化时间,考察凝胶化温度对蛋清蛋白凝胶性质的影响,结果见图2。
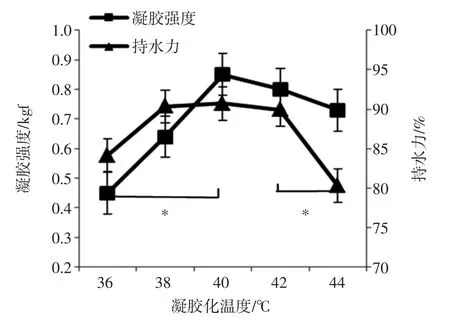
图2 凝胶化温度对蛋清蛋白凝胶白凝胶强度和持水力的影响Fig.2 Effect of gelation temperature on gel strength and water holding capacity of egg albumin
图2表明,随着凝胶化温度的增加,蛋清蛋白的凝胶强度和持水力均呈现先增加后减小的变化,当凝胶化温度为40℃时,蛋清蛋白的凝胶强度达到最大值0.85 kaf,明显高于温度较低的样品(P<0.05),持水力达到最大值90.70%。陈晓等[14]研究发现蛋清蛋白在25℃加热时,便能促进隐藏的—SH的暴露和氧化,加快—SH与S—S键的相互转化,增强凝胶结构。40℃以后凝胶强度下降不显著(P>0.05)这是因为在40℃以后加热时,较高的温度会破坏蛋白质交联的氢键,阻碍蛋白质进一步吸附水分。在50℃加热时,凝胶还可能因为分解而失去弹性[15]。结合分析可知,凝胶化温度为40℃为较优反应温度,应采用其进行后续优化试验。
2.3 凝胶化时间对蛋清蛋白碱诱导凝胶性质的影响
固定NaOH用量和凝胶化温度,考察凝胶化时间对蛋清蛋白凝胶性质的影响,结果见图3。

图3 凝胶化时间对蛋清蛋白凝胶白凝胶强度和持水力的影响Fig.3 Effect of gelation time on gel strength and water holding capacity of egg albumin
图3表明,随着凝胶化时间的增加,蛋清蛋白的凝胶强度和持水力均呈现先增加后减小的变化,当凝胶化时间为4 h时,蛋清蛋白的凝胶强度达到最大值0.87 kgf,明显高于凝胶化时间较短的样品(P<0.05),当凝胶化时间为3.5 h时,持水力达到最大值86.93%。当时间超过4 h时,凝胶强度显著下降(P<0.05),这是由于氢氧化钠与蛋白质反应时间过长,过量的碱会使蛋白质带上较多的负电荷,从而产生较大的静电斥力,破坏蛋白质分子间的结合,以及蛋白质和水分子间的结合[16],使凝胶结构变得松散并液化,使部分结合水又变回自由水,降低持水力,出现“碱伤”现象[17]。孙静等对皮蛋工艺的研究发现热处理时间在0~4 h的持水力、凝胶性质、弹性以及硬度较为理想[18],相对于热诱导凝胶最后趋于形成较大的硬度[19],轻度碱伤的皮蛋也能够恢复原本的形态。综合分析可知,凝胶化时间4 h为较优反应时间,应采用其进行后续优化试验。
2.4 蛋清蛋白凝胶化最佳工艺条件的确定
2.4.1 响应面试验设计及结果
在单因素试验基础上,利用Design Expert8.0软件,采用Box-Behnken试验设计,以NaOH用量、凝胶化温度和凝胶化时间为自变量,以凝胶强度为响应值,对蛋清蛋白凝胶化条件进行优化,因素水平见表1,试验结果见表2。
2.4.2 回归模型的建立与检验
使用Design Expert8.0软件对表2中的试验数据进行二次多项回归拟合,可得到凝胶强度(y)对自变量X1(NaOH用量)、X2(凝胶化时间)、X3(凝胶化温度)的回归方程式(1):

表1 因素水平表Table 1 Factor and level

表2 Box-Behnken试验设计及结果Table 2 Experimental design and results of Box-Behnken
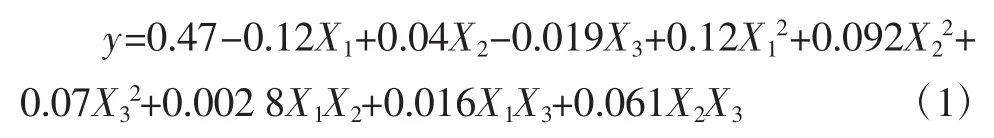
回归方程方差分析见表3。
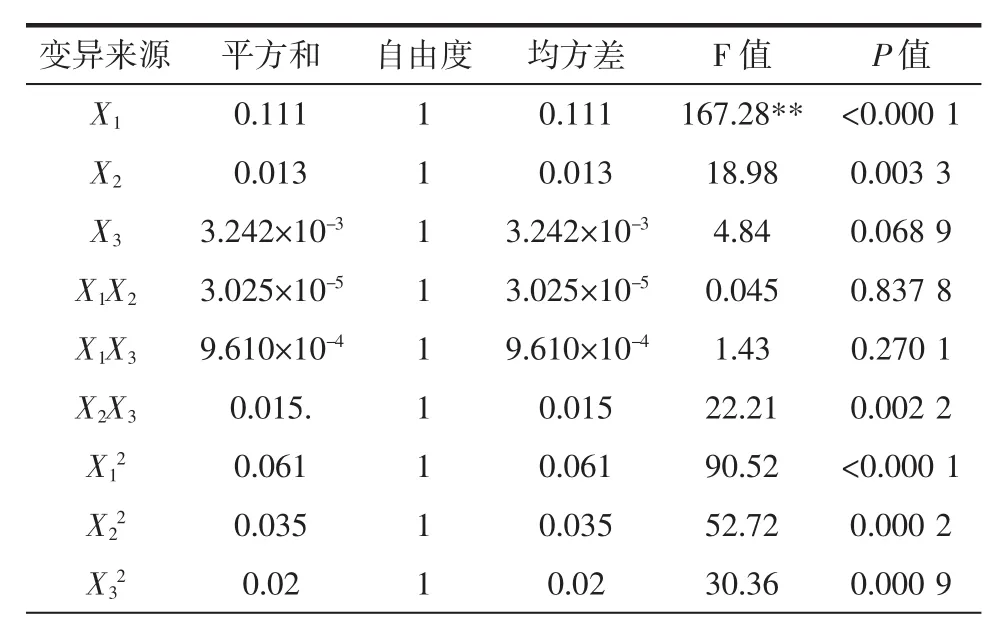
表3 回归方程方差分析Table 3 Variance analysis of regression equation

续表3 回归方程方差分析Continue table 3 Variance analysis of regression equation
由表3可知:显著性检验:**P<0.000 1,在 α=0.01水平上差异极显著,建立的模型与实际情况较相符,试验误差小,说明回归方程能较合理的预测凝胶化处理条件对蛋清蛋白凝胶强度的影响;失拟性检验:*P=0.471 1>0.05,在α=0.05水平上失拟差异不显著,即不存在失拟因素,得到的模型与期望的函数模型较相符,模型拟合度高[20]。各凝胶化条件的回归方程一次项的回归系数的绝对值大小之比为X1>X2>X3,表明了凝胶化条件对蛋清蛋白的影响大小及顺序为:NaOH用量>凝胶化温度>凝胶化时间。
另外,而 X1、X2、X12、X22、X32、X2X3在 α=0.01 水平上差异极显著(**P<0.01),X3、X1X2、X1X3、在 α=0.05 水平上差异不显著(P>0.05),说明三者共同作用时,凝胶化时间与凝胶化温度对蛋清蛋白凝胶强度的影响大,三者单一作用时均对凝胶强度有较为明显的影响。去除失拟项后得到如下方程(2):
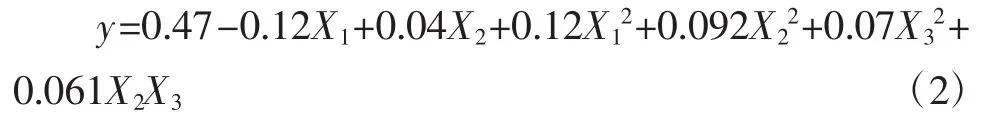
2.4.3 交互作用分析
响应面分析图直观地显示了凝胶化过程中各因素之间的交互作用,考察在某一个因素固定为中心值不变时,其他两个因素的交互作用对凝胶强度的影响[21]。根据回归方程,作出响应面分析图和等高线图,部分因素的交互作用如图4~图6所示。
响应曲面图可直观地看出各因素交互作用对凝胶强度的影响,曲面越陡峭,说明该因素对其影响越大,交互作用越显著。等高线形状为椭圆表示两因素间的交互作用显著,圆形等高线表示交互作用不显著[22-23]。由图4可以看出凝胶化时间与NaOH用量之间的交互作用较弱,凝胶化时间对凝胶强度的影响略大于NaOH用量;由图5可知凝胶化温度与NaOH用量之间的交互作用较为明显,在固定凝胶化温度和时间的条件下,减少NaOH用量有助于提高凝胶强度;最后两张图表明凝胶化时间与凝胶化温度之间的交互作用显著,表现为响应面曲线较陡峭,等高线较密集且呈现椭圆形。以上结果均与回归分析结果相吻合。
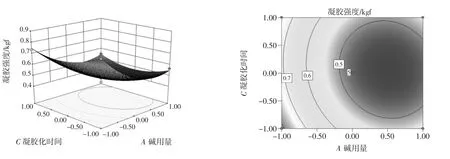
图4 NaOH用量和凝胶化时间对蛋清蛋白凝胶强度的响应面图和等高线图Fig.4 Response surface and contour plot of alkali dosage and gelation time on egg albumin gel strength
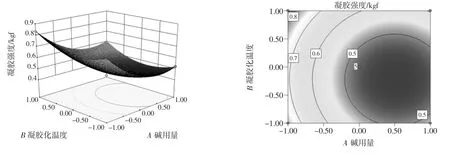
图5 NaOH用量和凝胶化温度对蛋清蛋白凝胶强度的响应面图和等高线图Fig.5 Response surface and contour plot of alkali dosage and gelation temperature on egg albumin gel strength
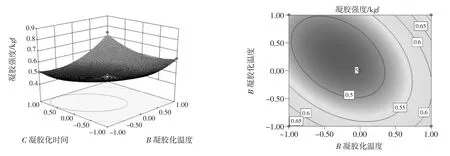
图6 凝胶化温度和凝胶化时间对蛋清蛋白凝胶强度的响应面图和等高线图Fig.6 Response surface and contour plots of gelatinization gel temperature and gelation time on egg protein gel strength
2.4.4 蛋清蛋白最优凝胶化条件的确定与验证
Design Expert8.0软件对回归模型求解后得出的最佳凝胶化条件为:NaOH用量0.8%,凝胶化温度42℃,凝胶化时间4 h,最大凝胶强度为0.936 kgf。以此为凝胶化条件,最后进行3组平行试验,得出的蛋清蛋白凝胶强度为0.933 kgf,与理论预测值0.936 kgf的相对误差为1.003%,小于2%,表明二者数值相近,预测值与实际值较为符合。
3 结论
NaOH用量、凝胶化温度和凝胶化时间对蛋清蛋白凝胶强度均有不同程度的影响,通过响应面法获得优化条件为NaOH用量0.8%,凝胶化温度42℃,凝胶化时间4 h,综合在不同条件下持水力的变化趋势,在最优凝胶化条件下凝胶强度的预测值为0.936 kgf,实际值为0.933 kgf,二者相近,优化结果可靠。目前就改性对于蛋清蛋白凝胶性质影响的研究尚处于探索阶段,暂时还没有一种很好的改性方法能够使蛋清蛋白的凝胶弹性、强度、稳定性和透明性等有目的地加以改变,如果在这个领域能有所突破,那么将可以利用其提高肉制品,方便面制品的营养价值和对其理化性质进行改良,所以对此方面的研究应该更深入的进行下去,这将会成为今后蛋清蛋白研究领域的一个重要的趋势,也是食品深加工行业的一种趋势。目前大家对于蛋清蛋白起泡性、乳化性等方面的研究还不太深入,由于蛋白质的各项功能特性之间是相互关联的,因此加强蛋清蛋白凝胶性与其溶解性、乳化性以及起泡性等之间关系的研究也是有很大的实用价值。
