超微血管成像结合TI-RADS鉴别诊断甲状腺良恶性结节
2020-06-02陶玲玲詹维伟樊金芳李伟伟
陶玲玲,詹维伟,樊金芳,李伟伟,王 怡,徐 皪,周 伟*
(1.上海交通大学医学院附属瑞金医院卢湾分院超声科,上海 200020;2.上海交通大学医学院附属瑞金医院超声科,上海 200025)
2017年美国放射学会(American College of Radiology, ACR)发布了甲状腺影像-报告和数据系统(thyroid imaging reporting and data system, TI-RADS),对甲状腺结节提出新的风险分层方法[1],为规范化超声诊断报告指明了方向,然而实际应用中风险率仍有所出入[2]。针对彩色多普勒技术用于鉴别诊断甲状腺良恶性结节还存在一定争议,且不同超声仪器之间血流敏感性不一致,故ACR并未将其纳入。随着越来越多的超声新技术应用于临床,超微血流成像(superb micro-vascular imaging, SMI)技术在乳腺、甲状腺、淋巴结等浅表器官的应用成为目前研究热点[3]。SMI通过新的成像技术使得血流信号与组织信号分离,保留低速血流信号,以显示微小血管[4],相比CDFI能更真实地反映结节内血流分布及血管走行特征。本研究旨在探讨SMI与TI-RADS分类结合鉴别诊断甲状腺良恶性结节的价值。
1 资料与方法
1.1 一般资料 回顾性分析2017年1月—2018年12月179例拟于上海交通大学医学院附属瑞金医院卢湾分院接受外科手术治疗的甲状腺结节患者,共187个结节,其中男50例,女129例,年龄19~76岁,平均(48.3±12.9)岁。纳入标准:①超声所示结节大小、位置与术后病理所见对应;②能于一个超声切面内完整显示结节;③取得最终手术病理结果。排除甲状腺实质血流信号异常丰富者。
1.2 仪器与方法 采用Toshiba Aplio 500彩色多普勒超声诊断仪,高频探头PLT-1005BT,频率14 MHz,动态范围60,并配备SMI成像软件。嘱患者平卧、头后仰,充分暴露颈部。先行常规超声扫查,观察并记录结节位置、大小、成分、回声、形状及边缘等情况;启动SMI功能,嘱患者禁止吞咽,避免对结节加压,调节取样框大小至略大于结节,适当调整血流增益至刚好显示微小血管而不出现外溢。将所获图像以静态及动态模式存储至本机,随后导入硬盘进行脱机分析。
1.3 图像分析 由2名具有10年以上超声工作经验的主治医师在不知晓病理结果的情况下分析图像,有分歧时经讨论达成一致。采用常规超声根据TI-RADS将甲状腺结节分为TR 1~5类。对下列各项进行评分:①成分(囊性或海绵征0分,囊性为主或实性为主1分,实性2分);②回声(无、高、等回声0分,低回声2分,极低回声3分);③形状(宽度>高度0分,宽度<高度3分);④边缘(光滑或边界不清0分,分叶或不规则2分,腺体外侵犯3分);⑤强回声(无或伴大彗尾征0分,粗大1分,边缘或环形2分,点状3分),其中强回声评分为叠加分数。将各项得分相加,所得即为总分,0分为TR l类,2分为TR 2类,3分为TR 3类,4~6分为TR 4类,≥7分为TR 5类。将SMI检测到微小穿支血管的结节判读为恶性,存在内部血管、周边血管或混合性血管而无穿支血管者判读为良性。穿支血管定义为自结节周边进入其内部,且贯穿长度达结节最大径2/3以上的细线状微小血管[5]。发现结节内微小穿支血管时,将TR分类上调一级,而TR 5类维持不变。见图1。
1.4 统计学分析 采用SPSS 20.0及SAS 9.4统计分析软件。计量资料以±s表示,计数资料采用χ2检验或Fisher精确概率法。采用ROC曲线,计算AUC,根据约登指数确定最佳截断值,计算敏感度、特异度、阳性预测值、阴性预测值及准确率。采用Z检验对校正前后诊断效能进行比较。P<0.05为差异有统计学意义。
2 结果
2.1 病理结果 良性结节103个,其中结节性甲状腺肿76个,腺瘤24个,亚急性甲状腺炎2个,结节样增生1个;恶性结节84个,包括乳头状癌82个、滤泡癌2个。
2.2 校正前、后风险分层与诊断结果对比 根据TI-RADS分别将187个甲状腺结节归类于TR 1~5,各类别中实际恶性率分别为0、0、5.00%、37.74%和64.29%。经SMI校正后各类别实际恶性率分别为0、0、5.56%、23.26%和66.36%。良恶性结节之间,有无穿支血管差异有统计学意义(P<0.05,表1)。
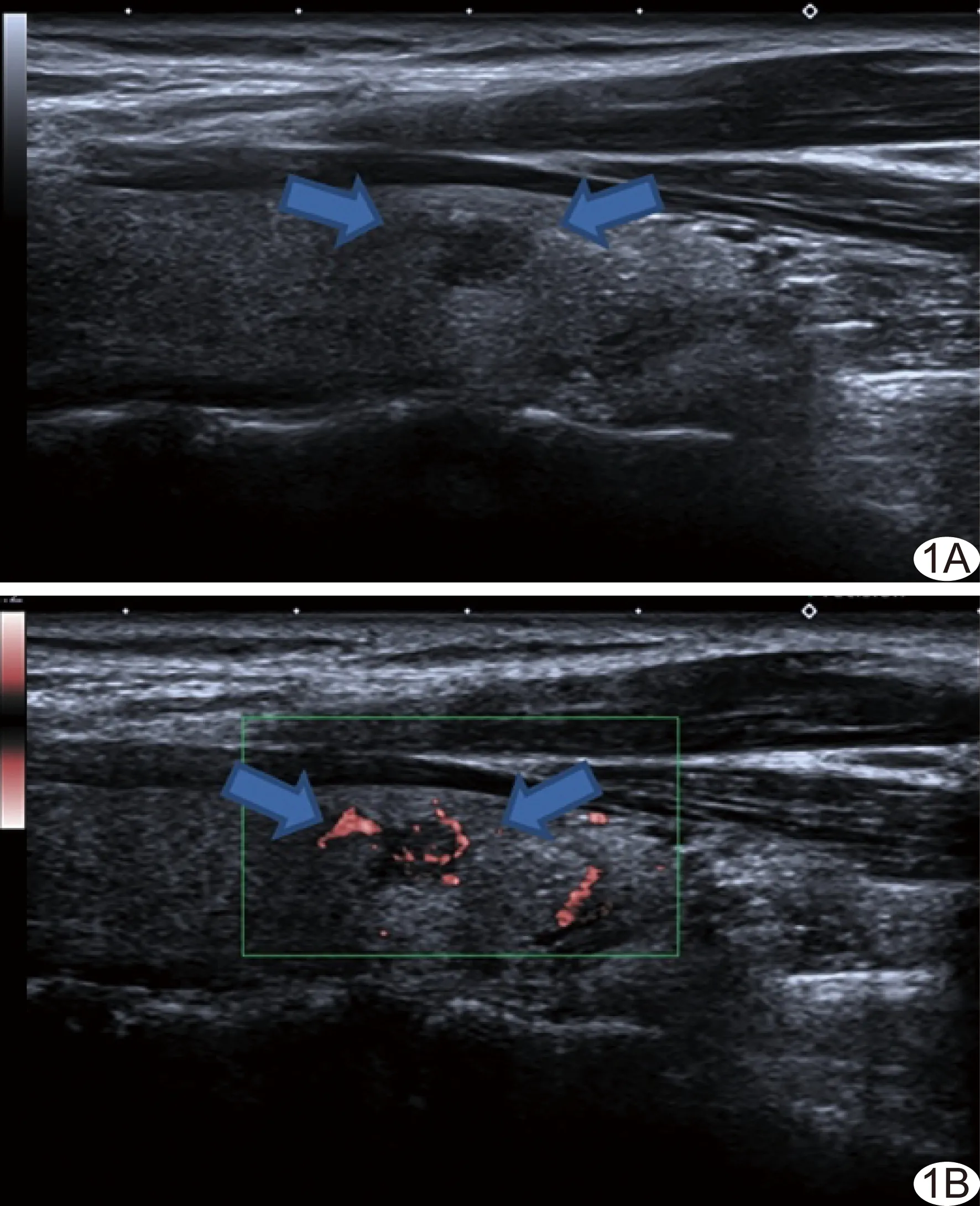
图1 患者女,43岁,甲状腺乳头状微小癌(箭) A.声像图显示甲状腺结节实性2分、低回声2分、宽度>高度0分、边缘光滑0分、无强回声0分,总分4分,归为TR 4类; B.SMI示结节内微小穿支血管,校正后归为TR 5类

表1 穿支血管与甲状腺结节的关系(个)
2.3 SMI校正前后ROC曲线及诊断效能比较 SMI校正前后TI-RADS分类诊断对于甲状腺良恶性结节差异均有统计学意义(P均<0.05),见表2。校正前后最佳截断值均为4.5,故定义TR 5类为阳性,TR 1~4类为阴性。SMI校正后的AUC高于校正前(Z=-2.616,P=0.009),敏感度也高于校正前(Z=-1.988,P=0.047),其余各诊断效能差异均无统计学意义(P均>0.05),见表3、图2。
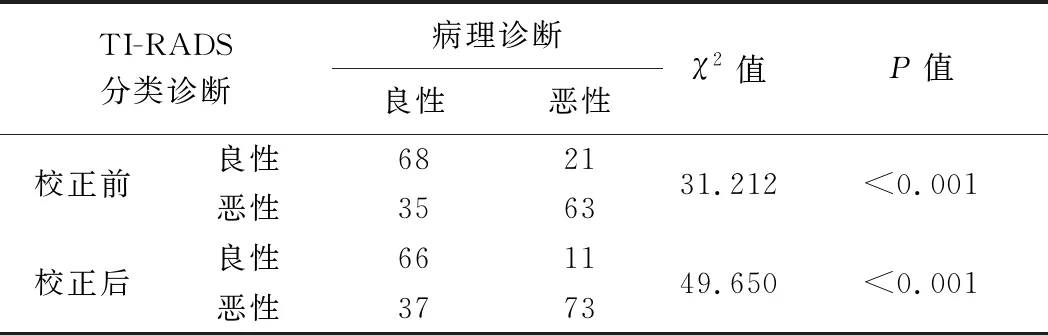
表2 SIM校正前、后TI-RADS分类诊断甲状腺结节与病理诊断比较(个)
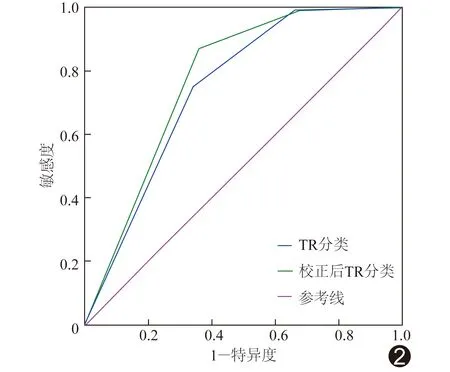
图2 SMI校正前后TI-RADS分类诊断甲状腺结节的ROC曲线
3 讨论
近年来,甲状腺癌发病率及死亡率上升已是成为全球性问题[6-7],故明确甲状腺结节良恶性的诊断标准尤为重要。自2009年以来,一些专业机构及学者陆续发表了不同版本的TI-RADS[8-10],直至2017年ACR制订甲状腺标准化风险分层系统,但目前对其诊断价值的研究结果尚不明确。有学者[11]认为该分类系统对恶性结节的敏感度高;也有学者[12]认为TI-RADS整体诊断效率良好,但低于其他风险分层。根据TI-RADS建议的风险分层,TR 1~5类恶性率分别为≤2%、≤2%、5%、5%~20%和≥20%。本研究将187个甲状腺结节分别归类于TR 1~5类,实际恶性率分别0、0、5.00%、37.74%和64.29%,得出TR 4的恶性率高于TI-RADS的结果,可能与入选人群总体恶性比例较高有关,有待扩大样本进一步验证。
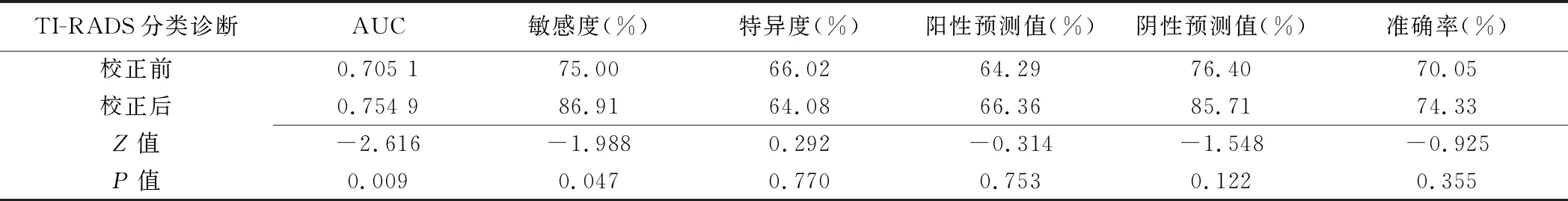
表3 SMI校正前后TI-RADS分类诊断效能比较
SMI又称“魔镜”技术,是对超声多普勒血流成像技术的颠覆性的发展和创新,具有高帧频、高空间分辨率和少运动伪像的特点。与常规超声相比,SMI显示甲状腺结节外周和内部微血管流动和血管分支更为详细、清晰,血管检出率高于常规彩色血流显像,也为超声造影提供了一种安全且低成本的替代方案,对鉴别诊断甲状腺良恶性结节具有一定价值[13]。本研究尝试利用SMI技术对TI-RADS进行校正,发现经SMI校正后各类别结节的实际恶性率与TI-RADS验证结果存在一定差距。有学者[14]解读TI-RADS后认为该系统恶性率低于以往分类研究,故无必要以只推荐的各分类恶性率来进行临床验证,相反应根据临床结果对该系统加以验证。上述观点直指问题核心,有待今后开展前瞻性研究加以探讨。
本研究据ROC曲线分析得出校正前后TI-RADS最佳诊断界点均为TR 5,与刘红等[15]的研究相符。黄于洁等[16]认为穿支血流可作为鉴别甲状腺良恶性结节的依据。SMI对穿支血管较常规彩色血流显像、能量多普勒血流显像更敏感,有望成为鉴别甲状腺良恶性结节的超声新指标。本研究在TI-RADS基础上联合SMI技术进行诊断,除特异度略有降低外,其他诊断效能指标均较单纯TI-RADS有所提升,且AUC和敏感度较前差异均有统计学意义,说明联合SMI技术能够更为准确地判断甲状腺结节的性质,可增强超声医师的诊断信心,并为临床选择治疗方案提供更为准确的参考。
本研究的不足之处:仅以有无穿支血管作为鉴别甲状腺良恶性结节的指标有失全面,对其权重有待进一步考量。
综上所述,SMI技术能显示甲状腺结节内的穿支血流,与TI-RADS结合可提高鉴别诊断甲状腺良恶性结节的价值;而TI-RADS恶性风险分层的价值尚待开展大样本前瞻性研究进一步观察。
