基于斑马鱼模型的熊果酸治疗非酒精性脂肪肝病的作用及其机制研究
2020-06-02范福玲陈月琴刘腊梅
范福玲,陈月琴,赵 美,刘腊梅
1漯河医学高等专科学校护理系,漯河 462000;2郑州大学内科教研室,郑州 450001
非酒精性脂肪肝病(nonalcoholic fatty liver disease,NAFLD)是肝脏脂肪代谢异常所导致的肝内三酰甘油(triglyceride,TG)蓄积过多的一种病理状态[1],以肝细胞内脂肪堆积为主的临床病理综合征。NAFLD已成为一项发病率较高的慢性疾病,我国NAFLD发病率为24.47%~29.70%,男性发病率高于女性[2],且发病率呈现上升趋势。NAFLD常见的危险因素主要是肥胖、血脂异常、糖尿病和代谢综合征[3],具有发病复杂的进程特点,从一开始的“第1次打击”导致的肝脏脂肪堆积;到“第2次打击”导致脂肪变性的肝细胞发生炎症、坏死最后导致肝纤维化、肝硬化[4]。NAFLD的危害性很大,但目前并没有研发出治疗NAFLD的特效药,NAFLD并不能被完全治愈,市场上最有效、最常见的治疗药物主要是具有降脂作用的他汀类药物,但是他汀类药物具有损伤神经系统和肝功能的作用[5]。鉴于NAFLD的现状,不少临床研究者发现一些天然植物具有治疗NAFLD的作用。
目前,国内外研究己经证实哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)介导脂质堆积的关键环节之一是mTOR的活化。其中,动物雷帕霉素靶蛋白复合体1(mTOR complex 1,mTORC1)调控脂质代谢信号及全身代谢稳态的平衡,参与代谢疾病的发生,例如:脂肪肝。mTOR在斑马鱼体内主要以mTOR复合物1(mTORC1)和2(mTORC2)两种形式存在,其中mTORC1参与脂肪细胞的活化,脂肪的生成和葡萄糖的摄取,mTORC2的活性与胚胎发育,细胞骨架重建,细胞迁移,蛋白质翻译和修饰有关[6]。mTORC参与众多通路之一的mTORC/SREBP-1c信号通路,是调节细胞脂质代谢的关键途径,与NAFLD的发病密切相关[7],固醇调节元件结合蛋白-1C(sterol regulatory element binding protein-1c,SREBP-1c)作为mTOR的下游基因,主要参与脂肪合成相关基因的表达,并受胰岛素、葡萄糖等因素的调控,是代谢综合征中重要的基因调控连结点[8],乙酰辅酶A羧化酶(acetyl-coAcarboxylase,ACC1)和脂肪酸合成酶(acidsynthase,FASN)作为SREBP-1c的下游基因,与脂肪合成有关,从而影响NAFLD的发病。
熊果酸(ursolic acid,UA),又名乌苏酸,作为天然植物山楂、连翘、构骨叶等天然植物的主要成分,具有抗氧化、抗炎、抗肿瘤、抗微生物、抗糖尿病、免疫调节、保肝、调脂、减肥、抗动脉粥样硬化作用[9],并且具备活性强、安全性高、毒性低等特性。因此,越来越多地国内外学者开始关注UA对肝脏保护作用方面的研究,加上UA降血脂的作用近几年被频繁报道证实[10],其在NAFLD方面的研究也逐渐引以为重视,有研究认为,UA治疗NAFLD的机制与脂质代谢、抑制炎症反应,改善胰岛素抵抗和氧化应激有关[11,12],可以说UA对NAFLD的治疗涉及了其整个范围。斑马鱼是研究发育和疾病的优势生物模型,具有透明、高繁殖力和发育快的特点,深受科学实验的欢迎。其肝胆系统在受精后5天(dpf)时发育完全,成年斑马鱼和幼虫斑马鱼都容易发生肝脂肪变性,已有几种肝脂肪变性的药理和遗传模型在该物种中建立了起来。其中,Sapp等[13]以葡萄糖作为对照,使用4%的果糖对斑马鱼幼鱼进行模型构造,并在48 h后成功建立斑马鱼NAFLD模型,操作简单易行,成功率高,且重复性较好。有研究结果表明,高果糖饮食可独立诱导斑马鱼肝脏脂肪变性,促进肝脏脂质堆积[14]。
斑马鱼幼鱼全体通透的优点,非常适合进行肝脏疾病的研究,在显微镜下可直接观察到肝脏病理的变化。因此,为了使UA的治疗研究更加清晰简便,我们采用斑马鱼模型拟对UA进行深入的治疗作用机制研究,以便为UA的疗效和机制研究提供一种新型简单的方案,也从斑马鱼模型上对UA治疗NAFLD的作用及机制进行可行性的验证。

图1 熊果酸的化学结构
本研究采用果糖对斑马鱼进行NAFLD模型的构造,根据前期的实验研究基础,选取了5、10、20 μg/mL的UA作为治疗斑马鱼非酒精性脂肪肝的低、中、高剂量的治疗浓度,通过对各组肝脏油红染色,体脂含量的测定和肝脏病理切片的观察,确认药物对NAFLD的治疗效果,再通过RT-qPCR测定mTOR、SREBP-1c、ACC1和Fasn mRNA的含量变化,以此进一步阐释UA对非酒精性脂肪肝斑马鱼模型的保护作用机制。
1 材料
1.1 试剂和仪器
油红O(Sigma,美国),苏木素和伊红(Sigma,美国),无水乙醇和1,2-丙二醇(国药集团化学试剂有限公司,中国),果糖和葡萄糖(Sigma,美国),熊果酸(Sigma,批号为U6753,纯度为98.67%),甘油三酯(TG)和总胆固醇(TC)检测试剂盒(南京建成生物制品公司,中国),Trizol试剂(Invitrogen),RNase ddH2O(Solarbio,北京),反转录试剂盒和SYBR Premix TaqTMⅡ(Til RNaseH Plus)(TaKaRa,日本),光学显微镜(Olympus,日本),酶标仪(上海科华实验系统有限公司,中国),冰冻切片机(莱卡,德国),基因扩增仪(Bio-rad,美国)。引物合成由北京擎科生物科技有限公司完成,其引物序列见表1。
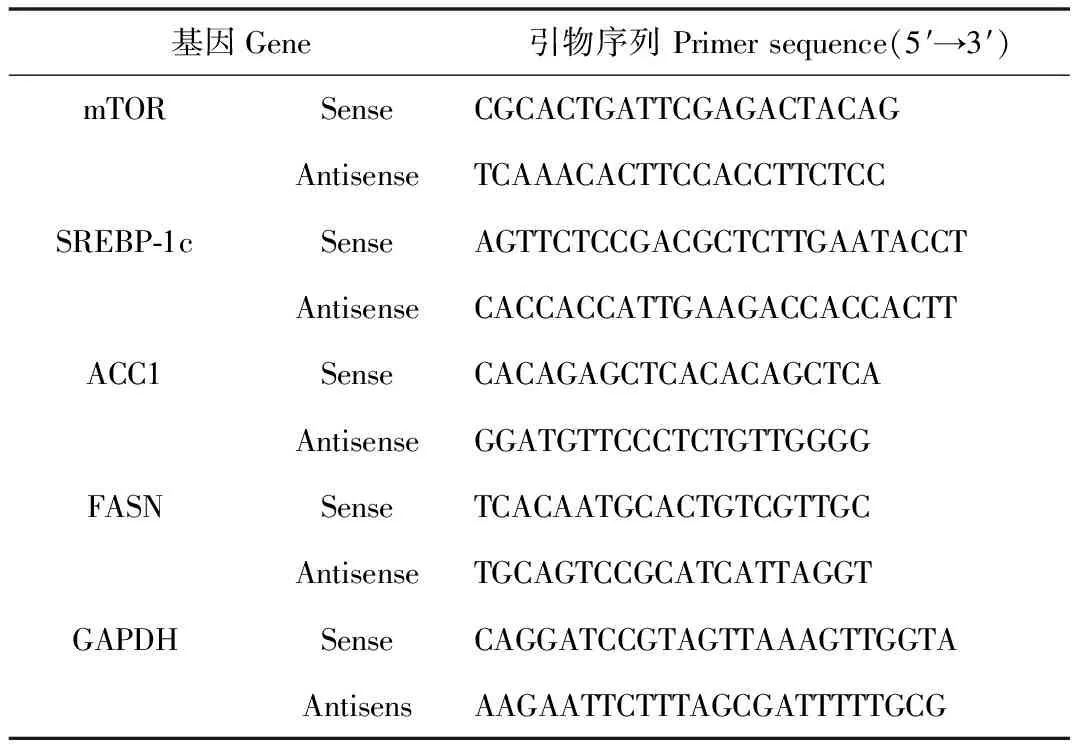
表1 PCR 引物序列及扩增片段大小
1.2 实验动物
野生型AB品系斑马鱼(购自上海费曦生物科技有限公司),挑选正常雌雄成鱼交配产卵,收集受精卵培育5天,孵化的幼鱼用于实验。饲养基础用水为28 ℃,每1 L反渗透水中加入200 mg速溶海盐,电导作用为480~510 μs/cm;pH为6.9~7.2;硬度为53.7~71.6 mg/L CaCO3。
1.3 斑马鱼模型的构建及分组
将5天大的斑马鱼随机分为4组,每组40只,分为正常对照组、模型组、熊果酸高剂量组、熊果酸中剂量组、熊果酸低剂量组,放于培养皿中培育。其中正常组给予3.5%葡萄糖,模型组给予3.5%果糖,将熊果酸溶解在3.5%的果糖溶液中,使其浓度达到20、10、5 μg/mL作为熊果酸高、中、低剂量组进行给药,持续96 h。
2 方法
2.1 斑马鱼肥满度的测定
从各组取出6尾幼鱼,用1%的Tricane将幼鱼进行麻醉,待检测斑马鱼禁食24 h后,用滤纸吸干鱼体表面的残留水分,测体长(cm)、体质量(g)、计算肥满度(condition factor)。
肥满度=体质量×100/体长3
2.2 整体油红O染色
收集斑马鱼于染色皿中,10%的多聚甲醛固定过夜,丙二醇从低浓度到高浓度(20%、50%、80%)依次进行渗透,0.5%油红避光孵育过夜。同样浓度丙二醇从高浓度到低浓度洗净背景,于20%丙二醇4 ℃冰箱保存。每组随机挑选15条,Olympus szx10体式显微镜下观察肝脏脂肪变性情况,并进行拍照记录。
2.3 TG、TC含量的测定
分别从各组中随机取40尾幼鱼,按照重量(g)∶体积(μL)=1∶10加入生理盐水并匀浆,在4 ℃,2 500 rpm条件下离心10 min,取上清液,使用甘油三酯测试盒和胆固醇测试盒测定TG和TC的含量,实验重复3次。
2.4 肝脏苏木素-伊红染色(HE)染色
4%多聚甲醛固定幼鱼过夜,脱水、包埋制成蜡块标本,4 μm厚切片后脱蜡,苏木素染色10 min,浸入1%盐酸酒精中分化10 s左右,之后放入伊红染液中染色10 min,梯度酒精脱水,二甲苯透明,中性树脂封片。显微镜下观察肝脏病理变化,拍照并保存。
2.5 mTOR、SREBP-1c、ACC1和Fasn mRNA表达水平检测
设计mTOR、SREBP-1c、ACC1、Fasn和GAPDH基因引物,见表1。分别从各组中随机取70尾幼鱼,用PBS洗净,Trizol试剂提取总RNA,D260/D280为1.80左右。根据反转录试剂盒将各样品RNA进行反转录。荧光定量RT-qPCR反应体系(20 μL),SYBR Premix Ex TaqTMⅡ扩增条件为:预变性95 ℃ 5 min,40个循环(95 ℃ 20 s,57 ℃ 25 s,72 ℃ 25 s),反应结束后制备溶解曲线。采用2-ΔΔCT法分析荧光定量结果,实验重复3次,用统计学软件进行单因素方差分析。
2.6 统计学方法
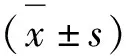
3 结果
3.1 斑马鱼肥满度的测定
模型组体长(P<0.05)、体重(P<0.05)和BMI值(P<0.05)显著高于对照组和熊果酸组(表2)。

表2 各组幼鱼体重、体长、肥满度的比较
注:与模型组比较,*P<0.05,**P<0.01。
Note:Compared with the model group,*P<0.05,**P<0.01.
3.2 斑马鱼整体油红O染色
油红O染色显示相比对照组,果糖处理后的斑马鱼肝脏区域油红O着色明显加深,提示肝脏内有大量的脂滴沉积,除此之外,肝脏外形呈现不同程度的肿大(如图2,黄色箭头指向肝脏),说明果糖处理能导致肝脂肪变性,给与熊果酸后,肝脏染色变浅,肝脏肿大的程度减轻,说明熊果酸可改善肝脏脂肪变性和肿大现象。

图2 斑马鱼整体油红O染色
3.3 斑马鱼整体TG和TC含量的测定
与正常对照组对比,模型组斑马鱼体内TG和TC含量升高,差别有统计学意义(P<0.05)。与模型对照组对比,熊果酸组TG和TC含量降低,差别有统计学意义(P<0.05)。
3.4 斑马鱼肝组织HE染色结果
结果显示在果糖喂养组相对空白组可观察到较大的脂肪性空泡的形成,而熊果酸组相对于模型果糖组,脂肪性空泡明显减小,肝细胞排列恢复正常,随着熊果酸浓度的增加,肝脏脂肪性空泡减小,图中红色箭头指向肝脏(图3)。

表3 各组喂养96 h后幼鱼体脂的变化
注:与模型组比较,*P<0.05,**P<0.01。
Note:Compared with the model group,*P<0.05,**P<0.01.
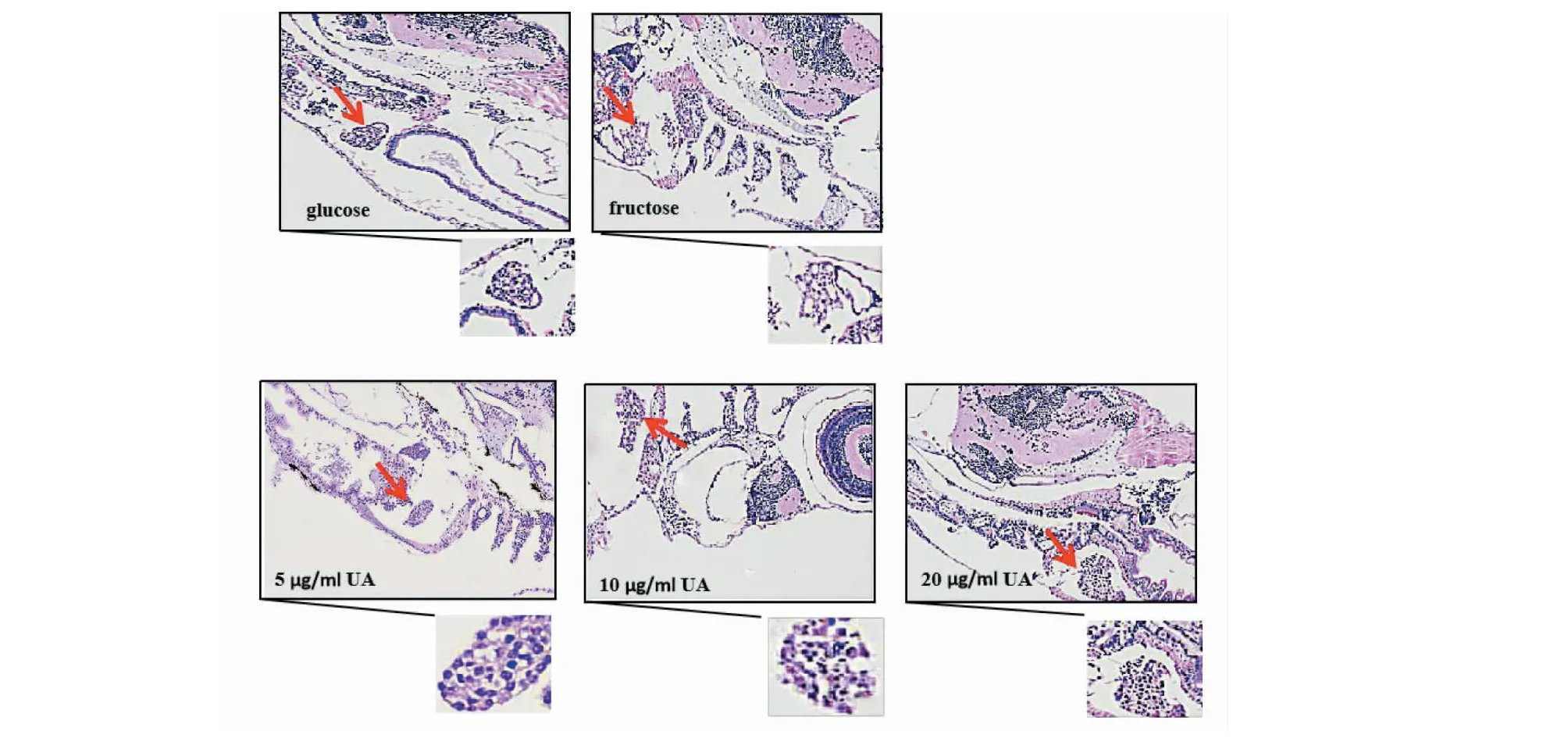
图3 各组幼鱼肝脏病理组织情况(×400)
3.5 斑马鱼体内mTOR、SREBP-1c、ACC1和Fasn mRNA的表达水平结果
与空白组对比,模型组的mTOR、SREBP-1c、ACC1和Fasn mRNA的表达量均上升,差异具有统计学的意义(P<0.01),与模型组相比,熊果酸组的mTOR、SREBP-1c、ACC1和Fasn mRNA的表达量均降低,差异具有统计学的意义(P<0.05),由此可知,熊果酸可显著降低果糖诱导的NAFLD斑马鱼体内mTOR、SREBP-1c、ACC1和Fasn mRNA的表达。
4 讨论与结论
非酒精性脂肪肝病目前已成为严重危害人类健康的一类慢性疾病,随着NAFLD发病率的增高,NAFLD的治疗已经逐渐被引起重视。目前认为,NAFLD的发病与脂质代谢异常有关。TG参与到了NAFLD脂质代谢的异常中,肝脏是合成TG的主要部位,当体内的TG合成增多时,高脂饮食、高脂血症和脂肪组织动员增加引起的游离脂肪酸进入肝脏增多,并在肝脏转化合成TG酯,导致肝脏脂质的堆积,从而引发NAFLD[15]。
有关报道称[16],熊果酸可通过降低肝脏及血清中TG、TC的含量,并抑制炎症因子的表达,达到治疗非酒精性脂肪肝的作用。在本实验中,熊果酸可有效降低斑马鱼体内TG、TC的含量,通过RT-qPCR实验发现,熊果酸降脂主要是通过改善脂质代谢途径,mTOR参与体内多种生理反应,其中就包括脂质代谢,有研究表示,mTOR是胰岛素刺激SREBP-1c表达所必需的一个靶点受体,可直接激活SREBP-1c的表达,而mTORC1或是通过促进SREBP-1c的裂解和核蓄积来诱导SREBP-1c的活性[17]。在mTOR调控SREBP-1c,从而调控与脂肪合成相关的靶点基因ACC1和Fasn的表达过程中,mTOR作为肝脂肪生成的主要受体,是肝胰岛素抵抗与高血糖和高血脂相关的分子机制统一整合的重要发展机制。SREBP-1c为调控脂质合成的关键的转录因子,其靶向的脂质合成相关酶包含ACC1和Fasn。SREBP-1c、ACC1和Fasn的表达均在TG的合成中起着主要作用[18],因此,调控mTOR的活性可以调节下游一系列脂质合成相关因子的转录与表达,提示mTOR可能为NAFLD治疗的一个潜在关键作用受体。
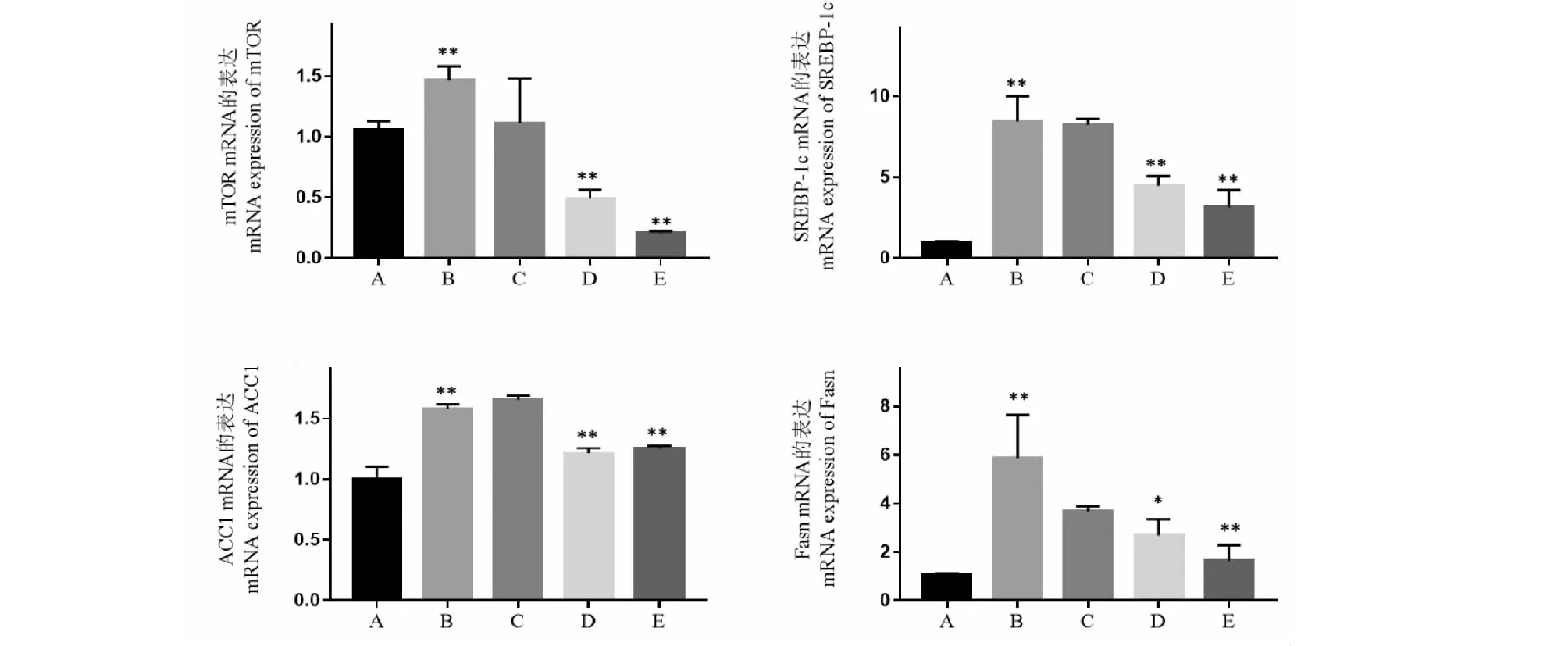
图4 熊果酸对斑马鱼mTOR、SREBP-1c、ACC1、Fasn mRNA表达水平的影响
近几年,斑马鱼作为一种新型的模式动物,在疾病的研究方面已愈发成熟。斑马鱼具有繁殖迅速,在胚胎和幼体时期身体透明,因此适合基于疾病表型的高通量筛选[19]。常规的动物模型,例如:大鼠、小数、猪、狗、猴,具有实验周期长、成本高的特点,对药物研发的进度有一定的影响,由于斑马鱼模型既有哺乳动物实验预测性高、可比度高的优点,也有实验快速、高效、费用低的优势。因此,斑马鱼逐渐成了科学研究的理想疾病模式动物。斑马鱼NAFLD的建立,近几年也被大量报道,Sapp等人利用果糖成功创建斑马鱼NAFLD模型,造模时间仅48 h,方法简便快速,然而改方法用在小鼠模型上需要10周[20]。而高脂饲料对斑马鱼NAFLD的构建只需要10天[21],这一模型在大鼠模型上需要4周[22]。由此可见,斑马鱼在NAFLD模型的构造上,相对常用的大鼠、小鼠模型,具有高速、高效的优势。
综上,熊果酸对NAFLD有良好好的治疗作用,治疗机制与调节脂质代谢信号通路有关,并且这一治疗效果在斑马鱼上的到了良好的验证,也为熊果酸治疗NAFLD的深入研究提供了一种简单易行的方法。
