磁性氧化石墨烯的制备及用于乳制品中邻苯二甲酸酯类塑化剂的测定
2020-06-01邢翠娟董丽丽申文龙边晓巧
于 玲,邢翠娟,何 旭,董丽丽,赵 哲,申文龙,边晓巧
(邢台学院化学与化工学院,河北 邢台 054001)
邻苯二甲酸酯(phthalate esters,PAEs)是一类人工合成有机化合物,添加后可使微粒分子更均匀分布,因此具有增加延展性、柔韧性和弹性的功效,加之其成本低廉,常作为增塑剂和软化剂应用于塑料工业。然而,该类物质会干扰神经和内分泌系统的正常调节,部分PAEs及其主要代谢物和降解产物可引起多种器官系统的毒性作用,包括肝脏、生殖道、肾脏和心脏,这引起了人们对PAEs导致生殖和发育不良可能性的极大关注[1]。近年来,琳琅满目的乳制品因其营养美味走进寻常百姓家。然而,乳制品大多由塑料盒或塑料袋包装,而PAEs具有脂溶性,很容易从塑料包装迁移到乳制品中;另外,在乳制品的生产过程中不可避免的会使用塑料工具进行采奶、加工和贮存,这些环节都会导致PAEs溶入乳制品中进而危害人体健康。因此,我国于2008年针对不同种类添加剂在包装材料中的使用和管控发布了相关标准GB 9685—2008《食品容器、包装材料用添加剂使用卫生标准》[2],其中对部分PAEs从包装材料到食品的特定迁移量做了严格的规定。
氧化石墨烯(graphene oxide,GO)是一种可以通过天然石墨氧化合成的层状化合物,其基面和边缘装饰有各种含氧官能团,可与有机分子间形成π-π作用,具有新颖的质量迁移特性,在吸附和分离方面潜力巨大。磁性材料具有快速分离性能,引入磁性材料是提高分离实验效率的重要手段,将GO和磁性材料Fe3O4结合起来形成一种新型复合材料,即磁性氧化石墨烯(magnetic graphene oxide,Fe3O4/GO),其兼具GO的超强吸附性能和磁性材料的快速分离性能,可作为一种高萃取率的新型材料。近年来,Fe3O4/GO在分析化学领域的应用越来越广泛。Wu Jianrong等[3]将Fe3O4/GO与离子液体相结合,提取、测定生物样品中5 种头孢菌素;Guo Lihui等[4]将Fe3O4/GO与分子印记聚合物结合用于富集水中6 种PAEs;Lamei等[5]采用深度共晶溶剂改性Fe3O4/GO用于测定尿和血浆中的美沙酮;Zhang Xiaoting等[6]采用Fe3O4/GO作为基质分散固相萃取的吸附剂从食物样品中提取5 种偶氮染料。
目前,食品中PAEs的样品前处理方法主要有固相萃取法[7-8]、固相微萃取法[9-12]和分散液液微萃取法[13-15]等。这些方法或操作耗时费力,或有机试剂消耗量大污染环境,或只适用于简单基质样品,它们通常涉及许多步骤,导致分析物的损失。因此,样品前处理的发展趋势是集中开发更简单、更可靠、更快速、更经济的方法。乳制品基质复杂,脂肪和蛋白质含量高,能否高效去除这些杂质是实验成败的关键。由Anastassiades等[16]开发的QuEChERS方法已成为测定不同样品基质中待测物的一种非常流行的技术。该方法包括2 个连续步骤:盐析液液萃取和分散固相萃取净化,其核心原理是根据目标化合物的分配机制,通过加入萃取剂和吸附材料等净化剂去除杂质。该方法取代了传统方法中许多复杂的操作步骤,分析成本低,只需要少量溶剂和简单的玻璃容器,时间成本低,工作量小。目前QuEChERS方法已普遍应用于果蔬、粮谷、水产品及环境中农药残留的检测[17-24]。
本实验以石墨为原料,采用Hummers方法和化学共沉淀法逐步合成Fe3O4/GO。通过傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)、X射线衍射(X-ray diffraction,XRD)和拉曼光谱(Raman spectroscopy,RS)等方法对其结构进行表征,利用Fe3O4/GO改进QuEChERS前处理技术结合气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)联用实现对乳制品中16 种PAEs的定性和定量分析。本研究基于Fe3O4/GO的特性改进QuEChERS技术,充分发挥Fe3O4/GO对牛奶基质较强的去除能力和对目标组分有效的保留能力。Fe3O4/GO在完成净化程序后可以通过施加外部磁场替代传统的离心步骤达到吸附剂从溶液中快速分离的效果,该方法简便快捷、准确可靠,尤其适合用于乳制品这样基质复杂的样品分析。
1 材料与方法
1.1 材料与试剂
实验所用纯牛奶、酸奶、乳饮料等20 种乳制品均购自邢台某超市。
16 种PAEs混合标准品(1 000 μg/mL,批号1701066):邻苯二甲酸二甲酯(dimethyl phthalate,DMP)、邻苯二甲酸二乙酯(diethyl phthalate,DEP)、邻苯二甲酸二异丁酯(diisobutyl phthalate,DIBP)、邻苯二甲酸二丁酯(dibutyl phthalate,DBP)、邻苯二甲酸二(2-甲氧基)乙酯(dimethylglycol phthalate,DMEP)、邻苯二甲酸二(4-甲基-2-戊基)酯(bis(4-methyl-2-pentyl)phthalate,BMPP)、邻苯二甲酸二(2-乙氧基)乙酯(bis(2-ethoxyethyl) phthalate,DEEP)、邻苯二甲酸二戊酯(dipentyl phthalate,DPP)、邻苯二甲酸二己酯(di-n-hexyl phthalate,DNHP)、邻苯二甲酸丁基苄基酯(butyl benzyl phthalate,BBP)、邻苯二甲酸二(2-丁氧基)乙酯(bis(2-butoxyethyl) phthalate,DBEP)、邻苯二甲酸二环己酯(dicyclohexyl phthalate,DCHP)、邻苯二甲酸二(2-乙基)己酯 (di(2-ethylhexyl) phthalate,DEHP)、邻苯二甲酸二苯酯(diphenyl phthalate,DPHP)、邻苯二甲酸正辛酯(di-n-octylo phthalate,DNOP)、邻苯二甲酸二壬酯(dinonyl phthalate,DNP) 北京坛墨质检科技有限公司。
N-丙基乙二胺(primary secondary amine,PSA)(40~60 μm) 武汉市伟琪博星生物科技有限公司;无水MgSO4、浓硫酸、石墨粉 天津市河东区红岩试剂厂;乙腈、KNO3、KMnO4、30% H2O2、FeCl3·6H2O、FeCl2·4H2O、氨水(均为分析纯) 天津市永大化学试剂有限公司。
1.2 仪器与设备
GCMS-QP2010 GC-MS联用仪、XRD-6100射线衍射仪 日本岛津公司;WQF-510A FTIR 北京瑞利分析仪器有限公司;INVIA显微共焦拉曼光谱仪 英国Renishaw公司;SC-3612低速离心机 安徽中科中佳科学仪器有限公司;KQ-50E超声波清洗器 昆山市超声仪器有限公司;Milli-Q超纯水仪 美国Millipore公司。
1.3 方法
1.3.1 Fe3O4/GO的制备
采用Hummers法[25]制备GO。将盛有120 mL浓硫酸的烧杯放置到预先准备好的冰水浴中,将4 g石墨粉和2 g KNO3混合,缓慢加入到浓硫酸中,调节搅拌速度,均匀搅拌30 min。分批缓慢将12 g KMnO4加入浓硫酸中,为防止氧化以应剧烈,整个过程完全在冰水浴条件下进行,继续搅拌2 h。为了使其充分氧化,把容器放入预热好的40 ℃恒温水浴锅中,以应24 h。以应结束后,依次加入400 mL超纯水和30 mL双氧水,混合均匀,静置4 h,洗涤沉淀至中性,真空干燥制得GO。
采用化学共沉淀法制备Fe3O4/GO[26]。在500 mL超纯水中加入1.5 g GO,超声30 min;另在500 mL超纯水中加入10 g FeCl3·6H2O和4 g FeCl2·4H2O超声1.5 h,使其完全溶解。各取上述2 种溶液各200 mL混匀,再加入30%的氨水调节pH值至9~10,超声2 h后静置,洗涤沉淀至中性,真空干燥制得Fe3O4/GO。
1.3.2 GC条件
色谱柱:RXI-5si1MS(30 m×0.25 mm,0.25 μm);程序升温:80 ℃保持1 min,以10 ℃/min升温至220 ℃保持1 min,以5 ℃/min升温至280 ℃保持10 min;载气(He)流速1.0 mL/min;进样口温度280 ℃;恒压模式;进样量1 μL;不分流进样。
1.3.3 MS条件
离子源温度230 ℃;离子源接口温度280 ℃;定性采用全扫描模式,质量扫描范围40~400m/z;定量采用选择离子监测模式(selected ion monitoring,SIM);溶剂延迟3 min;16 种PAEs的保留时间和SIM参数见表1。

表1 16 种PAEs的保留时间和SIM参数Table 1 Retention times and selected ion monitoring parameters for 16 PAEs
1.3.4 标准溶液的配制
取1 000 μg/mL的PAEs混合标准溶液0.1 mL,用乙腈配制成质量浓度为10 μg/mL的标准储备液,置于4 ℃冰箱保存。将标准储备液分别用乙腈和空白基质溶液稀释至20、50、100、200、500、1 000 μg/L的标准工作溶液,现用现配。
1.3.5 样品前处理
准确称取1.000 0 g试样于10 mL玻璃离心管中,加入2 mL乙腈,充分振荡,再加入0.2 g NaCl,明显观察到盐析现象,然后3 000 r/min离心3 min,收集上清液,待净化。取上述乳制品上清液1 mL,分别加入30 mg PSA、25 mg Fe3O4/GO、100 mg无水MgSO4,超声3 min,通过外加磁场使之分离,取1 μL注入GC-MS。
1.3.6 基质效应(matrix effect,ME)
通过GC-MS分别测定乙腈、空白基质标准工作液的PAEs离子响应强度,从而得到2 种系列标准工作液的标准曲线,通过两者标准曲线斜率比得出ME。计算公式如下:

式中:K乳制品基质为乳制品空白基质标准曲线斜率;K乙腈为乙腈溶剂标准曲线斜率。
2 结果与分析
2.1 材料表征
2.1.1 Fe3O4/GO的FTIR分析
由图1可知,3 397 cm-1处为—OH的伸缩振动峰,说明—OH与邻近的水分子中氧原子生成了氢键。曲线于1 211、1 463 cm-1以及1 587 cm-1附近出现的3 个峰,分别归属于GO的C—O—C、COO-和C=O的伸缩振动。此外,在576 cm-1处还可观察到由Fe—O伸缩振动所引起的Fe3O4特征峰,由此可以证明Fe3O4已经成功负载在GO上。
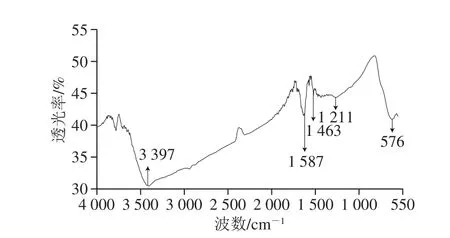
图1 Fe3O4/GO的FTIR图Fig. 1 FTIR spectrum of Fe3O4/GO
2.1.2 Fe3O4/GO的XRD分析
通过XRD对合成的GO和Fe3O4/GO结构进行分析对比。由图2可知,虚线显示在2θ为10.6°处观察到了GO所具有的典型单个衍射峰。实线显示Fe3O4/GO在2θ为30.3°、35.5°、43.2°、53.5°、57.3°和62.8°处有显著的波峰,这与Fe3O4纳米粒子的XRD图谱一致[27],说明该复合材料中已成功引入Fe3O4。同时,在2θ为10.6°处没有发现GO的特征衍射峰。这是由于Fe3O4的影响使GO的有序堆积受到了破坏从而导致衍射峰消失。XRD分析结果可进一步表明该复合材料为Fe3O4/GO。

图2 GO和Fe3O4/GO的XRD图Fig. 2 XRD patterns of GO and Fe3O4/GO
2.1.3 Fe3O4/GO的RS分析
RS是表征GO及其共价衍生物的最有效方法之一。如图3所示,2 条曲线在1 300 cm-1和1 600 cm-1附近均出现2 个明显的吸收峰,前者为GO的D峰而后者则对应于其G峰。两者的相对强度之比R(ID/IG)可以映材料微观结构的无序化程度。普遍认为,R值越高,材料中所存在的缺陷就越多,无序化的程度也越高[28]。本研究中,Fe3O4/GO的R值为2.3,相较于GO的R值(1.4)有所升高,表明经过磁性处理后引起sp2平面域产生更多的缺陷致使其结构域紊乱,这可以理解为GO中引入大量Fe3O4所致。

图3 GO和Fe3O4/GO的RS图Fig. 3 Raman spectra of GO and Fe3O4/GO
2.2 提取剂的选择
目前对样品中PAEs使用较多的提取试剂为乙腈、正己烷和乙酸乙酯3 种。本研究采用以上3 种试剂对加标乳制品样品进行分析检测。结果表明,采用乙腈提取时塑化剂回收率较高,达到64.4%~97.6%;采用正己烷提取时回收率偏低,为58.3%~73.6%;而乙酸乙酯对乳制品中蛋白质的提取量较大,杂质干扰严重,且气味刺鼻,故选取乙腈作为提取剂。在后续操作中NaCl作为盐析剂使乙腈与水层明显分离,无乳化现象,供进一步净化使用。
2.3 净化剂用量的选择
在QuEChERS净化中,考察吸附剂PSA、无水MgSO4以及Fe3O4/GO的用量对PAEs回收率的影响。在考察一个条件时,其他条件均保持不变且采用已优化的结果。
2.3.1 PSA用量的优化
虽然乳制品中大多数蛋白质已经在乙腈提取时去除,但仍会有少量蛋白质和脂肪酸被萃取到乙腈提取液中。基于PSA对有机酸、脂肪酸有较强的吸附性,分别考察PSA用量为10、20、30、40、50 mg时,对PAEs回收率的影响。结果表明:PSA用量为10、20 mg时,部分PAEs回收率低于50%;随着PSA用量的增加,回收率明显提高,当PSA用量为30 mg时,回收率达到最优为65.4%~116%;继续增加PSA用量,会导致DEHP的回收率偏高为125%,故PSA用量选择30 mg。
2.3.2 无水MgSO4用量的优化
无水MgSO4吸水能力比较强,且与有机物不发生以应,故可用于除去基质溶液中的水分。考察无水MgSO4用量为100、150、200 mg时,对PAEs回收率的影响。无水MgSO4的用量为150、200 mg时,DEP、DBP两种塑化剂回收率均大于140%;而用量为100 mg时,16 种PAEs回收率为71.9%~118.4%,故无水MgSO4用量选择100 mg。
2.3.3 Fe3O4/GO用量的优化
采用Fe3O4/GO作为新型杂质吸附剂改进QuEChERS方法,在获得满意回收率的同时也达到了良好的除杂效果。在最佳前处理条件下,净化前后纯牛奶空白基质标准添加(500 μg/L)总离子流色谱图见图4。经净化处理后杂质峰明显变少且对16 种目标组分有更大的保留。同时,借助外加磁场可以使吸附剂从溶液中快速分离,有效减少了前处理的时间。考察Fe3O4/GO用量分别为10、15、25、40 mg时,对PAEs回收率的影响。结果表明,随着Fe3O4/GO用量的增加,16 种PAEs回收率逐渐升高。但用量为10、15 mg时,BMPP、DBEP和DEHP 3 种塑化剂回收率低于60%;用量为25、40 mg时回收率在78%~112%之间,且两者无太大差异,为节约成本,故Fe3O4/GO用量选择25 mg。

图4 净化前(A)、净化后(B)纯牛奶空白基质标准添加(500 μg/L)总离子流色谱图Fig. 4 Total ion current chromatograms of PAEs extracted from puremilk blank matrix with standard addition (500 μg/L) before (A) and after (B) purification
2.4 样品ME
由于样品中存在部分基质,会对待测物造成增强或抑制,将乙腈与纯牛奶空白基质溶液分别配制的标准溶液进行检测,按照1.3.6节方法,将两者的响应值相比较,结果见表2。16 种PAEs表现出不同程度的基质增强效应,ME为1.15~1.56,为消除纯牛奶基质的影响,采用空白基质标准曲线进行研究。
2.5 线性范围及检出限
以空白基质标准溶液浓度为横坐标,峰面积为纵坐标,得到标准曲线方程,16 种PAEs在20~1 000 μg/L具有良好的线性关系,R≥0.998 4。按3 倍信噪比计算得到16 种PAEs的检出限为0.5~2.5 μg/kg,按10 倍信噪比计算得到其定量限为2.0~7.5 μg/kg,具体参数见表2。
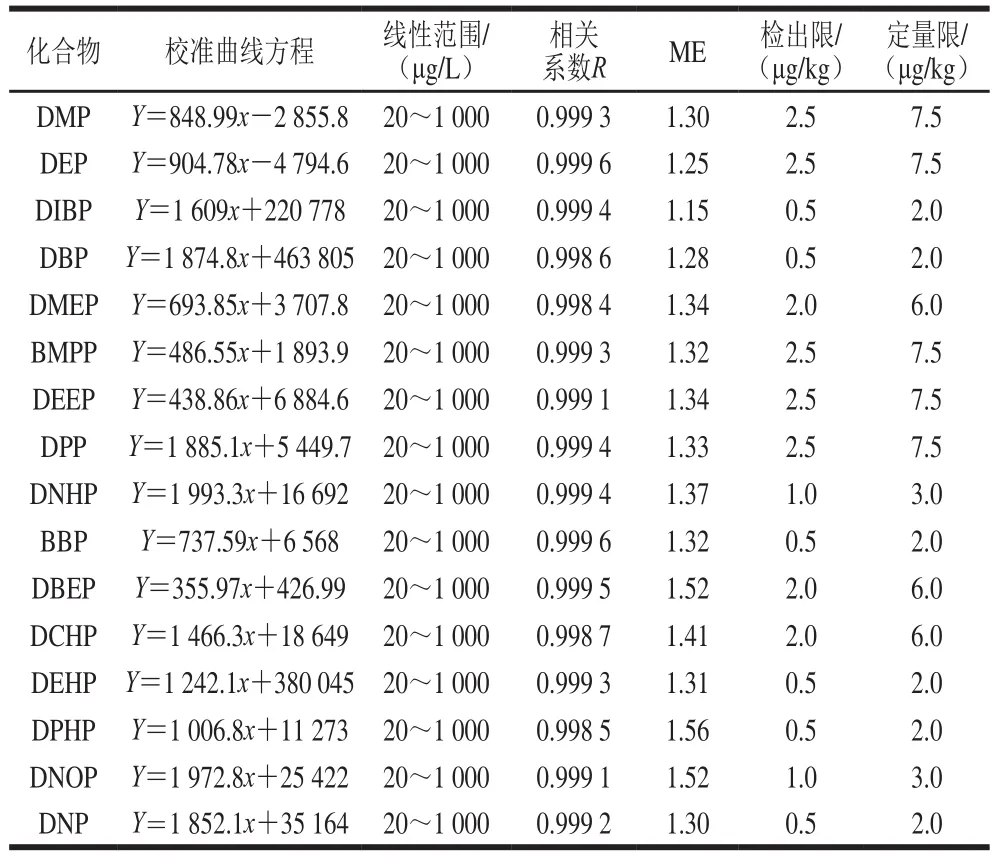
表2 线性系数、ME、检出限及定量限Table 2 Linearity parameters, detection limits and quantitation limits
2.6 准确度和精密度测定结果
按照最佳前处理条件,在纯牛奶空白样品中进行加标回收率实验,分别添加3 个水平(50、100、200 μg/kg)的16 种PAEs混合标准溶液,每一浓度平行实验6 次,结果如表3所示。标准添加回收率在85.7%~117.7%之间,相对标准偏差不大于7.6%,准确度精密度良好,可满足乳制品中16 种PAEs的日常监测。

表3 加标回收率和精密度实验(n=6)Table 3 Recoveries and precision of 16 PAEs from spiked blank samples (n= 6)

续表3
2.7 与其他方法的比较
本实验与文献报道的方法进行比较,结果见表4。本实验有机试剂用量少,每处理1 g样品,采用分散液液微萃取方法,需要有机试剂约4.6 mL;采用经典QuEChERS方法,需要有机试剂约4 mL;采用本实验方法仅需2 mL乙腈,绿色环保。其次,本实验净化剂用量少,除杂效果好,节约实验成本;最后,快速的磁性分离取代了传统的离心,节约了时间成本。

表4 本实验方法与其他文献方法比较Table 4 Comparison of this method with existing methods in the literature
2.8 实际样品的测定结果
选用最佳前处理条件对实际样品进行检测,对市售的20 种纯牛奶、酸奶、乳饮料进行分析。测定结果表明,20 种乳制品均含有DBP和DIBP,其中DBP含量在28.9~102.8 μg/kg之间,低于国家标准规定的限定值0.3 mg/kg[2],DIBP含量在53.3~83.8 μg/kg之间,而DIBP国家暂无明确的允许迁移限量。部分乳制品中含有DEHP,含量为42.9~251.8 μg/kg,低于国家标准规定的迁移量1.5 mg/kg[2]。
3 结 论
本研究成功制备并表征了Fe3O4/GO并将其用于QuEChERS前处理技术,充分发挥了两者磁分离和净化的优势,再结合GC-MS建立了对乳制品中16 种PAEs的分析检测方法。该方法的平均回收率为85.7%~117.7%,相对标准偏差不大于7.6%,整个前处理过程控制在8 min内,且只需2 mL乙腈和155 mg净化剂,该方法将提取、分离和净化合并到一个步骤,省时高效的同时也保证了良好的净化能力,是对经典QuEChERS方法的扩展和应用。
