潺槁树根皮中生物碱类化学成分的研究*
2020-05-31林晓婉孙万莹唐晓亮
林晓婉,金 燕,孙万莹,张 璐,唐晓亮
(1 哈尔滨商业大学药学院,药物工程技术研究中心,黑龙江 哈尔滨 150076;2 海南医学院第一附属医院,海南 海口 570102;3 海南医学院中医学院,海南 海口 571199)
潺槁树(Litseaglutinosa)又称潺槁木姜子,常绿小乔木或乔木,高3~15 m,生长于海拔500~1900 m的山地林缘、溪旁、疏林或灌木丛中[1],主要分布于我国广东、广西、福建及云南南部,越南、菲律宾及印度也有分布[2]。将根皮和叶入药,具有清湿热、消肿毒、治腹泻、外服治疮痈的功用[3]。潺槁树根皮中具有多种化学成分,其中生物碱为其特征性成分。研究表明,潺槁树中的多种生物碱类成分表现出了较好的抗菌、抗氧化、及降糖等药理活性[4-6]。植物一直是一种很好的药物来源,从天然植物中提取这些活性成分相比西药来讲来源更为广泛,也具有治疗效果温和持久、毒副作用小等优点。因此,对于潺槁树根皮中的生物碱类成分进行提取、分离和纯化具有重要意义。本文对潺槁木姜子根皮的生物碱成分进行研究,分离得到10个化合物,并分别鉴定为N-methylcoclaurineN-oxide (1)、(Z)-N-formyllaurolitsine (2)、(E)-N-formyllaurolitsine (3)、Thalifoline (4)、Maculosidine (5)、吴茱萸春 (6)、Pteleine (7)、乌药碱 (8)、波尔定碱(9)、新木姜子碱(10)。其中化合物1~7为首次从该植物中分离得到,其结构见图1。
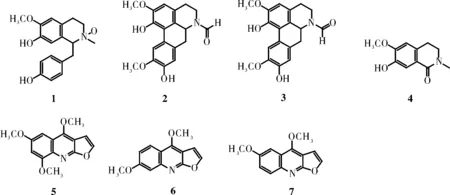
图1 化合物1~7的结构图
1 仪器与材料
核磁共振波谱仪,赛默飞世尔科技公司;RE-201D旋转蒸发仪,上海保玲仪器设备有限公司;SHB-Ⅲ型循环水真空泵,上海霓玥仪器;手提暗箱式紫外分析仪,上海嘉鹏科技有限公司;薄层层析硅胶板,青岛海洋化工厂;柱色谱硅胶(100~200目,200~300目),青岛海洋化工厂;Sephadex LH-20,Pharmacia biotech Sweden;LC-10AD二元低压半制备液相色谱仪,日本岛津;半制备色谱柱(Phenyl,2.5 mm×25.0 cm,5 μm),Agilent;有机试剂,西陇化工有限公司;氘代试剂,中国科学院武汉波谱公司。
潺槁树根皮采自海南省文昌市铜鼓岭,并经海南医学院曾念开教授鉴定。
2 提取与分离
将潺槁树根皮(10.0 kg)切碎后,浸泡至95%乙醇溶液中,采用回流提取法,重复提取3次,每次2 h。使用旋转蒸发仪减压回收溶剂,直至蒸干且乙醇味消失。加入1% 硫酸水溶液(质量分数),调节pH值为3~4,用氯仿(6 L)萃取3次,除去脂溶性成分。酸水溶液中加入1% 的NaOH(质量分数)碱水溶液调节pH为9~10,继而用乙酸乙酯(6 L)萃取3次,减压浓缩后得到潺槁树根皮总生物碱25 g。
称取20 g总生物碱置于烧杯中,加入100 mL乙酸乙酯溶解均匀,采用硅胶柱色谱法进行分离,以二氯甲烷-丙酮为溶剂进行梯度洗脱,经薄层色谱法检测合并后共得到Fr.A~Fr.E 6个组分。Fr.A用凝胶柱色谱分离,然后用反相高效液相制备色谱进一步分离,得到化合物9(52.0 mg)和10(285.0 mg)。Fr.B采用硅胶柱色谱、凝胶柱色谱、反相高效液相制备色谱分离,得到化合物8(20.0 mg)。Fr.C经硅胶柱色谱、凝胶柱色谱、反相高效液相制备色谱分离,得到化合物2(3)(12.0 mg)、5(8.0 mg)、6(10.0 mg)、7(15.0 mg)。由于化合物2和3为同分异构体,经过多次尝试,未实现拆分。Fr.D采用硅胶柱色谱、凝胶柱色谱、反相高效液相制备色谱分离,得到化合物1(12.0 mg)。Fr.E采用硅胶柱色谱、凝胶柱色谱、反相高效液相制备色谱分离,得到化合物4(12.0 mg)。
3 结构鉴定
化合物1:黄色粉末,1H-NMR (600 MHz, CD3OD)δ: 6.99 (2H, d,J=8.4 Hz, H-2′, 6′), 6.66 (2H, d,J=8.4 Hz, H-3′, 5′), 6.66 (1H, s, H-5), 6.27 (1H, s, H-8), 4.26 (1H, brd,J=12.8, H-1), 3.57 (1H, m, H-3α), 3.70 (1H, m, H-3β), 3.10 (1H, brd,J=12.0 Hz, H-7′α), 2.67 (1H, dd,J=12.0, 9.0 Hz,H-7′β), 3.04 (2H, m, H-4), 2.98 (3H, s,N-CH3), 3.70 (3H, s, -OCH3)。13C-NMR (150 MHz, CD3OD)δ: 78.7 (C-1), 62.8 (C-3), 25.8 (C-4), 53.4 (N-CH3), 36.9 (C-7′), 56.0 (-OCH3), 111.9 (C-5), 114.8 (C-8), 130.1 (C-2′, 6′), 121.7 (C-4a), 127.3 (C-8a), 128.7 (C-1′), 146.4 (C-7), 116.8 (C-3′, 5′), 156.7 (C-4′), 147.5 (C-6)。以上数据与文献[9]报道一致,故化合物1鉴定为N-methylcoclaurineN-oxide,首次从潺槁树根皮中分离得到。
化合物2:白色粉末,1H-NMR (600 MHz, CD3OD)δ: 8.20 (1H, s, -CHO), 7.95 (1H, s, H-11′), 6.70 (1H, s, H-8), 6.60 (1H, s, H-3), 4.68 (1H, dd,J=12.0, 4.2 Hz, H-6α), 3.88 (1H,J=12.0, 4.2 Hz, H-7α), 3.28 (1H, td,J=12.0, 2.4 Hz, H-7β), 2.71 (2H, t,J=7.2 Hz, H-5), 2.60 (2H, t,J=7.2 Hz, H-4)。13C-NMR (150 MHz, CD3OD)δ: 162.8 (-CHO), 150.1 (C-2), 149.7 (C-9), 149.6 (C-10), 143.7 (C-1), 129.9 (C-1a), 129.7 (C-7a), 127.4 (C-3a), 122.9 (C-3b), 122.8 (C-11a), 116.8 (C-11), 116.1 (C-8), 112.6 (C-3), 59.7 (10-OCH3), 56.1 (1-OCH3), 49.9 (C-6a), 41.7 (C-5), 33.5 (C-7), 30.4 (C-4)。以上数据与文献[10]报道一致,故化合物2鉴定为(Z)-N-formyllaurolitsine,为首次从潺槁树中分离得到。
化合物3:分子式为C21H24NO5,1H-NMR (600 MHz, CD3OD)δ: 8.33 (1H, s, -CHO), 7.94 (1H, s, H-11′), 6.73 (1H, s, H-8), 6.60 (1H, s, H-3), 4.45 (1H, dd,J=12.0, 4.2 Hz, H-6α)。13C-NMR (150 MHz, CD3OD)δ: 162.8 (-CHO), 150.1 (C-2), 149.7 (C-9), 149.6 (C-10), 143.6 (C-1), 131.0 (C-1a), 129.6 (C-7a), 127.4 (C-3a), 123.0 (C-3b), 122.9 (C-11a), 116.9 (C-11), 116.1 (C-8), 112.6 (C-3), 59.7 (10-OCH3), 56.1 (1-OCH3), 53.0 (C-6a), 37.0 (C-5), 35.6 (C-7), 29.3 (C-4)。以上数据与文献[10]报道一致,故化合物3鉴定为(E)-N-formyllaurolitsine,为首次从潺槁树中分离得到。
化合物4:1H-NMR (600 MHz, CD3OD)δ: 2.90 (2H, t,J=7.2 Hz, H-4), 3.06 (3H, s, N-CH3), 3.54 (2H, t,J=7.2 Hz, H-3), 6.76 (1H, s, H-5), 7.34 (1H, s, H-8)。13C-NMR (150 MHz, CD3OD)δ: 26.8 (C-4), 33.8 (N-CH3), 48.2 (C-3), 55.0 (-OCH3), 109.4 (C-5), 113.6 (C-8), 121.2 (C-8a), 131.2 (C-4a), 145.0 (C-7), 150.0 (C-6), 165.7 (C-1)。以上数据与文献[11]报道一致,故化合物4鉴定为Thalifoline,为首次从该植物中分离得到。
化合物5:白色粉末,1H-NMR (600 MHz, CD3OD)δ: 7.74 (1H, d,J=3.6 Hz, H-2), 7.62 (1H, brd, H-5), 7.31 (1H, d,J=3.6 Hz, H-3), 7.21 (1H, brd, H-7), 4.50 (3H, s, 4-OCH3), 3.99 (3H, s, 6-OCH3), 3.96 (3H, s, 8-OCH3)。13C-NMR (150 MHz, CD3OD)δ: 163.0 (C-8b), 105.3 (C-7), 142.5 (C-2), 148.0 (C-8), 153.2 (C-4), 156.3 (C-6), 141.5 (C-8a), 100.3 (C-5), 112.7 (C-4a), 104.8 (C-3), 102.1 (C-3a), 61.7 (8-OCH3), 59.0 (6-OCH3), 56.8 (4-OCH3)。以上数据与文献[12]报道的一致,故化合物5鉴定为Maculosidine,为首次从潺槁树中分离得到。
化合物6:无色无定形粉末,1H-NMR (600 MHz, CD3OD)δ: 3.93 (3H, s, 7-OCH3), 4.50 (3H, s, 4-OCH3), 8.18 (1H, d,J=8.4 Hz, H-5), 7.76 (1H, d,J=3.6 Hz, H-2), 7.35 (1H, d,J=3.6 Hz, H-3), 7.23 (1H, d,J=2.4 Hz, H-8), 7.12 (1H, dd,J=8.4, 2.4 Hz, H-6)。13C-NMR (150 MHz, CD3OD)δ: 54.6 (7-OCH3), 58.6 (4-OCH3), 101.8 (C-3a), 104.5 (C-3), 106.1 (C-8), 113.1 (C-4a), 116.3 (C-6), 123.6 (C-5), 142.6 (C-2), 147.0 (C-8a), 157.8 (C-4), 161.6 (C-7), 164.7 (C-8b)。以上数据与文献[13]一致,故鉴定化合物6为吴茱萸春,为首次从潺槁树中分离得到。
化合物7:白色粉末,1H-NMR (600 MHz, CD3OD)δ: 7.80 (1H, d,J=3.6 Hz, H-2), 7.78 (1H, d,J=8.4 Hz, H-8), 7.56 (1H, d,J=2.4 Hz, H-5), 7.35 (1H, d,J=3.6 Hz, H-3), 7.38 (1H, dd,J=8.4, 2.4 Hz, H-7), 4.50 (3H, s, 4-OCH3), 3.90 (3H, s, 6-OCH3)。13C-NMR (150 MHz, CD3OD)δ: 54.6 (6-OCH3), 58.6 (4-OCH3), 100.0 (C-5), 103.5 (C-3a), 104.7 (C-3), 118.9 (C-4a), 122.3 (C-7), 127.6 (C-8), 140.4 (C-8a), 143.7 (C-2), 156.2 (C-6), 156.3 (C-4), 162.7 (C-8b)。以上数据与文献[14]报道的一致,故化合物7鉴定为Pteleine,为首次从潺槁树中分离得到。
化合物8:白色粉末,1H-NMR (600 MHz, CD3OD)δ: 3.81 (3H, s, -OCH3), 6.62 (1H, s, H-5), 6.73 (1H, s, H-8), 6.77 (2H, d,J=8.4 Hz, H-3′, 5′), 7.10 (2H, d,J=8.4 Hz, H-2′, 6′)。13C-NMR (150 MHz, CD3OD)δ: 24.6 (C-4), 39.0 (C-3), 39.4 (C-7′), 55.0 (-OCH3), 56.3 (C-1), 111.2 (C-5), 112.8 (C-8), 116.5 (C-3′, 5′), 122.4 (C-4a), 123.9 (C-8a), 125.7 (C-1′), 130.2 (C-2′, 6′), 146.2 (C-7), 147.7 (C-6), 156.7 (C-4′)。以上数据与文献[15]报道一致,故化合物8鉴定为乌药碱。
化合物9:无定形粉末,碘化铋钾阳性。1H-NMR (600 MHz, CD3OD)δ: 7.96 (1H, s, H-11), 6.73 (1H, s, H-8), 6.53 (1H, s, H-3), 3.86 (3H, s, 10-OCH3), 3.56 (3H, s, 1-OCH3), 3.00 (2H, m, H-7a, 4b), 2.90 (1H, m, H-5a), 2.64 (1H, m, H-6a), 2.51 (3H, s,N-CH3), 2.47 (1H, m, H-5b), 2.43 (1H, m, H-7b)。13C-NMR (150 MHz, CD3OD)δ: 151.2 (C-2), 148.3 (C-10), 147.7 (C-9), 144.9 (C-1), 131.2 (C-7a), 130.5 (C-3a), 128.0 (C-1a), 127.1 (C-1b), 125.3 (C-11a), 116.4 (C-8), 115.5 (C-3), 113.3 (C-11), 64.5 (C-6a), 54.8 (C-5), 60.8 (1-OCH3), 57.1 (10-OCH3), 44.4 (N-CH3), 35.4 (C-7), 29.8 (C-4)。以上数据与文献[16]报道一致,故化合物9鉴定为波尔定碱。
化合物10:结晶性粉末,碘化铋钾阳性。1H-NMR (600 MHz, CD3OD)δ: 7.98 (1H, s, H-11), 6.70 (1H, s, H-8), 6.50 (1H, s, H-3), 3.76 (1H, dd,J=13.2, 3.6 Hz, H-6a), 3.86 (3H, s, 10-OCH3), 3.57 (3H, s, 1-OCH3)。13C-NMR (150 MHz, CD3OD)δ: 151.5 (C-2), 148.4 (C-9), 147.7 (C-1), 145.0 (C-10), 130.6 (C-7a), 130.3 (C-3a), 128.2 (C-1b), 126.6 (C-1a), 125.2 (C-11a), 116.3 (C-8), 116.0 (C-11), 113.4 (C-3), 60.8 (C-6a), 57.1 (1-OCH3), 56.3 (10-OCH3), 44.1 (C-5), 37.0 (C-7), 29.0 (C-4)。以上数据与文献[6]报道一致,故化合物10鉴定为新木姜子碱。
4 结 论
本文利用采用溶剂提取法和色谱法对潺槁树根皮部位中的生物碱类成分进行分离纯化,得到了10个生物碱类化合物,为潺槁树根皮中的主要化学成分。文献报道,对潺槁树根皮中总生物碱药理活性进行研究,发现其表现出了较好的降糖活性。本课题组将继续对潺槁树根皮中的生物碱类化学成分进行全面的研究,为潺槁树的进一步开发利用及药理活性的探索提供科学依据。
