Ag/γ-Al2O3催化剂的制备及其对亚甲基蓝的降解性能
2020-05-29刘丽,许杰
刘 丽,许 杰
(1.江西中医药高等专科学校公共基础部,江西抚州 344000;2.常州大学石油化工学院,江苏常州 213164)
近年来,印染行业快速发展,各种新型染料和助剂的加入,为人们提供了丰富多彩的纺织品,同时也产生了大量的染料废水。如果染料废水不经有效处理就排放,将会严重污染环境,破坏生态平衡,甚至危害人体健康[1-2]。染料废水是最难处理的工业废水之一,常用的染料废水处理方式有化学还原、光降解、凝聚、反渗透等。这些处理方式虽然能有效降低染料废水的危害,但也存在各自的不足,如能耗较高、对染料降解具有选择性、副产物易造成二次污染等[3-7]。因此,研究环境友好、高效低耗的染料废水处理方法十分必要。近年来,利用纳米金属颗粒催化降解染料废水受到越来越多的关注,这是由于纳米金属颗粒具有大量的反应活性位点、良好的电子迁移能力、较高的比表面积和优良的热稳定性,催化活性高、选择性好,能够降解多种有机染料[8-10]。但纳米金属颗粒较高的比表面积导致其容易团聚,团聚后的纳米金属颗粒反应活性位点减少,催化能力降低;另外纳米金属颗粒尺寸太小,不利于催化剂的回收再利用[11-13]。为避免纳米金属颗粒的团聚,增加稳定性,利于回收再利用,可将纳米金属颗粒附着在基材上,常用的基材有ZnO、TiO2和Fe3O4等[14-16]。本实验以AgNO3和γ-Al2O3为原料,NaBH4和PVP 分别作为还原剂和表面活性剂,将纳米银颗粒分散于γ-Al2O3表面,得到Ag/γ-Al2O3复合材料;以亚甲基蓝溶液为模拟染料废水,NaBH4为还原剂,研究Ag/γ-Al2O3的催化活性和稳定性,并优化催化反应条件。
1 实验
1.1 材料与仪器
材料:γ-Al2O3、聚乙烯吡咯烷酮(PVP)、AgNO3、NaBH4(均为分析纯)。
仪器:UV-1810DPC 紫外-可见分光光度计(UVVis),SU-70B X 射线衍射仪(XRD),JEOL JEM-2100透射电镜(TEM),FBT-5比表面仪(BET)。
1.2 Ag/γ-Al2O3催化剂的制备
称取0.1 g PVP 加入有100 mL 去离子水的烧杯中,搅拌30 min,加入适量γ-Al2O3和AgNO3,剧烈搅拌1 h,逐滴加入10 mL 1 mol/L 的NaBH4溶液,持续搅拌12 h,过滤,分别用乙醇和去离子水清洗3 次,200 ℃干燥6 h,得到的样品记为Ag/γ-Al2O3。不添加γ-Al2O3,采用同样的方法制备得到的样品记为Ag。
1.3 降解性能测试
在玻璃反应容器中加入100 mL 100 mg/L 的亚甲基蓝溶液,再加入10 mg Ag/γ-Al2O3催化剂,搅拌30 min,迅速注入50 mL 0.5 g/L 的NaBH4溶液并持续搅拌。每隔10 s 取出10 mL 溶液,离心后取上层清液,利用紫外-可见分光光度计测试660 nm 处的吸光度(将催化降解后的溶液过滤并用去离子水清洗3 次,以回收催化剂),降解率=(1-At/A0)×100%,其中,A0、At分别表示初始、t时刻亚甲基蓝溶液的吸光度。
2 结果与讨论
2.1 表征
2.1.1 XRD
由图1 可以看出,除具有γ-Al2O3的衍射峰外,Ag/γ-Al2O3在2θ=38.0°、44.1°、64.9°和77.4°处还出现了衍射峰,分别对应Ag 的(111)、(200)、(220)和(311)晶面(JCPDS No.04-0783),无其他杂峰出现,表明Ag以单质形式与γ-Al2O3结合[17];另外γ-Al2O3衍射峰的位置未发生明显变化,表明Ag 的加入并没有明显影响γ-Al2O3的晶体结构。
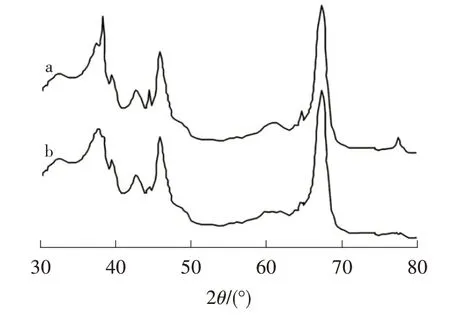
图1 Ag/γ-Al2O3(a)和γ-Al2O3(b)的XRD 图谱
2.1.2 TEM
由图2 可知,Ag 纳米颗粒的直径为3~8 nm,较为均匀地附着在γ-Al2O3表面,具有良好的分散性,没有出现颗粒团聚现象。

图2 Ag/γ-Al2O3的TEM 图
2.1.3 BET
由图3 可知,γ-Al2O3和Ag/γ-Al2O3的N2吸附-脱附等温曲线都属于第Ⅳ型H1滞后环,表明γ-Al2O3和Ag/γ-Al2O3都是介孔材料。γ-Al2O3的N2吸附-脱附等温曲线的滞后环陡峭,说明γ-Al2O3呈现统一的介孔结构;Ag/γ-Al2O3的N2吸附-脱附等温曲线滞后环陡峭程度明显下降,且滞后环向低压方向移动,说明负载Ag后γ-Al2O3的有序介孔结构出现了坍塌[18]。

图3 γ-Al2O3(a)和Ag/γ-Al2O3(b)的N2吸附-脱附等温曲线
2.2 催化活性研究
由图4 可知,随着反应时间的延长,亚甲基蓝溶液的吸光度逐渐降低。

图4 亚甲基蓝溶液的UV-Vis 图
由图5 可看出,不添加催化剂时,随着反应时间的延长,亚甲基蓝溶液的降解率几乎无变化,说明单独加入NaBH4几乎不能降解亚甲基蓝。加入γ-Al2O3并搅拌30 min 后,亚甲基蓝溶液的质量浓度降为初始时刻的78.2%;加入NaBH4后,溶液的质量浓度不再明显变化。这是由于γ-Al2O3的比表面积较大,亚甲基蓝附着在催化剂表面,导致溶液质量浓度降低;而加入NaBH4后,溶液的质量浓度不再明显降低,说明γ-Al2O3不具有催化活性。以Ag 为催化剂,在加入NaBH4后,亚甲基蓝溶液的降解率逐渐增大,60 s 后降解率为31.4%,远低于Ag/γ-Al2O3催化剂的95.7%。这主要是由于Ag 颗粒本身容易团聚,与亚甲基蓝溶液的有效接触面积较小,反应活性位点较少,反应速率缓慢,Ag 附着于γ-Al2O3表面后,虽然孔洞结构有所坍塌,比表面积有所减小,但仍远高于Ag的比表面积,能够提供更多的反应活性位点,催化降解率增大。另外,在降解反应开始前,大量亚甲基蓝吸附在Ag/γ-Al2O3表面,加入NaBH4后,在催化剂表面形成的反应活性位点能快速地与亚甲基蓝反应,促使亚甲基蓝降解。随着反应的持续进行,溶液中的亚甲基蓝逐渐减少,催化剂表面的反应活性位点不能被充分利用,降解率逐渐降低,直到平衡状态。

图5 不同催化剂降解亚甲基蓝溶液的催化活性
2.3 催化条件优化
2.3.1 催化剂用量
由图6 可知,当催化剂用量低于1.5 g/L 时,随着催化剂用量的增加,亚甲基蓝的降解率逐渐增大;当催化剂用量高于1.5 g/L 时,随着催化剂用量的增加,亚甲基蓝的降解率几乎不变,说明催化剂用量超过1.5 g/L 的部分成为无效催化剂。

图6 亚甲基蓝溶液降解率与催化剂用量的关系
2.3.2 搅拌速率
Ag/γ-Al2O3催化降解亚甲基蓝的反应为悬浮液(包括催化剂颗粒、亚甲基蓝溶液和氧气)相反应,搅拌速率影响溶液中的含氧量,从而影响降解率。由图7 可知,当搅拌速率低于500 r/min 时,随着搅拌速率的增大,亚甲基蓝的降解率逐渐增大,这是由于搅拌速率增大,亚甲基蓝溶液中的含氧量增加,有利于亚甲基蓝的降解;当搅拌速率高于500 r/min 时,增大搅拌速率,亚甲基蓝溶液的降解率逐渐减小,这是由于搅拌速率过大时,悬浮液的均一性受到影响,不利于亚甲基蓝的降解。

图7 亚甲基蓝溶液降解率与搅拌速率的关系
2.3.3 重复使用次数
由图8 可知,重复使用5 次后,Ag/γ-Al2O3的催化活性没有明显降低,说明催化剂具有较好的稳定性,可重复用于催化降解亚甲基蓝染料废水。

图8 Ag/γ-Al2O3的重复使用性能
3 结论
以AgNO3和γ-Al2O3作为原料,NaBH4和PVP 分别作为还原剂和表面活性剂,制备得到Ag/γ-Al2O3介孔复合材料。Ag 纳米颗粒的粒径为3~8 nm,分散附着在γ-Al2O3表面,γ-Al2O3附着Ag 后仍呈现介孔结构。Ag/γ-Al2O3具有良好的催化活性,当催化剂用量为1.5 g/L、500 r/min 搅拌60 s 后,亚甲基蓝的降解率达到95.7%,催化剂可多次回收使用。
