铀氧化物溶解尾气治理技术研究
2020-05-25唐儒煜
唐儒煜
(中核二七二铀业有限责任公司,湖南 衡阳 421002)
目前国内最大的天然铀纯化生产基地,采用硝酸溶解—TBP萃取—微硝酸反萃取—重铀酸铵沉淀—三碳酸铀酰铵结晶联合净化工艺流程,将铀氧化物纯化生产核纯级UO2。在硝酸溶解铀氧化物制备硝酸铀酰的过程中,硝酸被还原产生较多的NOx(氮氧化物,下同),而NOx是大气的主要污染物之一。为了保护环境,消除污染,曾采用水吸收、碳酸铵吸收等方法进行尾气治理溶解。但硝酸溶解铀氧化物过程是非连续操作,产生的NOx间断式排放,瞬间排放浓度高,水吸收、碳酸铵吸收等方法对该工况的适应性较差。为此,在分析NOx的来源及酸性尿素溶液对NOx的吸收机制的基础上,研究了酸性尿素溶液对NOx的吸收效果。
1 溶解尾气中NOx的来源
1.1 发烟硝酸
采用发烟硝酸(质量分数≥98%)配制浓度为6 mol/L的酸化水溶解铀氧化物;而发烟硝酸有强挥发性和不稳定性,在光或空气中会分解放出NO2,这是NOx的来源之一,硝酸分解反应为
4HNO3→4NO2↑+O2↑+2H2O。
(1)
1.2 铀氧化物溶解反应
铀氧化物主要为U3O8和UO2,均为粉末状颗粒,在投入盛有酸化水的溶解槽进行溶解反应时,会产生较多的棕黄色烟,其主要成分为NO2和NO,这是铀氧化物溶解尾气的最主要来源。主要反应为
U3O8+8HNO3→
3UO2(NO3)2+2NO2↑+4H2O,
(2)
3U3O8+20HNO3→
9UO2(NO3)2+2NO↑+10H2O,
(3)
UO2+4HNO3→UO2(NO3)2+2NO2↑+2H2O,
(4)
3UO2+8HNO3→3UO2(NO3)2+2NO↑+4H2O。
(5)
2 NOx的危害
铀氧化物溶解尾气中的NO2、NO等都有较大的毒性,对人和环境可造成较大的危害。NO是一种无色无味、难溶于水的有毒气体,易与血液中的血红蛋白结合,造成血液缺氧而引起中枢神经麻痹。NO2是一种棕红色、有刺激性臭味的有毒气体,由呼吸系统侵入人体肺部,对肺组织产生强烈的刺激及腐蚀作用,引起支气管炎、肺炎、肺气肿、甚至肺癌,而且对心脏和肾脏以及造血组织等也有影响。NO2和NO在大气和云雾液滴中会转化为HNO3和HNO2,形成酸雨、酸雾,造成环境污染。NO2与碳氢化合物会形成具有强烈的刺激作用的光化学烟雾,该烟雾能引起眼红流泪、头痛、气喘、咳嗽等症状,还会降低大气能见度,造成橡胶制品老化、脆裂等问题[1]。
3 NOx的净化
铀氧化物溶解过程为槽式溶解、非连续性操作,溶解尾气具有间歇性排放、NOx瞬间浓度高等特点。经工业生产实践检验,采用水吸收、碳酸铵吸收处理溶解尾气,NOx的去除效率不佳,难以保证NOx排放浓度达到标准的要求。这主要是由NOx的性质所决定的(表1),为此,研究酸性尿素溶液吸收技术[3],重点研究分析了酸性尿素溶液在治理铀氧化物溶解尾气工业应用上的影响因素,为工业生产操作和工艺参数控制探索最佳条件。

表1 氮氧化物的物理性质
4 酸性尿素溶液吸收NOx技术
4.1 反应机制
尿素是一种较强的还原剂,在酸性条件下,可以较快地将亚硝酸还原为氮气。尿素吸收氮氧化物的反应过程是放热反应,其反应原理如下[4]。
首先,尾气中的NO2和NO,相互间存在的主要反应为
2NO+O2→2NO2,
(6)
2NO2→N2O4,
(7)
NO+NO2→N2O3。
(8)
反应(6)~(8)的产物可以被液相吸收,液相主要反应为
2NO2+H2O→HNO2+HNO3,
(9)
N2O4+H2O→HNO2+HNO3,
(10)
N2O3+H2O→2HNO2。
(11)
在酸性介质中,尿素和NOx的液相吸收产物产生强烈的氧化还原反应,主要反应为
2HNO2+(NH2)2CO→2N2↑+CO2↑+3H2O,
(12)
HNO2+(NH2)2CO+HNO3→
N2↑+CO2↑+NH4NO3+H2O。
(13)
总反应为[5]27
6NO2+4(NH2)2CO→7N2↑+4CO2↑+8H2O,
(14)
6NO+2(NH2)2CO→5N2↑+2CO2↑+4H2O。
(15)
NOx吸收反应主要由反应(9)和(12)完成。
4.2 酸性尿素溶液吸收NOx工艺流程
铀氧化物溶解产生的尾气,先进入气液分离器进行气液分离;再进入水喷射真空机组进行水吸收,回收的硝酸溶液回用;余气进入三级吸收塔,利用酸性尿素溶液进行循环吸收,吸收后的尾气经除沫后由风机送入排气筒达标排放。尾气治理循环吸收过程中,尿素将被消耗,可利用尾气间断排放的间隙,把吸收塔内的低浓度尿素溶液,通过泵输送回酸性尿素溶液配制槽,补加尿素原料、回用硝酸等使其符合工艺要求,然后再重新泵入吸收塔。如此闭路循环利用,既使尾气得以治理,又不造成新的污染。酸性尿素溶液吸收NOx的工艺流程如图1所示。

图1 酸性尿素溶液吸收尾气NOx流程示意图
4.3 酸性尿素溶液吸收NOx主要设备
酸性尿素溶液吸收NOx的主要设备有搅拌配制槽、水喷射真空机组、不锈钢吸收塔、不锈钢风机等,见表2。
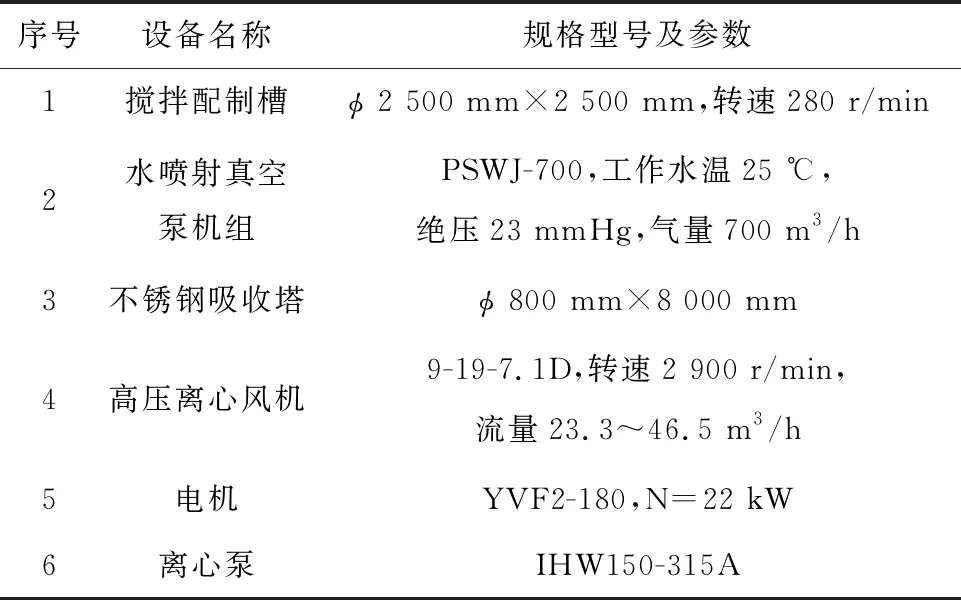
表2 酸性尿素溶液吸收NOx主要设备
4.4 酸性尿素溶液吸收效率影响因素
酸性尿素溶液吸收NOx受尿素溶液的浓度、pH、吸收温度、反应时间、进风量、填料传质效率等因素影响,研究中使用自动烟尘(气)测试仪(型号3012H),对吸收塔的进气和尾气排气筒的气态流出物中的NOx排放浓度进行检测。
4.4.1 尿素质量分数对NOx吸收率的影响
NOx的吸收为化学吸收,传质机制遵循双膜理论,由于液相有化学反应(12)等进行,极大地提高了传质速率,故适当增加溶液中尿素的质量分数有利于反应进行。操作条件:每批3桶铀氧化物,风机转速1 400 r/min,填料体积1.5 m3,填料为Dg38阶梯环。保持其他操作条件不变,改变溶液中尿素的质量分数,考察尿素质量分数对NOx吸收率的影响。试验结果如图2所示。
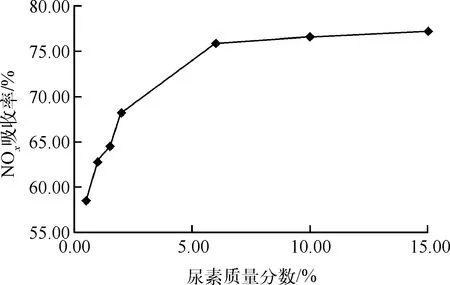
图2 尿素质量分数对NOx吸收率的影响
由图2可看出,随着溶液中尿素质量分数的增加,NOx吸收率增加,尿素质量分数超过6%以后,NOx的吸收率增加比较缓慢。从经济成本角度考虑,溶液中尿素质量分数控制在10%左右为宜。
4.4.2 pH对NOx吸收率的影响
吸收液的pH是影响NOx吸收率的主要因素之一,保持其他操作条件不变,尿素溶液质量分数10%,改变尿素溶液pH,考察尿素溶液pH对NOx吸收率的影响。试验结果见图3。可以看出,NOx的吸收率随着pH的增加而下降,当pH=1~2时,尿素溶液对NOx的吸收率比较高(≥82.00%)。所以,酸性尿素溶液可以使用水喷射真空机组回收的硝酸溶液或工业生产产生的酸性废水(萃取余水pH=1)来配制,这样既可节约成本,又不会产生新产物引起二次污染。
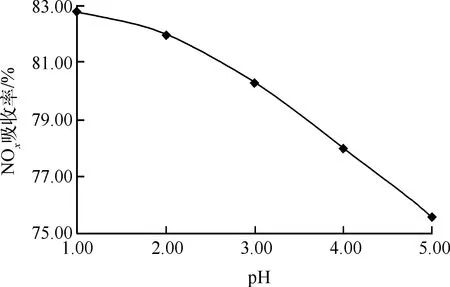
图3 pH对NOx吸收率的影响
4.4.3 温度对NOx吸收率的影响
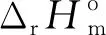
(16)
由式(16)可知,lnK正比于1/T,随着温度T升高,平衡常数K减小,不利于反应的进行,表明NOx的吸收反应宜在低温下进行。
结合Arrhenius公式,反应式(9)的反应速率常数与温度存在以下关系[5]28:
lnk=-Ea/RT+lnA,
(17)
式中:k为反应速率常数;Ea为活化能;A为指前因子。由式(17)可知温度T升高,反应速度升高,即温度升高,可以提高反应的速率,这与平衡常数和温度的关系相矛盾。因此温度的影响要从两方面来考虑,通过工业实际探索合适的反应温度。
保持其他操作条件不变,尿素溶液pH=1,
改变吸收塔内的温度,考察温度对NOx吸收率的影响,试验结果如图4所示。
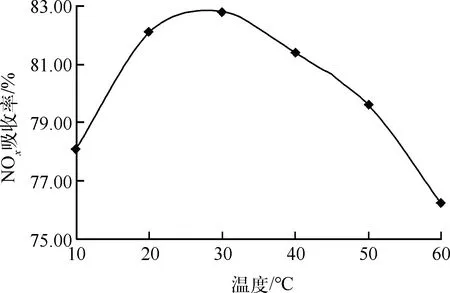
图4 温度对NOx吸收率的影响
由图4可看出,当温度为30 ℃时,酸性尿素溶液对NOx的吸收率最大,之后随着温度升高,NOx的吸收率有所下降,其适宜温度为30 ℃左右。在工业生产中,从操作便利及经济性考虑,采用常温进行吸收操作。
4.4.4 其他因素对NOx吸收率的影响
1)填料环。NOx的吸收传质机理遵循双膜理论,传质效率对NOx吸收率有较大影响。吸收塔内初期使用陶瓷拉西环(型号Dg40、规格40×40×5),需要规则填充,工作量较大,且存在液体分布不均匀和严重的壁流沟流等现象。经调研对比分析,塑料阶梯环(型号Dg38)高径比仅为拉西环的一半,而且侧端增加了锥形翻边,能促进液膜表面更新和液体混合作用。吸收塔更换为塑料阶梯环后,使气液分布均匀,增加了气液接触表面而提高了传质效率,尾气吸收效果较好。塑料阶梯环的性能参数见表3。

表3 塑料阶梯环的性能参数
2)高压离心风机。进风量是影响NOx吸收率的一个重要方面,通过加装变频器来调节风机转速,实现根据铀氧化物溶解反应情况,对进风量进行调节。
5 治理效果
采用塑料阶梯环为填料环,将高压离心风机加装变频器,用pH=1、尿素质量分数为10%的酸性尿素溶液,在常温条件下,吸收铀氧化物溶解尾气中的NOx。2018年,该公司对调整后的铀氧化物溶解尾气排气筒(高度32 m)的NOx排放浓度进行检测,检测结果见表4。
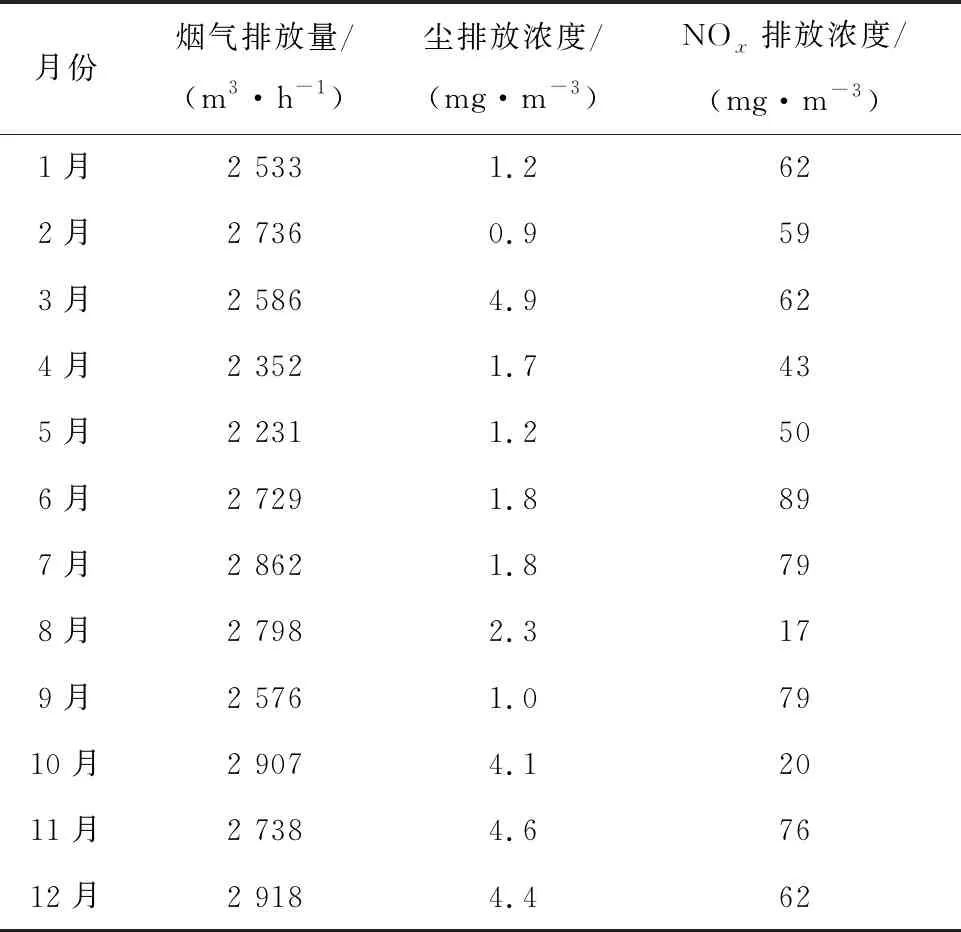
表4 溶解尾气排气筒气态流出物排放浓度及排放量
由表4可看出,2018年铀氧化物溶解尾气中NOx排放浓度范围为17~89 mg/m3,低于GB 16297—1996《大气污染物综合排放标准》规定的限值(420 mg/m3),实现了100%达标排放。
6 结论
对酸性尿素溶液吸收NOx技术及影响因素进行了分析和试验研究,确定了工业生产适宜的操作条件:采用塑料阶梯环为填料环,将高压离心风机加装变频器,以pH=1、尿素质量分数为10%的酸性尿素溶液,在常温条件吸收铀氧化物溶解尾气中的NOx。工业应用证明,酸性尿素溶液吸收NOx工艺可以与铀氧化物投料溶解同步开车,具有投资省、净化效果好、无二次污染等特点,能够很好地适应铀纯化的生产条件,具有一定的优越性。
