ExacTrac图像引导系统结合六维床在SRS治疗摆位中的可靠性研究
2020-05-23罗日顺邓官华周巧敏蔡林波
罗日顺 戴 鹏 邓官华 周巧敏 黄 庆 蔡林波*
现代放射治疗技术已经进入精确定位、精确设计和精确治疗的“三精”时代,其中立体定向放射外科(stereotactic radiotherapy surgery,SRS)技术因其能将高能射线聚焦于靶区内,使得肿瘤组织受到高剂量照射,周围正常组织受量减小的特点成为脑转移瘤治疗的重要手段[1]。而图像引导放射治疗(image guided radiation therapy,IGRT)技术是实现SRS精确治疗和确保疗效的关键所在[2-4]。目前图像引导系统有超声引导、电子射野成像引导、锥形束CT(conebeam CT,CBCT)和扇形束CT引导、核磁引导、电磁追踪以及ExacTrac图像引导等,其成像原理、技术参数、应用环境、成像质量以及速度和模式很大程度上影响了放射治疗的结果。医院在用图像引导系统有Varian Unique直线加速器自带的电子射野影像装置(electronic portal imaging device,EPID),同时包含后期升级后配置的ExacTrac图像引导系统和六维床自动摆位系统。两套图像引导系统完全独立,互不干扰,应用的环境和运算算法也各不相同,对于精度更高的ExacTrac图像引导系统修正后的位置可靠性如何,能否满足临床需求,相关文献报道较少。本研究旨在探讨ExacTrac图像引导系统结合六维床修正SRS摆位误差数据的可靠性。
1 资料与方法
1.1 一般资料
选取2018年2月至2019年3月在广东三九脑科医院就诊的62例实施放射治疗患者,其中男性34例,女性28例;年龄10~80岁,中位年龄45岁。根据治疗方法的不同,将其分为观察组(32例)和对照组(30例)。观察组患者应用ExacTrac图像引导系统结合六维床摆位并利用电子射野影像装置EPID拍片验证后行SRS治疗;对照组患者应用EPID系统拍片验证后行常规调强放射治疗(intensity modulated radiation therapy,IMRT)。两组患者在年龄、性别等临床资料相比均无统计学差异,具有可比性。
1.2 纳入与排除标准
(1)纳入标准:①患者意识清醒,能配合治疗;②结合临床表现、影像学检查、病理等确诊为头颈部肿瘤且需放射治疗。
(2)排除标准:①合并精神疾病,沟通障碍等;②躁动,依从性差者。
1.3 仪器设备
采用Varian Unique型直线加速器(美国Varian公司),放射治疗计划系统为Varian Eclipse 13.6;BrainLab ExacTrac图像引导系统(德国博医来公司)和六维床及Varian Unique自带的EPID影像板;16排大孔径CT模拟机(德国西门子公司)。
1.4 CT模拟定位及放射治疗计划
(1)定位结构:CT模拟定位由定位头架、定位膜和定位框组成。将定位膜(Klarity R408)放入65~70 ℃恒温水箱中浸泡2~3 min,软化后将底膜置于定位板(BrainLab)头枕上,协助患者平躺,头部在底膜上,适当调整患者体位并保持不动,然后将中膜置于患者额头和上唇位置,取出鼻根塑形膜捏成倒T状贴合在额头与鼻梁之间,防止头部上下、左右旋转;将顶膜覆盖到中膜上,将鼻和下颌塑成形使面膜与脸紧密贴合,待30 min面膜完全冷却后取下[5]。CT模拟定位结构见图1。

图1 CT模拟定位示意图
(2)CT定位:戴上专用定位框,扫描层厚1.5 mm,管电压为120 kV,管电流为350 mAs。将获取的CT图像传输至Varian Eclipse TPS 13.6计划系统,由医生勾画靶区和危及器官,物理师制作放射治疗计划,最后将治疗计划和重建图像数据分别传输至Unique加速器和ExacTrac 线图像引导系统。
1.5 摆位修正与精度配准
1.5.1 观察组摆位与配准
患者仰卧于治疗床上,采用制定好的面膜固定患者头部于碳素纤维延长头架上,戴上无框架SRS定位架,运用红外线光学定位仪检测头架上6个定位标记球的位置进行预摆位,利用机架两侧的X射线装置拍摄kV级正交图像,通过与计划系统中数字化重建影像(digitally reconstructed radiographs,DRR)配准后,得到患者在x、y和z的3个方向的平移误差及相应旋转误差(Rx、Ry和Rz),并利用六维治疗床修正此次配准误差。精度配准:①重复图像验证过程,直至修正后的患者摆位误差在可允许的范围(平移方向<0.5 mm,旋转角度<0.5°);②利用EPID拍摄患者0°和90°验证片,通过骨性配准与DRR图像配准后,得到患者在x、y和z方向的平移误差,当此误差满足临床要求时则开始治疗。
1.5.2 对照组摆位与配准
患者仰卧于治疗床,治疗师利用已制定好的面膜给患者固定和摆位,然后利用定位框和摆位纸将患者肿瘤中心移置治疗中心点,做好标记方便下次治疗,然后通过EPID拍摄0°和90°验证片,得到患者在x、y和z方向的平移误差,当平移误差满足临床要求时开始治疗。
1.6 统计学方法
采用SPSS22.0软件进行数据分析。计量资料以均值±标准差()表示,配对数据采用非参数Wilcoxon符号秩检验;组间比较采用非参数Mann-Whitney秩和检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组EPID验证摆位误差比较
观察组采用ExacTrac图像引导系统,修正摆位误差后得到的EPID摆位,用ExacTrac修正后再用EPID拍摄得到的x、y和z的3个方向摆位误差与对照组在x、y和z的3个方向摆位误差比较,误差与对照组直接获取的EPID摆位误差在x、y和z方向的差异均具有统计学意义(Z=-3.696,Z=-3.810,Z=-3.436;P<0.05),见表1。
表2 观察组ExacTrac图像引导修正前后摆位误差比较()
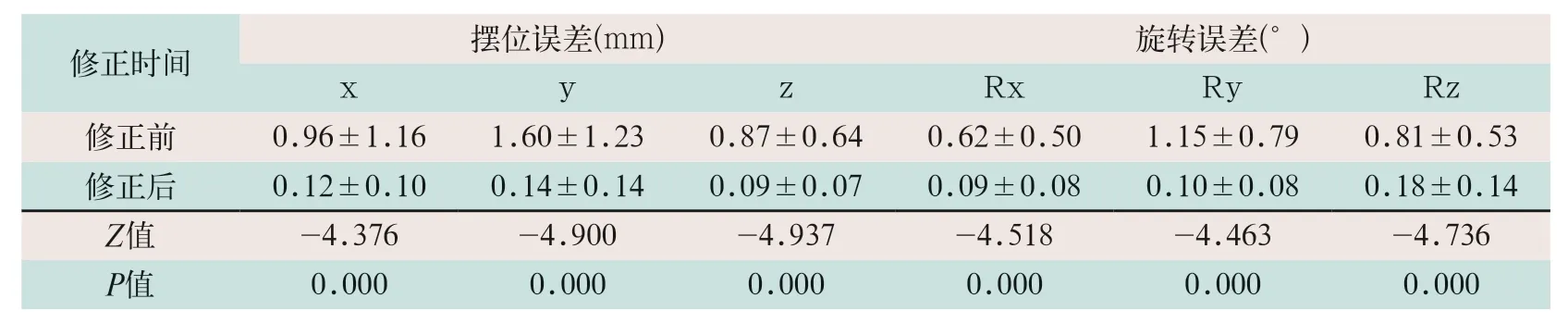
表2 观察组ExacTrac图像引导修正前后摆位误差比较()
注:表中x为左右方向误差;y为头脚方向误差;z为腹背方向误差;Rx、Ry和Rz表示其对应的旋转误差
表1 两组EPID验证摆位误差比较()
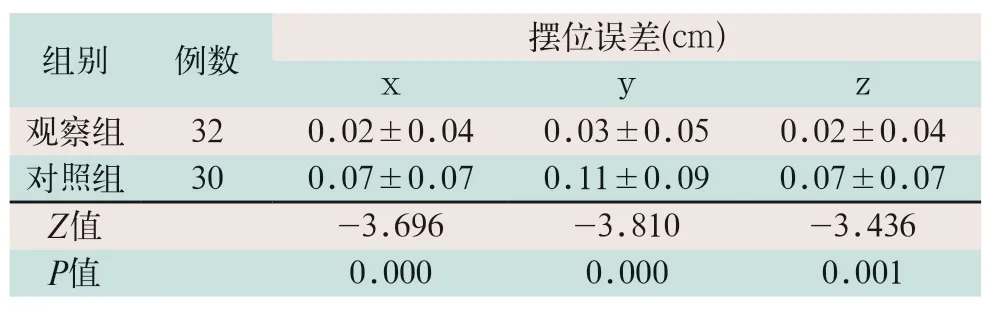
表1 两组EPID验证摆位误差比较()
注:表中x为左右方向误差;y为头脚方向误差;z为腹背方向误差
2.2 观察组ExacTrac图像引导修正前后摆位误差比较
观察组在ExacTrac图像引导修正前与修正后的摆位误差在x、y和z方向的平移误差及相应的旋转误差(Rx、Ry和Rz)比较,差异均有统计学意义(Z摆位误差=-4.376,Z=-4.900,Z=-4.937;Z旋转误差=-4.518,Z=-4.463,Z=-4.739;P<0.05),且修正后3个平移方向误差值均<0.3 mm,见表2。
2.3 修正前后摆位误差分布
观察组横向摆位误差主要分布在0~0.1 cm范围内,而对照组横向摆位误差主要分布在0~0.3 cm范围内。经ExacTrac图像引导系统修正后,患者摆位误差明显缩小。两组摆位误差情况见图2。
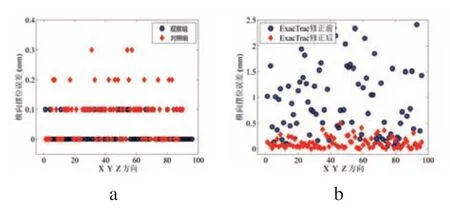
图2 摆位误差散点分布图
3 讨论
随着影像引导放射治疗的发展和CBCT及其图像配准软件的应用,摆位误差已能被精确测量。图像引导包括二维方向、三维方向及六维方向,不同的配准方式可能有不同的配准结果,并非所有加速器都配置CBCT和六维治疗床,从而无法做到从三维平移误差校正精确到三维平移误差加三维旋转误差校正[6-7]。
Varian加速器自带的EPID图像验证系统使用兆伏(MV)级X射线,ExacTrac图像引导系统属千伏(kV)级X射线,可同时结合六维床自动摆位及修正。两套图像引导系统属相互独立的二维成像系统,但拍摄的角度,所应用的运算算法不同,因此所得的精度也不同。对于精度可达亚毫米级的ExacTrac图像引导系统,应用其数据经六维床修正后得到的位置是否可靠,相关文献报道较少。本研究通过EPID图像引导系统对其修正后的位置再次拍摄验证片,但由于两者所得结果精度不一致而无法直接进行同级别比较,因此通过设立对照组将其与常规调强放射治疗时直接用EPID拍片验证所得的误差进行比较。结果显示,采用ExacTrac图像引导系统修正后再用EPID拍片验证在x、y和z方向的摆位误差比直接用EPID验证得到的摆位误差小,且差异具有统计学意义。由此表明,经过ExacTrac图像系统修正后的位置是有效可靠的。此外,从ExacTrac图像引导系统所得数据显示,修正后各平移方向误差均<0.3 mm,对应的旋转角度也<0.5 °,极大提高了摆位的精度,与周巧敏等[8]和钟伟伟等[9]关于ExacTrac X射线图像引导在SRS治疗时统计的结果一致。
在临床工作中,本研究发现ExacTrac图像引导系统具有以下优点。
(1)ExacTrac图像系统虽属二维系统,但可以实现6个方向上的位移,能提供亚毫米级的精度。王法宁等[10]通过模体实验和临床研究对比了三维CBCT和二维ExacTrac影像引导系统针对人体不同部位上的定位精度,分析实验结果显示在治疗头部肿瘤时,ExacTrac系统精度稍高。
(2)可以根据计划给定任意非共面床角下进行验证,本研究中并未对非共面床角进行联合验证,但张平等[11]关于ExacTrac 6D影像精确引导系统在脑转移瘤SRS中的应用中显示,在非共面治疗时3个线性方向误差值<0.5 mm及其对应的旋转角度<0.5°。
(3)患者接受额外照射量更小。研究报道显示,虽然kV级CBCT影像引导放射治疗技术对患者扫描区域点的辐射剂量较低,但每行CBCT扫描1次,将会分别有11.1 cGy、6.7 cGy和6.2 cGy等的额外辐照剂量传输至患者甲状腺、皮肤和晶体等器官,累积剂量叠加的效果亦不容忽略,频繁应用会使危机器官接收剂量超过最大限量值,增加患者第二原发癌发生率[12]。ExacTrac图像引导系统产生平均剂量为0.33~0.55 mGy,可极大减少了患者额外接收的照射剂量。
(4)旋转误差的修正能更加保证治疗的精准性,而ExacTrac系统能够结合六维床进行六维度修正。Handey等[13]报道,>2°的旋转误差会对图像配准结果产生影响。Gutfeld等[14]研究结果表明,>2°的旋转误差会使靶区剂量发生3%~5%的变化,即认为>2°的旋转误差需要校正。付秀根等[15]认为,旋转误差在临床摆位中应引起足够重视,旋转误差会影响线性误差。
(5)脑转移瘤一般多者可达十余个病灶,治疗时间长,患者中途可能需要多次休息而导致治疗中断,但ExacTrac系统可根据红外线追踪定位框上的6个标记球进行快速预摆位,准确查找治疗的等中心点,同时也可进行分次外的治疗,摆位方便快速而准确。
ExacTrac图像引导系统应用于SRS治疗同样存在缺点,如仅2幅交叉的二维DRR影像,图像质量劣于CBCT,靶区成像不高,病灶靠近边缘时不好配准等。由于图像质量等原因,目前ExacTrac图像验证主要应用于刚性和(或)骨性特点明显的病变部位或其邻近靶区,当应用于体部SBRT治疗时,应联合多种影像装置进行验证。此外,由于加速器仅配有EPID系统,如能通过CBCT验证ExacTrac图像引导系统的可靠性将更具有说服力。
4 结论
采用ExacTrac图像引导系统结合六维床进行SRS治疗摆位可靠,其精度可达亚毫米级别,能够极大提高放射治疗的精确度,减少正常组织受量,而且能有效缩短患者摆位时间,降低患者受照射量,适合于临床中要求高精度治疗时使用。
