HPLC 法测定丁朴凝胶贴膏中3 种成分
2020-05-12王奕博杜媛媛于颖超曲昌海尹兴斌董晓旭孙毅坤
王奕博,杜媛媛,于颖超,曲昌海,尹兴斌,董晓旭,孙毅坤,倪 健
(1.北京中医药大学中药学院,北京 102488;2.北京中医药大学中医药研究院,北京 100029)
丁朴凝胶贴膏是以北京中医药大学东方医院临床经验方——“胃瘫外敷方”为基础,原剂型为中药细粉与蜂蜜等黏合剂混合成外敷制剂,现将其改为凝胶贴膏剂。该方临床应用多年,尤其对寒症型术后胃瘫患者效果显著[1-2],它由丁香、姜厚朴、肉桂等中药组成,所含丁香酚、和厚朴酚、厚朴酚等成分具有促进胃肠蠕动、保护胃黏膜、增强胃动力的作用[3-7]。本实验建立HPLC 法测定这3 种成分的含有量。
凝胶贴膏性质黏稠,而且部分高分子材料不溶于有机试剂,不同方法对其提取率有较大影响。目前,相关提取方法包括冷浸法、超声法、分散后再处理法[8-11],但鲜有对其所得提取率进行比较,故本实验又考察了超声时间、冷浸时间、溶剂量、是否分散对丁朴凝胶贴膏提取率的影响,以期为后续研究提供借鉴。
1 材料
1.1 仪器 LC-20AT 型高效液相色谱仪(配置SPD-M20A PDA 检测器,日本岛津公司);UltiMate 3000 型高效液相色谱仪[赛默飞世尔科技(中国)有限公司];TLE204102型电子天平(瑞士梅特勒-托利多公司);KQ3200DE 型数控超声波清洗器(昆山市超声仪器有限公司);JY5002 型电子天平(上海衡平仪器仪表厂)。
1.2 试剂与药物 桂皮醛(批号110710-201720,质量分数98.7%)、丁香酚(批号110725-201716,质量分数99.6%)、和厚朴酚(批号110730-201614,质量分 数99.3%)、厚朴酚(批号 110729-201714,质量分 数100.0%)对照品均购自中国食品药品检定研究院。凝胶贴膏及缺肉桂、丁香、厚朴阴性贴膏均为自制。硅藻土(天津市福晨化学试剂厂,批号20180320)。甲醇为色谱纯(美国Fisher 公司)或分析纯(北京化工厂);水为纯净水(娃哈哈集团有限公司)。
2 方法与结果
2.1 凝胶贴膏制备 取处方量聚丙烯酸钠、氢氧化铝,混合均匀后加入甘油、中药挥发油搅拌均匀,作为油相;取处方量酒石酸、纯净水、厚朴流浸膏搅拌均匀,作为水相;将水相均匀加到油相中,以60 r/min 左右转速搅拌成型后置于无纺布上,将膏体均匀涂布于自制涂布框内,加盖压花膜,室温静置,即得(生药量15 g/贴)。
2.2 指标成分含有量测定
2.2.1 色谱条件 Agilent ZORBAX SB-C18色谱柱(4.6 mm×250 mm,5 μm);流动相甲醇-水,梯度洗脱,程序见表1;体积流量1 mL/min;柱温30 ℃;检测波长290 nm;进样量10 μL。
2.2.2 供试品溶液制备 取自制凝胶贴膏,揭下压花膜,不锈钢勺刮取0.5 g 置于蒸发皿中,精密称定质量,加入等量硅藻土,以钢勺不断挤压搅拌至硅藻土与凝胶贴膏完全混匀,具体表现为贴膏外观类似絮状且黏性消失,即为分散完成。将其置于具塞锥形瓶中,精密加入50 mL甲醇,称定质量,超声(100 W、40 kHz)10 min,放冷,甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
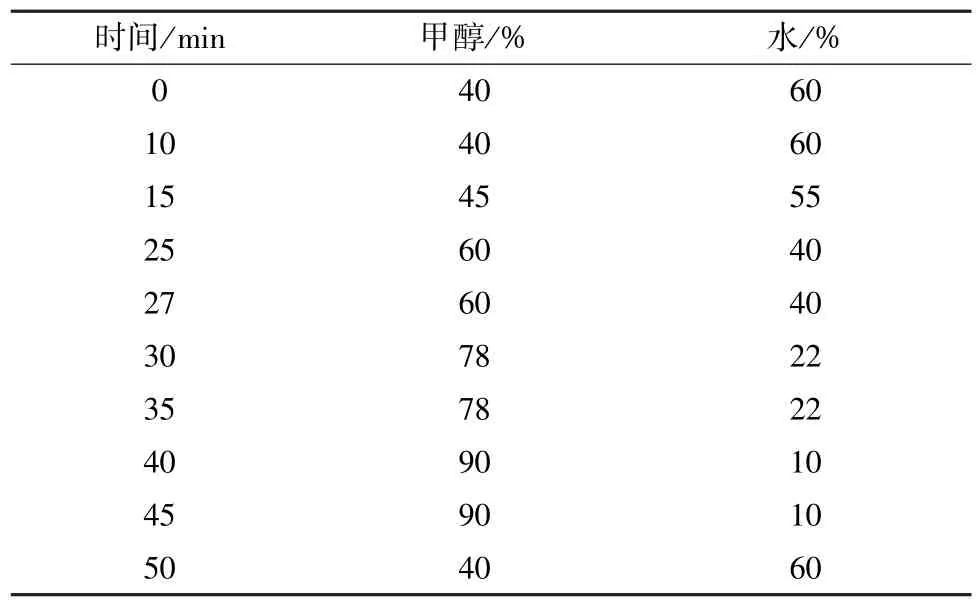
表1 梯度洗脱程序
2.2.3 对照品溶液制备 精密称取桂皮醛、丁香酚、和厚朴酚、厚朴酚对照品适量,加甲醇制成每1 mL 分别含四者0.107 24、1.073、0.158 6、0.334 mg,摇匀,即得。
2.2.4 阴性样品溶液制备 取等量缺肉桂、缺丁香、缺厚朴阴性样品,按“2.2.2”项下方法制备,即得。
2.2.5 专属性试验 精密吸取供试品、对照品、阴性样品溶液各10 μL,在“2.2.1”项色谱条件下进样测定,结果见图1,可知阴性无干扰,方法专属性良好。
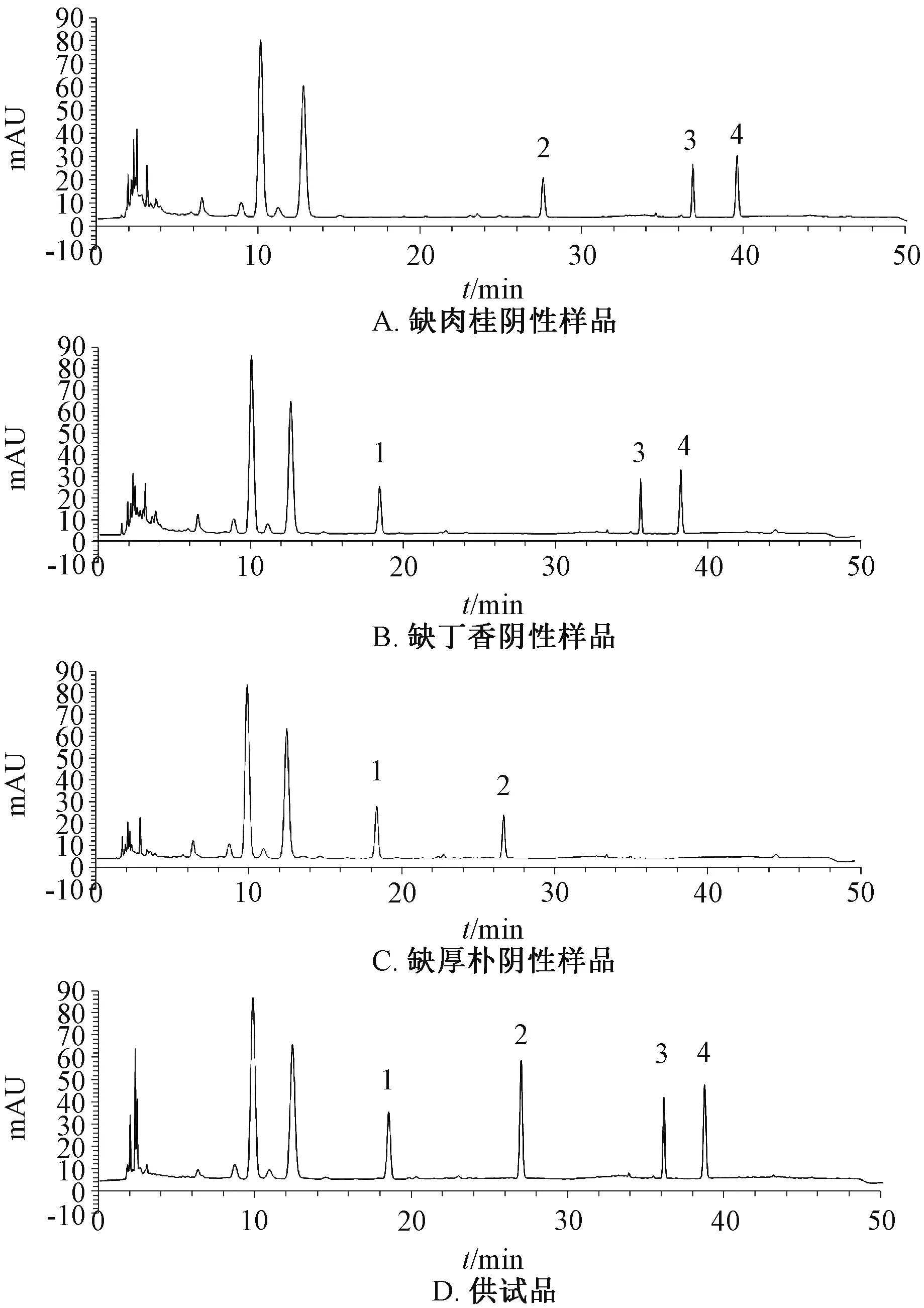
图1 各成分HPLC 色谱图
2.2.6 线性关系考察 精密吸取对照品溶液0.1、1.0、2.0、3.0、6.0 mL 置于10 mL 量瓶中,加甲醇至刻度,摇匀,在“2.2.1”项色谱条件下进样测定。以峰面积为纵坐标(Y),进样量为横坐标(X)进行回归,结果见表2,可知各成分在各自范围内线性关系良好。
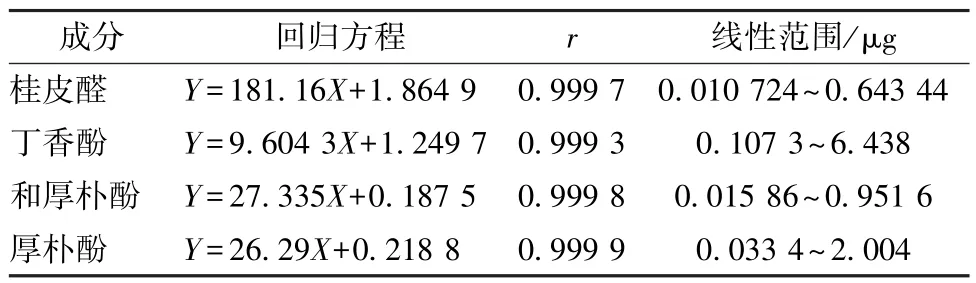
表2 各成分线性关系
2.2.7 精密度试验 精密吸取对照品溶液10 μL,在“2.2.1”项色谱条件下进样测定6 次,测得桂皮醛、丁香酚、和厚朴酚、厚朴酚峰面积RSD 分别为0.44%、0.50%、0.56%、0.38%,表明仪器精密度良好。
2.2.8 重复性试验 称取凝胶贴膏约0.5 g,共6 份,按“2.2.2”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样测定,测得桂皮醛、丁香酚、和厚朴酚、厚朴酚含有量RSD 分别为2.78%、2.73%、2.27%、1.61%,表明该方法重复性良好。
2.2.9 稳定性试验 取供试品溶液,于0、1、3、6、12、24 h 在“2.2.1”项色谱条件下进样测定,测得桂皮醛、丁香酚、和厚朴酚、厚朴酚峰面积RSD 分别为2.59%、0.48%、1.42%、1.20%,表明溶液在24 h 内稳定性良好。
2.2.10 加样回收率试验 精密称取同一批含有量已知的凝胶贴膏0.5 g,共6 份,按“2.2.2”项下方法制备供试品溶液,加入对照品溶液后在“2.2.1”项色谱条件下进样测定,计算回收率。结果,桂皮醛平均加样回收率为92.03%,RSD 为4.14%;丁香酚平均加样回收率为98.03%,RSD 为1.56%;和厚朴酚平均加样回收率为98.31%,RSD 为2.10%;厚朴酚平均加样回收率为99.06%,RSD 为1.32%。
2.3 提取方式考察
2.3.1 凝胶贴膏制备 取适量丁香、肉桂混合挥发油及厚朴流浸膏,加入处方量辅料,即得(每1 g 含丁香酚7.69 mg、桂皮醛1.28 mg、和厚朴酚1.05 mg、厚朴酚2.03 mg)。
2.3.2 正交试验 取0.5 g 凝胶贴膏,分别加入规定量硅藻土分散或不分散,并加50 mL 甲醇超声或冷浸规定时间,以丁香酚、厚朴酚、和厚朴酚平均提取率为评价指标,考察硅藻土分散比(A)、超声时间(B)、冷浸时间(C)对其的影响,因素水平见表3,结果见表4。由此可知,除A1B1C1外,各组合所得提取率相差不大,推测这3 个因素之间可能存在相互作用,故对其进行单因素试验考察。

表3 因素水平
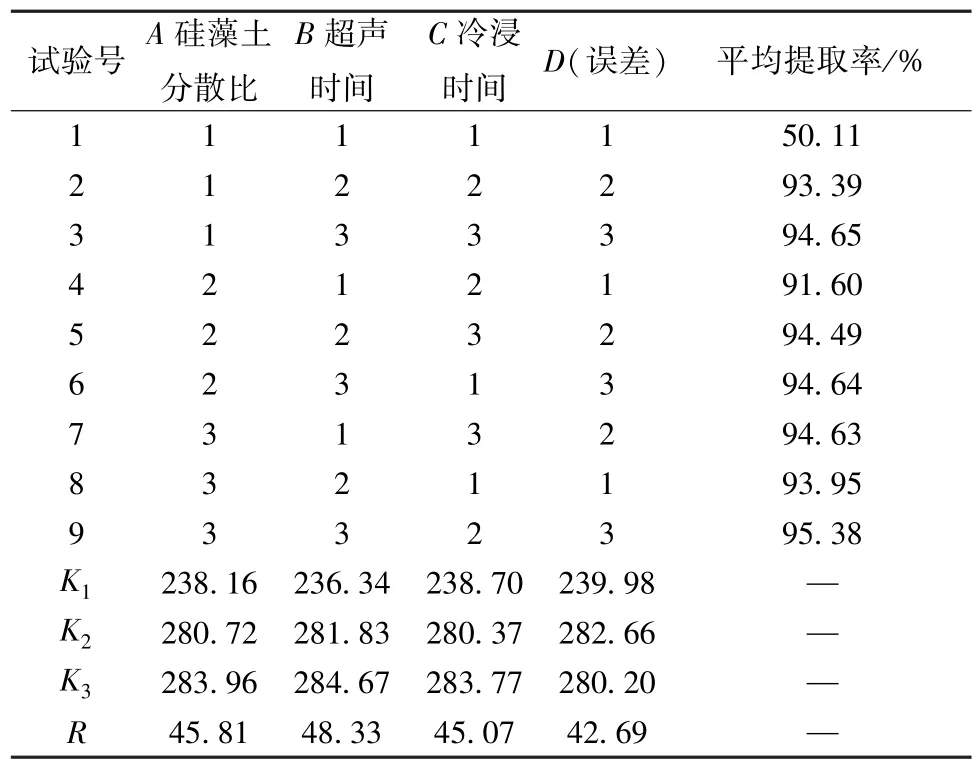
表4 试验设计与结果
2.3.3 料液比、冷浸时间 取凝胶贴膏0.5、1、2 g,加50 mL 甲醇(即料液比1∶100、1∶50、1∶25)冷浸后,于10、20、30、60、120、180、240、360、480、600、720、1 440 min 各取样1 mL,甲醇补足减失的质量,计算提取率,平行3 次,取平均值,结果见图2。由此可知,料液比1∶100、冷浸时间2 h 时可得到90%以上的提取率。
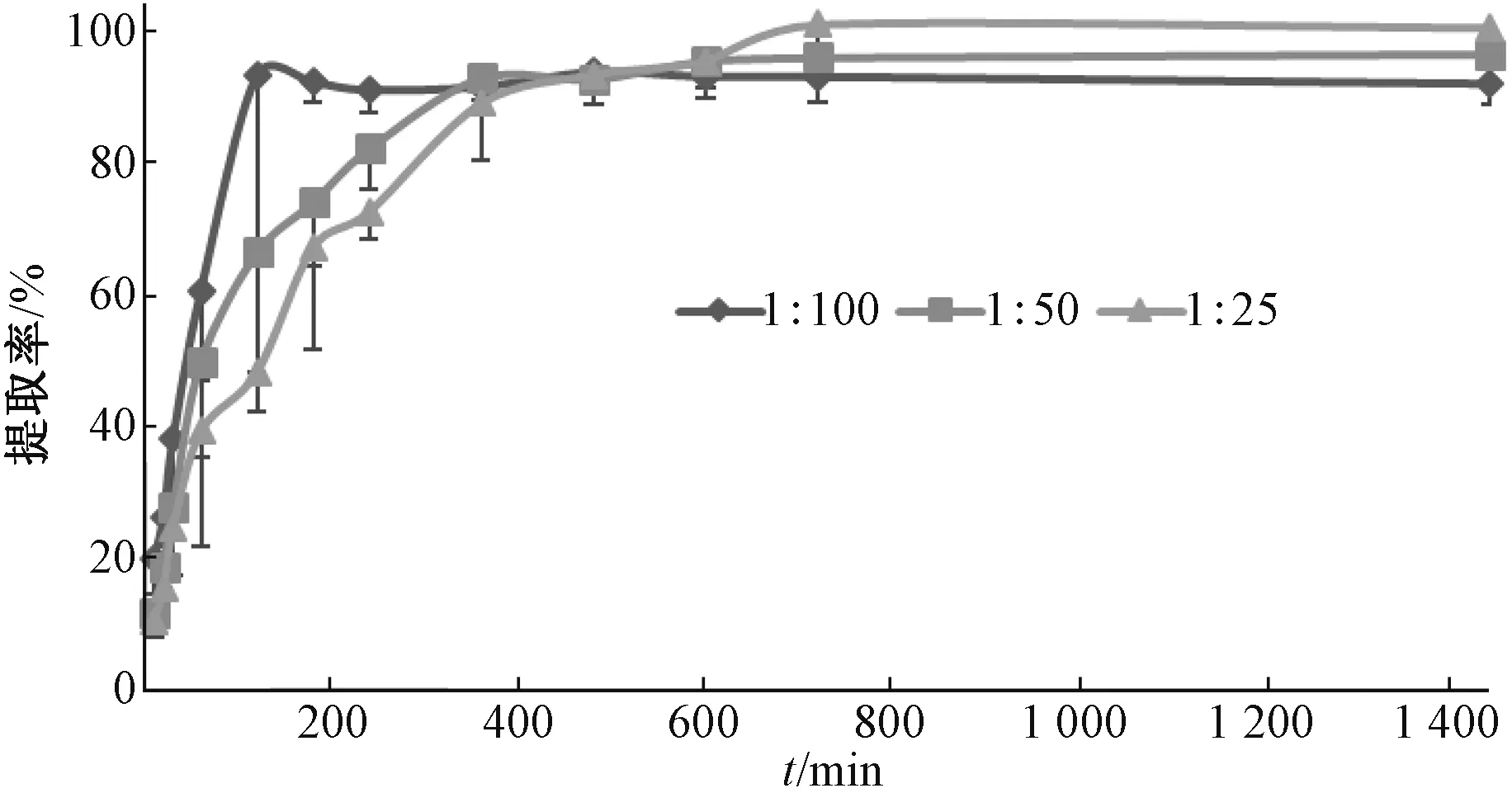
图2 不同料液比下冷浸时间对提取率的影响
2.3.4 不分散后超声时间 取凝胶贴膏0.5 g,加50 mL甲醇超声后,于10、20、30、40 min 各取样1 mL,甲醇补足减失的质量,计算提取率,平行5 次,取平均值,结果见图3。由此可知,提取40 min 时提取率仍不能达到90%,而且不同提取时间之间差异较大。
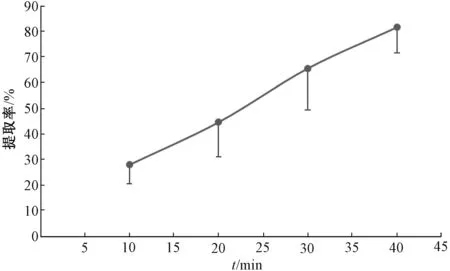
图3 不分散后超声时间对提取率的影响
2.3.5 分散后超声时间 取凝胶贴膏0.5 g,加等量硅藻土分散,加50 mL 甲醇超声后于10、20、30、40 min 各取样1 mL,甲醇补足减失的质量,计算提取率,平行5 次,取平均值,结果见图4。由此可知,提取10 min 时提取率即可达90%以上,而且不同提取时间之间差异较小,故确定最优提取方法为加1 倍量硅藻土分散后超声10 min。
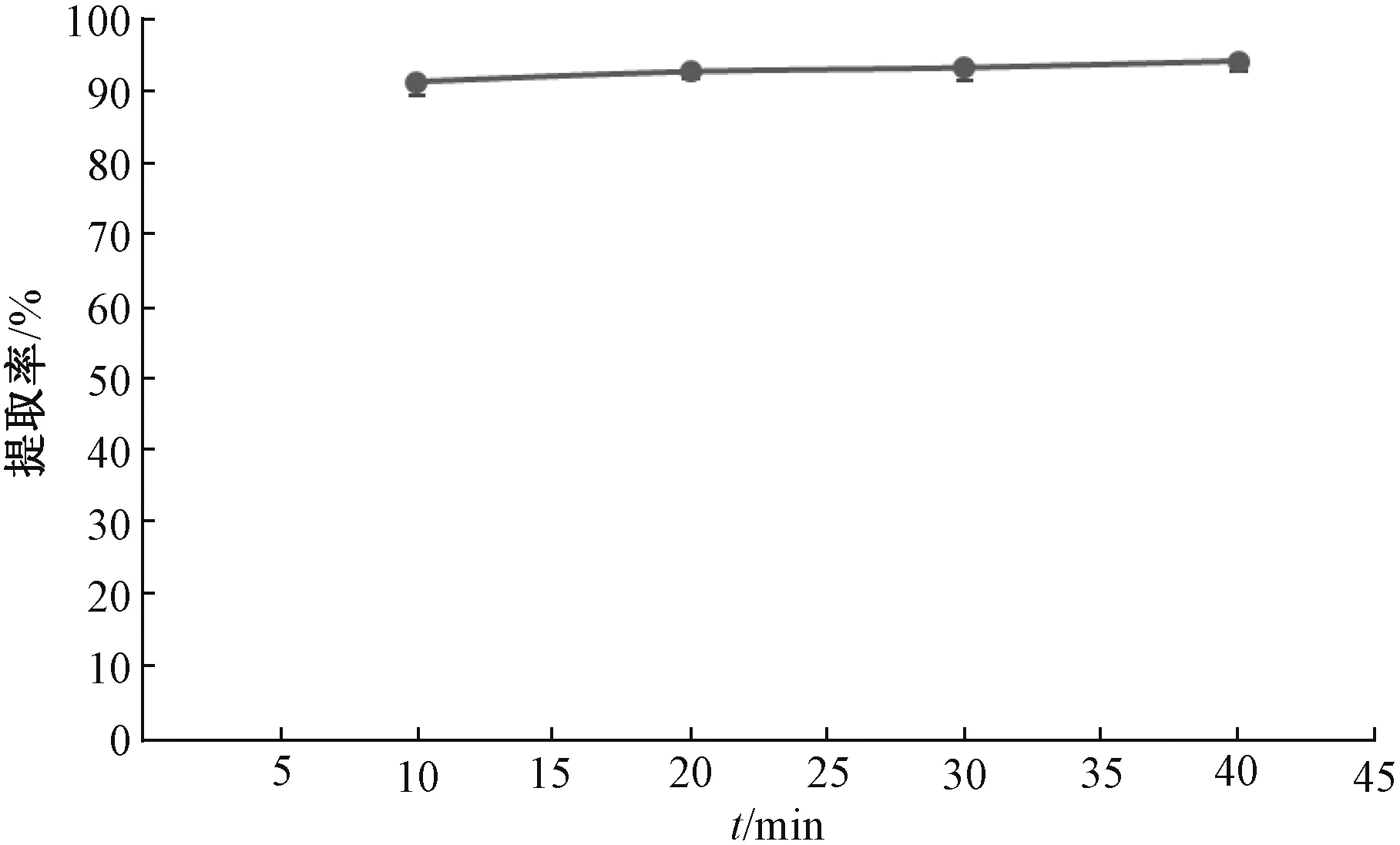
图4 分散后超声时间对提取率的影响
2.3.6 样品含有量测定 制备3 批样品,按上述方法进行测定,每批3 次。结果,丁香酚、和厚朴酚、厚朴酚平均含有量分别为7.54、1.00、1.79 mg/g。
3 讨论
本实验对丁朴凝胶贴膏中桂皮醛也进行了分析,发现在贴膏制备过程中其失达40%,即使保证避光条件其平均加样回收率亦仅为92.03%。桂皮醛在甲醇中的稳定性较差,而且样品分散可能导致其损失,故在提取含该成分的凝胶贴膏时应避免使用硅藻土,同时提取溶液可选择乙腈[12-13]。
考察冷浸时间时发现,取样量0.5、1、2 g 条件下所得提取率大致相同,而贴膏体积越大,所需冷浸时间越长。然后,对三者对未达到稳态部分的释放曲线进行拟合,发现均符合一级动力学方程(r分别为0.970 0、0.990 3、0.991 4),表明凝胶贴膏在有机试剂中并不会产生溶蚀作用,仅是类似于一种固体[14],成分由内而外被动扩散,进而解释了不分散时为何需要长时间超声才能达到90%以上提取率。
考察检测波长时发现,290 nm 下桂皮醛、丁香酚、和厚朴酚、厚朴酚峰面积大小适中,故确定其作为检测波长。
不使用硅藻土分散冷浸2 h 以上后,可充分提取0.5 g小块凝胶贴膏,并且贴膏体积越大,所需冷浸时间越长,虽然超声提取有助于指标成分溶出,但也需要长时间才能达到90%以上提取率,同时RSD 也较大,其原因可能是不分散时凝胶贴膏性质黏稠,取样表面积差异较大,导致扩散速度不同,从而放大误差;使用硅藻土分散后超声10、40 min 时,所得提取率基本接近,RSD 较小,为了节约时间、降低误差,本实验选择分散后超声提取10 min。
4 结论
本实验通过HPLC 法测定丁朴凝胶贴膏中丁香酚、和厚朴酚、厚朴酚的含有量,其专属性、精密度、重复性、稳定性、准确性均符合2015 年版《中国药典》 药品质量标准分析方法验证指导原则规定,可为该制剂质量控制提供参考。
