经冠状动脉微导管注射硝普钠在心肌梗死PCI治疗中的应用
2020-05-11张丽华王立君秦利强
杜 超,张丽华,江 平,王立君,卢 炜,秦利强
急性心肌梗死(AMI)是心血管内科常见急症,常见于冠状动脉不稳定斑块导致的急性血栓形成,引起冠状动脉完全或不完全闭塞,起病急骤,严重威胁病人生命[1]。急性ST段抬高型心肌梗死(STEMI)是急性心肌梗死中的急、重类型,病人冠状动脉完全闭塞,发病后早期实施有效的再灌注治疗,是救治此类病人的首选方案[2-3]。经皮冠状动脉介入治疗(PCI)是目前STEMI治疗的首选方法,可短时间内实现心肌再灌注,挽救病人生命[4]。但有报道称,AMI病人 PCI术后有5%~50%病人可出现心肌无复流现象,影响治疗效果[5]。本研究为观察PCI术中经冠状动脉微导管注射硝普钠在STEMI病人治疗中的作用及对PCI后冠状动脉无复流的影响,选取我院收治并行PCI治疗时发生无复流的STEMI病人,在发生无复流后,经冠状动脉微导管注射硝普钠,观察其对无复流的影响,现报道如下。
1 资料与方法
1.1 临床资料 选取我院2017年1月—2018年4月收治的行急诊PCI时发生无复流的STEMI病人80例,入选病人诊断符合2001年心血管病学分会发布的《急性心肌梗死诊断和治疗指南》中关于1型心肌梗死的诊断标准[6],均以心前区或胸骨后剧烈压榨性疼痛来院就诊,病人主诉疼痛向下颌、颈部、左上臂、背或肩部放射,含服硝酸甘油无法完全缓解;心电图检查显示有≥2个相邻 ST段抬高的情况,R波降低,伴或不伴病理性Q波;实验室检查显示肌酸激酶同工酶(CK-MB)、肌钙蛋白(cTn)动态升高,并高于正常范围。在PCI治疗过程中支架植入后即刻行冠状动脉造影提示心肌梗死溶栓试验(TIMI)血流≤1 级,且无内膜撕裂、夹层、血栓栓塞等机械性梗阻。排除严重高血压未有效控制、严重肝肾肺功能不全、主动脉夹层、脑血管意外史、活动性内脏出血及曾行冠状动脉旁路血管重建术或移植术病人,治疗前均向病人家属讲明治疗目的,并签署知情同意书。80例病人随机分为观察组与对照组,各40例。两组性别、年龄、发病至手术时间、梗死血管分布等比较差异均无统计学意义(P>0.05),具有可比性。详见表1。
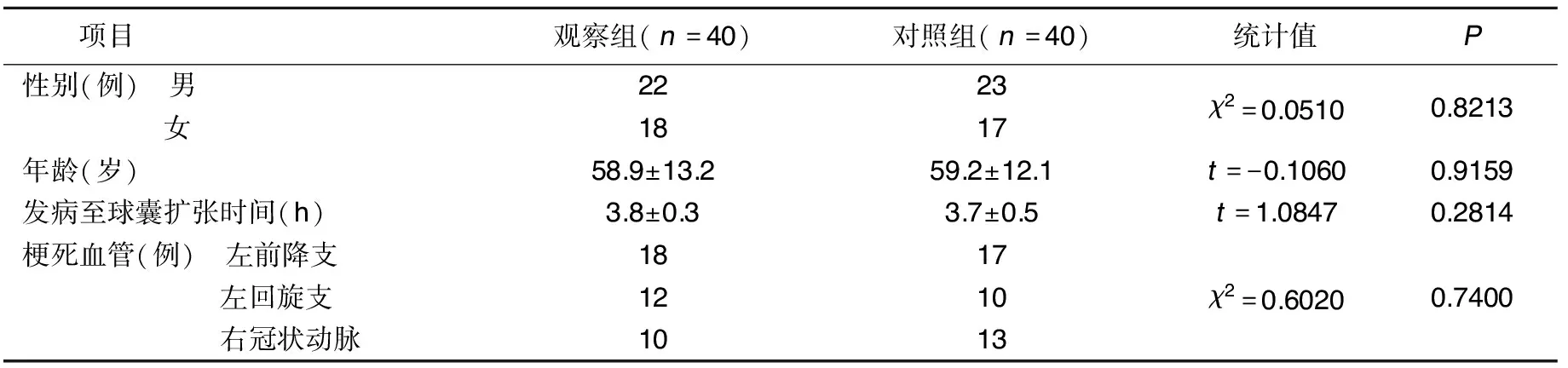
表1 两组临床资料比较
1.2 方法 两组病人均行PCI治疗,术前常规给予氯吡格雷600 mg、阿司匹林300 mg及阿托伐他汀钙片40 mg 口服;经桡动脉或股动脉途径置入鞘管,行常规冠状动脉造影,明确闭塞血管后,置入指引导管,导引导丝通过病变,经球囊预扩张,并植入支架,支架选择:长度为病变节段的1.3倍,直径为血管直径的1.0~1.1倍,释放支架压力为10~18 kPa;之后经冠状动脉微导管向冠状动脉远端注射相应药物。观察组病人注入硝普钠50~200 μg,对照组给予硝酸甘油100~200 μg,注药10 min后行冠状动脉造影,以评定靶血管 TIMI 血流分级。PCI术后两组均给予替罗非班0.075~0.150g/(kg·min) 输注,持续36 h,并予他汀类药物、β受体阻滞剂等常规治疗,术后定期复诊。
1.3 观察指标 给药10 min后行冠状动脉造影,评价靶血管 TIMI 血流分级。3级:病变血管处血流速与近端流速一致,造影剂远端血管可迅速显影;2级:病变血管可见造影剂通过,远端血管可显影;1级:病变血管仅可通过少量造影剂,远端血管显影不充分;0级:梗死相关动脉(IRA)完全闭塞,病变血管未见造影剂通过且无血流灌注。采用彩色超声心动图仪测量PCI术后7 d、30 d、60 d两组病人左心室收缩末期内径(LVESD)、左心室舒张末期内径(LVEDD)及左心室射血分数(LVEF),以评价心功能情况。于PCI术前、术后1周采集病人外周静脉血,采用荧光免疫法检测N末端脑钠肽前体 (NT-proBNP)水平;对比两组病人治疗后无复流现象发生率及心血管不良事件 (MACE)发生情况。

2 结 果
2.1 两组治疗后TIMI分级比较 观察组治疗后TIMI分级3级病人多于对照组(P<0.05)。详见表2。
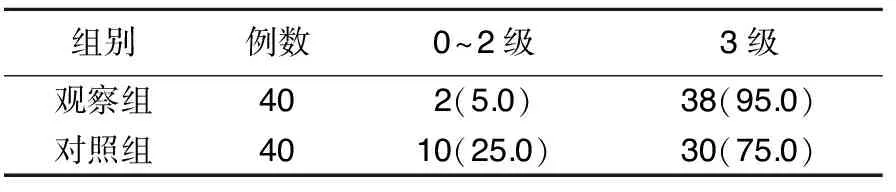
表2 两组治疗后TIMI分级比较 单位:例(%)
注:χ2=6.2750,P=0.0122。
2.2 两组治疗前后心功能比较 PCI术后7 d,两组LVESD、LVEDD、LVEF比较差异无统计学意义(P>0.05);术后60 d,观察组LVESD、LVEDD低于同期对照组(P<0.05),而LVEF则明显高于同期对照组(P<0.05)。详见表3。

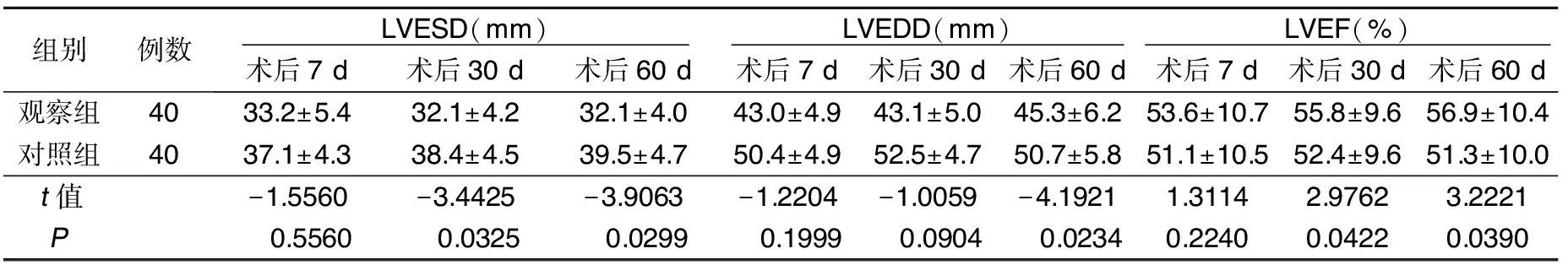
组别例数 LVESD(mm) 术后7 d术后30 d术后60 d LVEDD(mm) 术后7 d术后30 d术后60 d LVEF(%) 术后7 d术后30 d术后60 d观察组4033.2±5.432.1±4.232.1±4.043.0±4.943.1±5.045.3±6.253.6±10.755.8±9.656.9±10.4对照组4037.1±4.338.4±4.539.5±4.750.4±4.952.5±4.750.7±5.851.1±10.552.4±9.651.3±10.0t值-1.5560-3.4425-3.9063-1.2204-1.0059-4.19211.31142.97623.2221P 0.5560 0.0325 0.0299 0.1999 0.0904 0.02340.22400.04220.0390
2.3 两组治疗前后NT-proBNP水平比较 两组PCI术前NT-proBNP水平比较差异无统计学意义(P>0.05);治疗后两组NT-proBNP水平较治疗前明显下降(P<0.05),且观察组NT-proBNP较对照组降低明显(P<0.05)。详见表4。

表4 两组治疗前后NT-proBNP水平比较(±s) 单位:ng/L
与本组术前比较,①P<0.05。
2.4 两组MACE发生率比较 术后2个月随访,两组均未发生再梗死、恶性心律失常及室壁瘤等。
3 讨 论
STEMI是心血管科临床上最危急的疾病,致死率及致残率均极高,随着人们生活及饮食等习惯的变化,其发病呈逐年增加且呈年轻化趋势[7]。而治疗此类疾病的关键环节是挽救濒死心肌[8]。有研究表明,STEMI再灌注的“黄金时间”是发病后1 h以内,在此时间内达到有效的再灌注,所挽救的心肌数量和生命数量是最多的[9-11]。PCI是救治STEMI病人最为直接且有效的治疗方案,可有效缓解病人的临床症状,使STEMI病人病死率至少降低 25%以上,但是有部分STEMI病人PCI后会出现心肌无复流现象,严重影响了PCI近期和远期预后[11-14]。
PCI能够恢复STEMI病人闭塞冠状动脉供血区域,使心肌在最短的时间内恢复缺血再灌注,挽救缺血心肌细胞,改善病人预后[15]。有报道称,PCI治疗后即使罪犯血管前向血流恢复为TIMI 3级,但仍有部分病人会发生再灌注不良,影响远期疗效[16-17]。而PCI术后导致心肌组织再灌注不良发生的主要机制可能有以下几点[18],①冠状动脉微栓塞:因冠状动脉粥样硬化斑块破裂后血小板激活及聚集,会对心脏微循环血流造成影响,且球囊扩张及支架置入亦会导致冠状动脉管壁发生损伤,并进一步诱导斑块不稳定,致使微栓子脱落,直接造成微循环的再灌注障碍;②冠状动脉微血管痉挛:血栓破裂可释放缩血管因子,引起冠状动脉微血管痉挛;且冠状动脉缺血再灌注损伤后,可兴奋心脏交感神经,诱发微动脉的弥漫性痉挛发生;③冠状动脉微循环缺血再灌注损伤可引起血管内皮功能障碍、中性粒细胞聚集阻塞毛细血管、毛细血管通透性增加等,进而导致心肌组织再灌注不良;④冠状动脉血管结构破坏:在AMI发生后,在电镜下观察病变区毛细血管可见到明显的血管内皮损害,而在此时引起的无复流现象,使用药物治疗往往无反应。以上几点因素相互作用,可进一步加重AMI时的心脏微循环功能障碍,导致无复流现象发生[19]。硝普钠是速效血管扩张剂,能促进心肌组织血流灌注恢复,在心血管疾病治疗中疗效显著,是心血管疾病治疗中常用的药物[20]。有研究表明,硝普钠对冠状动脉慢血流现象具有明显的改善效果,可提高心血管疾病的治疗效果[21]。另有研究表明,冠状动脉内注射硝普钠可产生更持久的冠状动脉充血效应[22],因此,认为此法对PCI后无复流的预防具有一定效果。基于此判断,本研究中,观察组病人PCI术中支架置入后将微导管置入靶血管远端,注入硝普钠治疗,术后观察组治疗后TIMI 3级病人多于对照组(P<0.05),表明经冠状动脉微导管注射硝普钠可有效改善STEMI病人PCI后无复流现象。
有研究表明,硝普钠经冠状动脉微导管进入冠状动脉,进入血浆后,可释放一氧化氮,在血管内形成具有舒张血管平滑肌作用的缓激肽,进而发挥血管扩张作用,使冠状动脉血管平滑肌舒张,周围血管阻力降低;此改变有利于冠状动脉微循环、心肌组织再灌注及心功能的改善[23]。本研究结果显示,术后7 d,两组LVESD、LVEDD、LVEF比较差异无统计学意义(P>0.05);术后60 d观察组LVESD、LVEDD低于同期对照组(P<0.05),而LVEF则明显高于同期对照组(P<0.05);亦证实PCI术中经冠状动脉微导管注射硝普钠可显著改善STEMI 病人心功能,利于病人预后。另外,观察组PCI术后NT-proBNP较对照组降低(P<0.05);两组病人术后2个月随访,均未发生再梗死、恶性心律失常及室壁瘤等。表明PCI术中行经冠状动脉微导管注射硝普钠,可促进STEMI病人冠状动脉复流恢复及心功能改善,且能降低无复流现象,疗效显著。
综上所述,PCI术中经冠状动脉微导管注射硝普钠,可有效逆转STEMI病人PCI术治疗过程中无复流,改善病人微循环状态,提高疗效。
