慢性肾病患者血尿酸与动脉钙化的相关性研究
2020-05-07胡春兰吴泽成
周 龙, 胡春兰, 吴泽成, 赵 欢
(1.重庆三峡中心医院, 重庆 404000 2.湖北省十堰市中西医结合医院检验科, 湖北 十堰 442011)
我国研究显示,目前慢性肾脏病(chronic kidney disease,CKD)在普通人群中发病率约为10.8%,不同地区发病率有所不同,已成为我国严重的公共卫生问题[1]。研究表明,随CKD患者肾功能下降发生心血管疾病(cardiovascular disease,CVD)的风险增加,而CKD患者并发CVD是其主要死亡原因[2]。冠状动脉钙化作为CVD风险评估因素,也是CVD发病及其病死率的独立危险因素[3]。研究表明,CKD患者有较高的动脉钙化发生率,冠状动脉钙化可进一步引发心律失常、心脏瓣膜功能异常及心肌缺血等心血管事件,严重影响CKD患者预后[4]。相关危险因素研究表明,血尿酸水平能够反映动脉粥样硬化状况,与动脉钙化有关[5]。但血尿酸水平与CKD患者动脉钙化的关系尚未见报道。因此本研究分析CKD患者血尿酸水平及其与动脉钙化的关系,旨在为临床治疗CKD,改善预后提供参考。
1 资料与方法
1.1一般资料:选择2016年4月至2019年1月在重庆三峡中心医院诊治的142例CKD患者作为研究对象,根据《慢性肾脏病筛查诊断及防治指南》中的诊断标准进行确诊[6],记录所有患者性别、年龄、身高、体质量指数(BMI)、吸烟史、饮酒史及高血压、糖尿病、慢性肾炎等基础疾病。纳入标准:①规律随诊且符合慢性肾脏病诊断标准;②年龄>18岁且透析龄≥6个月;③均使用自体动静脉内瘘,入组维持性血液透析患者尿素清除指数均( urea clearance index,KT /V)≥1.2。排除标准:①近期内服用过骨化三醇、钙剂、降脂药物、磷结合剂等影响血脂水平、钙磷代谢的药物;②合并恶性肿瘤或有恶性肿瘤病史;③除甲状旁腺切除术后、心律失常、多发性骨髓瘤、淀粉样变性、恶性肿瘤或合并严重感染者和其他原因无法配合检查者。经钙化检测及积分评定为动脉钙化的CKD患者使用Fresenius医疗4008s血液透析机,聚砜膜透析器Fx60(面积1.4m2,一次性使用);碳酸氢盐透析液,透析液钙浓度为1.5mmoL/L,流速500mL/min,血流量200~260mL/min,低分子量肝素钙抗凝剂50~80U/Kg。本研究经重庆三峡中心医院伦理委员会审批通过;所有研究对象均签署知情同意书。
1.2方 法
1.2.1分组及治疗:所有患者入院时均进行X线监测动脉钙化情况。血管钙化检测及积分评定:使用X光机检查患者骨盆正位片、双手正位X线片、侧位腹平片,分别评价股动脉、髂动脉、手指动脉、桡动脉钙化情况;参照X线片血管钙化评分标准[7]:水平线和垂直线将骨盆X线平片分为4部分,分别位于股骨头切面和脊柱;双手正位片共分为4部分,双手各作为一部分,掌骨上方做水平线进行分隔;平L2、L3椎间隙将腹部上下分隔。共计10个部位,每个部位根据有无钙化分为1和0分,最终总分为0~10分。1~3分为轻度钙化,4~6分为中度钙化,>6分为重度钙化。由2位及以上放射科医师采用盲法阅片及评分。根据钙化评分结果,142例患者中动脉钙化66例,占比46.48%,分为钙化组,另76例无钙化患者分为非钙化组。钙化组患者进行血液透析滤过治疗。
1.2.2血液生化指标检测:采集所有患者入院时空腹肘静脉血,同时采集钙化组患者血液透析6个月时肘静脉血,采用罗氏cobas C701全自动生化分析仪检测血尿酸(uric acid,UA)、尿素氮(blood urea nitrogen, BUN)、血肌酐(serum creatinine,SCr)、血钙(Serum Calcium,Ca)、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、血红蛋白(hemoglobin,Hb)、血清白蛋白(albumin,Alb)、空腹血糖(fasting plasma glucose,FPG)、C反应蛋白(C-reactive protein,CRP)水平和24h尿蛋白定量,采用罗氏cobas E602全自动免疫分析仪检测患者全段甲状旁腺素(intact parathyroid hormone,iPTH),计算估计肾小球滤过率(estimated glomerular filtration rate,eGFR),eGFR=186×SCr-1.154×年龄-0.203×性别系数(男性为1,女性为0.742)

2 结 果
2.1两组一般资料比较:钙化组和非钙化组性别、年龄、身高、BMI、吸烟史、饮酒史、糖尿病等一般资料比较差异无统计学意义(P>0.05);两组高血压病例和慢性肾炎史比较差异有统计学意义(P<0.05),钙化组高血压比例、慢性肾炎史比例高于非钙化组(P<0.05),见表1。
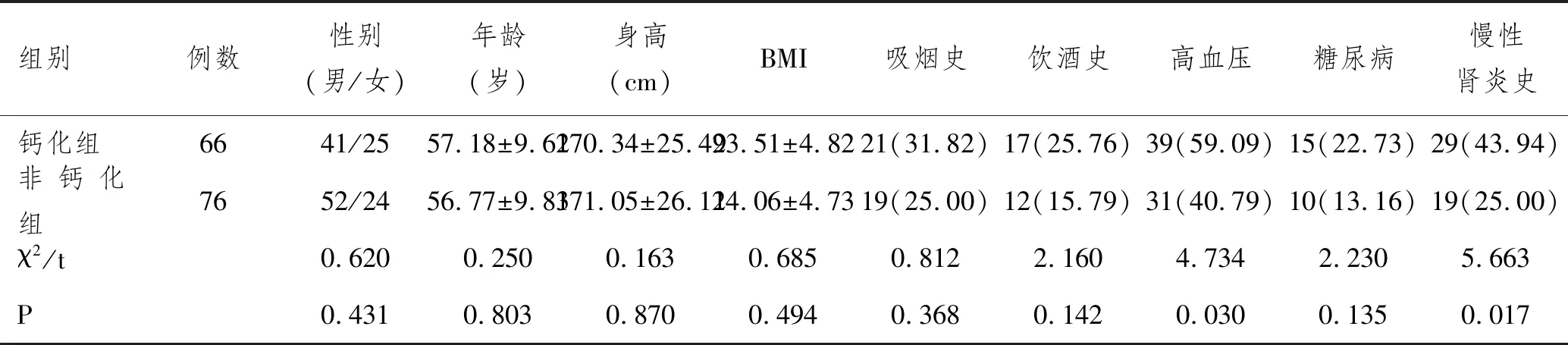
表1 钙化组和非钙化组一般资料比较
2.2两组生化指标比较:钙化组和非钙化组生化指标比较结果,BUN、SCr、Ca、TC、FPG、Alb、iPTH差异无统计学意义(P>0.05);钙化组TG、CRP、24h尿蛋白定量显著高于非钙化组(P<0.05),Hb、eGFR低于非钙化组(P<0.05),见表2。
2.3动脉钙化评分及血尿酸水平:钙化组经过至少6个月的血液透析滤过后动脉钙化评分和UA水平比较差异有统计学意义(P<0.05),透析后动脉钙化评分和UA水平均低于透析前(P<0.05),见表3。

表2 钙化组和非钙化组生化指标比较
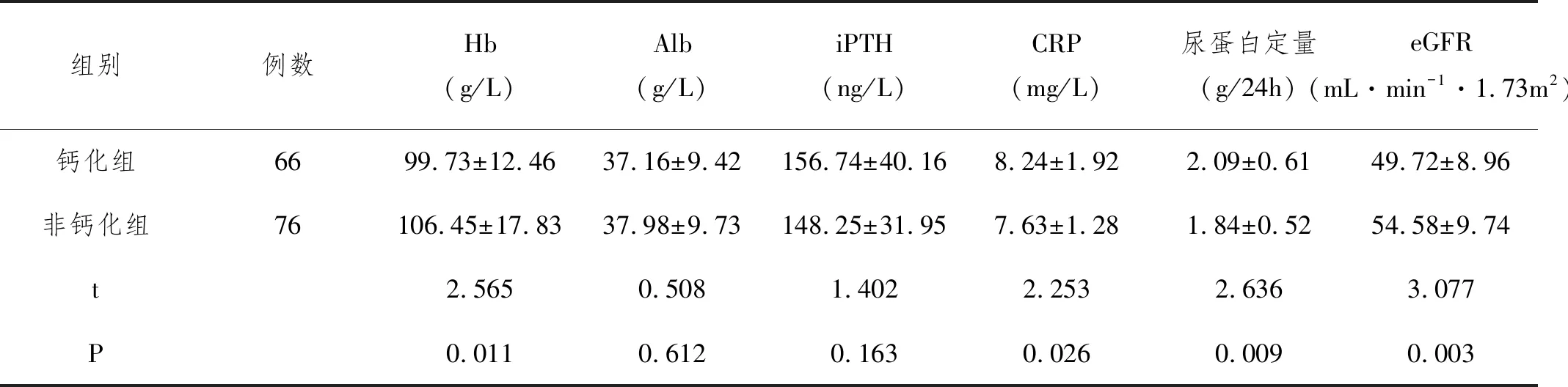
组别例数Hb(g/L)Alb(g/L)iPTH(ng/L)CRP(mg/L)尿蛋白定量(g/24h)eGFR(mL·min-1·1.73m2)钙化组6699.73±12.4637.16±9.42156.74±40.168.24±1.922.09±0.6149.72±8.96非钙化组76106.45±17.8337.98±9.73148.25±31.957.63±1.281.84±0.5254.58±9.74t2.5650.5081.4022.2532.6363.077P0.0110.6120.1630.0260.0090.003

表3 钙化评分及血尿酸水平
2.4动脉钙化评分与UA水平的关系:相关性分析显示,CKD患者动脉钙化评分与UA水平呈正相关(r=0.719,P=0.002)。见图1。
2.5血管钙化情况:66名(46.48%)CKD患者存在血管钙化。血管钙化患者中大动脉(腹主动脉)钙化患者43名(30.28%),中动脉(髂动脉和/或股动脉)钙化患者17名(11.97%),小动脉(桡动脉和/或手指动脉)钙化患者6名(4.23%)。
2.6动脉钙化危险因素分析:以UA、高血压、慢性肾炎及TG、Hb、CRP、24h尿蛋白定量和eGFR为自变量,进行Logistic多因素回归分析,结果显示UA和eGFR是影响CKD患者动脉钙化的危险因素,见表4。
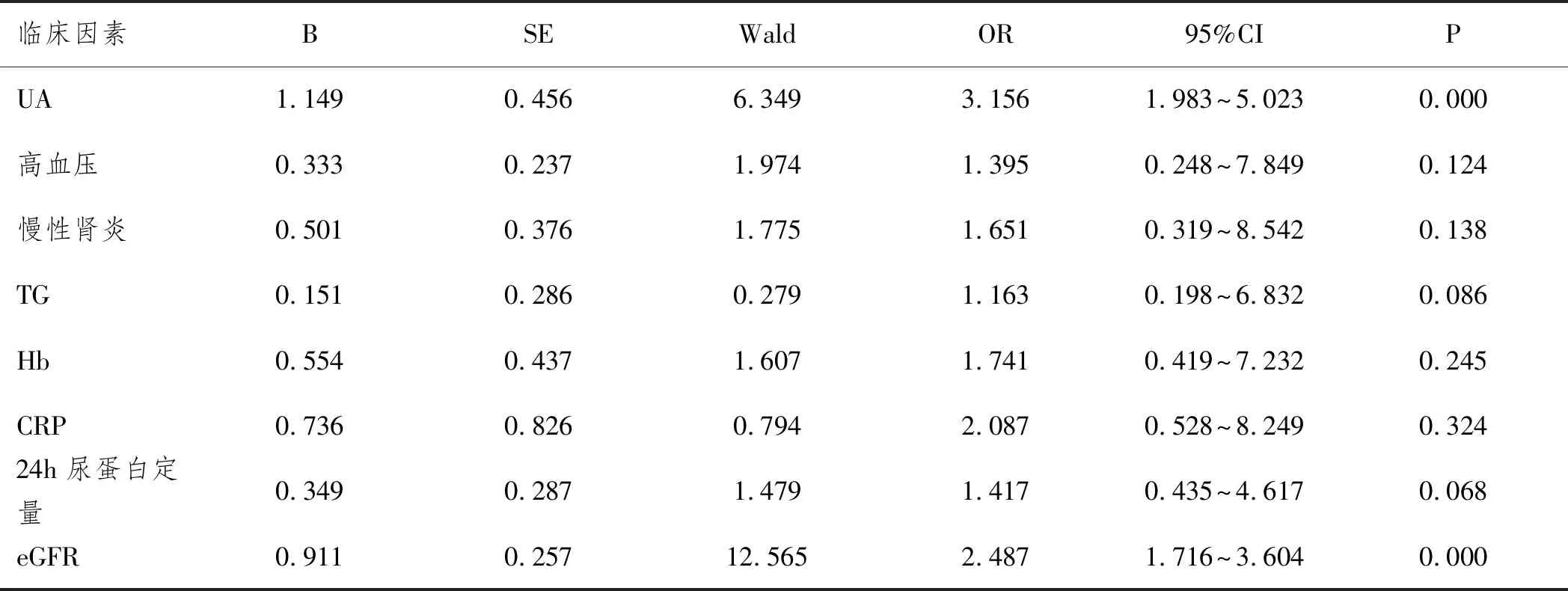
表4 动脉钙化危险因素分析

图1 动脉钙化评分与血尿酸水平的相关性
3 讨 论
血管钙化是指钙盐沉积于动脉壁,它是慢性肾脏病-矿物质和骨代谢异常(chronic kidney disease-mineral and bone disorder,CKD-MBD)患者较常出现的一种病理表现。透析患者的血管钙化分为血管中膜钙化和动脉粥样硬化基础上的内膜钙化,前者呈不规则斑片状,后者呈轨道样和线样[8]。动脉钙化无典型临床症状,但能降低血管顺应性,增加血管僵硬度,最终导致心功能不全,心律失常及心脏缺血性疾病等动脉钙化事件发生,是心血管疾病的潜在危险因素[9]。本研究检测142例CKD患者中66例存在动脉钙化,发生率46.48%。观察钙化组和非钙化组一般资料及血液生化指标发现,钙化组高血压比例、慢性肾炎史比例、TG、CRP及24h尿蛋白定量显著高于非钙化组,Hb、eGFR低于非钙化组。提示CKD患者可能具有较高的冠状动脉钙化发生率,且可能与高血压、高血脂等传统危险因素有关。
电子束 CT(electron beam computed tomography,EBCT)或多层螺旋CT(multislice spiral computed tomography,MSCT)是评估血管钙化的金标准,主要特点是高特异性和敏感性,但昂贵的设备费用使其不能作为常规检测手段普遍使用。检测血管钙化时,腹部X线片比EBCT具有更好的相关性[10],又因其方法简单、价格便宜、高特异性和灵敏度等优点成为血管钙化更为适用的检测手段。北京大学人民医院采用X线平片诊断动脉钙化的特异性和敏感性最高可达100%和60.2%。因此本研究采用X线平片检查不同部位动脉血管,同时进行钙化积分评定。
UA是嘌呤代谢的终末产物,正常生理状态下,机体内UA生成和排出处于动态平衡,当机体发生病理变化时,UA过多产生而在体内潴留,会引起高尿酸血症[11]。近年来大量研究证实,高尿酸血症作为CKD的独立危险因素可加剧肾脏病进展,其潜在作用机制可能与促进血管钙化、氧化应激、诱发炎症反应等有关[12]。本研究发现,动脉钙化组CKD患者UA水平明显高于非钙化组患者,对钙化组患者进行6个月血液透析滤过后,UA水平和动脉钙化评分均明显下降,说明UA水平可能与动脉钙化有关,长期规律血液透析滤过治疗有助于清除UA,降低动脉钙化水平。Jun等[13]研究动脉钙化和非钙化患者之间尿酸水平发现,动脉钙化患者尿酸水平显著高于非钙化患者,且存在明显的线性关系。本研究相关性分析显示,CKD患者UA水平与动脉评分呈正相关,提示UA水平可能与动脉钙化之间存在密切的联系。因此给予UA干预治疗可能是降低CKD患者并发动脉钙化事件,改善预后的有效方法。
高尿酸血症流行病学调查发现,UA水平升高与高血脂、高血压等主要心血管危险因素呈正相关关系[14]。结合本研究结果,可推测高UA水平可能与心血管事件发生有一定的联系。易扬等[15]研究报道,年龄、eGFR、钙磷乘积及血磷是影响CKD患者动脉钙化的独立危险因素。本研究Logistic多因素回归分析显示,UA和eGFR是CKD患者动脉钙化的独立危险因素。提示UA水平可作为参考指标用于临床检测反映CKD患者动脉钙化情况,预测心血管事件发生风险。
综上所述,并发动脉钙化的CKD患者UA水平较高,且UA水平与动脉钙化程度呈正相关,给予适当血液透析滤过能够清除UA,降低动脉钙化程度,提示联合血液透析滤过可能是改善CKD患者动脉钙化的有效方法,对临床预测及预防心血管事件发生,降低CKD病死率具有重要指导意义。
