血流感染患者利奈唑胺血药浓度监测与临床评价
2020-05-06张瑶谢凤杰范明辉
张瑶 谢凤杰 范明辉
[摘要] 目的 應用高效液相色谱法(HPLC)建立快捷稳定准确的利奈唑胺血药浓度测定方法,为血流感染患者个体化精准应用利奈唑胺提供参考。 方法 色谱柱Column-XB-C18(5 μm,4.8×250 mm),流动相乙腈-水(26-74)含0.4%乙酸,流速1.0 mL/min,色谱柱温度 30℃,波长254 nm,内标物质为氯霉素。应用该方法测量10例血流感染患者的血药浓度,为个体化精准应用利奈唑胺提供参考。 结果 血清利奈唑胺的浓度在(0.2~25.6)mg/L范围内有较的线性关系(r=0.9996),10例血流感染患者中利奈唑胺血药浓度波动明显,在(0.35~13.24) mg/L,其中有3例患者血药浓度低于最低抑菌浓度MIC(MIC=2 mg/L)。 结论 该方法可快速、稳定、准确的测定血流感染患者的利奈唑胺血药浓度,应用该方法可为临床血流感染患者提供个体化精准的给药方案。
[关键词] 利奈唑胺;高效液相色谱法;血药浓度检测;血流感染
[中图分类号] R978.1 [文献标识码] B [文章编号] 1673-9701(2020)06-0120-03
[Abstract] Objective To establish a rapid,stable and accurate method for determination of plasma concentration of linezolid by high performance liquid chromatography(HPLC), and to provide a reference for individualized and precise application of linezolid in patients with bloodstream infection. Methods Chromatographic column Column-XB-C18 (5 μm,4.8×250 mm),mobile phase acetonitrile-water(26-74) containing 0.4% acetic acid,with a flow rate of 1.0 mL/min, a column temperature of 30℃,and a wavelength of 254 nm. Chloramphenicol was used as internal standard substance. This method was used to determine the plasma concentration of 10 patients with bloodstream infection,to provide reference for the individualized and precise application of linezolid. Results A linear relationship of serum linezolid concentration was found in the range of(0.2-25.6) mg/L(r=0.9996). It was found that the blood concentration of linezolid fluctuated significantly in 10 patients with bloodstream infection,ranging from 0.35 mg/L to 13.24 mg/L. Three out of ten patients had plasma concentration lower than the minimum inhibitory concentration MIC (MIC=2 mg/L). Conclusion The method can determine the plasma concentration of linezolid in patients with bloodstream infection rapidly,stably and accurately. It can be applied on individualized and precise administration of linezolid for patients with bloodstream infection.
[Key words] Linezolid; High performance liquid chromatography; Blood concentration determination; Bloodstream infection
利奈唑胺是人工合成的恶唑烷酮类抗生素,2000年获得FDA批准用于临床。该药与细菌50S亚基的23S核糖体RNA上的位点结合,阻断形成功能性70S始动复合物,从而抑制细菌生长。与人体其他部位感染相比,如肺部感染、泌尿系感染、腹腔感染等,血流感染更为严重。利奈唑胺在中国人群中的药物代谢模型特点表明,体重和年龄等因素均会影响利奈唑胺的体内代谢过程[1],并且血流感染的患者会出现病理生理学改变,血流动力学和药物代谢动力学不稳定[2-5]。但未见关于血流感染患者利奈唑胺血药浓度检测的报道,因此有必要建立测定血流感染患者利奈唑胺血药浓度的方法。本文旨在建立稳定、快捷、准确的HPLC测定血药浓度方法,使血流感染患者个体化精准的应用利奈唑胺治疗感染,现报道如下。
1 材料与方法
1.1 实验仪器、试剂及药品
Waters 高效液相色谱仪、四元高压数码梯度泵、120位自动进样器、Waters 2487双波长紫外检测器、EMPOWER 2 工作站。PRP美容高速离心机、上海力辰分析天平,-80℃和利冰箱。试剂:利奈唑胺对照品(百灵威公司,产品编号:343910,纯度>98%)、乙腈 (色谱纯,迈瑞尔产品编号F30001)、氯霉素对照品(Tmstandard-1,产品编号:70671,纯度99.6%)、纯净水。药品:利奈唑胺注射液(规格:300 mL:600 mg,厂家:辉瑞,国药准字:H20190305)。
1.2 方法
1.2.1 HPLC色谱条件 色谱柱Column-XB-C18(5 μm,4.8×250 mm),流动相比例乙腈-水(26-74)含0.4%乙酸,流速1.0 mL/min,色谱柱温度30℃,波长254 nm,进样量 20 μL,内标物质为氯霉素。
1.2.2 对照品、内标物及样品的处理 利奈唑胺对照品及内标物用流动相溶解,配置浓度均为0.2 mg/L备用。取300 μL血浆,加入2 mL的离心管中,再加入200 μL的甲醇沉淀蛋白,涡旋30 s,之后3000 r/min 离心10 min,取上清液20 μL进样。
1.2.3 专属性考察 取2份血浆,将一定浓度的利奈唑胺和氯霉素标准品放入血浆中,按照“1.2.2”项样品处理方法进样测定。
1.2.4 线性关系考察 用移液枪吸取空白血浆1 mL加入备用利奈唑胺溶液及氯霉素溶液,配制成系列利奈唑胺药物浓度0.2 mg/L、0.4 mg/L、0.8 mg/L、1.6 mg/L、3.2 mg/L、6.4 mg/L、12.8 mg/L、25.6 mg/L的溶液,按照“1.2.2”项样品处理方法进样。
1.2.5 精密度实验、回收率实验、稳定性实验 取空白血浆按照“1.2.2”项样品配制方法配制成浓度0.4 mg/L、0.8 mg/L、1.6 mg/L的样品备用,分别于1 d内测3次,及连续3 d每天测一次,考察其精密性。测定该3种浓度的峰面积,与标准方程计算量进行对比,计算回收率。将3种浓度的样品分别在室温条件下放置24 h,样品处理后复溶24 h,-80℃冷冻10 d后复溶,测定其稳定性。
1.2.6 血流感染患者血药浓度检测 10例临床诊断为血流感染患者(均为革兰阳性细菌感染)在0.6 g Q12 h的条件下,48 h后再次给药前10 min静脉取血2 mL,每例患者测定6次血药浓度,按照“1.2.2”项方法测定患者血浆利奈唑胺的血药浓度,根据患者的血药浓度实际情况,个体化精准调整患者的给药方案。根據患者的临床表现,如体温情况、血肌酐情况、患者主诉、患者精神状态、血流动力学情况,其中有两项及以上临床症状未改善,视为无效,三项及以上临床症状改善视为有效。
2 结果
2.1 专属性考察
色谱图基线平稳,利奈唑胺与内标物完全分离,未受内标物的影响。利奈唑胺保留时间TR=5.3 min,氯霉素保留时间TR=7.6 min,见图1、图2。
2.2 标准曲线的绘制
根据最小二成法计算标准曲线,得回归方程为Y=0.362C-0.0052(r=0.9996),其中Y为利奈唑胺面积与内标物面积之比,C为利奈唑胺的浓度,利奈唑胺浓度C线性范围应该控制在(0.2~25.6)mg/L。
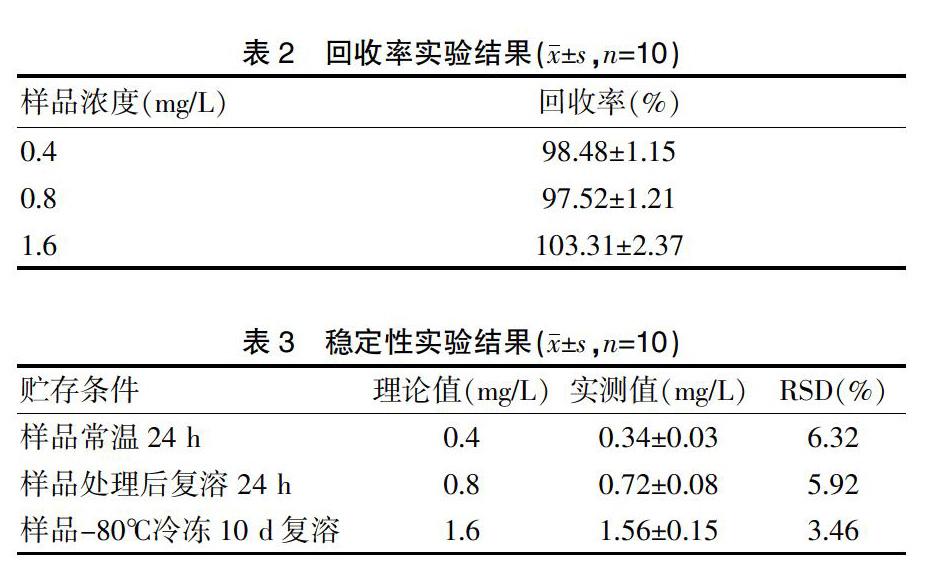
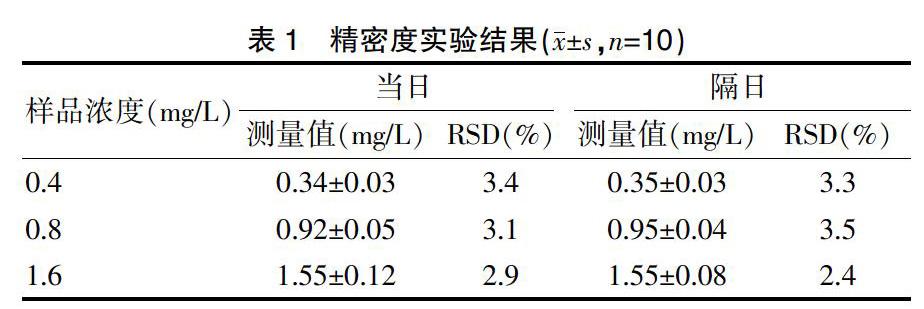
2.3 精密度、回收率实验、稳定性实验结果
精密度实验结果RSD波动在2.4%~3.5%,回收率实验结果均值波动在97.52%~103.31%,稳定性试验结果RSD波动在3.46%~6.32%。说明该方法符合测定利奈唑胺的血药浓度要求。见表1~3。
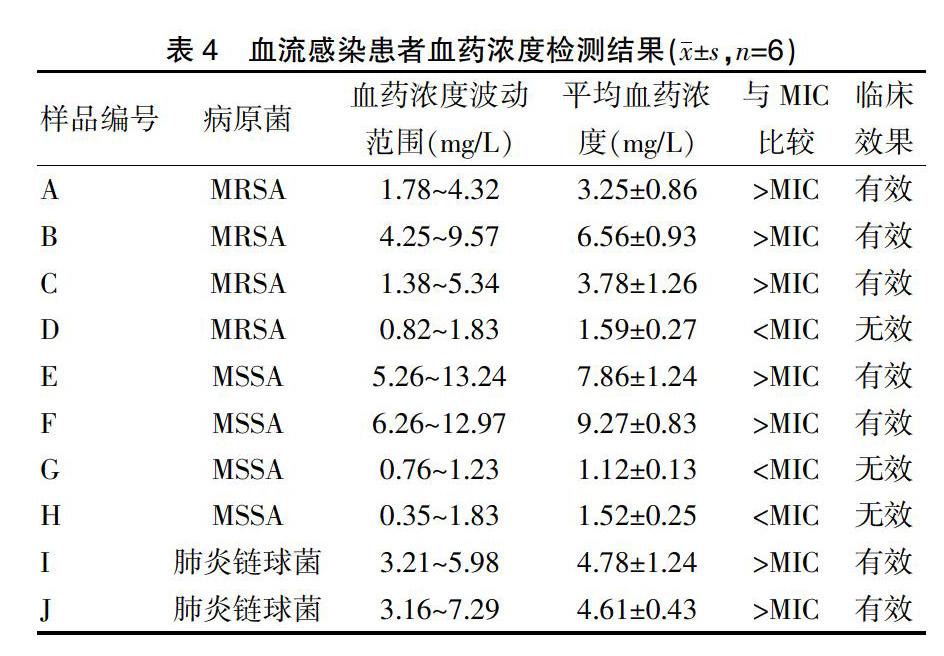
2.4 血流感染患者血药浓度检测结果
10例应用利奈唑胺治疗血流感染患者的血药浓度波动范围在(0.35~13.24) mg/L,其中有3例小于MIC(MIC=2 mg/L),且临床无效。见表4。
3讨论
本研究建立了快捷、稳定、准确的HPLC测定利奈唑胺血药浓度的方法,该方法利奈唑胺的保留时间更短[6],节省了分析时间,分析方法更加快捷,本研究采用内标法,内标法建立的回归方程因变量是内标物和对照品的峰面积或峰高的比值,因此内标法回归方程的计算与进样量无关,并且适合测定微量组分。当前耐甲氧西林金黄色葡萄菌MRSA已经成为院内感染首要的致病菌[7]。2017年全国耐药监测网显示我国西藏MRSA检出率为52%。更加严重的是日本及美国已经有报道出现了万古霉素耐药的金黄色葡萄球菌VISA[8]。而我国也已经分离出万古霉素中介的菌株hVISA[9]。临床常用治疗血流革兰阳性菌药物主要包括万古霉素、利奈唑胺、达托霉素。目前利奈唑胺可能是革兰阳性细菌的最后一道防线,相关研究表明利奈唑胺治疗MRSA感染疗效优于万古霉素[10-11],且万古霉素有一定的肾毒性[12],利奈唑胺和达托霉素治疗血流感染的疗效和安全性相似[13]。本研究选择利奈唑胺治疗血流感染,其中有3例患者血药浓度小于利奈唑胺的MIC,且临床表现为无效。血药浓度长时间低于MIC可能导致耐药菌的产生[14],因此当临床在应用利奈唑胺血药浓度低于MIC时应更加引起重视,值得注意的是,MIC可能会随着抗生素的广泛应用而改变[15]。
本研究的结果表4显示,血流感染患者的血药浓度波动在(0.35~13.24)mg/L,波动百分率为97.36%(计算公式为Cmax-Cmin/Cmax),血药浓度波动较大。血流感染患者通常继发于人体其他部位的感染,且血流动力学发生改变,血液中细菌的感染程度及细菌本身的毒性亦各不相同,可能是血药浓度波动明显的原因。血药浓度波动较大可能增加药物的不良反应的发生,但还需要观察更多血流感染患者的利奈唑胺血药浓度波动与不良反应之间的关系来进一步明确。
综上所述,本研究建立了快捷、稳定、准确的HPLC测定人血浆中利奈唑胺浓度方法,使血流感染的患者能够更加安全有效的应用利奈唑胺,有一定的应用价值,值得临床广泛推广。
[参考文献]
[1] 张雷,白楠,刘又宁,等. 利奈唑胺在中国人的群体药代动力学特点[J]. 中华结核和呼吸杂志,2016,39(12):924-928.
[2] 董海燕,董亚琳,杨华,等. 利奈唑胺在不同疾病患者中药动学变化的临床意义[J]. 中国新药与临床杂志,2010, 29(3):170-174.
