添加液去白洗涤红细胞在保存中的质量观察
2020-04-20郑井滨张丽姚美辰李静旗王雅卿毕聪玺
郑井滨 张丽 姚美辰 李静旗 王雅卿 毕聪玺
洗涤红细胞是输血治疗中一种常用的血液制剂,是采用特定的方法将保存期内的全血、悬浮红细胞用大量等渗溶液洗涤,去除几乎所有血浆成分和部分非红细胞成分,并将红细胞悬浮在生理盐水或红细胞添加液中所制成的红细胞成分血[1]。常规洗涤红细胞的制备方法是用生理盐水作为洗涤液和悬浮液来制备,保存期只有24小时。因此,临床使用洗涤红细胞时需采用预约的方式,现制现用,临床输血的及时性较难保证[2]。预约、制备、运输的时间耽搁可能会造成部分患者尤其是急诊患者不能及时输血而影响疾病的治疗。虽然目前部分采供血机构向临床提供了可保存的添加液洗涤红细胞,但保存期限相差悬殊[3-7],为了解可保存的去白洗涤红细胞在保存期内的质量情况,我们进行了系统观察,现报告如下。
材料与方法
1 添加液去白洗涤红细胞的制备 随机选取8袋全血(红细胞保养液为ACD),采集时间6 h内过滤法制备去白细胞悬浮红细胞,悬浮液为MAP(甘露醇-腺嘌呤-磷酸盐),然后将每袋去白细胞悬浮红细胞平均分为6份,1份直接置于2~6 ℃冰箱中保存(对照组),用于血液长期保存过程各项指标的对比观察,其余5份用生理盐水或MAP进行洗涤,再分别用生理盐水、MAP及ACD(枸橼酸-枸橼酸钠-葡萄糖)中的一种进行悬浮。根据洗涤液和悬浮液的不同分组如下:生理盐水洗涤-生理盐水悬浮组(N-N组)、生理盐水洗涤-MAP悬浮组(N-M组)、生理盐水洗涤-ACD悬浮组(N-A组)、MAP洗涤-MAP悬浮组(M-M组)、MAP洗涤-ACD悬浮(M-A组)。制备方法同常规洗涤红细胞[8],制备后置于2~6 ℃冰箱中保存。
2 仪器与试剂 电解质分析仪(日本富士 FDC-800)、多参数测试仪(Mettler Toledo SG78)、全自动生化分析仪(罗氏 C111)、血细胞计数仪(日本Sysmex XT-1800i)、大容量血细胞计数盘(Nageotte)、离心机(贝克曼 J-6B)、无菌接口机(泰尔茂 TSCD-II)、冰箱(日本三洋 SR1410)。脑脊液与尿蛋白测定试剂盒(北京利德曼),血浆游离血红蛋白测定试剂盒(北京瑞尔达)、硫乙醇酸盐培养基及胰酪大豆胨培养基(南京乐诊)。生理盐水、MAP、ACD均来自上海输血技术有限公司。
3 检测方法 各组去白细胞洗涤红细胞制备完成后立即取样进行如下项目检测:K+浓度、pH、游离血红蛋白、血红蛋白含量、上清蛋白含量、白细胞残留量、无菌实验。之后按照保存的时间间隔1天、3天、7天、14天、21天、28天、35天分别取样进行K+浓度、pH、游离血红蛋白项目检测。测量方法:K+浓度采用离子选择电极法测量(K+浓度低于1 mmol/L时显示over range,为了便于统计分析,取1 mmol/L进行计算),pH采用多参数测试仪电极法进行测量,其它项目按照试剂盒说明书进行检测。血红蛋白含量、上清蛋白含量、白细胞残留量测得的结果均乘以3转换成标准1U去白细胞洗涤红细胞中的结果。
4 统计学处理 利用SPSS19.0统计软件进行统计分析,数据以均值±标准差( ±s)表示,洗涤后即刻检测的项目(血红蛋白、上清蛋白、白细胞残留量),各洗涤实验组采用单因素方差分析。其它项目根据不同的分组与各时间间隔按照重复测量的析因设计进行方差分析,差异有统计学意义时,两组间比较采用统计软件包中的LSD检验,P<0.05表示差异有统计学意义。
结 果
1 去白洗涤红细胞制备后即刻检测的血红蛋白含量、上清蛋白含量、白细胞残留量和无菌试验项目结果见表1。
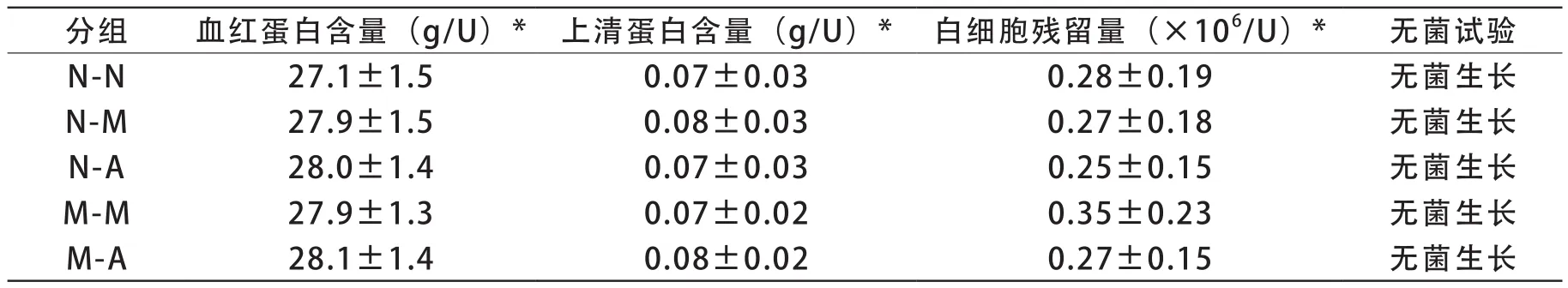
表1 去白洗涤红细胞即刻检测项目检测结果
2 K+浓度检测结果 在保存过程中,去白细胞悬浮红细胞(对照组)及各洗涤实验组上清液中K+浓度、pH值及FHb含量变化情况见表2。各“时间”点对应的F=2 733.303,P<0.05,说明不同时间点之间的差异有统计学意义;“时间*分组”所对应的F=28.678,P<0.05,时间与分组的交互作用有统计学意义;“分组”对应的F=438.233,P<0.05,不同分组之间差异有统计学意义。LSD分析结果:对照组、N-M组与M-M组,三组间差异无统计学意义(P>0.05);其余各组间差异有统计学意义(P<0.05)。洗涤后0天,N-M组和M-M组K+浓度为1.3 mmol/L,之后逐渐升高,在第3天时达到去白细胞悬浮红细胞(对照组)水平。N-N组在第7天后K+浓度显著升高,但低于N-A组与M-A组。(见图1)
3 pH值检测结果 在储存期间,pH变化结果见表2,趋势走向情况见图2。各“时间点”对应的F=2.829,P<0.05;“分组”对应的F=60.376,P<0.05;“时间*分组”所对应的F=3.869,P<0.05。不同时间点、分组之间差异有统计学意义,时间与分组存在交互作用。LSD分析结果:对照组与N-N组;N-M组与M-M组;N-A组与M-A组小组内两组差异无统计学意义(P>0.05),而与其它组差异有统计学意义(P<0.05)。
4 FHb含量检测结果 在保存过程中,上清中FHb情况见表1。各“时间点”对应的F=569.242,P<0.05,说明不同时间点之间的差异有统计学意义;“时间*分组”所对应的F=47.016,P<0.05,时间与分组的交互作用有统计学意义;“分组”对应的F=74.899,P<0.05,不同分组之间差异有统计学意义。LSD分析结果:对照组、N-M组与M-M组之间无统计学差异(P>0.05);N-N组与N-A组无统计学差异(P>0.05),M-A组与其他各组均有统计学差异(P<0.05)。5 综合K+、pH和FHb三项实验结果,在5个实验组中,M-M组及N-M组保存效果较为理想,以N-M组最佳。

表2 保存过程中K+浓度、pH值及FHb含量变化(n=8)
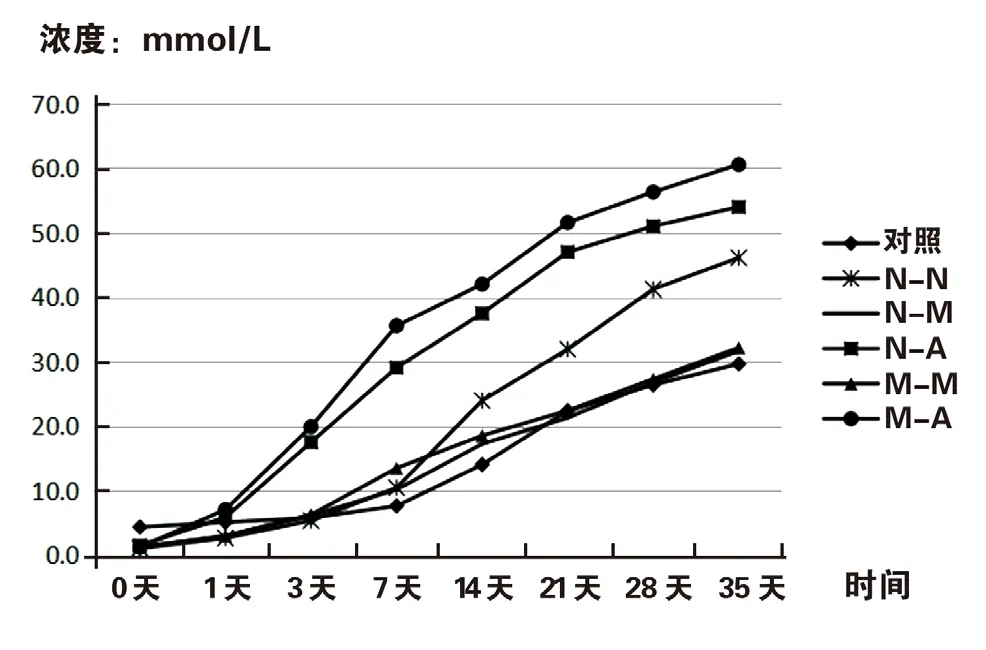
图1 保存过程中K+浓度变化情况
讨 论
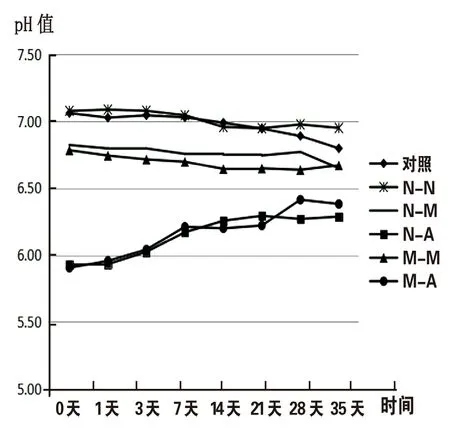
图2 保存过程中pH值变化情况
输血作为一种重要的治疗手段,被临床广泛应用,但输血同时也会使受血者产生各种输血不良反应。不同的血液成分制品可引起的输血不良反应种类、程度及发生概率也会有所不同。洗涤红细胞制品因在制备过程中去除了大部分白细胞、细胞碎片、血浆蛋白等成分,可以有效减少输血发热、过敏等不良反应。目前临床上洗涤红细胞制品主要用于输入全血或者血浆后发生过敏反应(荨麻疹、血管性神经性水肿、过敏性休克等)的患者、高血钾症及肝、肾功能障碍需要换血的患者等[9]。常规洗涤红细胞的保存期只有24小时,预约洗涤机制不利于患者的及时救治,可长期储存的洗涤红细胞应用前景广泛。通过本次实验结果可以看出,无论采用何种洗涤液(生理盐水、MAP)何种悬浮液(生理盐水、MAP、ACD)制备的去白洗涤红细胞,即刻检测出的血红蛋白含量、上清蛋白含量、白细胞残留量和无菌试验结果均满足国家相关标准要求,各组间差异无统计学意义。随着储存时间的延长,各种血液成分中K+浓度都有增高的趋势,未洗涤对照组及经过洗涤制备的N-N组、N-M组、M-M组在保存3天时有部分样本浓度超过了正常人参考区间[10],而N-A组和M-A组则在保存第1天就已经超过此范围。本次实验结果趋势与文献基本一致,检测值略有不同[3,5,11-13],这可能与加工制备的血液原料类别、制备的时间、加工方式等有一定关系。MAP组成成分中由于腺嘌呤的加入,可提高血液ATP在4℃贮存期间的活性水平,延长血液的保存时间,但对于其成分过敏者及新生儿溶血病的换血治疗时禁止使用该添加液。也有文献表明应用300mg/(kg·d)大剂量(远高于保养液中的含量)腺嘌呤对动物灌胃三周左右,可用来制备动物肾衰竭模型,出现肾间质纤维化,肾功能异常[14]。ACD与MAP比较,血液保存期只有21天,其成分中不含甘露醇、腺嘌呤、氯化钠和磷酸二氢钠,组成成分更单一,输入患者体内后负担可能更小,为此本文尝试利用ACD对洗涤红细胞进行保存。但从本次实验结果可以看出,当用ACD来替代MAP对洗涤红细胞进行保存时,没有取得理想的预期效果,甚至劣于生理盐水的保存效果。无论用生理盐水进行洗涤还是MAP进行洗涤,当用ACD进行悬浮保存时,由于ACD的pH(4.5~5.5)比MAP(5.0~6.0)更偏酸性,会使红细胞一直处于pH较低的酸性环境,此时对于细胞损伤比较严重,会加速其溶血,溶血程度甚至高于N-N组。通过图2也可以看出,利用ACD进行保存时,其产品pH在储存期间一直在上升,与其它实验组对照组的下降趋势刚好相反,通过本次实验可以看出对于MAP保存的去白悬浮红细胞不适宜以ACD作为添加液来制备可保存的洗涤红细胞,但能否通过改变起始血液成分,从ACD抗凝的全血直接制备洗涤红细胞,有待于后续进一步研究。
综合K+、pH和FHb三项实验结果,在5个实验组中,M-M组及N-M组保存效果较为理想,以N-M组最佳。虽然大量输注保存期3周以上的血液有引起患者高血钾的风险,但输血速度不超过(100~150)mL/min,很少会发生严重的高血钾[15]。当输血量不多时,成分血中的K+迅速被患者体内的血液及细胞外液所稀释,一般不会有明显的血钾变化[9]。大量输血时,如果短时间内输入大量保存期较长的成分血,则可能出现高血钾或者低血钾,这与患者自身的基础代谢情况有关。如果患者肾功能正常,当血钾增高时,机体内醛固酮、抗利尿激素和糖皮质激素分泌增加,促进肾脏排钾;Na+-K+-ATP泵对温度变化高度敏感,4℃时几乎丧失功能,输入患者体内的血液随着pH及温度环境的改善,Na+-K+-ATP泵功能逐渐恢复,也可以促进血K+向细胞内转移,使钾离子趋向正常范围。另外,血液保养液中含有枸橼酸盐成分,枸橼酸盐在肝脏可迅速转化为碳酸氢钠,出现代谢性碱中毒,细胞内的氢离子与细胞外的钾离子,氢钾交换来缓冲碱中毒,出现低血钾;当机体出现碱中毒时,肾脏排钾增加,也会使血钾下降。目前国家标准中尚没有对于洗涤红细胞(储存期24 h)和可长期保存的洗涤红细胞(保存期同悬浮红细胞)中K+浓度的质量控制要求,若以K+浓度不超过5.5 mmol/L作为限值,通过本次实验结果分析及相关资料了解,我们认为对于无高钾血症、肝肾功能正常的患者可以输注在有效期内的添加液去白洗涤红细胞,但对于一些特殊患者,如自身有高K+血症倾向患者建议使用储存期为24 h的生理盐水洗涤红细胞,或保存期在3天内的MAP添加液去白洗涤红细胞。
综上,洗涤红细胞(储存期24 h)和可长期保存的洗涤红细胞(保存期同悬浮红细胞)并非是完全相同的两种血液产品,而是应该根据患者的临床病情,针对性选择,对于肝脏、肾脏无功能障碍,肾脏循环血量正常的贫血患者,可任意选择其一,但是对于患者自身存在高钾血症、肾功能代谢障碍(如尿毒症或有大量严重创伤合并肾功能不全)代谢性酸中毒等特殊患者,为了安全起见,建议输用3天内的MAP添加液去白洗涤红细胞或传统生理盐水悬浮的洗涤红细胞(储存期24 h)。
